全氟辛酸和全氟辛烷磺酸的提取和检测技术应用
徐双双 王 尉 汤 桦 贺天雨 赵新颖
(1.北京市理化分析测试中心,北京 100094;2.中国计量科学研究院,北京 100029;3.北京电子科技职业学院,北京 100176)
1 前言
全氟辛酸(Perfluorooctanoic acid,PFOA)和全氟辛烷磺酸(Perfluorooctane sulfonic acid,PFOS)是具有超疏水性的重要工业前体,在印染、涂料、纺织和化工等领域具有极其重要的应用[1-5]。该类化合物能够经受较强光、热、化学和微生物作用以及动物的代谢,很难降解[6],也是一类新型持久性有机污染物。近年来,大量报道PFOA和PFOS在土壤、水、食品和生物样品都有检出[7-9]。尤其引起关注的是PFOA和PFOS具有很强的生物累积性,哺乳动物、蚤类和其他水生生物食物链等高生态位的水生生物对PFOA和PFOS具有很强的生物富集作用[10,11],分布于血液和肝脏,能引起器官病变、生殖干扰、免疫毒性和致癌性[12]。目前,世界各国对PFOA和PFOS的危害和污染已达成共识。美国环保署饮用水指南规定PFOA的限值为70 ng/L,欧洲议会和理事会修改指令规定内陆地表水中PFOS及其衍生物的含量限制为0.65 ng/L。我国规定饮用水中氟化物含量不得超过1.0 mg/L,但尚未制定PFOA和PFOS单体的限值[13-15]。
PFOA和PFOS检测难点在于样品基质的多样(包含土壤、水、水品和生物组织等),目标物含量低,同系物数量多;具有超级疏水性,在紫外、二极管阵列等检测器上均无响应。因此,PFOA和PFOS的分离和检测都有一定的困难。本文从常规分析测试角度出发,概述了我国近5年中各类样品中PFOA和PFOS的提取方法,介绍了常用的色谱以及色谱质谱联用的检测方法,为PFOA和PFOS的日常检测提供了一些参考。
2 样品提取方法
样品提取方法应当快速简捷,成本低,能满足大批样品的检测需求,避免浪费溶剂,减少二次污染。PFOA和PFOS分布广泛在食品、动物内脏、土壤、空气颗粒物等基质中,样品状态有固体、半固体和液体,且含量处于痕量水平。因此,提取方法需要同时达到提取、净化和高倍富集的效果。目前,实验室常用的有液液萃取法、超声萃取法、固相萃取法、加速溶剂萃取法和QuEChERS法[16],见表1。
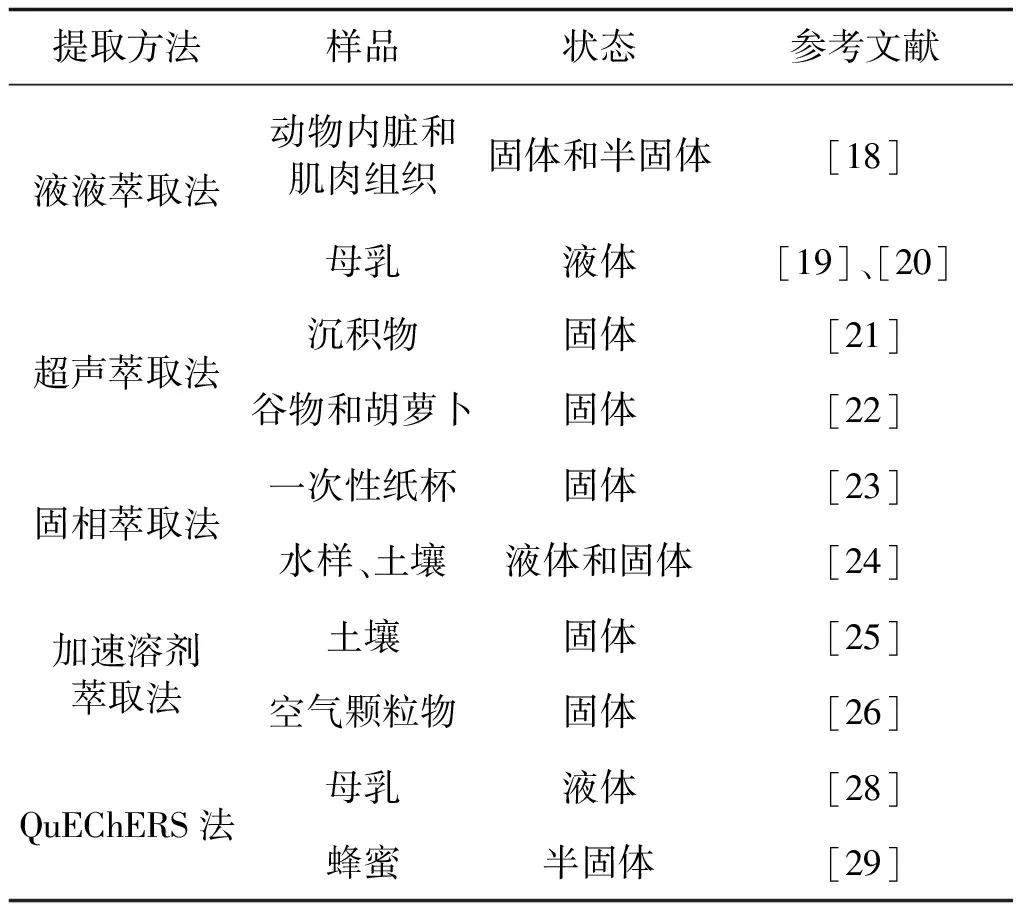
表1 样品提取方法、名称和状态
2.1 液液萃取法
液液萃取法利用目标物在不同溶剂中溶解性的差异,对其进行提取富集,常用萃取剂有甲基叔丁基醚(MTBE)、四丁基铵(TBA)和乙腈等[17]。王杰明等[18]采用MTBE作为萃取剂对动物内脏和肌肉组织中PFOA进行液液萃取。取样本1g,加入2 mL碳酸钠缓冲溶液(pH 10),提取液过WAX柱,洗脱液用氮气吹至约0.5 mL,定容至l mL,离心检测。结果显示,方法检出限为0.018 μg/L,加标回收率为82.9%~113.3%。Thomsen等[19]和Lankova等[20]采用乙腈作为萃取剂对母乳中PFOA进行液液萃取,加标0.15 ng/mL或1.5 ng/mL时回收率分别为92%~106%和93%~117%。液液萃取法是最传统的提取方法,操作程序相对繁琐,耗费的萃取剂量较多,不适于大批量样品的检测,目前已逐渐被其他提取方法替代。
2.2 超声萃取法
超声萃取法利用超声波辐射压强产生的强烈空化应效应、机械振动、扰动效应、高的加速度、乳化、扩散、击碎和搅拌作用等多级效应,增大物质分子运动频率和速度,加速目标成分进入溶剂,促进提取的进行。实际检测中,这种技术主要应用于固体样品中PFOA和PFOS的提取,如土壤、底泥、灰尘等。黄东仁[21]采用甲醇作萃取剂对沉积物中的PFOA进行超声提取,70℃持续60 min。结果显示,PFOA加标回收率为(103.2±9.2)%, PFOS加标回收率为(82.5±9.2)%,定量限(LOQ,S/N = 10)为0.08 ng/g。Xiang等[22]以谷物和胡萝卜等可食用作物为研究对象,比较了甲基叔丁基醚(MTBE)、乙腈/水、四氢呋喃/水)的萃取效果,发现采用乙腈/水为溶剂进行超声萃取效果最好。超声萃取法的优势是无需高温、方便快捷、普适性好;缺点在于只适用于简单样品的提取,对于生物样品等复杂样品的适用性需进一步研究,且大部分样品经过超声萃取后要经过旋转蒸发仪浓缩,操作繁琐,方法稳定性不高。
2.3 固相萃取法
固相萃取利用吸附剂将目标物吸附,再经过洗脱液洗脱或解吸附,达到对目标物分离和富集的目的。PFOS等含氟表面活性剂具有较长的烷基链,可利用同相萃取法来进行富集提取。目前,样品提取使用较多的固相萃取柱是C18柱和HLB柱。刘征辉等[23]利用WAX固相萃取小柱对一次性纸杯中PFOA和PFOS进行富集,结果显示,在0.1~2.0 ng/mL范围内线性关系良好,平均加标回收率为81.27%~97.12%,相对标准偏差(RSD)为2.9%~7.4%,为食品接触材料中全氟化合物的迁移限量标准提供了技术支持。杨文龙等[24]分别将水样、土壤样品经过WAX柱进行提取。结果显示,水中的PFOA和PFOS的检出限分别为0.1 ng/L和0.3 ng/L;土壤检出限分别为4 ng/kg和7 ng/kg,PFOA和PFOS的添加回收率分别介于88.4%~98.8%和 88.0%~97.3%之间,RSD小于14%。回收率分别介于98.6%~113%和96.8%~111%之间,RSD小于7%。该方法灵敏、准确、可靠,可以满足环境水与土壤介质中痕量PFOA和PFOS的监测要求。固相萃取法是目前应用最广泛的萃取技术,优势萃取效率高、有机溶剂消耗低、易收集、操作方便,是富集环境、食品包装材料等样品中的PFOS和PFOA的首选提取方法。
2.4 加速溶剂萃取法
加速溶剂萃取法是在较高的温度(50~200℃)和压力(10.3~20.6 FMPa)下,用相应的溶剂对固体或半固体的样品进行提取的方法。王懿等[25]采用甲醇作为萃取剂运用该方法对土壤中PFOA进行富集,在浓度范围0.518~3.520 pg/g之间,回收率为71.2%~119.2%。杨运云等[26]采用甲醇-丙酮(1∶1, V/V)作为萃取剂,对空气颗粒物样品中的PFOA进行萃取,回收率为80%~100%。与其提取方法相比,加速溶剂萃取法的使用温度更高,且可以增加一定的压力,效率高,有机溶剂用量少、耗时较短以及自动化程度高,在科研类分析实验室中的普及程度和利用率逐步提高。
2.5 QuEChERS
QuEChERS是Anastassiades教授等[27]于2003年开发的一种用于除杂净化的快速样品提取方法,利用吸附剂填料与基质中的杂质相互作用,吸附杂质,从而达到净化的目的。李磊等[28]采用乙腈提取母乳中的PFOA和PFOS等全氟化合物,母乳中的脂肪和水分分别通过QuEChERS法净化,净化液经氮吹定容后能直接用于LC-MS/MS定量分析。李帅等[29]采用改进的QuEChERS方法对蜂蜜进行提取,用含1.5%甲酸的乙腈溶液振荡提取PFOA和PFOS,用氯化钠/硫酸镁除去水分,C18柱和N-丙基乙二胺吸附剂除去糖类物质,蜂蜜中20种全氟化合物的提取在16 min内即可完成,简化了前处理流程,缩短了分析时间。该法设备简单、溶剂使用量少,操作简单、重现性好、回收率高等优点,为复杂样品尤其是食品样品中PFOA和PFOS的前处理提供了新的思路。但是对于含水量低或者脂肪含量高的样品,净化效果不理想,提取效率低、净化过程损失较大。
3 检测方法
由于样品基质复杂,干扰物多,即使经过前处理,还是需要具有分离功能的仪器进行定量检测。目前,主要有气相色谱法(GC)、液相色谱法(LC)、气相色谱质谱法(GC-MS)和液相色谱质谱法(LC-MS)。
3.1 色谱法
PFOS是全氟化化合物,沸点260℃,较难衍生,气相色谱法不能实现定量测定;且没有紫外吸收基团和荧光基团,常用的液相色谱紫外法和液相色谱荧光法也不能实现定量测定。PFOA也是全氟化合物,沸点189℃,末端具有羧基。因此,通过衍生化,可以利用气相色谱法和液相色谱法实现定量测定。但是,衍生化过程步骤多,繁琐,且样品损失大,测定结果不准确,报道较少。
GC法的衍生方法有酰化反应和酯化反应,衍生过程中更易产生有毒气体,应用上受到一定程度的限制[13]。Yang等[30]将血清冷冻干燥以后先用乙酰氯将PFOA衍生成酯以后采用电子捕获测器(Electron Capture Detector,ECD)检测器测定。Kudo等[31]人用重氮甲烷将PFOA甲酯化,然后用GC-ECD对小鼠肝组织中的PFOA进行了测定;夏静芬等[32]使用2,4-氟苯胺为衍生剂,N,N′-二环己基碳二亚胺为脱水剂,9种全氟羧酸均可发生衍生反应生成酰胺衍生物,据此建立了柱前衍生-GC-ECD法同时测定水中9种全氟羧酸,检出限为0.62~1.38 μg/L。
HPLC的衍生主要是在紫外基团。单国强等[33]选用3,4-二氯苯胺为衍生化试剂,通过碳二亚胺合成法,将PFOA转化为酰胺化衍生物,用LC-UV进行定性和定量分析。黄可等[34]采用苄胺作为紫外衍生剂建立了柱前紫外衍生的HPLC-UV法检测纺织品中的PFOA,浓度范围为6.67 μg/L ~ 0.974 mg/L,回收率为82.15%~120.77%。程小艳[35]探讨了采用w-苯溴乙酮作为紫外衍生剂,建立了柱前紫外衍生的HPLC-UV法,检测水体和尿液中PFOA,浓度范围为0.007 mg/L~ 60 mg/L,水样和尿样的回收率分别为92.7%~107.1%和85.3%~116.0%。黄永周等[36]选择3-BrAC丙酮溶液作为衍生试剂,四丁基溴化铵作为催化剂,用于垃圾渗滤液中PFOA的测定,检出限为0.007 mg/L,加标回收率为86%~95.8%。
3.2 色谱质谱联用法
与紫外、荧光、ECD等检测器相比,质谱的灵敏度高,可以进行定性和定量分析,有效解决同系物共存的问题。色谱质谱联用技术是目前分析实验室的检测PFOA和PFOS的首选方法。
3.2.1GC-MS
PFOS和PFOA的挥发性低,使用GC-MS法测定时,还是需要进行衍生,因此应用并不广泛,主要报道依旧集中在PFOA的检测。Chu等[37]利用固相萃取法有效地从复杂样品中分离出PFOS,再利用四丁基氢氧化铵(TBAH)通过原位热解烷基化反应对PFOS衍生化,GC-MS法检测到PFOS,检出限为0.09~0.46 ng/g。Monteleone等[38]采用固相萃取法提取,全氟羧酸衍生化,GC-MS检测PFOA,检出限和定量限分别为0.11 ng/L和0.24 ng/L。张书驰等[39]采用GC-MS法检测防油纸中PFOA的残留以及迁移量,以盐酸/甲醇为衍生化试剂,衍生温度为60℃,衍生时间为60 min,采用内标法进行定量。这种方法可以用于测定包装材料中的PFOA残留。
3.2.2HPLC-MS
HPLC-MS不需要对PFOA和PFOS进行衍生,可以直接检测。Ericson等[40]采用HPLC-MS内标法进行定量定量测定自来水中的PFOS和PFOA分别在0.39~0.87 ng/L和0.32~6.28 ng/L范围内;江水中PFOS和PFOA的浓度分别小于0.24~5.88 ng/L和0.22~24.9 ng/L。赵逸松等[41]建立了HPLC-MS测定血清中的PFOS的方法。样品经固相萃取后,进行电喷雾质谱分析,结果显示在线性范围0~120μg/L内,回收率为76.88%。方祥光等[42]采用HPLC-MS/MS法分析检测我国10个城市的大气颗粒物中的PFOS和PFOA。杨文龙等[24]建立了HPLC-MS/MS技术测定环境水体与土壤中的PFOA和PFOS。此外,孔蓉等[43]通过LC-MS/MS法测定QT脂质体注射液用镀膜胶塞中PFOS和PFOA的迁移,采用Symmetry C18(150 mm×3.0 mm,5μm),以0.01 mol/mL乙酸铵-乙腈(55∶45)为流动相,采用电喷雾离子源(ESI)、负离子模式检测方式进行定量分析。结果显示,QT脂质体注射液用镀膜胶塞中PFOS和 PFOA在8~200 ng/mL范围内线性良好,最低检测限分别为2.000、2.074 ng/mL,平均回收率分别为103.7%、105.9%,RSD分别为7.2%、7.5%,HPLC-MS/MS法是文献报道最多的检测PFOS和PFOA的方法,突出的优点是能提供比单级更详细MS的结构信息,定性更加准确,选择性好、灵敏度高[13]。
3.3 其他
光谱法、酶联免疫法、电化学等传统的分析方法也可以用于PFOA和PFOS的分析,然而更值得关注的是近年来基于这些原理发展的快检方法。Kong等[44]提出了巯基聚苯乙烯修饰的金纳米粒子(AuPS)比色检测PFOA,通过肉眼可观察到AuPS溶液的颜色从红色变为蓝紫色,实现快速检测。Chen等[45]报道了分子印迹修饰的超薄石墨氮化碳纳米片作为探针电化学传感器检测PFOA,在0.02~ 40.0 ng/mL和50.0~400.0 ng/mL浓度范围内,检出限为0.01 ng/mL,用于水样中PFOA的检测,方便快速。但是快检方法的定量能力还有待提升,应用并不广泛。
4 总结与展望
目前,PFOA和PFOS的检测对象主要是土壤、水、食品(及包装材料)和生物样品,分析测试中首选方法是固相萃取技术结合LC-MS分析,可以去除基质中的干扰物,高效富集PFOA和PFOS,直接实现定性定量检测。方法成熟、灵敏度高、适用范围广。基于光谱、电化学的快检技术也有一定程度的发展,现阶段直接用于实际样品的定量检测还有技术瓶颈尚未突破,这也是未来研究的重点方向。
——以离子色谱法测定冬瓜中亚硝酸盐含量为例

