荧光金属有机骨架材料在离子检测中的应用*
张爱琴,郭 斌,柳利龙
(1 甘肃省农业科学院畜草与绿色农业研究所,甘肃 兰州 730070;2 甘肃省农业科学院农业质量标准与检测技术研究所,甘肃 兰州 730070)
1 荧光金属有机骨架材料的发光机理
荧光MOFs自身具有丰富的发光中心,其发光来源可分为金属离子发光、配体发光、电荷转移发光及客体分子诱导发光等[5]。金属离子发光主要是通过“天线效应”敏化镧系金属离子发光。配体发光是指具有π共轭体系的有机配体在适当波长的激发光激发下,电子从基态跃迁到单重激发态,当电子从激发态回到基态时释放出的能量即为有机配体发出的荧光。电荷转移主要包括金属离子向配体电荷转移(MLCT),配体向金属离子电荷转移(LMCT)和配体到配体的电荷转移(LLCT)三种[6],经常出现在d10过渡金属MOFs中。客体分子诱导发光是基于MOFs材料具有多孔的特点,向其中引入具有发光性质的物质,如稀土金属离子[3]、量子点[7]、荧光染料试剂[8]等。
2 荧光金属有机骨架材料的合成
MOFs的合成一般是在液相体系中进行的,合成方法众多,关键是要合理选取有机配体和金属离子,探索合适的反应条件,合成荧光性能卓越的MOFs。可通过向MOFs中引入功能性官能团来增强其荧光性能从而达到特异性识别的目的[9],但是常见的水热/溶剂热法在合成过程受很多因素的影响,使得直接向MOFs中引入功能性官能团受到阻挠。后合成修饰(PSM)法为构筑荧光MOFs提供了一种新的策略。许多有机官能团,如胺类、亚胺类和叠氮类等,以及镧系金属离子都可以通过PSM法引入到MOFs孔道中,从而调节MOFs的荧光性能,增强MOFs的荧光传感性能[10]。此外,也可通过利用π共轭有机配体制备荧光MOFs传感材料。
3 荧光金属有机骨架材料用于离子检测
3.1 金属阳离子检测
3.1.1 重金属离子
Hg2+是毒性和危害性最大的元素之一,而且汞被细菌甲基化后形成具有神经毒性的甲基汞,从而引发致命性疾病,因此,美国国家环境保护局(US EPA)规定饮用水中Hg2+的最高含量不得超过10 nmol/L。但是大部分基于MOFs的Hg2+荧光传感器的检测限高于10 nmol/L,只有少数MOFs的检测限低于US EPA规定的限量值[11-13]。由于Hg2+与氮原子有较高的亲和力,因此检测Hg2+的荧光MOFs大部分含有氮原子位点[11,13],也有少数MOFs是基于氧原子或硫原子位点的[14-15]。Asha等[11]制备了一种超灵敏检测Hg2+的金属有机骨架{[Zn(4,4′-AP)(5-AIA)]·(DMF)0.5}n(Zn-MOF,4,4′-AP=4,4′-偶氮吡啶,5-AIA=5-氨基间苯二甲酸,DMF=N,N′-二甲基甲酰胺),检测限低至9.9×10-3nmol/L。Zn-MOF在405 nm处有一个荧光发射,可将其归因于配体5-AIA的电子跃迁。向Zn-MOF水溶液中加入Hg2+,Hg2+与Zn-MOF孔道中-N=N-相互作用,电子从偶氮基团向Hg2+转移,扰乱了Zn-MOF的电子共轭体系,从而引发荧光猝灭,荧光猝灭常数KSV为1.011×109M-1。Zn-MOF能够高灵敏度和高选择性地识别Hg2+,对其它金属离子具有良好的抗干扰能力。也有个别荧光MOFs对Hg2+的检测是基于骨架坍塌机理[12]。
Cr3+虽是一种人体必需的生物元素,在人体新陈代谢方面起着重要的作用。但是过量的Cr3+会与DNA结合,导致细胞突变或恶性肿瘤。近年来一些对Cr3+有荧光识别性能的MOFs荧光传感器被报道。但是由于Cr3+的顺磁特性,大部分MOFs检测Cr3+都是基于荧光猝灭效应,通过荧光增强检测Cr3+的MOFs并不多。Lv等[16]报道了turn-on型检测Cr3+的金属有机骨架[Zn2(TPOM)(NH2-BDC)2]·4H2O(NH2-Zn-MOF,NH2-BDC=2-氨基对苯二甲酸,TPOM=四(4-吡啶氧亚甲基)甲烷),检测限为4.9 μmol/L。NH2-Zn-MOF中没有配位的羧基氧原子和氨基氮原子与Cr3+螯合,形成一个新的六元环,共轭平面变大,使π电子更容易被激发,从而导致荧光强度增加。然而基于对苯二甲酸的Zn-MOF(与NH2-Zn-MOF同构)的荧光实验结果表明,Cr3+几乎对Zn-MOF荧光强度没有影响,说明氨基基团在Cr3+识别过程中起着重要作用。
荧光MOFs作为荧光传感器,也可以检测Cd2+和Pb2+等重金属离子[17-18]。Xu等[17]用一步溶剂热法制备了金属有机骨架材料Uio-66-NH2-Eu(Uio-66-NH2=Zr6O4(OH)4(BDC-NH2)6)。由于配体对Eu3+的敏化作用,Uio-66-NH2-Eu展现出Eu3+的特征荧光发射峰580,593,617,651,700 nm,对应于5D0-7Fj(J=0-4)电子跃迁,同时Uio-66-NH2-Eu还在468 nm处展示出较宽的Uio-66-NH2发射。向Uio-66-NH2-Eu悬浊液中加入0.01 mol/L Cd2+,Uio-66-NH2-Eu荧光显著增强,在几分钟内荧光强度就增长至原来的13倍,在紫外灯照射下,溶液从蓝色变为红色。在0.22~500 μmol/L浓度范围内,Uio-66-NH2-Eu荧光强度随着Cd2+浓度升高而线性增强,响应时间小于5 min。这是由于Cd2+可与MOFs中氨基氮原子相互作用,改变了配体的电荷密度,进而影响了电荷跃迁,导致Uio-66-NH2-Eu荧光增强,实现了Cd2+turn-on型检测。
3.1.2 微量金属离子
Fe3+作为生物体不可缺少的元素之一,浓度过高或过低都会引起生理失调甚至诱发癌症[2]。Luo等[1]报道了Pb3O2L(H2L=4-羟基苯基-1H-四唑)对Fe3+的检测。Pb3O2L的水溶液在320 nm处有强的荧光发射峰,加入Fe3+后,Fe3+与四氮唑环相互作用,Pb3O2L向Fe3+的电子转移和共振能量转移共同导致荧光猝灭。利用Pb3O2L制备了能够快速检测Fe3的荧光检测板,将Fe3+滴加到检测板上,在紫外灯照射下,检测板的颜色由白色变为黑色,这种颜色变化用肉眼很容易识别。Wu等[2]报道了了[Tb(HMDIA)(H2O)3]·H2O(Tb-MDIA,H4MDIA=5,5’-亚甲基二间苯二甲酸)对Fe3+的turn-off 型识别,即使在Cr3+,Al3+,Cu2+等金属离子存在的情况下,Tb-MDIA依然对Fe3+有高的选择性。
碳量子点(CQDs)具有优越的光学性能,可以装载到MOFs的孔道中,扩展MOFs在荧光化学传感器领域的应用。Fan等[7]报道一种检测Cu2+的CQDs/MOFs(MOFs=Zn4O(NH2-BDC)3,NH2-BDC=2-氨基对苯二甲酸)。通过CQDs的羟基与MOFs中2-NH2BDC的氨基之间的氢键作用将CQDs引入到MOFs中形成CQDs/MOFs。羟基作为给电子基团可以增强苯环的共轭效应,因此2-NH2BDC在460 nm处有荧光发射峰。形成Zn-MOFs后,Zn与羟基配位,使π电子的共轭效应减弱,导致荧光强度下降。引入CQDs 后,由于CQDs与MOFs之间的氢键提高了π电子的共轭效应,因此CQDs/MOFs的发光强度高于Zn-MOFs。加入Cu2+后,Cu2+与N原子配位,由于金属离子与有机配体N原子的配位作用强于氢键,使CQDs与MOFs分离,导致CQDs/MOFs荧光猝灭。其它金属离子对CQDs/MOFs荧光强度的影响极小,因此CQDs/MOFs作为一种“on-off”荧光传感器可选择性检测Cu2+。由于CQDs/MOFs具有低毒性,因此可用细胞内Cu2+的识别。有时,由于Co2+,Ni2+,Fe2+和Fe3+等3d金属离子的外层电子处于不饱和状态,可作为电子的接受体,干扰MOFs对Cu2+选择性识别,含有吡啶基或氰基的MOFs对Cu2+有高的选择性,可以有效避免其它3d金属离子的干扰[6]。
3.1.3 其它金属离子
基于MOFs的荧光传感器也被用于检测Al3+和Ag+离子[3,19]。聚集诱导发光(AIE)材料具有抗聚集荧光猝灭(ACQ)现象,将具有AIE性质的有机配体引入到金属有机骨架中,配体中分子的旋转或振动受到抑制,减少了非辐射跃迁引起的能量损失,发光增强。Li等[19]用羟基功能化有机配体HTABDC和Zn2+合成了具有AIE效应的金属有机骨架Zn(HTABDC)(DMF)2(MOF 1,HTABDC=4,4’-((Z, Z)-1,4-二苯基丁-1,3-二烯-1,4-二基)二(2-羟基苯甲酸))。然后通过引入辅助配体4,4’-联吡啶(Bpy)合成了Zn(HTABDC)(Bpy)·DMF(MOF 2),MOF 2可实现Al3+的turn on型检测。光谱分析表明,有机配体HTABDC具有AIE性质,在474 nm处有强的荧光发射峰,绝对量子产率是17%。MOF 1的最强荧光发射峰位于457 nm处,量子产率为50%。然而MOF 2几乎没有荧光发射,量子产率降至0.99%。研究表明,在MOF 1中,HTABDC通过配位键密集堆积在金属有机骨架中,有机配体的苯环旋转受到限制,非辐射能量减少,MOF 1的荧光强度和量子产率都增加。引入辅助配体Bpy,由于HTABDC到Bpy光诱导电子转移(PET),使MOF 2发生荧光猝灭效应。向MOF 2中加入Al3+,Al3+通过羧基和去质子化的酚羟基与HTABDC螯合,形成HTABDC-Al3+化合物,Bpy被释放到溶液中,MOF 2分解,使HTABDC到Bpy的PET过程消失,HTABDC的AIE性质恢复,溶液的荧光强度增加,检测限为3.73 ng/mL。
3.2 阴离子检测
3.2.1 含氧酸根阴离子
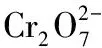
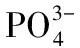
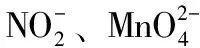
3.2.2 卤素阴离子
硼酸基团中的硼原子是缺电子的,硼原子与F-有较强的亲和力,可以作为F-的识别位点。Ebrahim等[28]制备了[Eu(tctb)(H2O)]·2DMF(SION-105,H3tctb=三(对羧酸)三十二烷基硼),SION-105呈现出螺旋桨式的结构,硼原子位于螺旋桨中心,硼原子周围的四甲苯基产生的空间位阻使得B…F相互作用在本质上属于静电作用,弱的静电作用使SION-105在识别F-后具有良好的稳定性和优秀的再生性能。SION-105展现出Eu3+的特征荧光发射,加入F-,由于F-和配体tctb3-B之间的静电作用,形成非辐射衰减通道,导致Eu3+荧光明显猝灭。硼酸也可被用于调控镧系MOFs的发光性能以实现F-的比率型检测。Yang等[29]用5-硼间苯二甲酸(5-bop)和Eu3+制备了一种检测F-的硼酸功能化镧系金属有机骨架Eu-MOF。研究表明,硼酸基团的存在改变了间苯二甲酸(isp)的能量水平,使Eu-MOF中同时存在配体5-bop自身的发光(366 nm)和Eu3+(590~750 nm)的特征荧光发射。当加入F-,366 nm处的配体发光增强,而625 nm Eu3+的发光强度减弱。有机配体5-bop中硼原子拥有pπ空轨道,F-与硼原子共价结合后,阻断了硼与芳香基团间的共轭作用,减小了配体5-bop的系间窜越效率,使得5-bop的荧光增强而Eu3+的特征发射由于天线效应的影响而减弱。
3.2.3 氰根阴离子
金属有机骨架具有可调节的孔道,可以作为荧光染料等客体分子的装载平台,通过引入功能性客体分子,可以扩展MOFs在荧光检测领域的应用。Karmakar等[8]通过离子交换将阳离子染料DAAC(3,6-二氨基吖啶阳离子)成功引入到稳定性高的阴离子骨架[Zn8(ad)4(BPDC)6O·2Me2NH2]·G(bio-MOF-1,G=DMF和H2O,BPDC=联苯二羧酸,ad=腺嘌呤)孔道中形成bio-MOF-1⊃DAAC。由于聚集荧光猝灭效应,bio-MOF-1⊃DAAC发射出微弱的荧光。加入CN后,CN-与DAAC染料分子中的亲电位置(C9位置)发生Michael加成反应形成共价键,阳离子染料DAAC变为中性分子,从孔道中释放出来进入溶液中,中性DAAC在液相体系中具有很强的荧光性质。在CN-存在的情况下,bio-MOF-1⊃DAAC荧光强度增加了近16倍,从而实现了CN-的turn-on型检测,检测限为5.2 ng/mL。MCF-7(人体乳腺癌细胞)细胞的体外实验研究表明,bio-MOF-1⊃DAAC甚至可以定量检测细胞质内微量CN-。
4 结 语
荧光MOFs是一类优秀的离子检测材料,具有响应时间短、选择性和灵敏度高的优点。本文主要综述了近几年荧光MOFs在金属阳离子和阴离子检测领域的应用进展,并总结了LMOFs发光机理和离子识别机制。利用荧光MOFs的孔道结构和功能化活性位点,将荧光染料、聚集诱导发光材料和量子点等材料结合,创造出检测性能卓越的荧光传感器也引起了科研工作者的关注。由于阴离子的反应活性低,反应位点少,故利用荧光MOFs特异性检测阴离子的报道并不多。尽管基于MOFs的荧光传感器在离子识别领域已经取得了很大的进展,但依然面临很多挑战,大多数荧光MOFs检测离子的过程都是turn-off型,为了提高离子检测的灵敏度和精确度,应该深入探索turn-on型和比率型荧光MOFs的设计及合成方法。离子的检测基本都是在液相中进行的,荧光MOFs的稳定性差会导致检测的结果误差大,因此在提高荧光MOFs的水稳定性方面依然需要深入的研究。纳米荧光MOFs由于粒径超细,水分散型好,可以用于细胞内离子的检测,但目前纳米荧光MOFs的研究还处于初始阶段。随着荧光MOFs研究的深入,稳定灵敏的、选择性高、尺寸可控的MOFs荧光传感器将会有更广阔的应用前景。

