藻蓝色素稳定性的研究
任顺成,王凤雯,曹 悦,李林政,潘天义
1.河南工业大学 河南省天然色素制备重点实验室,河南 郑州 450001 2.河南中大恒源生物科技股份有限公司,河南 漯河 462600
藻蓝色素是一种天然的具有光捕获功能的水溶性色素蛋白,不仅可以被当作天然着色剂应用到食品[1]和美容化妆品中[2],而且因其特殊的营养特性以及生化特性还被广泛应用到医疗保健(抗氧化[3]、抗肿瘤[4]、抗动脉粥样硬化[5]和保护肾脏和肝脏的作用[6])以及生化领域(荧光探针[7]、光敏剂[8])中,发展前景非常广阔。
藻蓝色素是由脱辅基蛋白(apoprotein)和线性四吡咯化合物藻蓝胆素PCB(phycocyanobilin)通过一个或两个硫醚键共价连接而成的色素蛋白复合物[9],广泛存在于蓝藻中。它能够吸收550~630 nm的光,最大吸收波长为610~620 nm[10],分子质量为44~260 kDa。藻蓝色素的两个基本构成单元分别为α亚基(2个半胱氨酸和2个甲硫氨酸残基,12~19 kDa)和β亚基(3个半胱氨酸和5个甲硫氨酸残基,14~21 kDa)[11],每种亚基都含有160~180个氨基酸序列[12]。藻蓝色素的α、β亚基易集聚成二聚体αβ单体,αβ单体进一步聚集形成环状三聚体(αβ)3,两个三聚体再组装成六聚体圆盘((αβ)3)2。六聚体为藻蓝色素的主要形式,直径为11 nm[13]。
藻蓝色素中的藻蓝胆素与载脂蛋白结合后,将被迫伸展构象。藻蓝胆素和蛋白质形成的扩展双键系统将引起特征光谱变化。如果发色团和蛋白质之间的稳定键丢失,那么发色团将会重新排列成在能量上有利的环状构象[14]。因藻蓝色素特殊的色素蛋白复合结构,容易受到周围基质的影响而不稳定,由此造成它的使用范围受到了很大的限制[15]。藻蓝色素的降解取决于蛋白质的聚集状态,该状态受光、温度、pH值和蛋白质浓度等参数的影响[16]。梁霄等[17]得出藻蓝色素在pH 6.0~7.0、 4~30 ℃、避光条件下相对稳定。Wu等[18]研究发现藻蓝色素在100 μmol·m-2·s-1光照强度下比50 μmol·m-2·s-1有着更大的降解率。Zhang等[19]通过向藻蓝色素溶液中添加乳清蛋白,发现乳清蛋白比豌豆蛋白在藻蓝溶液pH 3.0时更能有效地防止聚集现象的产生。Braga等[20]通过向藻蓝色素中掺入纳米纤维并测定其降解速率常数和半衰期,发现其在55~75 ℃条件下热稳定性得到提高。关于藻蓝色素稳定性的系统研究,特别是在添加多种金属离子以及多酚条件下的稳定性研究鲜有报道。因此,作者通过研究藻蓝色素在不同pH值、温度、光照条件下的稳定性,不同浓度的糖、抗氧化剂、金属离子、十二烷基硫酸钠(SDS)以及不同种类的多酚对藻蓝色素稳定性的影响,以期为进一步改善藻蓝色素的稳定性提供一定的理论参考。
1 材料与方法
1.1 材料与试剂
藻蓝色素:河南中大恒源生物科技股份有限公司;单宁酸、没食子酸、绿原酸、儿茶素(纯度均>96%):南京龙源天然多酚合成厂;迷迭香酸(纯度>96%):上海源叶生物有限公司;其他试剂均为分析纯。
1.2 仪器与设备
PHS-3C型酸度计:上海仪电科学仪器股份有限公司;TDL-5A型离心机:济南赛信机械有限公司;WSC-S型色差仪:上海仪电物理光学仪器有限公司;UV-6000PC型紫外可见分光光度计:上海元析仪器有限公司。
1.3 方法
1.3.1 pH值对藻蓝色素稳定性的影响
分别使用柠檬酸和柠檬酸钠、碳酸钠和碳酸氢钠配置成pH 2.5、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0的缓冲溶液。称取9份藻蓝色素分别溶于不同pH值的缓冲溶液中,使其质量分数均为0.05%。之后进行全波长扫描[16]和色差分析[19],观察其特征峰以及L*、a*、b*值的变化。全扫描波长范围200~800 nm,在色差分析测量前使用校准白板进行色度校准,定量称取所测样品进行色差L*、a*、b*值测定,3次平行。
1.3.2 温度对藻蓝色素稳定性的影响
配制7份质量分数为0.05%的藻蓝色素溶液,置于温度分别为4、25、35、45、55、65、75 ℃的水浴锅中进行稳定性试验,测其A620 nm,每隔0.5 h测量1次,一共测8次,3次平行,根据下式计算保存率。
1.3.3 光照对藻蓝色素稳定性的影响
用蒸馏水配制4份质量分数为0.05%的藻蓝溶液,分别置于室外强光、室内强光、室内弱光、避光条件下进行光照稳定性试验,测其A620 nm,每隔1 h测定1次,共测6次,3次平行,计算保存率。
1.3.4 糖对藻蓝色素稳定性影响
配制质量分数为0.05%藻蓝色素溶液以及质量分数均分别为0、2%、4%、6%、8%、10%的葡萄糖溶液、蔗糖溶液、果糖溶液。分别依次吸取5 mL藻蓝溶液和5 mL不同质量分数的葡萄糖溶液、蔗糖溶液以及果糖溶液进行混合、摇匀、静置,每隔24 h进行A620 nm测定,测定3次,计算保存率。
1.3.5 金属离子对藻蓝色素稳定性的影响
配制质量分数为0.05%藻蓝色素溶液以及质量分数均分别为0、2%、4%、6%、8%、10%的氯化钠、氯化钾、硫酸铵、硫酸钠、氯化钙、硫酸镁、硫酸铜溶液,分别依次吸取5 mL藻蓝溶液和5 mL不同质量分数的氯化钠、氯化钾、硫酸铵、硫酸钠、氯化钙、硫酸镁、硫酸铜溶液,测定A620 nm,计算保存率。
1.3.6 抗氧化剂对藻蓝色素稳定性的影响
配制质量分数为0.05%的藻蓝色素溶液以及质量分数均分别为0、2%、4%、6%、8%、10%的抗坏血酸、柠檬酸溶液,分别依次吸取5 mL藻蓝溶液和5 mL不同质量分数的抗坏血酸、柠檬酸溶液,测定A620 nm,计算保存率。
1.3.7 pH 2.5条件下SDS对藻蓝色素稳定性的影响
准确称取8份藻蓝色素,溶于pH 2.5的柠檬酸钠缓冲液使其质量分数均为0.05%,再依次添加SDS,使其在溶液中质量分数分别为0.01%、0.02%、0.04%、0.06%、0.08%、0.10%、0.20%、0.40%,之后进行全波长扫描和色差分析。
1.3.8 pH 2.5条件下多酚对藻蓝色素稳定性的影响
准确称取5份藻蓝色素,溶于pH 2.5的柠檬酸钠缓冲液使其质量分数均为0.05%,再依次分别添加单宁酸、迷迭香酸、没食子酸、绿原酸、儿茶素,使其在藻蓝溶液中质量分数均为0.01%,之后进行全波长扫描和色差分析。
1.3.9 统计分析
使用SPSS 22统计软件分析所有数据, 结果表示为平均值±标准偏差(n=3)。P<0.05表示具有显著差异。
2 结果与分析
2.1 pH值对藻蓝色素稳定性的影响
由图1a可知,藻蓝色素除620 nm处的特征吸收峰外,还有280 nm、350 nm处的吸收峰,分别对应芳香族氨基酸、藻蓝胆素。溶液pH<3.0时,在可见光区出现了两个峰,并向长波长方向移动;pH>3.0时,只有一个最大吸收峰,并且峰的强度随着pH值增高先增大后减小;在pH 5.0、6.0时有着比较高的峰值。而在紫外光区的最大吸收峰强度则正好和可见光区相反。在图1b中,Avis/Auv为可见光区最大吸收峰强度值与紫外光区最大吸收峰强度之比。(Avis/Auv)>1时,发色团为伸展的构象;(Avis/Auv)<1时,发色团为卷曲的构象[21]。由图1b可知,藻蓝色素的Avis/Auv在pH 2.5、3.0时在1附近,而后随着pH值的增加Avis/Auv先增大后变小,在pH 6.0时达到最大值。蛋白质所处溶液pH值偏酸或偏碱,都会造成蛋白质一定程度的变性,因而会对蛋白发色团结构产生一定的影响。当结构受到破坏时,发色团虽然还结合在蛋白质上,但它是一种更倾向于卷曲或更折叠的构象,而天然藻蓝色素发色团的构象则是一种更加伸展的构象。发色团构象的变化会引起π电子系统形状不同,从而会产生不同的吸收光谱。如图1c所示,在pH 6.0时b*值最低,说明藻蓝色素溶液在此pH值下蓝色最深;在pH<6.0时,溶液的L*值随着pH值的降低而增大,说明在偏酸时,溶液的颜色更亮,a*值和b*值也都随着pH值的降低而增大,说明藻蓝色素在偏酸环境中更趋于绿色;pH>6.0时,溶液的L*值随着pH值的增大也增大,说明藻蓝色素溶液在偏碱时更亮,a*值和b*值随着pH值的增大也增大,说明偏碱环境不利于藻蓝色素蓝色的呈现。藻蓝色素在不同pH值条件下的实物图如图1d所示,在pH 2.5、3.0时,藻蓝色素不仅由蓝色变为绿色,而且还有沉淀生成,在偏碱环境下,也出现了不同程度的褪色。因此,藻蓝色素应在pH 4.0~7.0条件下保存。
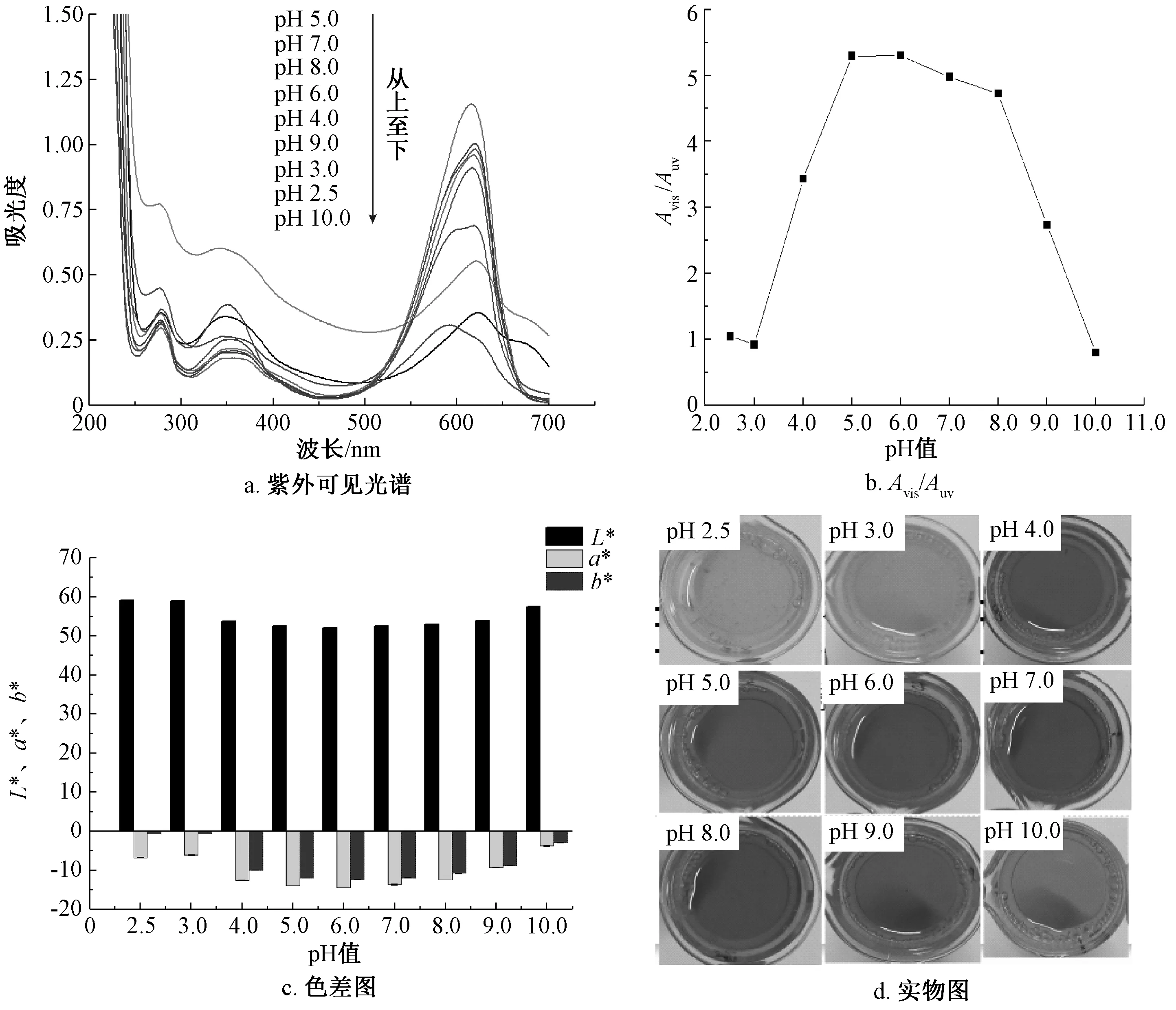
图1 pH值对藻蓝色素稳定性的影响Fig.1 Effect of pH on the stability of phycocyanin
2.2 温度对藻蓝色素稳定性的影响
由图2可知,藻蓝色素在4~55 ℃时有着较高的保存率,在高于55 ℃后,保存率开始出现明显的降低。高温会导致藻蓝色素中的蛋白质变性而使蛋白质发色团稳定的构象受到破坏,因而保存率下降。因此,藻蓝色素应低温保存。

图2 温度对藻蓝色素稳定性的影响Fig.2 Effect of temperature on the stability of phycocyanin
2.3 光照对藻蓝色素稳定性的影响
由图3可知,在室外强的日晒光照下,藻蓝色素的保存率出现了明显下降,因此,室外强光对藻蓝色素的破坏作用非常大。光照会破坏藻蓝蛋白的结构,从而使与之连接的发色团构象不稳定而造成藻蓝色素的保存率下降。在室内强光、弱光以及避光的条件下,藻蓝色素的保存率相差不大。因此,藻蓝色素应避光保存。

图3 光照对藻蓝色素稳定性的影响Fig.3 Effect of light irradiation on the stability of phycocyanin
2.4 糖类对藻蓝色素稳定性的影响
糖的添加会使藻蓝色素表面张力增加,糖覆盖其表面可以一定程度地维持和保护其化学结构[22]。糖在溶液中容易和水发生水合作用,使溶液的黏性增加,从而降低了晶核的生成速度而保护了藻蓝色素。如图4所示,在72 h时,藻蓝色素在3种糖溶液中的保存率均随糖质量分数的增加先增加而后降低,并分别在6%、4%、6%时达到最大值。由此可知,糖类的添加会对藻蓝色素的保存率有一定的提高作用,但是过高和过低的浓度均对保存率的提高意义不大。葡萄糖、蔗糖、果糖的最佳质量分数分别为6%、4%、6%。

图4 糖类对藻蓝色素稳定性的影响Fig.4 Effect of sugar on the stability of phycocyanin
2.5 金属离子对藻蓝色素稳定性的影响
由表1可知,金属离子除Na2SO4之外其他均出现了沉淀,并且颜色变浅,但添加Na2SO4的藻蓝色素溶液蓝色也会逐渐消失。这是由于金属离子可以与藻蓝色素中的蛋白质发生作用,使其变性,从而出现蛋白质聚集交联的沉淀[23]。

表1 金属离子对藻蓝色素稳定性的影响Table 1 Effect of metal ions on the stability of phycocyanin
2.6 抗氧化剂对藻蓝色素稳定性的影响
由图5可知,随着抗氧化剂质量分数的增加,藻蓝色素的保存率急剧下降,这可能是藻蓝蛋白中的活泼基团如—COOH、—NH2等和抗氧化剂发生了作用,从而导致蛋白质发色团构象被破坏,造成色素保存率下降。

图5 抗氧化剂对藻蓝色素稳定性的影响Fig.5 Effect of antioxidants on the stability of phycocyanin
2.7 在pH 2.5下SDS对藻蓝色素稳定性的影响
由图6a可知,在pH 2.5下空白组的藻蓝溶液最大吸收峰强度明显低于含有SDS的藻蓝溶液,在SDS质量分数为0.20%时出现了最高峰值。最高峰值从高到低对应的SDS的质量分数依次为0.20%、0.10%、0.08%、0.40%、0.06%、0.04%、0.01%、0.02%。在化学变性的条件下,蛋白质发色团结构将会受到影响,致使光谱性质发生变化[24]。
由图6b可知,添加SDS的藻蓝溶液和空白相比,b*值有着很明显的变化,当SDS质量分数<0.06%时,随着质量分数的升高,L*值整体出现降低,a*值则先出现升高而后又降低,b*值则逐渐降低;当SDS质量分数>0.06%时,随着质量分数的升高,L*值先降低之后又升高再降低,a*值先增大而后又减小,b*值趋于平缓。因此,SDS的添加对藻蓝色素在酸性条件下的稳定性有促进作用。b*值的变化非常明显,这可能是在添加SDS之后,藻蓝色素会被包埋在由SDS形成的阴离子胶束中,从而在一定程度上避免了外界的酸性破坏。因此,添加质量分数为0.06%的SDS对提高藻蓝溶液在pH 2.5下的稳定性有积极作用。
2.8 在pH 2.5下多酚对藻蓝色素稳定性的影响
多酚对藻蓝色素的作用,会使其功能结构特性和营养特性发生一定程度的改变[25]。由图7a可知,在添加单宁酸的藻蓝色素溶液全波长扫描分析中,在可见光区只有一个最大吸收峰,且强度最高,这可能与单宁酸和藻蓝色素的结合相对较强有关。其他4种多酚与空白相比峰形没有太大变化。从图7b来看,多酚的添加对提高藻蓝色素溶液在pH 2.5下的稳定性并不显著。分别添加不同多酚的藻蓝色素溶液的L*值基本没有发生明显变化,a*值在儿茶素中出现最低值,b*值在单宁酸中最大,其余则变化不明显。这可能与藻蓝蛋白在偏酸的环境下变性影响了与多酚的络合有关。因此,5种多酚未明显改善藻蓝色素在pH 2.5下的稳定性。
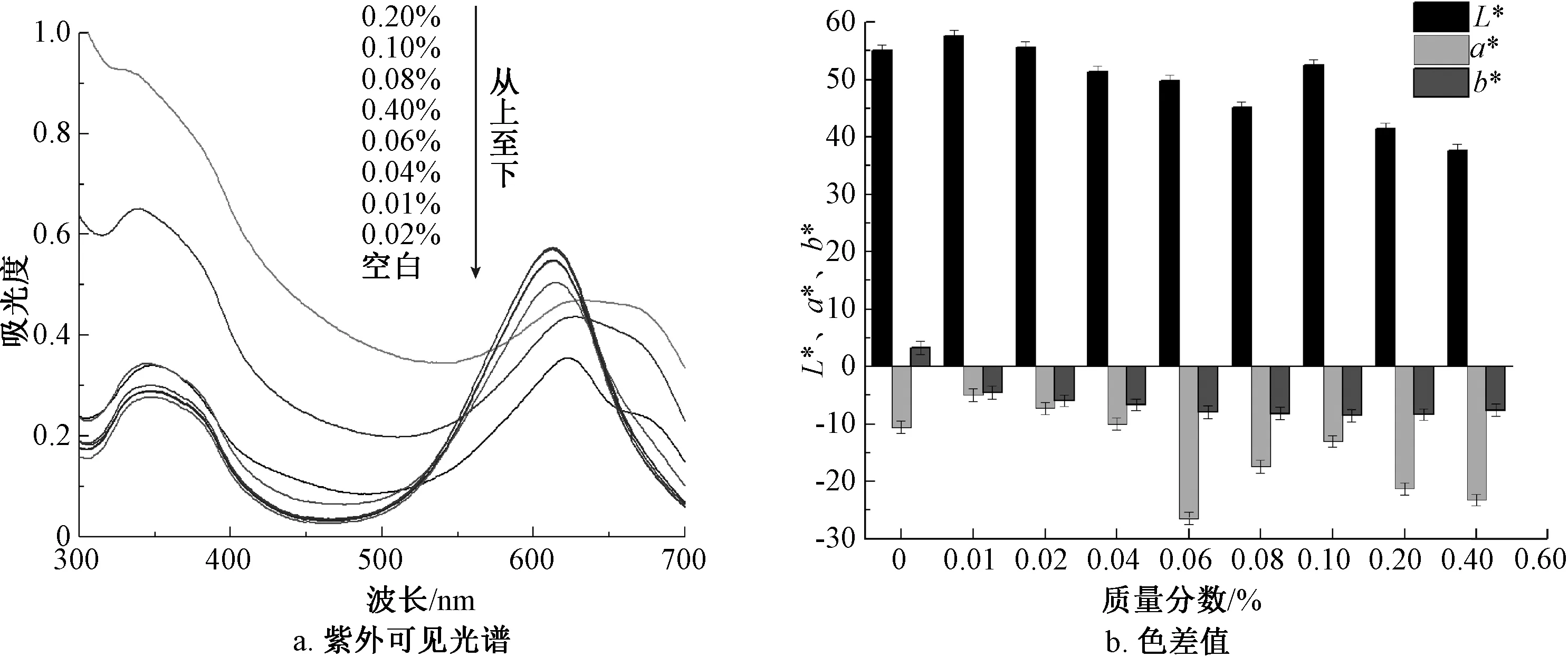
图6 在pH 2.5下SDS对藻蓝色素稳定性的影响Fig.6 Effect of SDS on the stability of phycocyanin at pH 2.5
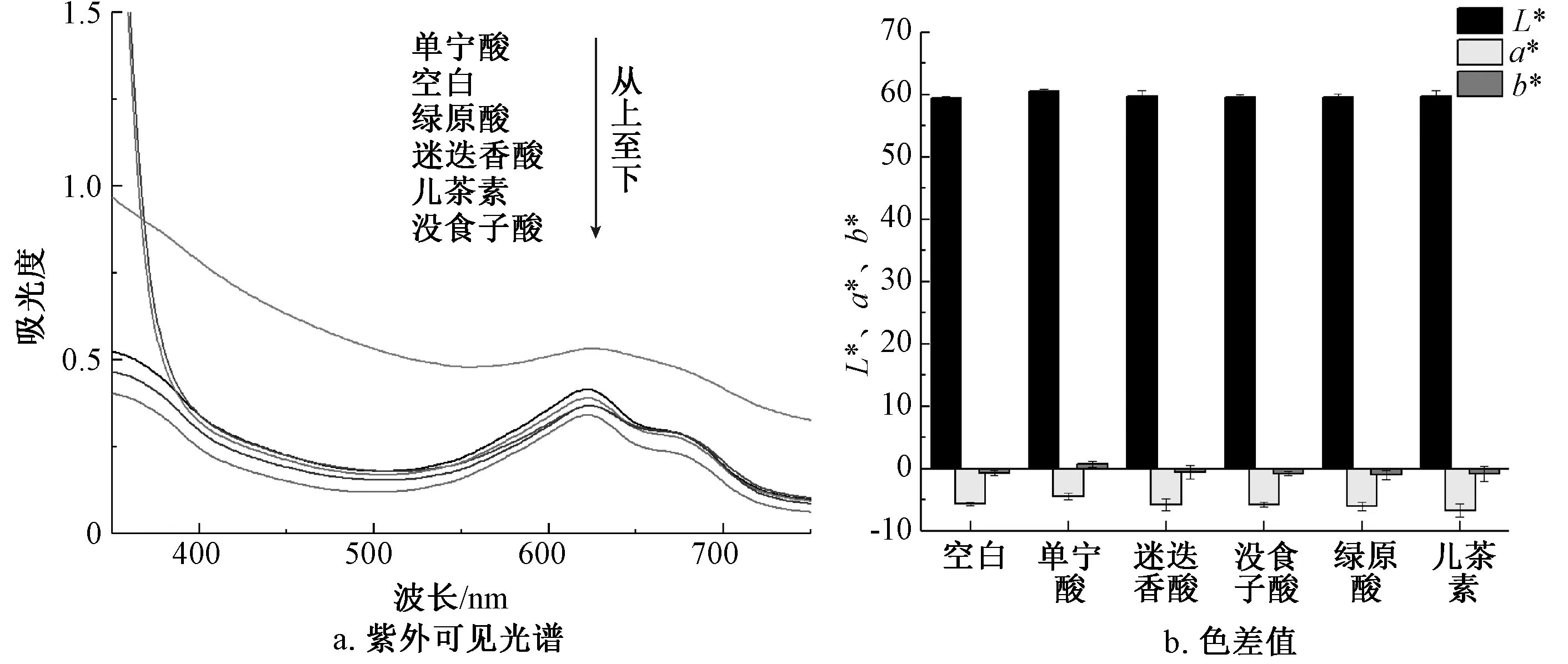
图7 在pH 2.5下多酚对藻蓝色素稳定性的影响Fig.7 Effect of polyphenols on the stability of phycocyanin at pH 2.5
3 结论
藻蓝色素在pH 4.0~7.0时能够使发色团蛋白质构象保持稳定而显示亮蓝色,而在偏酸或偏碱时,蓝色则转变为绿色,且在pH 2.5~3.0产生沉淀。温度低于55 ℃以及避光保存时,色素保存率比较高。添加质量分数分别为4%、6%、6%的蔗糖、葡萄糖、果糖对藻蓝色素在常温下的稳定性有促进作用。氯化钠、氯化钾、硫酸铵、氯化钙、硫酸镁、硫酸铜溶液均会使藻蓝色素溶液产生沉淀,硫酸钠虽不会使藻蓝色素溶液产生沉淀,但会使藻蓝溶液蓝色完全丧失。抗坏血酸、柠檬酸均会使藻蓝色素保存率下降。质量分数为0.06%的SDS能显著提高藻蓝溶液在pH 2.5下的稳定性,且藻蓝色素溶液无沉淀生成。5种多酚的添加没有明显改善藻蓝色素溶液在pH 2.5下的稳定性。

