湿法解毒技术对铬渣污染土壤的修复效果研究
周斌*,石燕,邵煜锟,杨流,刘子琳,葛一陈
(永清环保股份有限公司,长沙 410330)
自20 世纪50 年代起,我国陆续建设了70 余家重铬酸钠化工企业,由于当时生产工艺落后,生产每吨铬盐产品要排放2.5 t 甚至3t 高毒性铬渣,铬渣的无序堆存以及不正确处置造成铬盐生产场地土壤受到严重污染[1]。铬渣中Cr(Ⅵ) 的存在形式主要有易溶的四水铬酸钠,稍溶的铬酸钙,微溶的铬铝酸钙、碱式铬酸铁、化学吸附的Cr(Ⅵ),难溶的硅酸二钙-铬酸钙固溶体、铁铝酸钙-铬酸钙固溶体[2]。以固溶体形式存在于硅酸二钙、铁铝酸钙晶格内的Cr(Ⅵ),需要强酸破坏晶格后才能溶出。因此,常规还原稳定化技术无法有效处理铬渣混合污染土壤。
湿法解毒是将铬渣磨细浸解,酸溶性和水溶性的Cr(Ⅵ)在还原剂的作用下被还原成Cr(Ⅲ)。我国早在20世纪60年代就开始了铬渣综合治理的研究工作,已形成的湿法解毒方法包括无钙铬渣湿法解毒和硫酸亚铁湿法解毒等[3]。张淑玲等[4]利用硫酸亚铁湿法解毒工艺处理河南新密铬渣,规模化运行处理后的铬渣可完全达到一般工业固废填埋标准的控制要求。刘曦[5]用硫酸亚铁解毒无钙焙烧铬渣经水选分离后的细渣,确定较佳工艺条件为加入理论量180%的FeSO4,不加酸,反应温度50℃,处理时间2h,在此条件下解毒后的总Cr 和Cr(Ⅵ)浸出浓度均小于0.5mg/L。Wangxin 等[6]采用FeSO4和H2SO4处理铬渣,养护400d后,Cr(Ⅵ)浸出浓度满足《铬渣污染治理环境保护技术规范(暂行)》(HJ/T 301—2007)的要求,即Cr(Ⅵ)浸出浓度<1.5mg/L,说明采用FeSO4-H2SO4湿法解毒铬渣具有较好的稳定性。朱文会等[7]以我国某铬盐厂的铬渣污染土壤为研究对象,探讨了淋洗、稳定化、湿法解毒3 种异位修复工艺去除铬渣污染土壤中总 Cr 和 Cr(Ⅵ)的效果,实验结果表明,3 种异位修复工艺对铬污染土壤中Cr(Ⅵ)的去除效果为:湿法解毒>稳定化>淋洗,湿法解毒工艺对土壤中Cr(Ⅵ)的去除率高达 83.26%~92.94%,研究还发现土壤粒径越细,越有利于湿法解毒工艺对土壤中Cr(Ⅵ)的去除或还原[8]。
前期研究结果表明,湿法解毒工艺对铬渣中Cr(Ⅵ)的还原和稳定效果较好,但将其应用于铬渣污染土壤的研究相对较少。当前湿法解毒工艺产生的上清液需进入下端水处理系统处置,工艺较繁琐。本文以铬渣污染土壤为研究对象,探究湿法解毒技术对铬渣污染土壤的修复效果及其影响因素。
1 材料与方法
1.1 供试土壤
供试土壤为甘肃某铬盐厂场地表层土壤(0~20cm),呈绿色,土壤经自然风干后,去除碎石和植物残体,研磨过160 目筛,进行湿法解毒技术试验研究。供试土壤污染情况见表1。

表1 供试土壤污染情况
1.2 实验试剂
研究所用的浓硫酸为质量分数为98%的优级纯;FeSO4为含量大于99.5%的七水合硫酸亚铁,是生产钛白粉时的工业级副产品 (蓝色晶体颗粒);氢氧化钙为含量大于90%的分工业级产品(白色粉末)。指标分析测定所需试剂(氯化镁、磷酸二氢钾、磷酸氢二钾、二苯并碳酰二肼、重铬酸钾等)均为优级纯(国药)。
1.3 实验方法
1.3.1 硫酸亚铁添加量的确定
FeSO4反应速率快、价格低廉,一直是铬渣湿法解毒、铬污染土壤异位稳定化的主要药剂[7],因此本文选取FeSO4作为湿法解毒的还原剂。根据下式,将20gCr(Ⅵ)含量为16 641mg/kg 的试验土壤中的Cr(Ⅵ)全部还原为Cr(Ⅲ),所需FeSO4的1 倍理论剂量约为5.4g,对应质量添加比为27%;所需FeSO4的1.5 倍理论剂量约为8g,对应质量添加比为40%。
Cr6++3Fe2+→Cr3++3Fe3+
1.3.2 湿法解毒技术的效果研究
湿法解毒:称取20g 样品,按照表2,用纯水分别将0.54g 和0.8g 浓硫酸稀释至60mL,分别加入待处理土壤样品中,翻转振荡2h(转速为30±2r/min),静置30min,测定上清液pH 值,然后添加FeSO4,翻转振荡2h,静置30min,测定上清液pH 值,每个处理设置3 组重复(T1~T6),结果以平均值体现。
沉淀工艺:在湿法解毒处理后的溶液体系中,选择T2、T4 和T6 添加土壤质量比为0.8%的氢氧化钙,翻转振荡2h 后,静置30min,上清液置于真空抽滤机中抽滤,以上处理设置3 组平行。
测定T1~T6 处理上清液的pH 值、总Cr 和Cr(Ⅵ)浓度,过滤后固相土壤根据《固体废物浸出毒性浸出方法水平振荡法》(HJ 557—2009)制备浸出液,并测定其总Cr 和Cr(Ⅵ)浓度。此外,测定修复后土壤Cr(Ⅵ)含量。

表2 湿法解毒实验设计表
1.3.3 硫酸亚铁对湿法解毒修复效果的影响
称取20g 样品,用纯水将0.54g 浓硫酸稀释至60mL,分别加入待处理土壤样品中,翻转振荡2h(转速为30±2r/min),然后分别添加1 倍、1.2 倍、1.3 倍、1.4 倍和1.5 倍理论剂量的FeSO4,翻转振荡2h,添加0.8%的氢氧化钙,翻转振荡2h 后,静置30min,上清液置于真空抽滤机中抽滤,以上处理设置3 组平行。测定上清液总Cr 和Cr(Ⅵ)浓度,测定过滤后固相土壤总Cr 和Cr(Ⅵ)浸出浓度以及Cr(Ⅵ)含量。
1.4 测定与分析方法
土壤浸出方法参照《固体废物浸出毒性浸出方法水平振荡法》(HJ 557—2009),土壤pH 值采用电极法测定(PHS-3C),土水比例为1 ∶10;土壤重金属采用HNO3-HF-HClO4消解后进入ICP-OES(Thermo iCAP 6300)进行总量浓度测试;采用美国USEPA Method 3060A 碱式消解法对土壤进行预处理,然后采用美国USEPA Method 7196A 分光光度法测试消解液中的Cr(Ⅵ),最终通过质量衡算的方法计算出土壤中的Cr(Ⅵ)浓度[9]。
1.5 数据处理方法
研究中的实验数据均以平均值表示,利用Excel 2013 和Origin 8.0 软件对实验所得数据进行处理和制图,采用SPSS 18.0 对数据进行相关性和显著性分析。
2 结果与讨论
2.1 湿法解毒技术不同阶段上清液pH 值变化情况
从图1 可以看出,酸化反应结束后,添加2.7%和4%的浓硫酸使上清液pH 值分别显著降低至5.63~5.88(T1~T4 处理)和4.77~4.87(T5~T6处理),增加1.3%的浓硫酸可使反应溶液pH 值降低约0.9 个单位。王斌远等[10]研究铬渣的酸浸出特征时发现,将1kg 铬渣(平均pH 值为12.7)调节至中性需要1.17L 的浓盐酸(12mol/L)进行中和。Wangxin 等[6]采用FeSO4-H2SO4处理铬渣发现,将1kg 铬渣(平均pH 值为10.93)调节至中性需要添加10molH+,即需要0.28L 的浓硫酸(18mol/L)。本试验添加质量比为2.7%的浓H2SO4即可将其pH 值调节至5.63~5.88,这可能是由于铬渣中CaO 和MgO 的含量占比分别可达30.79%和18.45%[4]。还原反应结束后,将T3、T4与T1、T2 对比发现,增加0.5 倍理论剂量FeSO4可使反应溶液pH 值显著降低0.32~0.41 个单位(P< 0.01)。土壤pH 值显著降低的原因可能在于Fe2+水解过程中产生的H+会造成土壤酸化[11],而且此次使用的FeSO4为生产钛白粉的副产品,残留的硫酸也会降低土壤pH 值。王旌等[12]研究表明添加FeSO4可使Cr 污染土壤pH 值降低,且降幅随添加比例的增加而增加。将T2、T4、T6 分别与T1、T3、T5 对比可知,添加0.8%的氢氧化钙可使反应溶液pH 值增加至6.19~6.99,显著增加3.13~3.34 个单位。
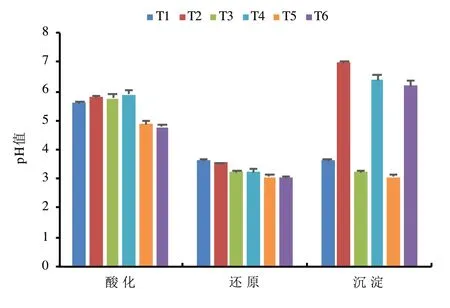
图1 不同处理对上清液pH 值的影响
2.2 不同湿法解毒工艺条件对铬渣污染土壤的修复效果
对比T3 和T5 可知,在未添加氢氧化钙的情况下,增加H2SO4的量可使上清液中总Cr 浓度从337mg/L 显著增至755mg/L(见图2a),使土壤总Cr 浸出浓度显著增加1.15 倍(P < 0.01),但土壤Cr(Ⅵ)含量无显著变化(见图2b)。当pH 值小于5 时,浸出液中Al 和Fe 的质量浓度随着酸量的增加而迅速升高,同时,Cr(Ⅲ)和Cr(Ⅵ)也被迅速释放出来,这说明赋存铬的矿物相被溶解[10]。有研究表明[2],铬渣中以固溶体形式存在于硅酸二钙、铁铝酸钙晶格内的Cr(Ⅵ),需要强酸破坏晶格后才能溶出,当硫酸调节终点pH 值为6.07 和5.12 时,对应的浸出率分别为94.6%和95.9%。Cr(Ⅵ)在较宽泛的pH 值范围内都能稳定存在,只是在不同的pH 值和浓度下Cr(Ⅵ)的主要存在形态会存在差异,但不会影响Cr(Ⅵ)的价态[13]。
从图2 可以看出,对比T1 和T3 可知,增加0.5倍理论剂量FeSO4可使上清液和浸出液Cr(Ⅵ)浓度均降低至0.02mg/L 以下,去除率和稳定化率约为100%,使土壤Cr(Ⅵ)含量从3917mg/kg 降低至68mg/kg,还原率约为98%(见图2b)。邹敏敏等[14]采用FeSO4处理电镀废水发现,当FeSO4的投加量为理论值的1.5 倍时,废水中Cr(Ⅵ)的质量浓度达到国家排放标准(< 0.5mg/L)。张晓辉等[15]采用FeSO4处理Cr(Ⅵ)浓度为100mg/L 的废水时发现,添加2 倍理论剂量的FeSO4对废水中Cr(Ⅵ)的去除率约为100%。张辉等[16]研究发现,投加FeSO4能够将土壤中活性大的可交换态和碳酸盐态铬转化为稳定的有机态和残渣态铬。另有研究表明,FeSO4对高浓度Cr 污染土壤(2 116~2 365mg/kg)的还原率为80%~99.5%[17,18]。
对比T1 和T2 可知,添加Ca(OH)2可使上清液中Cr和Cr(Ⅵ)浓度分别降低89.9%和87.3%(见图2a),使土壤浸出液中Cr 和Cr(Ⅵ)浓度分别降低81.0%和78.2%(见图2b)。对比T3 和T4 以及T5 和T6 可知,添加Ca(OH)2可使浸出液中Cr 浓度从17.2mg/L 以上降低至0.03mg/L 以下,稳定化率大于99.8%,但对土壤Cr(Ⅵ)含量无显著影响(见图2c)。研究表明,在还原剂将溶液中Cr(Ⅵ)还原成Cr(Ⅲ)之后,投加氢氧化钠或石灰等碱性物质,提高pH 值至6.5~8.0,可使Cr(Ⅲ)以Cr(OH)3沉淀形式去除[19]。此外,当pH>6.0 时,溶液中的Cr(Ⅵ)主要以CrO42-的形态存在[19],而此时铬渣中的Fe 和Al 的氧化物、氢氧化物或羟基氧化物对以CrO42-形式存在的Cr(Ⅵ)有较强的吸附作用[6,10]。
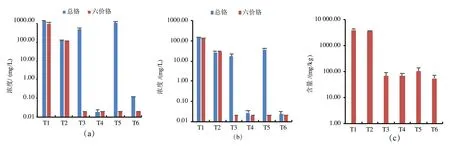
图2 湿法解毒工艺对上清液(a)、浸出液(b)和土壤(c)中总Cr 或Cr(Ⅵ)含量的影响
综上,浓硫酸可有效释放土壤中的总Cr,湿法解毒过程中,FeSO4可将上清液和土壤中的Cr(Ⅵ)还原为Cr(Ⅲ),Ca(OH)2可同时显著降低上清液和土壤浸出液中的总Cr 和Cr(Ⅵ)浓度。因此,采用湿法解毒技术能实现铬渣污染土壤和上清液的同步修复。
2.3 硫酸亚铁理论剂量倍数与六价铬浓度的线性关系
随着FeSO4理论剂量的增加,上清液和土壤浸出液中Cr(Ⅵ)浓度显著降低,且与FeSO4理论剂量倍数呈线性相关,R2adj分别为0.9723 和0.9194(见图3a、图3b);土壤中Cr(Ⅵ)含量随FeSO4理论剂量的增加而显著降低,且呈线性相关关系,R2adj为0.9108(见图3c)。张亭亭等[20]研究发现,随着Fe(Ⅱ)/Cr(Ⅵ)摩尔比的增加,Cr(Ⅵ)的浸出浓度以及稳定土壤中Cr(Ⅵ)含量显著降低,当摩尔比为3、5、10、20 时,Cr(Ⅵ)的浸出浓度分别约为5mg/L、2mg/L、0.4mg/L、0.05mg/L,Cr(Ⅵ)的含量分别约为130mg/kg、50mg/kg、25mg/kg、4mg/kg。试验所用的FeSO4明显高于理论剂量的原因可能在于土壤中含有的锰氧化物等物质将部分FeSO4氧化,这与Bartlett 等学者的研究结果一致[20]。综上,通过构建FeSO4理论剂量与Cr(VI)浓度的线性关系,可为湿法解毒工程提供参考依据。
3 结语
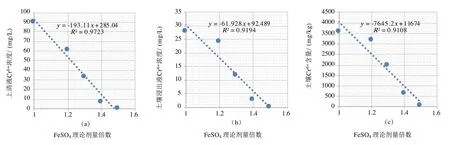
图3 FeSO4 理论剂量倍数与上清液(a)、浸出液(b)和土壤(c)Cr(Ⅵ)含量的线性关系
土壤中Cr(Ⅵ)浸出浓度和含量随着FeSO4用量的增加而显著降低,通过构建FeSO4理论剂量与Cr(VI)浓度的线性关系,可为湿法解毒工程提供参考依据。添加Ca(OH)2可同时显著降低上清液和浸出液中总Cr 和Cr(Ⅵ)的浓度,与湿法解毒有良好的协同作用。添加0.9%浓硫酸、40%硫酸亚铁和0.8%Ca(OH)2可将上清液和土壤中Cr 和Cr(Ⅵ)的浸出浓度降低至0.02mg/L 以下,Cr(Ⅵ)含量降低至67mg/kg,说明湿法解毒和沉淀工艺协同作用可在实现铬渣污染土壤稳定化修复的同时,解决湿法解毒上清液二次处理的问题。

