DPPH、ABTS和FRAP微量法测定山奈酚的抗氧化能力*
王 荣,罗 倩,冯 怡
(西安医学院药学院,陕西 西安 710021)
山奈酚是一类从蔬菜水果及中药材中提取得到的黄酮醇类物质,其具有抗氧化、抗癌、防治糖尿病、保护损伤细胞等多种功能[1]。研究显示,山奈酚具有较强的抗氧化活性,可作为抗氧化剂添加在药物中。已有文献报道山奈酚能够通过清除活性氧、保护抗氧化酶的活性抑制活性氧诱发人红细胞的溶血[2]。但目前未有实验评估山奈酚对自由基的清除活性及其总抗氧化能力。
目前对抗氧化物质的体外活性评价方法主要有自由基(DPPH自由基、ABTS自由基、超氧阴离子自由基、羟基自由基等)清除实验,脂质过氧化抑制实验和总抗氧化能力的测定等评价方法。本实验基于酶标仪-微孔板,建立微量DPPH自由基清除、ABTS自由基清除和总抗氧化能力测定法,从以上三个方面验证山奈酚的体外抗氧化作用,为其作用抗氧化剂的应用提供科学依据。
1 材 料
1.1 药品与试剂
山奈酚标准品(含量95.5%,批号110861-201611),中国食品药品检定研究院;抗坏血酸(Vc)(纯度99%),北京索莱宝科技有限公司;DPPH(1,1-二苯基-2-苦肼基自由基)(纯度97%),上海思域化工科技有限公司;ABTS([2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐])(纯度98%),萨恩化学技术有限公司;总抗氧化能力(T-AOC)测试盒,南京建成生物工程研究所;无水乙醇,天津市河东区红岩试剂厂。
1.2 仪 器
全波长酶标仪,美国Thermo Fisher Scientific公司;分析天平,奥豪斯仪器有限公司。
2 方法与结果
2.1 DPPH·清除能力的测定
2.1.1 DPPH·标准曲线的绘制
避光称取DPPH粉末82 mg,无水乙醇定容于50 mL量瓶中,得1.64 mg/mL的DPPH母液。以无水乙醇为溶剂将上述母液稀释至0.0615、0.05125、0.041、0.03075、0.0205 mg/mL。517 nm处测定其吸光度,以浓度为横坐标,以吸光度为纵坐标,绘制DPPH标准曲线。结果DPPH溶液在0.0205~0.0615 mg/mL范围内与吸光度呈良好的线性关系,其回归方程为y=11.4156x+0.1717,相关系数R2=0.9945。
2.1.2 山奈酚对DPPH·清除能力
称取适量山奈酚,加入无水乙醇配制成浓度为160 μmol/L的溶液,后用无水乙醇稀释成浓度梯度为160、80、40、20、10、5、2.5 μmol/L的溶液。精密吸取梯度样品溶液100 μL和0.1 mmol/L的DPPH溶液100 μL为实验组,对照组用100 μL无水乙醇代替DPPH溶液,以加入100 μL DPPH溶液和100 μL无水乙醇为标准组,避光反应30 min,之后用酶标仪在517 nm下测定吸光度。以Vc为对照。以上实验重复三次。由式(1)计算清除率,计算IC50值:
DPPH清除率=[1-(A实验组-A对照组)/A标准组]×100%
(1)
Vc和山奈酚对DPPH自由基的清除率与浓度呈正相关。IC50的数值可衡量被测抗氧化剂的半抑制浓度。IC50值越小,表明抗氧化活性越强。山奈酚的浓度为20 μmol/L时,清除率达47.86%,浓度为80 μmol/L时,清除率则高达88.83%,其IC50为16.17 μmol/L。Vc的清除能力较强,在浓度约为56 μmol/L时清除率就可达93.63%,Vc的IC50为9.57 μmol/L。显示山奈酚对DPPH自由基有一定的清除能力。
2.2 ABTS·清除能力的测定
避光称取ABTS自由基粉末30 mg,加超纯水8 mL溶解,得7.0 mmol/L的ABTS水溶液。秤取10 mg K2S2O8加15 mL超纯水溶解,将以上二种溶液按体积比1:1等量混合,制备ABTS·+母液,置于4 ℃冰箱保存10~12 h,备用。使用时,用无水乙醇稀释至吸光度在0.7±0.02 Abs范围内即可。配制30 μmol/L山奈酚溶液,无水乙醇稀释成浓度梯度分别为30、15、7.5、3.75、1.875、0.9375 μmol/L的溶液。精密吸取梯度样品溶液100 μL和ABTS水溶液100 μL为实验组,对照组用100 μL无水乙醇代替ABTS水溶液,以加入100 μL ABTS水溶液和100 μL无水乙醇为标准组,每个浓度设置3个复孔。避光反应30 min,之后用酶标仪在734 nm下测定吸光度。以Vc为对照。以上实验重复三次。由式(2)计算清除率,计算IC50值。
ABTS清除率=1-[(A实验组-A对照组)/A标准组]×100%
(2)
ABTS在氧化剂过硫酸钾作用下被氧化成绿色的阳离子自由基ABTS·+,在抗氧化剂存在时,ABTS·+的产生会被抑制,从而使反应体系颜色变浅,在734 nm处所测吸光度值变小,通过测定吸光度值的变化即可判断样品抗氧化能力的大小。Vc与山奈酚对ABTS自由基清除率与浓度均呈正相关,当浓度为15 μmol/L时,清除率可达54.25%,浓度为30 μmol/L时,清除率可高达90.12%,山奈酚的IC50为6.97 μmol/L。而Vc的浓度约为56 μmol/L时,清除率为99.84%,Vc的IC50为6.78 μmol/L,山奈酚对ABTS自由基具有较好的清除能力。
2.3 总抗氧化能力(FRAP法)的测定
2.3.1 FeSO4-7H2O标准曲线的绘制
精密称取27.8 mg FeSO4-7H2O标准品,超纯水溶解定容至1 mL,得浓度为100 mmol/L的母液,以水为溶剂将上述母液稀释至0.15、0.3、0.6、0.9、1.2、1.5 mmol/L。593 nm处测吸光度,以吸光度值为横坐标,对应的标准品浓度为纵坐标制成FeSO4-7H2O标准曲线。结果表明,FeSO4-7H2O溶液在0.15~1.5 mmol/L范围内,其浓度与吸光度呈现良好的线性关系,其方程为y=3.5563x+0.1898,其相关系数R2=0.991。
2.3.2 山奈酚的总抗氧化能力
避光称取山奈酚标准品适量,配制浓度为5 mmol/L的山奈酚乙醇溶液,后用无水乙醇稀释成浓度梯度分别为500、250、125、62.5、31.25、15.625 μmol/L的溶液。测定以上样品的吸光度,根据标准曲线求得与标准品相同吸光度值下的样品浓度。山奈酚的总抗氧化能力用标准物质FeSO4溶液的浓度来表示。
表1显示了不同浓度的山奈酚的总抗氧化能力。结果表明随山奈酚溶液浓度增大其总抗氧化能力增大。当山奈酚浓度在15.625~62.5 μmol/L时,其总抗氧化能力差异较小。当山奈酚浓度在125~500 μmol/L时,其总抗氧化能力显著提高。
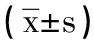
表1 山奈酚的总抗氧化能力
3 结 论
本研究分别建立了微量化DPPH自由基清除能力测定法、ABTS自由基清除能力测定法和铁离子还原/抗氧化力测定法(FRAP)评价山奈酚的体外抗氧化活性[3]。该方法建立在酶标仪和微孔板基础之上,微孔板的使用可大幅降低试剂的消耗,酶标仪可在短时间内快速同时测定样本,显著缩短了实验周期[4-6],该方法具有微量化、快速、准确性好等特点。
DPPH(1,1-二苯基-2-三硝基苯肼)自由基是一种以氮为中心的稳定有机自由基,它的稳定性来源于三个苯环的空间障碍和共振稳定作用,使夹在中间的氮原子上未成对电子不能发挥其应有的电子成对效应。其乙醇溶液显紫色,在517 nm处有最大吸收峰,当有抗氧化剂存在时,孤电子被配对,DPPH自由基溶液的颜色变浅,吸光度值变小,根据吸光度的变化可测得抗氧化剂的清除能力[7]。ABTS[2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐]自由基在适当的氧化剂(过硫酸钾、重铬酸钾等)作用下氧化成绿色的自由基阳离子ABTS·+,当有抗氧化物质存在时,ABTS·+的产生会被抑制,使反应体系褪色,吸光度值变小,在734 nm处测定吸光度即可计算出药物的清除能力[8]。总抗氧化能力的测定,利用“FRAP”法,在酸性条件下,抗氧化剂与Fe3+-TPTZ反应,使其还原成蓝色的Fe2+-TPTZ,在593 nm处测定吸光度,可以计算出抗氧化物质的总抗氧化能力[5,9]。以上评价方法均选用VC进行对照,从而来评价山奈酚抗氧化活性的强弱。本研究结果显示,山奈酚
对DPPH自由基和ABTS自由基具有良好的清除作用,其IC50分别为16.17 和6.97 μmol/L,山奈酚对DPPH自由基的清除作用弱于阳性药VC(P<0.05),但其对ABTS自由基的清除作用与VC相当(P>0.05);500 μmol/L山奈酚的总抗氧化能力为1.04 mmol/L。以上表明山奈酚具有一定的体外抗氧化能力。

