青霉胺修饰的银纳米簇的制备及其在Cu2+检测中的应用
陈宽,李娜,何瑜,宋功武
(湖北大学化学化工学院,湖北 武汉 430062)
0 引言
众所周知,铜离子(Cu2+)在生物体内发生的多种生理过程中起重要作用,也是重要的环境污染物之一.Cu2+广泛应用于许多工业过程如化学、电子、环境和生物领域,导致了在土壤、水和食物的广泛污染[1].然而,在浓度升高的情况下,Cu2+对某些藻类、真菌、细菌和病毒等生物具有高毒性[2].异常水平的Cu2+可导致生物体出现氧化应激反应,甚至与印度儿童肝硬化的发展有关,如朊病毒病、梅克斯病、帕金森病和威尔逊病[3].而且,人类若过量摄取Cu2+可能会导致严重的健康问题,包括缺血性心脏病、肾脏疾病、神经衰退性疾病以及贫血和骨骼疾病[4].美国环境保护署(USEPA)批准的饮用水中Cu2+的含量不能超过1.30×10-6mol/L[5].因此,开发高灵敏度、高选择性的检测实际样品中Cu2+的分析方法非常重要.
据报道,多种用于检测Cu2+的方法已经被开发并应用,包括有原子吸收/发射光谱法(AAS/AES)、电化学分析法、耦合等离子体质谱法(ICP-MS)和同步辐射X线光谱法(SRXRS)等[6].然而,这些方法中大多数耗时长、价格高昂,且需要经过复杂的样品处理和使用到繁复的仪器设备.因此,开发一种简易、环保的Cu2+传感器仍然十分必要.荧光分析法因其选择性好、灵敏度高、重复性好、时间消耗少、易于处理等优势受到了广泛关注.而且人们对纳米簇的研究也有了快速发展.因此,利用纳米簇的荧光性能用于金属离子的检测是一种具有应用前景的方法.
近几年,因为独特的理化性质以及在催化、光学和生物医学领域的应用,硫醇类修饰的金属纳米簇已经受到了人们极大的关注[7].本研究参考Luo课题组[8]制备青霉胺修饰铜纳米粒子的方法,以青霉胺为模板分子合成了具有红色荧光的水溶性银纳米簇.利用青霉胺的胺基与Cu2+之间的强烈作用,制备了一种高效、快速检测Cu2+的纳米传感器.
1 实验部分
1.1 试剂与仪器仪器:NICOLET iS10傅里叶红外光谱仪(Thermo Scientific),100SX 透射电子显微镜(日本JSM-6360LV公司),LS55荧光分光光度计(美国Perkin-Elmer公司).
试剂:青霉胺(DPA)、硝酸银(AgNO3)、氯化铬(CrCl3)、硝酸铅(Pb(NO3)2、氯化镉(CdCl2)、氯化钴(CoCl2)、氯化镍(NiCl2)、氯化铁(FeCl3)、氯化亚铁(FeCl2)、氯化银(AgCl)、氯化铜(CuCl2)、氯化汞(HgCl2)、氯化锌(ZnCl2)均购于中国阿拉丁试剂有限公司,氢氧化钠(NaOH)购于国药集团化学试剂有限公司,抗坏血酸(AA)、氯化钠(NaCl)、氯化钾(KCl)、氯化镁(MgCl2)均购于天津博迪化工股份有限公司,氯化钙(CaCl2) 购于江苏金坛县试剂厂,氯化钡(BaCl2)购于天津市苏庄试剂厂,氯化锰(MnCl2)购于天津市恒星化学试剂制造有限公司,以上试剂的纯度均为分析纯.
1.2 实验方法
1.2.1 青霉胺修饰的银纳米簇的制备与表征 将150 μL DPA (0.1 mol/L)和150 μL AgNO3(0.1 mol/L) 溶于4.5 mL超纯水中,在室温下快速搅拌5 min后加入80 μL NaOH(1 mol/L),再搅拌5 min,最后在50 ℃恒温水浴中搅拌并缓慢加入100 μL AA (0.5 mol/L),继续搅拌4 h,即得到5 mL红棕色的DPA-Ag NCs溶液.并通过TEM、FL、FT-IR对其进行了表征.
1.2.2 青霉胺修饰的银纳米簇作为荧光探针检测Cu2+
1)优化检测Cu2+的条件.探讨了DPA-Ag NCs检测Cu2+的最佳探针浓度、Cu2+的最佳反应时间以及检测的线性范围、检测的选择性、识别Cu2+的机理.
向稀释一定倍数的银纳米簇溶液中分别加入不同浓度Cu2+,研究该探针与Cu2+的作用时间.然后向稀释不同倍数后的银纳米簇溶液中分别加入10 mmol/L的Cu2+,用荧光分光光度计分别记录加入Cu2+前后DPA-Ag NCs在685 nm处的荧光强度的变化,探究DPA-Ag NCs检测Cu2+的最佳浓度.
通过用荧光分光光度计来记录向稀释一定倍数的DPA-Ag NCs溶液中分别加入不同浓度的新制的Cu2+前后的荧光光谱,来探究DPA-Ag NCs检测Cu2+的线性范围.
2)检测Cu2+的选择性.为了考察DPA-Ag NCs对于Cu2+相比于其他金属离子的选择性,使用了以下金属离子:Hg2+、Pb2+、Zn2+、Co2+、Fe3+、Fe2+、Ag+、Mn2+、Ba2+、Ca2+、Cd2+、Ce3+、K+、Mg2+、Na+、Ni2+.配制Cu2+与其他各金属离子溶液,然后适当浓度的金属离子溶液与稀释后的DPA-Ag NCs混合一定时间后进行荧光测量.
1.2.3 自来水分析 由含有不同浓度的Cu2+的DPA-Ag NCs的荧光强度相对于Cu2+浓度的标准曲线,来计算当地自来水中的Cu2+浓度,并与加标的Cu2+浓度作对比,得出回收率,验证本方法的实用性.
2 结果与讨论
2.1 青霉胺修饰的银纳米簇的表征首先对DPA-Ag NCs进行了结构表征,由图1(a)可知,所制备的DPA-Ag NCs表现出良好的单分散性,尺寸均一,其平均粒径为2 nm.由图1(b)所示,比较DPA-Ag NCs和DPA的红外曲线,可以发现,DPA的红外图中2 500~2 600 cm-1处所对应的S—H伸缩振动峰消失了,证明了DPA-Ag NCs的成功合成.

图1 (a) DPA-Ag NCs的透射电子显微镜图、(b) DPA-Ag NCs和DPA的红外谱图
对银纳米簇进行了光学性质表征:将DPA-Ag NCs溶液加入比色皿中,在575 nm的激发光下测定其荧光发射光谱.如图2所示,溶液在575 nm的光激发下于685 nm处发红光.证明了纳米簇的形成.
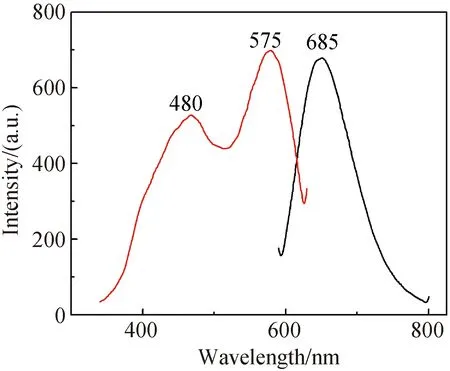
图2 DPA-Ag NCs的激发与发射荧光光谱图
2.2 青霉胺修饰的银纳米簇用于Cu2+的检测
2.2.1 探究检测Cu2+的最佳检测条件 向稀释一定倍数的DPA-Ag NCs溶液中,分别加入2 mmol/L,10 mmol/L,20 mmol/L Cu2+(图3b),经过不同时间的孵化后,观测685 nm处荧光强度变化情况(图3a),可以看出随着孵化时间增加,DPA-Ag NCs的荧光强度逐渐减弱,50 min以后,反应基本达到动态平衡.因此,选取50 min为DPA-Ag NCs与Cu2+的最佳孵化时间.
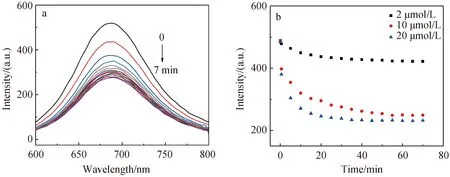
图3 (a) DPA-Ag NCs与Cu2+在不同时间下的荧光图和(b)不同浓度Cu2+加入到DPA-Ag NCs中荧光强度随时间的变化图
其次,为了提高DPA-Ag NCs检测Cu2+的灵敏度,对荧光探针的浓度进行研究.将制备的DPA-Ag NCs溶液原样分别稀释2、3、5、10、20倍,对比加入10 mmol/L Cu2+前后685 nm处的荧光强度变化情况,如图4,可以看出稀释10倍的荧光探针具有最佳的灵敏度,且相较于稀释20倍的探针有较强的荧光强度,能有效减小系统误差.
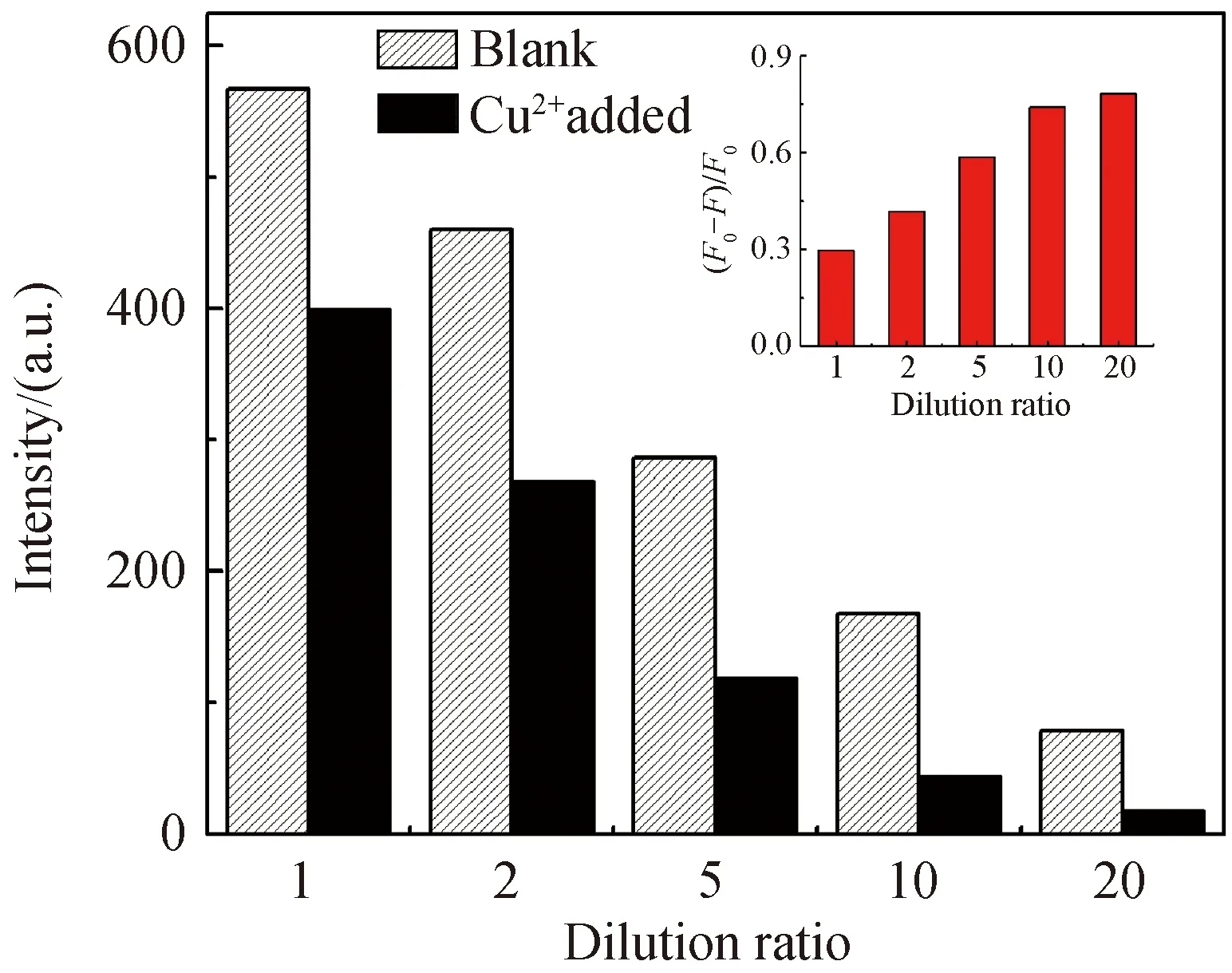
图4 不同稀释倍数的探针与10 mmol/L Cu2+作用后的荧光强度柱状图
2.2.2 探究荧光检测Cu2+的线性范围 为了评价DPA-Ag NCs检测Cu2+的灵敏度,对加入不同浓度Cu2+后685 nm处的荧光强度进行了检测,如图(5)所示DPA-Ag NCs在685 nm处的荧光强度随着其中Cu2+的浓度的增加而逐渐减弱.使用DPA-Ag NCs(超纯水稀释10倍)作为探针,Cu2+的浓度从0.05 μmol/L到10 μmol/L即能被检测,并且在0.05~4.5 μmol/L和4.5~10 μmol/L浓度范围内表现各不相同.分段拟合后得到两个线性方程:
F=32.13 [Cu2+](μmol/L)+ 7.43,(R2=0.986 9),
F=8.45 [Cu2+](μmol/L)+ 106.12,(R2=0.996 1).

图5 DPA-Ag NCs和不同浓度的Cu2+混合液的荧光发射光谱图(稀释10倍)
DPA-Ag NCs对Cu2+的检测限低至2.5 nmol/L,与所文献报道的其他探针相比,本方法提供了较宽的线性范围和测定Cu2+更低的检测限(表1).
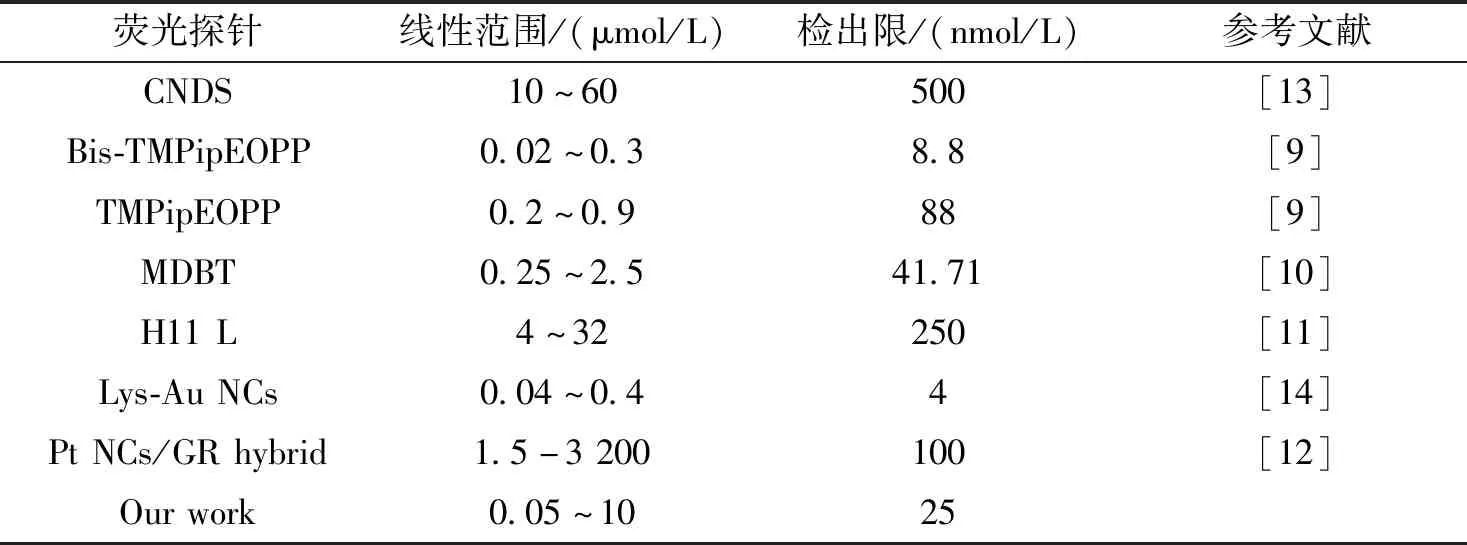
表1 不同荧光探针用于Cu2+检测的线性范围及检出限比较
2.2.3 离子选择性 为了考察DPA-Ag NCs这种荧光探针的选择性,探究了K+、Na+、Ca2+、Mg2+、Ba2+、Pb2+、Zn2+、Cd2+、Ag+、Fe2+、Co2+、Cu2+、Fe3+、Hg2+、Mn2+、Cr3+、Ni2+这17种金属离子对DPA-Ag NCs的荧光影响.在金属离子的检测中,只有Cu2+、Fe3+、Hg2+、Cd2+、Co2+和Ni2+猝灭了DPA-Ag NCs的荧光(图6).Fe3+、Hg2+、Cd2+、Co2+和Ni2+对银纳米簇的荧光强度影响不大,而Cu2+对银纳米簇的荧光影响非常显著,证明了DPA-Ag NCs对Cu2+有较高的选择性.
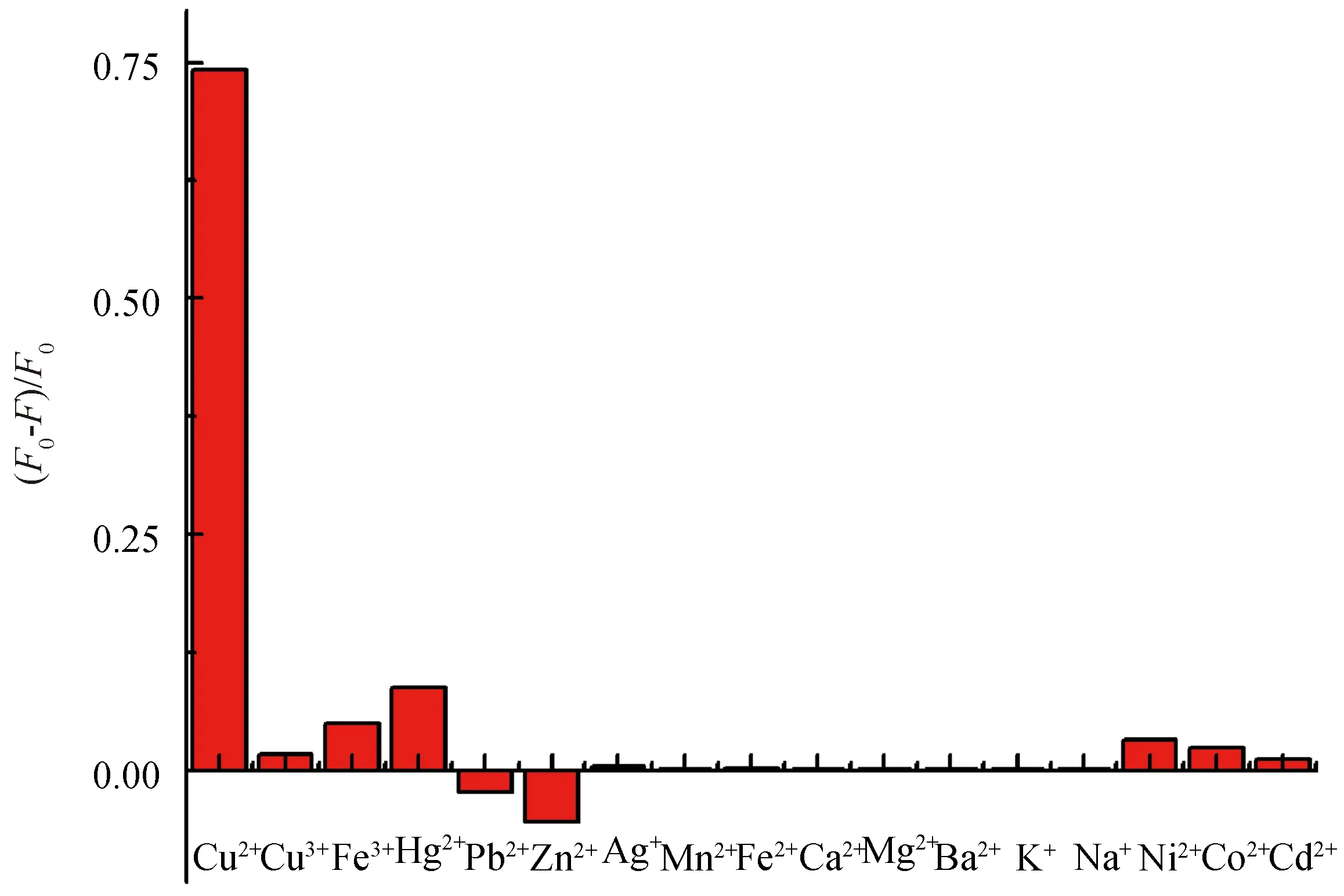
图6 DPA-Ag NCs对Cu2+选择性的荧光强度柱状图(稀释10倍)
2.3 探究检测Cu2+的机理荧光猝灭通常分为动态猝灭和静态猝灭.动态猝灭用Stern-Volmer方程(1)描述,静态猝灭用Lineweaver-Burk方程(2)描述:
F0/F=1+KSV[C]
(1)
1/(F0-F)=1/F0+KLB/F0[C]
(2)
如图7所示,F0、F分别是DPA-Ag NCs中加入Cu2+前后的荧光强度值,[C]是猝灭剂(Cu2+)的浓度,KSV是动态猝灭常数,KLB是静态猝灭常数.F0/F和Cu2+浓度的关系不符合Stern-Volmer方程,然而(F0-F)-1和[Cu2+]-1的线性关系表明荧光猝灭遵循Lineweaver-Burk 方程,属于静态猝灭.这些结果表明DPA-Ag NCs和Cu2+作用并在在银纳米簇表面形成了无荧光的化合物.
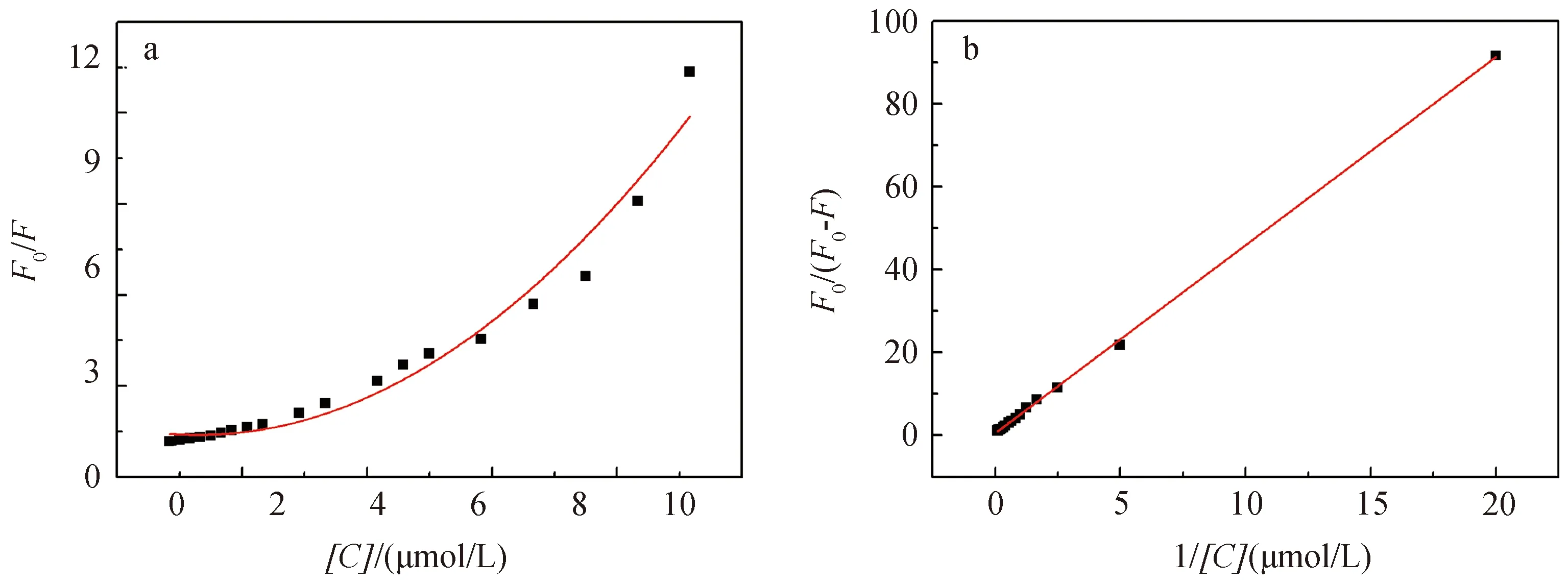
图7 加入不同浓度的Cu2+后DPA-Ag NCs的a) Stern-Volmer’s线性拟合图和b) Lineweaver-Burk线性拟合图
我们将DPA-Ag NCs的荧光猝灭归因于重金属诱导银纳米簇的聚集原理.TEM图是表征银纳米簇聚集的明显证据.如图8所示,在加入Cu2+前,银纳米簇尺寸均一,在电镜视野中分散均匀,而在加入5 μmol/L Cu2+后,银纳米簇明显密集起来,而且加入的Cu2+浓度越高,聚集情况越明显.

图8 DPA-Ag NCs 溶液中加入Cu2+ 前(a) 和加入Cu2+(b:5 μmol/L Cu2+,c:50 μmol/L Cu2+)后的TEM图
为了进一步探讨Cu2+诱导DPA-Ag NCs聚集的原因,将团簇加入Cu2+前后的样品进行红外测试,如图9所示,3 200 cm-1~3 400 cm-1属于N—H的伸缩振动吸收峰,1 622 cm-1处属于N—H的弯曲振动吸收峰,1 363 cm-1处属于C—N的伸缩振动吸收峰.从图9中可以看出,向DPA-Ag NCs溶液中加入一定量的Cu2+后,上述3处吸收峰均有所减弱,表明了Cu2+与DPA结构中的—NH2之间的强烈作用.说明该荧光探针能选择性的测定Cu2+,归因于青霉胺的—NH2与Cu2+特异性结合作用.

图9 DPA-Ag NCs中加入Cu2+前后的红外谱图
2.4 测定实际样品中的Cu2+为了验证DPA-Ag NCs作为Cu2+探针的实用性,检测了自来水中Cu2+的浓度.3次测定的结果显示在表2中.自来水样测试前用纯水稀释了3倍来消除背景干扰.样品的加标回收率分布在92%~99%之间,证明了DPA-Ag NCs作为荧光探针的应用价值.

表2 银纳米团簇对于实际样品的检测
3 结论
制备了青霉胺的修饰的具有红色荧光的银纳米簇,并对制备的DPA-Ag NCs进行了表征和分析,证明了DPA-Ag NCs的合成是通过青霉胺中S与Ag的相互作用实现的.模板分子青霉胺与Cu2+具有强烈相互作用,基于此建立了一种检测Cu2+的高灵敏手段.得到其检出范围为0.05~10 μmol/L,说明该检测方法具有简单快速、选择性好、灵敏度高等优点,并将其用于实际样品(自来水)中Cu2+的检测,得到了令人满意的结果,证明了该荧光探针的实用性.

