程序性细胞死亡蛋白-1抑制剂用于老年晚期非小细胞肺癌患者的文献分析*
占美,吴斌,陈昭燕,徐珽
(1.四川大学华西医院药剂科,成都 610041;2.四川大学华西药学院,成都 610041)
肺癌是发病人数和死亡人数均居首位的肿瘤[1-2]。肺癌发病率随着年龄增长而增加,约有一半肺癌患者年龄≥70岁,肺癌是老年人群最常见的肿瘤之一,且高龄肺癌患者的预后更差[1,3]。肺癌分为非小细胞肺癌(non-small cell lung cancer,NSCLC)和小细胞肺癌(small cell lung cancer,SCLC),其中NSCLC约占80%。近年来,随着肺癌早期筛查的普及,表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI)等靶向药物、帕博利珠单抗等免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)上市,极大改善了NSCLC患者生存,提高了患者生存质量[4-5]。目前用于肺癌的ICIs包括程序性细胞死亡蛋白-1(programmed death-1,PD-1)及其配体(PD-L1)抑制剂。纳武利尤单抗是在中国获批上市的首个免疫治疗药物。截至2020年8月1日,中国已上市的PD-1抑制剂包括帕博利珠单抗、纳武利尤单抗、信迪利单抗、特瑞普利单抗、卡瑞利珠单抗、替雷利珠单抗。其中帕博利珠单抗、纳武利尤单抗、卡瑞利珠单抗、替雷利珠单抗被国家食品药品监督管理局(National Medical Products Administration,NMPA)批准用于NSCLC患者。信迪利单抗、特瑞普利单抗暂未被NMPA批准用于NSCLC。目前PD-1抑制剂被中国临床肿瘤学会(Chinese Society of Clinical Oncology,CSCO)、美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)、美国癌症协会(American Joint Committee on cancer,ASCO)、欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)等制定的指南推荐用于IV期无驱动基因突变NSCLC一线标准治疗方案。PD-1抑制剂是NSCLC患者应用最多的ICIs,Keynote和CheckMate系列研究中纳入的老年患者比例较低,且临床试验纳入标准严格,参加临床试验的患者不同于真实世界的患者,其基础状况优于真实世界的患者。老年患者属于用药高风险人群,因此需整理PD-1抑制剂用于老年NSCLC的疗效和安全性的研究,为临床用药提供参考。
PD-1抑制剂用于老年晚期NSCLC患者的文献有限且零散,故笔者在本研究通过检索文献和指南,收集整理PD-1抑制剂在老年NSCLC应用的相关研究。预检索显示PD-1抑制剂在老年NSCLC患者的文献较少,研究间存在临床异质性和方法学异质性,不具备合并进行Meta分析的条件,故笔者在本文仅对PD-1抑制剂治疗老年晚期NSCLC的临床研究和指南中相关部分进行描述性分析。
1 资料与方法
1.1纳入与排除标准 对纳入研究中病例、干预措施及研究类型的选择标准:病理诊断为晚期或转移性NSCLC。虽然《中华人民共和国老年人权益保障法》规定,我国老年人的年龄起点标准是60岁。但目前对于老年患者的年龄划分存在争议,临床实际中设定老年患者年龄起点一般为65~75岁。前期文献分析ICIs在年龄≥75岁患者人群中的疗效存在争议[6-7]。故本研究纳入标准为针对老年NSCLC患者的研究和指南。干预措施:PD-1抑制剂包括帕博利珠单抗、纳武利尤单抗、信迪利单抗、特瑞普利单抗、卡瑞利珠单抗、替雷利珠单抗。无论PD-1抑制剂是否与化学治疗(化疗)等其他抗肿瘤药物联用均纳入。研究类型:指南、随机对照试验(randomized controlled trial,RCT)、队列研究、个案报道等。排除标准:仅有研究计划、未报道研究结果的研究。
1.2资料来源与检索策略 检索权威肿瘤学会网站:CSCO、ASCO、ESMO,收集相关指南。根据纳入排除标准,制定检索策略。检索PubMed、Ovid (Cochrane Database of Systematic Reviews and Cochrane Central Register of Controlled Trials)、中国知网(CNKI)、万方数据库、维普数据库。以PubMed为例,检索式为:(pembrolizumab or Nivolumab or Sintilimab or Camrelizumab or Toripalimab or Tislelizumab) [Title/Abstract]and(NSCLC or lung cancer)[Title/Abstract]and (older or aged or elderly) [Title/Abstract]。检索时间截至2020年8月。
1.3数据的提取与分析 由两名评价者背对背提取数据,并交叉核对,如遇争议,由第三名评价者裁决。文献的提取信息包括研究类型、研究对象、干预措施、结局指标。指南的提取信息包括推荐意见、证据级别和推荐强度。
2 结果
2.1指南分析 CSCO、ASCO、ESMO均定期发布NSCLC治疗指南。截至2020年8月,CSCO发表的最新涉及PD-1抑制剂用于晚期NSCLC的指南为《NSCLC诊疗指南》(2020版)[8],ASCO发布的最新的涉及PD-1抑制剂用于晚期NSCLC的指南为《Therapy for Stage IV Non-Small-Cell Lung Cancer Without Driver Alterations:ASCO and OH (CCO)Joint Guideline Update》[9],ESMO发表最新的涉及PD-1抑制剂用于晚期NSCLC的指南为《Metastatic non-small cell lung cancer:ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up》[10-11]。
目前,CSCO、ASCO和ESMO发布的指南均基于KEYNOTE-024、KEYNOTE-042、KEYNOTE-189推荐帕博利珠单抗用于不携带EGFR,间变性淋巴瘤激酶(Anaplastic Lymphoma Kinase,ALK)、ROS-1、BRAF基因突变的晚期或转移性NSCLC的一线治疗。根据PD-L1的表达决定是否联合化疗。对于PD-L1高表达[肿瘤细胞阳性比例分数(tumor proportion score,TPS)≥50%]的体力活动状态(performance status,PS)评分在0~1分的晚期NSCLC患者的一线治疗,CSCO(1A类证据)、ASCO(证据质量:高,推荐强度:强)和ESMO(1A)均推荐帕博利珠单抗单药治疗,对于无PD-L1表达的PS评分在0~1分的晚期NSCLC患者的一线治疗,CSCO(1A类证据)、ASCO(证据质量:中或高,推荐强度:强)和ESMO(1A)均推荐帕博利珠单抗联合化疗。三大指南均根据NSCLC病理类选(鳞癌或者非鳞癌)选择化疗方案,非鳞癌患者推荐的化疗方案是培美曲塞联合铂类,鳞癌患者推荐使用白蛋白结合型紫杉醇或紫杉醇联合铂类的化疗方案。ASCO对于不同的病理类型,证据质量存在差异,无PD-L1表达或PD-L1低表达(1%≤TPS≤49%)的非鳞癌患者选择帕博利珠单抗+卡铂+培美曲塞的证据质量是高,而无PD-L1表达或PD-L1低表达(1%≤TPS≤49%)的鳞癌患者选择帕博利珠单抗+卡铂+紫杉醇或者白蛋白结合型紫杉醇的证据质量是中。对于PD-L1低表达(1%≤TPS≤49%)的PS评分在0~1分的晚期NSCLC患者,虽然均是基于KEYNOTE-042试验[12],三大指南对于是否需要联合化疗,推荐意见存在差异。CSCO推荐帕博利珠单抗单药治疗(2A类证据)[8],ASCO推荐大多数患者可以选择帕博利珠单抗联合化疗(证据质量:高或中,推荐强度:强),如果患者不能接受含铂双药化疗,可以选择帕博利珠单抗单药治疗(证据质量:低;推荐强度:弱)。ESMO推荐PD-L1不表达或者低表达(1%≤TPS≤49%)的PS评分在0~2分的晚期NSCLC患者如果要用帕博利珠单抗,需与化疗联合(1A)。除PD-L1表达,ESMO还推荐根据肿瘤突变负荷(tumor mutational burden,TMB)的表达,TMB≥10个突变/Mb的晚期NSCLC,可以选纳武利尤单抗联合易普利单抗治疗(1A)。CSCO和ASCO均认为TMB可能预测ICIs的疗效,但高表达的取值存在争议,故暂未形成根据TMB表达选择ICIs的推荐意见。CSCO(1A类证据),ASCO(证据质量:高;推荐强度:强)和ESMO(1A)均推荐PS评分0~2分晚期NSCLC的既往未接受ICIs的患者二线治疗可以选择纳武利尤单抗,且不要求PD-L1的表达。NSCLC二线治疗选择帕博利珠单抗需要PD-L1 TPS≥1%。
除帕博利珠单抗和纳武利尤单抗,CSCO指南基于CAMEL试验[13]结果,对于晚期NSCLC无驱动基因的患者Ⅱ级推荐部分:新增卡瑞利珠单抗联合培美曲塞和铂类(1A 类证据)[8]。目前,CSCO指南暂未推荐其他国产的PD-1抑制剂用于无驱动基因的NSCLC患者,仅提到目前有一项III期临床研究(ORIENT-11,NCT03607539)评价信迪利单抗联合化疗在一线治疗非鳞状NSCLC的疗效及安全性,该试验期中分析达到预设的主要研究终点,PFS显著延长。
CSCO、ASCO和ESMO均根据PS评分选择治疗方案,虽然老年患者并发症多,基础状态较年轻患者差,但高龄并不一定PS评分差,不能仅仅根据年龄预测疗效和安全性[14]。只有ESMO指南按年龄推荐给药方案,但仅涉及化疗方案的调整,不涉及PD-1抑制剂,仅在“老年患者”提及目前老年患者使用ICIs的证据正在不断积累,目前尚无专门针对老年人的研究,根据现有临床试验的亚组分析,无论是帕博利珠单抗还是纳武利尤单抗在≤65岁和>65岁的患者人群中获益无差异。ESMO指南推荐对于年龄≥70岁的PS评分0~2分的晚期NSCLC患者选择单药不含铂的化疗方案。而对于年龄<70岁的患者,只有当PS评分为2分时,才考虑不含铂的单药化疗。ASCO于2018年发布了一部针对老年患者的指南,对于老年肿瘤需要化疗的患者,证据支持至少要评估功能、共存疾病、跌倒、抑郁、认知和营养状况[15]。目前无针对老年肿瘤患者使用ICIs的评估指南。
2.2文献检索结果 初检共获得文献325篇,其中PubMed60 篇,Ovid261 篇,CNKI 2 篇,维普数据库、万方数据库各1篇,查重、阅读摘要和全文后,纳入符合纳入排除标准的文献9 篇(图1)。
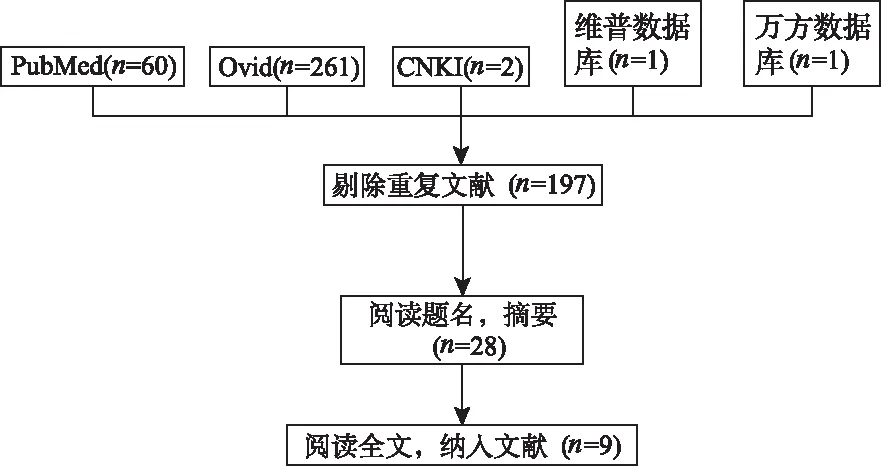
图1 文献筛选流程图
2.3文献分析 纳入的9篇研究中,3篇是系统评价[6-7,16],2篇是临床试验(CheckMate 171和CheckMate 153)中老年和PS较差人群的亚组分析[17-18],1篇是真实世界研究中老年患者的亚组分析[19]。2篇是个案报道[20-21],1篇是队列研究[22]。
3篇系统评价都是纳入成人患者的RCT,提取老年亚组人群数据,进行荟萃分析。其中2篇研究纳入RCT[6,16]的干预措施包括所有的ICIs,PD-1抑制剂包括帕博利珠单抗和纳武利尤单抗。纳入研究患者除晚期NSCLC,还有其他肿瘤。FUNAKOSHI等[16]纳入的患者除了NSCLC,还包括了前列腺癌、黑色素瘤、肾细胞癌。FUNAKOSHI等[16]和ZHANG等[6]这两个研究主要比较老年患者和年轻患者疗效方面差异,未报道安全性方面数据。FUNAKOSHI等[16]的研究结果显示,当按65~70岁划分老年和年轻患者时,老年患者可以通过ICIs治疗延长总生存期(overall survival,OS)。但该研究纳入的9个研究中,只有2个是针对NSCLC患者的,使用的ICIs都是纳武利尤单抗。因为该系统评价发表时间较早,而PD-1抑制剂最开始是在黑色素瘤中取得成功,所以该系统评价纳入9个研究中5个都是针对黑色素瘤。ZHANG等[6]纳入的均是肺癌患者,共12个RCT,其中10个RCT纳入的NSCLC患者,2个纳入的SCLC。从2016年到2019年,ICIs用于NSCLC的RCT不断涌现,治疗药物不仅包括PD-1抑制剂(帕博利珠单抗和纳武利尤单抗),还包括PD-L1抑制剂(阿替利珠单抗、度伐利尤单抗),CTLA-4抑制剂易普利单抗。该系统评价显示不同的年龄划分会得出不同的结果。当将65岁作为老年人和年轻人的分界线时,老年人可以和年轻人一样,可以通过ICI治疗获得OS的延长,但按75岁划分年龄段时,老年人不能通过免疫治疗获益,75岁以上亚组使用药物包括纳武利尤单抗、易普利单抗。该系统评价通过亚组分析解决临床异质性。NOSAKI等[7]是基于keynote系列研究开展的系统评价,相对前两个研究,临床异质性较小。该研究显示对于≥75岁、PD-L1阳性的晚期NSCLC患者,帕博利珠单抗与化疗相比可以明显延长OS,且不良事件(adverse events,AEs)发生率低于化疗(所有AE,68.5%和94.3%;≥3级AE,24.2%和61.0%)。在接受帕博利珠单抗治疗的老年患者中,疲劳是最常见的治疗相关AE(17.4%),其次是食欲下降(12.8%)和瘙痒(12.8%)。≥75岁人群中,帕博利珠单抗(10.7%)和化疗组(15.2%)分别有16例患者因AE停药,帕博利珠单抗组(1.3%)和化疗组(1.9%)分别有2例患者因治疗而死亡。帕博利珠单抗组导致老年患者死亡的治疗相关AE中1例为败血症,1例死亡原因不明,化疗组中感染、肺脓毒症各1例。<75岁人群中,帕博利珠单抗组AE的发生率为65.2%,导致停药和死亡的AE发生率分别为6.8%和1.3%。NOSAKI与ZHANG对于≥75岁晚期肺癌患者使用ICIs的疗效得出不同的结论,主要原因是使用的ICIs和研究对象均存在差异。ZHANG等[6]的研究中,≥75岁患者的4个研究中,RECK纳入的是易普利单抗+化疗vs安慰药+化疗用于SCLC的一线治疗,GOVINDAN纳入的是易普利单抗+化疗vs安慰药+化疗用于NSCLC的一线化疗,该方案目前不是指南推荐的无驱动基因阳性晚期NSCLC患者标准的一线首选治疗方案。BORGHAEI和BRAHMER纳入的是纳武利尤单抗vs多西他赛用于NSCLC的二线或者多线化疗。NOSAKI纳入的是PD-L1表达≥1%的NSCLC患者,使用的药物是帕博利珠单抗。因此ICIs对于老年患者的疗效,应根据不同的药物种类和研究对象确定。现有文献显示,PD-L1表达≥1%的老年NSCLC患者能从PD-1抑制剂帕博利珠单抗治疗中获益。而对于其他的ICIs治疗的疗效分析,建议根据药物种类和疾病(包括病理类型、肿瘤分期、PD-L1表达情况等)划分亚组进行分析。
目前针对老年患者的研究较少,提取全部人群的临床试验或真实世界研究中老年患者的数据进行分析是创造证据的可行方式之一。文献[17]是无对照组的Ⅱ期临床试验(CheckMate 171)的亚组分析,CheckMate 171共纳入接受过一线或多线治疗的晚期鳞状NSCLC患者811例,纳武利尤单抗3 mg·kg-1,每2周1次。其中≥70岁患者278例,≥75岁患者125例,PS 2分患者103例。该研究结果显示,不同人群的安全性相似,最常见的3~4级治疗相关AE为腹泻(1%)、丙氨酸氨基转移酶升高(1%)、肺炎(0.7%)、结肠炎(0.6%)和天冬氨酸氨基转移酶(0.5%)升高。总人群和年龄≥70岁和≥75岁患者的中位OS相似:分别为10.0个月、10.0个月和11.2个月。但PS评分 2分患者的中位OS仅为5.2个月。文献[18]是CheckMate 153的亚组分析,纳入556例(39%)年龄≥70岁和128例(9%)PS评分2分的至少接受过一线治疗的ⅢB~Ⅳ期NSCLC患者,纳武利尤单抗3 mg·kg-1,每2周1次。老年,PS较差人群和总体人群中,3~5级AE的发生率相似。老年人最常见AE是疲劳(22%),其次是腹泻(10%),最常见的3~4级AE是疲劳(4%)、腹泻(1%)和瘙痒(1%)。中位OS在总体人群为9.1个月和70岁以上患者为10.3个月。但中位OS在PS评分为2患者中较短,仅为4.0个月。文献[19]是意大利真实世界研究中老年人群的亚组分析,只发表了摘要,研究纳入70例(18.8%)年龄≥75岁的老年鳞状NSCLC,纳武利尤单抗3 mg·kg-1,每2周1次,中位无进展生存时间(progression-free survival,PFS)和OS分别为3.2个月和7.6个月。有8例(11.4%)因AE而停药。真实世界研究或者临床试验亚组分析均提示,老年NSCLC患者使用二线或多线治疗使用纳武利尤单抗能获益,但PS较差患者获益较差,老年患者使用纳武利尤单抗的安全性较好。目前,纳武利尤单抗为无驱动基因阳性的晚期NSCLC二线或者多线治疗的标准方案之一[8-11]。
2篇个案报道[20-21]均只纳入1例患者,均对其AE进行描述分析,1篇[20]简述了疗效。2篇个案报道使用的PD-1抑制剂都是纳武利尤单抗。张凭等[21]纳入的IV期肺腺癌患者患者,72岁,男,体质量68 kg,使用一线化疗(培美曲塞二钠+顺铂)后病情进展,二线采用纳武利尤单抗(200 mg,静脉滴注,q14d)联合放射治疗(放疗),患者使用免疫治疗未出现3度AE,轻度AE包括流感样症状、皮疹、腹泻、免疫相关性肺炎,对症处理后好转,可继续原方案治疗。崔玉忠等[20]纳入的肺鳞癌患者,84岁,给予纳武利尤单抗140 mg,静脉滴注,q14d。使用4个周期后,疗效评价为完全缓解。治疗期间发生免疫性肾功能损伤和甲状腺功能减退,对症处理后逐渐恢复正常,不良反应可耐受。
1篇队列研究[22]纳入至少接受过一线治疗的晚期非鳞状非小细胞老年肺癌患者或有中枢神经系统转移的患者,年龄≥70岁。其中522例患者≥70岁,232例患者≥75岁,队列研究显示,年龄≥70岁、≥75岁和全部人群的中位OS分别为11.5个月、12.0个月和11.3个月,中位PFS分别为4.0个月、4.2个月和3.0个月。AE发生率在总人群、老年和中枢神经系统转移的患者相似。总人群、≥70岁、≥75岁和有中枢神经转移人群的所有级别AE的发生率分别为33%,33%,34%和35%,3~4度AE发生率分别为6%,7%,7%和7%。最常见的AE是疲劳或乏力。
3 讨论
虽然真实世界研究中老年患者占比大,但临床研究中老年患者比例偏低。因为临床研究严格纳入排除标准,而真实世界老年患者基础状态较差,难以入组。临床试验中的人群和真实世界人群中的差异,导致药物的安全性数据在真实世界和临床试验中存在较大差异。如大部分临床研究中免疫性肺炎的发生率3%~4%,而真实世界研究发生率19%[2]。本研究所搜集的老年患者研究大多是临床试验亚组分析结果,真实世界中老年患者基础状态可能较差。因此,对于PD-1抑制剂用于老年NSCLC患者的安全性与总人群相似的结果应谨慎对待。因为真实世界中老年患者和临床试验纳入的老年患者存在差异,因此亟需在真实世界验证老年患者使用PD-1抑制剂的安全性及有效性。
目前,无论指南还是文献,PD-1抑制剂在老年患者使用的证据最充分的是纳武利尤单抗和帕博利珠单抗,因为这两个药上市时间较其他PD-1抑制剂早,尤其是纳武利尤单抗,是第一个用于NSCLC的PD-1抑制剂,所以涉及该药的文献数量最多。目前,无驱动基因的晚期NSCLC的一线免疫治疗,中国、美国和欧洲的指南均推荐帕博利珠单抗。对于PD-L1低表达(1%≤TPS≤49%)的PS评分在0~1分的无驱动基因的晚期NSCLC患者,CSCO推荐意见不同于ESMO和ASCO的原因是,KEYNOTE-042研究262例中国患者亚组结果显示,PD-L1(1%≤TPS≤49%)的NSCLC患者单药帕博利珠单抗治疗对比化疗的中位OS也显著延长[23-24]。目前,指南只根据PS评分推荐不同的治疗方案,暂未根据年龄推荐调整PD-1抑制剂的治疗方案。对于老年的年龄划分,文献大多以70岁为分界,因此建议开展PD-1抑制剂用于老年NSCLC的研究以70岁为分界,而不是法律规定的60岁。个案报道文献存在信息不完整的情况,其中一篇个案报道未报道患者的体质量,纳武利尤单抗按体质量给药,建议使用了对于按体质量或者体表面积给药的药物治疗方案的案例分析都应补充体质量或者体表面积。PD-1抑制剂用于老年NSCLC的安全性观察及AEs的处理也应该是今后研究中不可忽视的重要部分。
本研究的局限性主要在于原始研究缺乏。目前无专门针对老年患者使用PD-1抑制剂的高质量临床研究,现有证据主要从已发表的临床试验中进行亚组分析。真实世界研究尤其匮乏,目前仅有的一篇真实世界研究,仅发表了摘要,研究信息不完整,且是针对意大利的老年患者。临床试验严格的纳入排除标准导致临床试验中的老年患者与真实世界存在差异,故PD-1抑制剂在真实世界中老年患者的疗效和安全性尚需进一步的验证。受限于药品上市时间,目前老年NSCLC使用PD-1抑制剂证据最充分的是最先上市的纳武利尤单抗和帕博利珠单抗,笔者尚未见老年患者使用国产的PD-1抑制剂的疗效及安全性研究报道。
总体而言,目前老年患者PD-1抑制剂的证据较匮乏,尤其缺乏真实世界研究证据,而真实世界研究对于评估老年患者的疗效和安全性尤为重要,有必要开展老年NSCLC患者使用PD-1抑制剂的真实世界研究为临床用药提供参考。

