湿法处理铅膏制备氧化铅技术研究
何宗云,符世继,卢文鹏,马雁鸿
(云南驰宏锌锗股份有限公司,云南 曲靖 655011)
随着汽车、电动自行车、能源、电信等工业的飞速发展,铅酸蓄电池应用日益广泛,近年我国乃至世界铅产量的80%用于铅酸蓄电池生产[1]。我国每年有300万吨的铅酸蓄电池由于寿命到期而报废,大量废旧铅酸蓄电池的资源化利用研究具有重要的意义和作用[2]。废旧铅酸蓄电池由塑料外壳、隔板、电极、铅膏和硫酸组成,铅膏占了一半多的比重并且其成分复杂,是回收利用的重点和难点[3],因此规模化、集约化和环保清洁化的铅膏回收处理技术成为当前铅冶炼、回收企业的重要需求。
对于废旧铅酸蓄电池铅膏,一般采取火法冶炼和湿法处理回收利用其中的铅资源[4]。国外火法冶炼和湿法处理方式均有采用,国内目前多采用火法冶炼,湿法处理研究较多产业化应用较少[5-7]。火法处理通常将铅膏与铅精矿混合后通过顶吹炉或底吹炉使其转化为富铅渣,再利用侧吹还原等技术生产粗铅,再生产成精铅或电铅。而湿法处理关键是如何处理铅膏中大量的硫酸铅和二氧化铅并使其转化为铅或铅化合物。
1 原料及湿法处理工艺原理
铅膏样品来自云南驰宏锌锗股份有限公司市场采购的废旧汽车蓄电池、电动车电池和UPS电源,电池混合破碎→过筛分离电极→重力分选隔板和塑料→压滤所得铅膏。铅膏为棕红色,其成分见表1:

表1 铅膏样成分(干燥后)
铅膏原料为粗颗粒状,呈红褐色,其中夹杂有塑料颗粒,含有20%左右的水分。为分离其中的杂质,并使其中的铅尽量生成所需的氧化铅,本研究制定铅膏湿法处理工艺思路为:转化硫酸铅为碳酸铅→把二氧化铅还原为一氧化铅→硝酸浸出→硫酸沉铅→氢氧化钠脱硫转化制备氧化铅,其具体的工艺路线见图1:
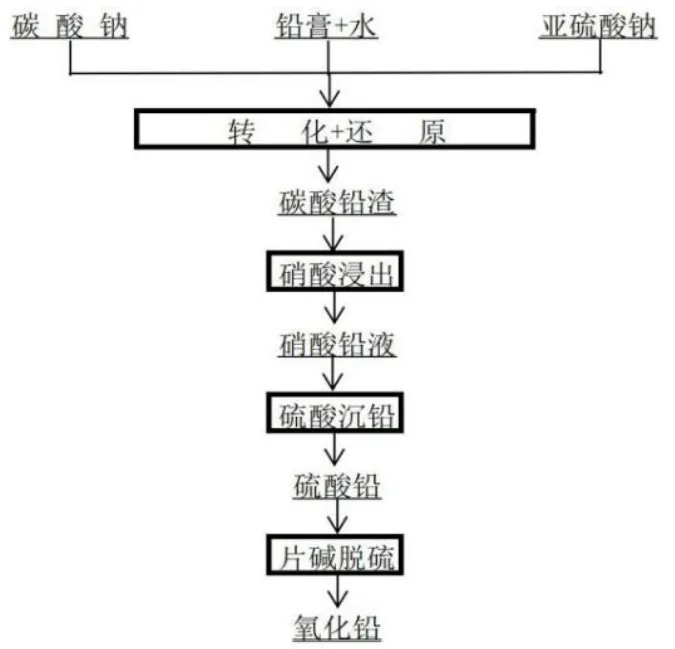
图1 铅膏湿法处理工艺流程
铅膏转化还原的工艺原理为:

在18℃、碱性环境下,硫酸铅的溶度积常数Ksp为1.6×10-8,而同样条件下碳酸铅的溶度积常数Ksp为3.3×10-14,同时反应的吉布斯自由能为负,转化反应可正常进行。同时二氧化铅作为强氧化剂,亚硫酸钠是强还原剂,在碱性环境中二氧化铅可还原为氧化铅。
硝酸浸出铅的工艺原理为:
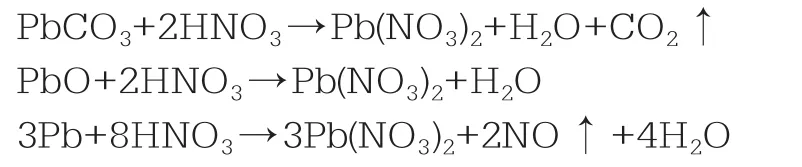
因为铅的还原电位比氢低,硝酸是强酸,可同金属铅反应生成一氧化氮和水。而氧化铅作为碱性氧化物,而碳酸铅是碱性化合物,硝酸呈酸性,硝酸同氧化铅、碳酸铅的反应很快,并可放出大量的热。
硫酸沉铅的工艺原理为:

由于硫酸铅为难溶化合物,并且其溶度积常数小,硫酸沉铅的化学反应非常快,在室温下短时间即可反应完全。
硫酸铅脱硫转化的工艺原理为:
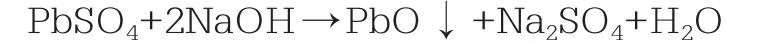
利用氢氧化钠脱硫并使硫酸铅转化为氧化铅,其反应过程实质是先生成[Pb(OH)4]2-,然后在陈化作用下分解为氧化铅和水。另外当反应中氢氧化钠浓度控制不当,过得系数较大,生成的氧化铅会被氢氧化钠溶解,生成NaPb(OH)3。
本试验原料经过105℃干燥,并经过研磨后过120目筛网;所使用的化学试剂为:浓硫酸(浓度为98%以上)、氢氧化钠(纯度96%以上)、硝酸(浓度为65%~68%)、碳酸钠(工业级,纯度为98%以上)、无水亚硫酸钠(纯度为99.5%)、水(普通生活水)。
试验中各样品的成分采用化学分析和X-Ray结构分析来综合确定,粒度分析采用激光粒度仪;样品质量采用精度0.02g级数字电子秤称量;液体体积采用量筒和量杯量取;反应加热80℃及以下采用水浴锅加热,90℃采用电热盘加热,相关温度用100℃红线温度计校准;搅拌采用数字式搅拌装置;化学反应容器采用石英烧杯;过滤采用陶瓷漏斗、双层滤纸、机械泵负压过滤;样品干燥采用玻璃表皿盛装后用热风干燥箱在105℃后干燥;所有的样品化学成分分析委托昆明冶金研究院和云南驰宏资源综合利用有限公司完成,X-Ray结构分析和粒度分析委托昆明冶金研究院完成。
2 试验结果及讨论
2.1 铅膏是硫酸铅的转化和二氧化铅的还原
铅膏中大量的硫酸铅和二氧化铅是铅膏湿法处理的关键环节,直接影响铅的直收率和工艺经济性。结合生产实际,从工业化、规模化生产角度出发,最好选择价格低廉、容易获得的工艺常见原料作为还原剂和转化剂。项目组选择碳酸钠作为转化剂,选择亚硫酸钠作为还原剂。由于转化和还原反应均可在碱性环境中进行,二者不冲突,而且由于转化反应和还原反应均是属于扩散控制的反应,二者同步进行有利于硫酸铅的转化和二氧化铅的还原更彻底,经济性也更好。硫酸铅的转化率按(铅膏中所含硫酸铅质量-转化后物料所含硫酸铅质量)/转化前铅膏所含硫酸铅质量×100%进行计算;二氧化铅还原率按(铅膏中所含二氧化铅质量-转化后物料所含二氧化铅质量)/铅膏中所含二氧化铅质量×100%进行计算。红褐色铅膏经还原转化后,其中的硫酸铅转化为白色硫酸铅,红色二氧化铅被还原为白色碳酸铅,反应后物料呈灰白色。
2.1.1 温度对还原和转化过程的影响
研究反应温度对铅膏还原和转化过程的影响时,铅膏投料200g,碳酸钠过量系数为1.5倍,亚硫酸钠过量系数为2倍,液固比为4:1,反应时间为2h,中速搅拌350r/min。
随着温度的升高,硫酸铅的化学活性增强,溶解度增大,碳酸钠对硫酸铅的转化效果持续升高,尤其在80℃以后,转化效果大幅提升,90℃时硫酸铅转化率甚至能达到98.4%。50℃以下,亚硫酸钠对二氧化铅的还原效果并不好,当温度超过60℃以后,还原效果大幅提升,温度继续升高,还原率提升并不明显(见图2)。

图2 硫酸铅转化二氧化铅还原温度影响图
2.1.2 碳酸钠和亚硫酸钠过量系数影响
研究过量系数对转化还原过程的影响,铅膏投料200g,温度90℃,液固比为4:1,反应时间为2h,中速搅拌350r/min。
随着碳酸钠过量系数的增大,碳酸根离子浓度的提高加大了与硫酸铅颗粒接触的机率和反应可能性,在搅拌作用下有助于碳酸根离子向硫酸铅颗粒内部的扩散,硫酸铅的转化率快速提升,碳酸钠过量系数达到1.4后硫酸铅转化率变慢(见图3)。随着亚硫酸钠过量系数增大,亚硫酸根离子浓度提高加大了与二氧化铅粒子接触机率,在搅拌作用下有助于亚硫酸根离子的扩散和还原能力的提升,二氧化铅与亚硫酸钠的反应得到加速,二氧化铅的还原率缓慢提升,当过量系数超过1.5后,还原率快速提升,当过量系数达到2后,其提升速率变缓(见图4)。

图3 碳酸钠过量系数对硫酸铅转化率影响

图4 亚硫酸钠过量系数对二氧化铅还原率影响
2.1.3 铅膏浆化液固比值的影响
研究浆化浓度对转化还原过程的影响,铅膏投料200g,温度90℃,碳酸钠过量系数1.5,亚硫酸钠过量系数2,反应时间为2h,中速搅拌350r/min。
随着铅膏浆化液固比值增大,反应体系体积增大,相关反应物的浓度有所下降,但在搅拌作用下,反应物之间接触的几率增加,尤其是铅膏粒子的水化作用更加明显,更有利于固相粒子与液相离子间的接触、反应,因此随着浆化液固比的加大,硫酸铅的转化和二氧化铅的还原效果逐渐提升,尤其浆化液固比由2增加到3的过程中,反应效果大幅提升,但当液固比达到4以后,硫酸铅的转化和二氧化铅的还原速率逐渐变慢,当浆化液固比达到4以后,反应速率几乎没有提升,甚至在浆化液固比达到4.5以后,反应速率不仅没有提升,反而有所下降,这与碳酸根离子与亚硫酸根离子浓度的大幅下降有关(见图5)。
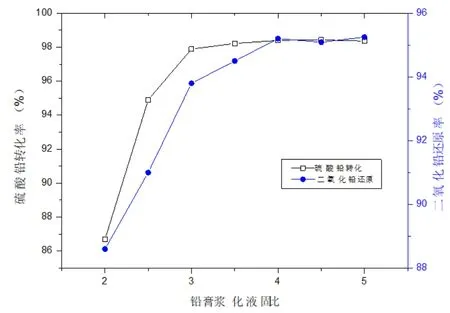
图5 铅膏浆化液固比对硫酸铅转化和二氧化铅还原影响
2.1.4 反应时间的影响
研究反应时间对转化还原过程的影响,铅膏投料200g,浆化液固比值为4,温度90℃,碳酸钠过量系数1.5,亚硫酸钠过量系数2,中速搅拌350r/min。
随着反应时间的增加,铅膏颗粒在搅拌作用下不断水化,铅膏粒子的外围边界与碳酸根离子、亚硫酸根离子发生接触,外围硫酸铅、二氧化铅先发生转化和还原反应,反应生成的碳酸铅与氧化铅从反应界面不断扩散到液相中,同时大量的碳酸根和亚硫酸根向铅膏粒子内部扩散,增加了反应速率,在20分钟至100分钟,反应程度持续增加,当反应时间达到120分钟后,反应接近尾声(见图6)。
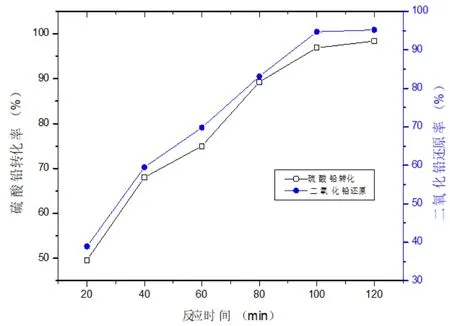
图6 反应时间对硫酸铅转化二氧化铅还原的影响
2.2 硝酸浸出碳酸铅渣
碳酸铅渣指的是铅膏完成转化还原反应并过滤干燥的物料,其中大多数物料以碳酸铅状态存在。碳酸铅渣中铅以碳酸铅、氧化铅和金属名存在,其余还包括二氧化硅、塑料片等杂质,以及没有参加反应的少量硫酸铅和二氧化铅。要尽量浸出其中的铅,最恰当的浸出剂是硝酸和乙酸,但由于生产现场更易获得硝酸,本试验采用硝酸开展浸出试验。出试验先将碳酸铅渣进行浆化再进行浸出试验。浸出率按(碳酸铅渣质量-浸出渣质量)/碳酸铅渣质量×100%计算。
碳酸铅渣用硝酸浸出时,硝酸浓度的影响对最终浸出率影响不明显,唯一影响的是反应时间。硝酸与碳酸铅渣的反应速度主要受反应控制,硝酸浓度低时,氢离子与碳酸铅、氧化铅和铅的接触几率相对较低,导致浸出速率低,反应时间长,机械搅拌可降低这一影响。
2.2.1 温度对浸出过程的影响
研究温度对硝酸浸出过程的影响,以转化还原后的碳酸铅渣为原料,浆化液固比值为4,硝酸过量系数为1.2,中速搅拌350r/min,反应时间主2h。
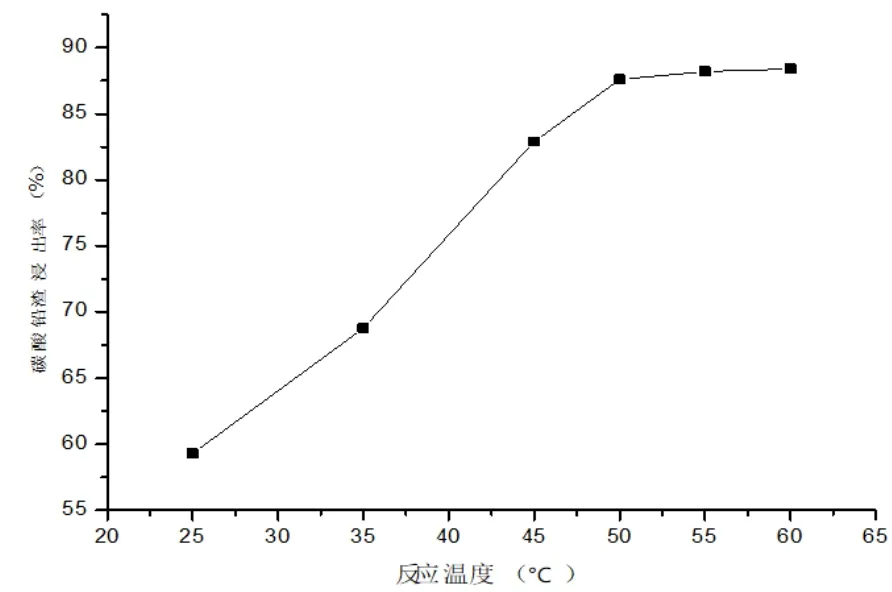
图7 反应温度对硝酸浸出率的影响
随着温度的升高,硝酸浸出率不断提升,当温度达到50℃以后浸出率上长缓慢,达到55℃后浸出率几乎达到极限。在搅拌作用下,碳酸铅渣中的碳酸铅、氧化铅和金属铅水化的活性增强,硝酸浸出反应控制因素是反应控制和扩散控制,升高反应温度有助于降低反应活化能,从而加快浸出过程。当反应温度达到55℃,反应2h以后,碳酸铅渣中大部分能与硝酸反应的物质基本浸出完成,未被浸出的物料中主要是二氧化硅、少量硫酸铅、少量二氧化铅和塑料。
2.2.2 硝酸过量系数对浸出过程影响
研究过量系数对硝酸浸出过程的影响,以转化还原后的碳酸铅渣为原料,浆化液固比值为4,反应温度55℃,中速搅拌350r/min,反应时间2h。
随着硝酸过量系数的加大,硝酸对碳酸铅渣出率提高。当过量系数达到1.2时,硝酸浸出率不再提升,未被浸出的物料不与硝酸发生反应。过量系数大于1的原因在于,硝酸的消耗量是通过碳酸铅渣中参与反应的碳酸铅、氧化铅和金属铅发化学反应式计算得到,但在实际反应过程中,并非是所有硝酸分子均参与反应,另外碳酸铅中还含有少量的铜、锑、钙、铁等化合物可与硝酸发生反应,使得硝酸需求量大于理论计算值。

图8 硝酸过量系数对碳酸铅渣浸出率的影响
2.2.3 反应时间对硝酸浸出碳酸铅渣的影响
以转化还原后的碳酸铅渣为原料,浆化液固比值为4,反应温度55℃,中速搅拌350r/min,硝酸过量系数为1.2。

图9 反应时间对硝酸浸出碳酸铅渣的影响
硝酸浸出碳酸铅渣时,液相中的氢离子先同碳酸铅、氧化铅或铅发生溶解反应,生成的硝酸铅不断溶解到溶液中,液相中的氢离子不断向固相颗粒内部扩散,固相颗粒尺寸因不断溶解而变小。随着反应时间延长,碳酸铅渣浸出不断提高,当反应时间达到120min以后,浸出反应几乎停止。
2.3 硝酸铅溶液用硫酸沉铅
硝酸铅溶液与硫酸接触时,反应速度非常快,并放出大量的热。硫酸沉铅反应温度没有要求,在室温下应快速反应;另外硫酸的浓度对反应也没有太大的影响;反应时间通常需长一些,主要是因为硝酸铅与硫酸作用时,硫酸铅的形核很快,在液相中形成大量的白色硫酸铅微粒,延长时间可通过陈化作用使硫酸铅粒子长大,便于过滤分离。
2.4 硫酸铅的脱硫转化
将白色的硫酸铅物料用水浆化,将氢氧化钠用水配制成溶液,将硫酸铅混合液加热设计温度,将氢氧化钠溶液缓慢加入,开启搅拌使之充分反应,实现硫酸铅脱硫并转化为氧化铅。硫酸铅的转化率按(脱硫转化反应前硫酸铅质量-氧化铅样品中硫酸铅质量)/脱硫转化反应前硫酸铅质量×100%计算。
2.4.1 温度的影响
将白色硫酸铅物料用水浆化,液固比为4:1,氢氧化钠溶液浓度10%,氢氧化钠过量系数为1.2,反应时间为2h,中速搅拌350r/min。
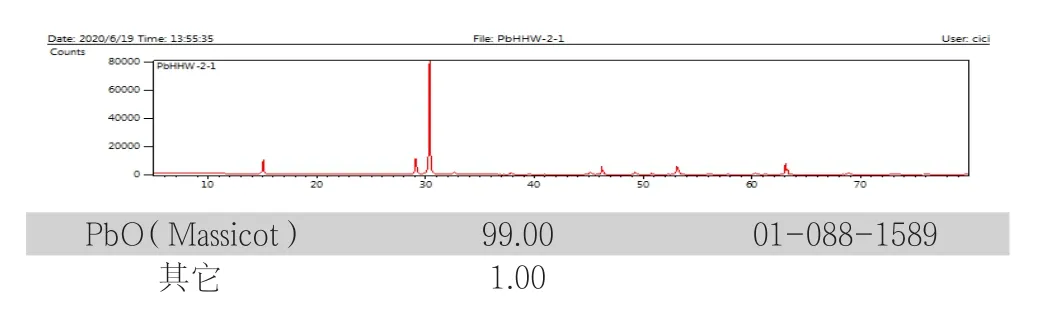
图10 氧化铅样(45℃反应)X-ray分析

图11 氧化铅样(55℃反应)X-ray分析

图12 氧化铅样(65℃反应)X-ray分析
温度低于40℃反应极其缓慢,主要是由于温度低,硫酸铅粒子与氢氧化钠的反应活化能低,影响反应速率。当温度在40℃~50℃间,反应较缓慢,生成黄色的氧化铅粒子;当温度在50℃~60℃间,反应较快,生成红色的氧化铅粒子,并伴随生成微量二氧化铅;当温度大于60℃,反应极快,生成红色氧化铅,伴生有微量的二氧化铅,同时由于反应速率太快,少量的硫酸铅被新生成的氧化铅包裹形成三盐基硫酸铅。
2.4.2 氢氧化钠浓度的影响
将白色硫酸铅物料用水浆化,液固比为4:1,氢氧化钠过量系数为1.2,反应温度为45℃,反应时间为2h,中速搅拌350r/min。
当氢氧化钠溶液浓度小于10%时,氢氧根离子在液相中浓度低,与硫酸铅粒子的接触几率较低,反应生成的氧化铅粒子少,影响反应速率;当氢氧化钠溶液浓度大于20%后,氢氧根离子在液相中浓度高,与硫酸铅粒子接触几率大,反应生成的氧化铅粒子多,反应速度快,容易形成氧化铅包覆硫酸铅的复合物;当氢氧化钠溶液浓度在10%~15%时,氢氧化钠与硫酸铅的反应速率比较适中,能确保硫酸铅脱硫转化为氧化铅,同时也能保证新生成的氧化铅粒子脱离硫酸铅外表面并扩散到溶液中。
2.4.3 氢氧化钠过量系数的影响
将白色硫酸铅物料用水浆化,液固比为4:1,氢氧化钠溶液浓度为10%,反应温度为45℃,反应时间为2h,中速搅拌350r/min。
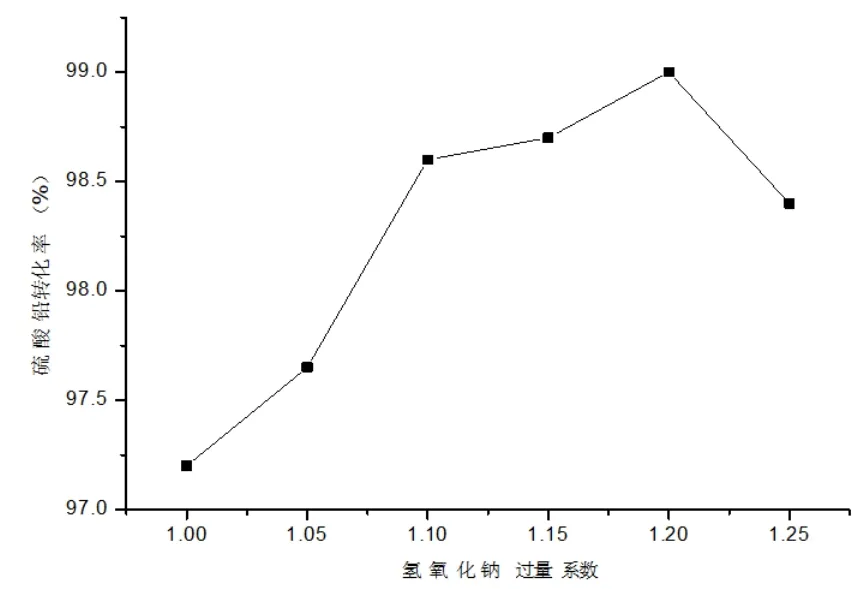
图13 氢氧化钠过量系数对硫酸铅转化率影响
氢氧化钠与硫酸铅的反应控制步骤主要是扩散控制,而氢氧根离子由于半径较大,硫酸铅晶体结构为正交晶型,氢氧根离子先包围在硫酸铅分子周围,逐步取代硫酸根,形成[Pb(OH)4]2-结构,并逐步转变为PbO和水。由于水合作用影响,并非是所有的氢氧根离子均参与发生反应,因此当过量系数为1(即氢氧化钠加入量刚好等于理论计算需求量),并不能使所有的硫酸铅均反应生成氧化铅;并且随过量系数不断增大时,参与反应的硫酸铅越来越多,当氢氧化钠过量系数达到1.2时,硫酸铅脱硫转化为氧化铅达到极限,继续提高氢氧化钠过量系数,会使已生成的氧化铅溶解生成NaPb(OH)3。
2.4.4 反应时间的影响
将白色硫酸铅物料用水浆化,液固比为4:1,氢氧化钠溶液浓度为10%,氢氧化钠过量系数为1.2,反应温度为45℃,中速搅拌350r/min。
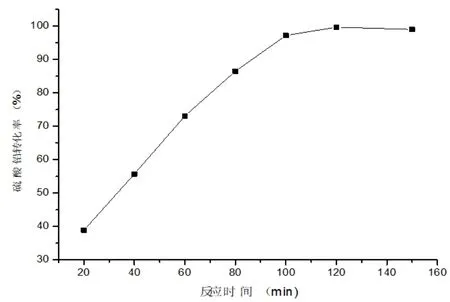
图14 反应时间对氢氧化钠转化硫酸铅的影响
随着反应时间的延长,参与反应的硫酸铅粒子越多,生成的氧化铅粒子不断脱离硫酸铅表面,使得化学反应连续进行,因此硫酸铅转化率不断提高。当反应时间接近100min时,硫酸铅粒子的脱硫转化接近尾声,当反应时间超过120min时,硫酸铅粒子的转化几乎不再进行。
3 结论
(1)反应温度升高,可使铅膏中硫酸铅的转化率和二氧化铅的还原率不断提升,当反应温度达到90℃时,硫酸铅的转化率可达到98.4,二氧化铅的还原率可达到95.2%;要使铅膏中的硫酸铅尽量转化为碳酸铅,碳酸钠的过量系数提高到1.5最好;另外亚硫酸钠的过量系数达到2时,二氧化铅的还原效果最好;铅膏浆化液固比值达到4时,硫酸铅转化和二氧化铅的还原效果均较为理想;随着反应时间延长铅膏的转化还原率不断提升,2h以后延长反应时间效果并不明显;
(2)硝酸浸出碳酸铅渣时,反应温度升高浸出率不断提升,当达到55℃以后,提高温度效果并不明显;硝酸过量系数提高,有利于浸出率的提升,硝酸过量系数达到2时浸出效果最好;另外硝酸浸出碳酸铅渣2h后,浸出反应几乎不再进行;
(3)硫酸沉淀硝酸铅溶液中的铅,在室温下即可快速进行;硫酸浓度对沉铅反应没有太大影响;硫酸沉铅反应是典型的沉淀反应,反应时间的延长,并不影响沉铅效果,仅会使生成的硫酸铅粒子陈化长大;
(4)氢氧化钠溶液脱硫转化硫酸铅时,反应温度控制在45℃效果较好;氢氧化钠的浓度控制在10%~15%期间可获得较纯的氧化铅;氢氧化钠过量系数在1.2时,反应效果较好,超过1.2后生成的氧化铅会溶解生成NaPb(OH)3;脱硫转化时间控制在2h可使氧化铅产率高而且粒径适中。

