Pd-MOX(Mn,Mo,Sn)催化剂在电化学甲醛传感器中的应用
李思达,张 鼎,邢 巍,苏 怡
(1.中国科学院长春应用化学研究所,吉林长春 130022;2.中国科学院大学,北京 100049)
0 引言
随着复合板材在装修中的大量使用[1],甲醛成为了室内空气污染的主要污染物[2]。气体传感器因其响应迅速、操作简便、高稳定性等优点,成为甲醛检测的主要设备[3-4]。目前,半导体型传感器因其制造成本低而得到广泛应用,但因其选择性差、湿度敏感等缺点[5],容易在检测甲醛时产生误报。电化学型传感器灵敏度高,抗干扰性强,适用于甲醛检测[6],但高昂的制造成本(以铂黑作为敏感材料)限制了传感器大范围应用。因此,开发廉价、高效的敏感材料成为电化学甲醛气体传感器的研发重点。
Pd因其高催化活性、抗毒性强以及相对低廉的价格,成为替代铂黑的备选材料[7]。但Pd的催化甲醛氧化活性(FOR)低于Pt,直接用于电极敏感材料,会导致传感器的灵敏度降低。目前,有大量研究工作对提高钯基催化剂的催化活性进行了探讨[8-9]。根据甲醛的氧化机理[10],制备金属氧化物掺杂的合金催化剂可以提升Pd催化剂活性。在水溶液中,OH-可在金属氧化物表面富集[11],可以促进甲醛氧化过程中产生的中间产物氧化。此外,金属氧化物(W,Mn,Mo等)歧化产生的高价态离子对有机分子具有强氧化性,是促进氧化反应的重要中间体[12]。Dong等人报道了原位生成的SnOx可以促进PdSn催化剂的催化甲酸氧化活性[13]。Han等人的工作[14]证明,掺杂少量WO2.9可以提高Pt催化剂的甲醛催化活性,以 Pt-WO2.9(15%)为敏感材料的甲醛传感器灵敏度为53 μA/ppm。虽然,大量工作证明金属氧化物MOx(M=Mn、Mo、Sn等)掺杂可以提高Pd基催化剂催化剂活性[15-17],但优化催化剂组分依然是一个挑战。
本文制备了10% 金属氧化物MOX(M =Mn、Mo、Sn)掺杂的Pd基催化剂,系统地表征了催化剂的物理性质,并通过循环伏安法测试了催化剂的催化甲醛氧化活性。最后通过组装传感器以及传感器测试,探讨了敏感材料对传感器性能的影响。
1 实验
1.1 仪器与试剂
本实验使用的仪器如下:X-射线衍射仪(XRD,D8 Advance);透射电子显微镜(TEM,JOEL-2010);CHI 660d电化学工作站;电化学测试采用三电极体系:直径3 mm的玻碳电极作为工作电极,铂电极为辅助电极,饱和甘汞电极(saturated calomel electrode,SCE)为参比电极。文中的电位均相对于SCE电极。氯化钯(PdCl2)、甲醛水溶液(HCHO,37%~40%)、硼氢化钠(NaBH4)、异丙醇[(CH3)2CHOH]、无水乙醇(C2H5OH)、硫酸(H2SO4)、盐酸(HCl)、高锰酸钾(KMnO4)、钼酸铵[(NH4)6Mo7O24·4H2O]、氯化亚锡(SnCl2·2H2O)、Nafion溶液、聚四氟乙烯乳液(PTFE)、高纯氮气(N2,99.99%),所有试剂在使用前没有进一步纯化。
1.2 催化剂的制备
所有催化剂均采用顺序浸渍法制备。第一步,制备钯纳米粒子。将25 mL 10 g/L PdCl2溶液在冰水浴中搅拌30 min,然后加入过量新制NaBH4溶液。再搅拌2 h,然后离心分离并用去离子水洗涤,在烘箱中70 ℃烘干。
第二步,合成Pd基催化剂。将制得的Pd纳米粒子置于30 mL去离子水中超声分散。分别以(NH4)6Mo7O24·4H2O、KMnO4、SnCl2·2H2O作为Mo、Mn和Sn源,按Pd∶MOX(M =Mn、Mo、Sn)质量比9∶1加入反应液中,还原剂为硼氢化钠,稀盐酸酸化,充分搅拌后离心分离。将得到的样品置于管式炉中,在N2保护下300 ℃烧结2 h。
1.3 传感器制备及性能测试
以Pd-Mn3O4催化剂作为工作电极敏感材料,铂黑为对电极敏感材料制备甲醛电化学气体传感器。将敏感材料粉末、20%聚四氟乙烯乳液、异丙醇超声混合处理30 min,制成敏感材料油墨。通过丝网印刷涂抹到聚氯乙烯(PVC)隔板上,制成膜电极组件。然后,用去离子水清洗油墨中的溶剂,并压制膜电极。最后,用0.5 mol/L H2SO4电解液浸泡膜电极,并组装传感器。
在传感器测试中,为保证准确性,需要现制标准气体。第一步,将95 μL甲醛溶液(37%)注入气体发生器中汽化,制备高浓度甲醛气体2 500 ppm(1 ppm=10-6)。第二步,根据测试需求,将适量高浓度气体泵入5 L铝箔集气袋中,通入空气稀释甲醛气体从而得到标准气体。在传感器性能测试中,将标准气体以0.3 L/min的流速泵入测试腔。使用CHI 660d测量传感器产生的电流。每次测试结束后,向测试腔泵入新鲜空气30 s,以清除残留的测试气体。
2 结果与讨论
2.1 敏感材料的物理表征
图1为Pd-Mn3O4、Pd-MoO3、Pd-SnO和Pd敏感材料的XRD图像。在上述催化剂的XRD图中,位于40°、46°、68°、82°、86°处的衍射峰对应着Pd(JCPDS no.87-0639)的(111)、(200)、(220)、(311)和(222)晶面。此外,在Pd-Mn3O4的XRD中,位于26°、32°、57°处的3个弱衍射峰对应着Mn3O4(JCPDS no.86-2337)的(220)、(111)和(511)晶面。在Pd-MoO3的XRD中,位于22°、30°、54°处3个弱衍射峰可归属为MoO3单斜结构(JCPDS no.73-1536)的(010)、(205)、(019)面。而在Pd-SnO的XRD图像中,30°和57°处的衍射峰可归属为SnO(JCPDS no.85-0712)的(101)面和(211)面。与Pd的XRD图谱相比,合金中Pd的衍射峰向低角度方向移动,表明敏感材料中合金相的形成。

图1 催化剂的XRD图
图2为上述催化剂的TEM图。Pd-Mn3O4、Pd-MoO3、Pd-SnO和Pd催化剂的平均纳米粒子尺寸分别为5.4、7.4、3.95、3.5 nm。少量金属氧化物的掺杂对催化剂的形貌没有影响。4种催化剂的HRTEM图像为其晶体结构提供了更多的信息。对于Pd-Mn3O4,0.16 nm和0.31 nm对应Mn3O4的(220)和(511)面的晶面间距,见图2(b),0.22 nm对应Pd的(111)面的晶面间距。对于Pd-MoO3,0.16 nm和0.31 nm对应MoO3的(010)和(019)面的晶面间距,见图2(c)。对于Pd-SnO,0.17 nm和0.43 nm对应着SnO的(101)和(211)面的晶面间距,见图2(d)。TEM图证明金属氧化物成功掺杂到催化剂中。

(a)Pd

(b)Pd-Mn3O4

(b)Pd-MoO3

(d)Pd-SnO
2.2 敏感材料的电化学表征
图3为上述催化剂在0.5 mol/L H2SO4溶液中循环伏安曲线,扫描电压为-0.3~1.1 V,扫描速率为0.05 V/s。从图3可看出,催化剂的循环伏安曲线均显示出Pd的氢吸脱附行为,在-0.2~0.2 V间有2个氢吸脱峰,分别对应于氢的强吸附和弱吸附。本文根据氢脱附峰面积估算了催化剂的电化学活性表面积。Pd-Mn3O4、Pd-MoO3、Pd-SnO和Pd催化剂的电化学活性面积分别为20.6、41.6、19.6、27.7 m2/g。
图4为上述催化剂在0.5 mol/L H2SO4和0.5 mol/LHCHO混合溶液中催化甲醛氧化的循环伏安曲线。从图4可以看出,各样品都表现出典型的甲醛电化学氧化的循环伏安曲线。甲醛在各催化剂上氧化的起始电位约为0.55 V,在0.68~0.84 V间分别得到催化甲醛氧化的峰电流。按电化学活性面积对峰电流进行归一化,即为催化剂的FOR活性。其中,Pd-Mn3O4的FOR活性(3.5 mA/cm2)高于Pd-MoO3(2.8 mA/cm2)、Pd-SnO(2.1 mA/cm2)和Pd(1.3 mA/cm2)。该实验现象证明氧化物的掺杂提高了纯Pd催化剂的FOR活性。催化活性最佳的是Pd-Mn3O4,归因于:OH-在Mn3O4表面的富集[18]和Mn3O4的氧化能力[19]。氧气可通过化学吸附在Mn3O4表面从而产生了氧活性物种,从而促进甲醛氧化。

(a)Pd-Mn3O4

(b)Pd-MoO3
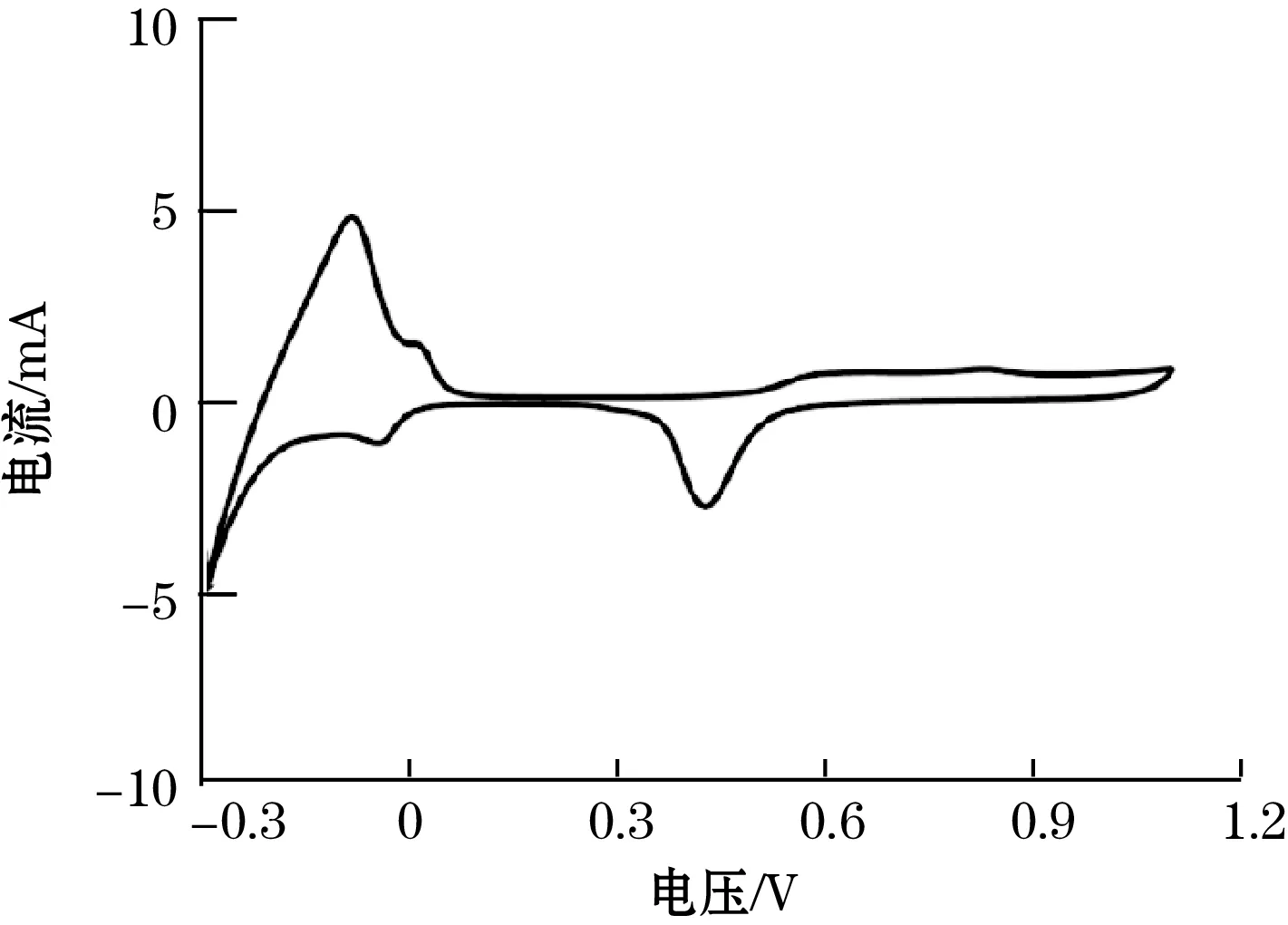
(c)Pd-SnO

(d)Pd图3 催化剂的循环伏安曲线
图5为上述催化剂在0.65 V恒电位下,在0.5 mol/L H2SO4和0.5 mol/L HCHO混合溶液中催化甲醛氧化的计时电流曲线。由图5可以看到,随着测试时间延长,4条曲线均发生衰减,在300 s后逐渐平缓。在1 000 s时,4种催化剂的极限电流密度分别为0.48、 0.41、0.29、 0.11 mA/cm2。催化剂的稳定性顺序为Pd-Mn3O4>Pd-SnO>Pd-MoO3>Pd。由上可知,Pd-Mn3O4的对甲醛电催化性能最佳,稳定性好。

图4 催化剂的FOR循环伏安曲线
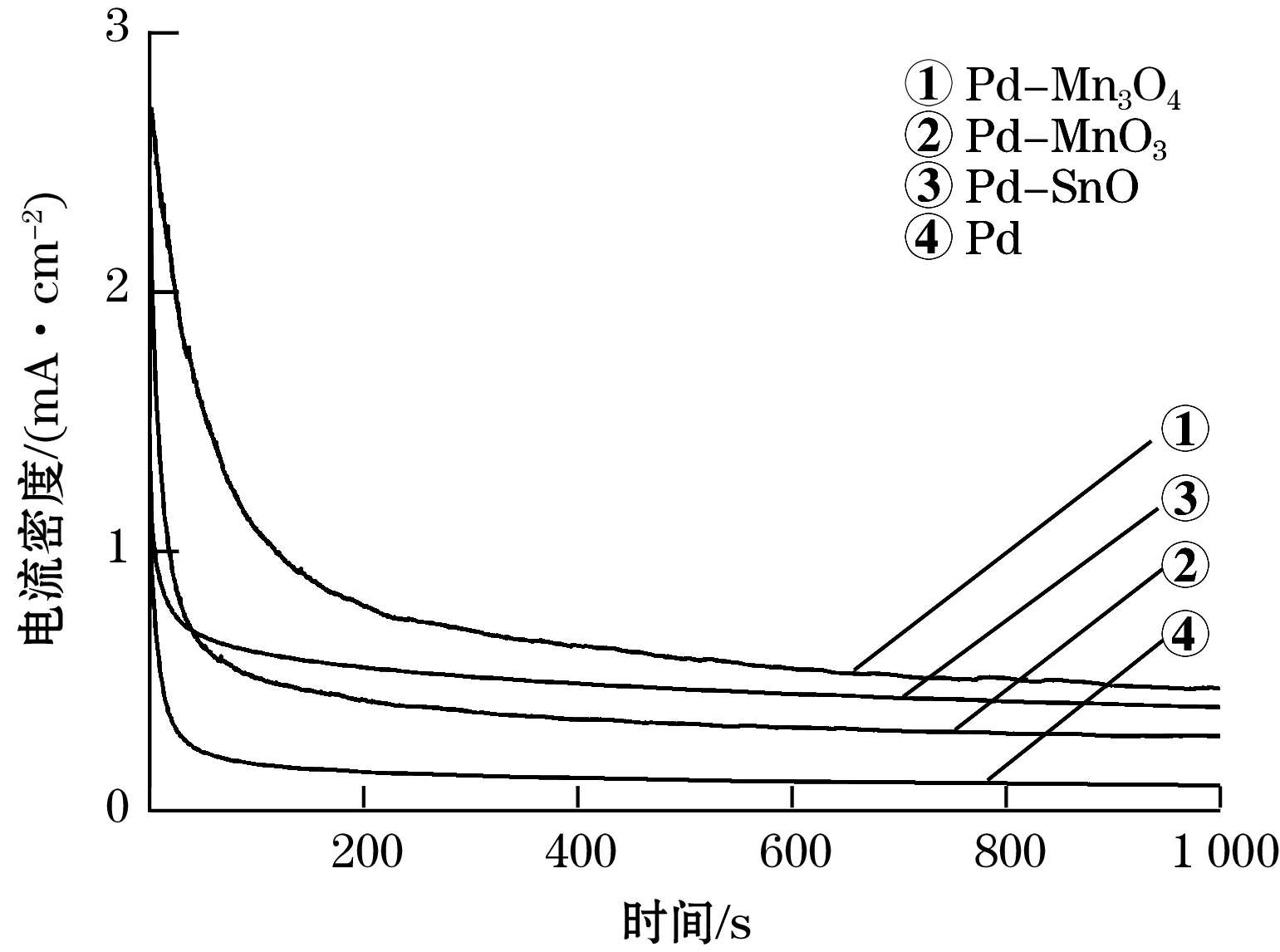
图5 催化剂的计时电流曲线
2.3 传感器性能测试
基于上述实验结论,选择Pd-Mn3O4作为传感器的工作电极敏感材料进行传感器测试。同时,选取商品化甲醛传感器进行对比(以铂黑为敏感材料,标记为Pt传感器)。图6(a)和图6(b)为Pd-Mn3O4传感器和Pt传感器在0 V外加电位(vs.Pt/O2)下对甲醛的响应信号。2种传感器的响应信号随着甲醛气体浓度的增加而增大。根据连续检测相同浓度甲醛气体的响应信号,计算响应信号的离散系数(标准差/平均值×100%)后发现,不同甲醛浓度下响应信号的变异系数小于15%,表明传感器具有良好的重复性。图6(c)所示Pd-Mn3O4传感器的灵敏度为1.5 μA/ppm,线性相关系数R2=0.995;Pt传感器的灵敏度为22 μA/ppm,线性相关系数R2=0.961。Pd-Mn3O4传感器的高线性度说明,Pd-Mn3O4传感器的精度更高。
响应时间和恢复时间是传感器性能的重要参数。图6(d)所示为传感器响应时间。其中,通入1 ppm甲醛气体时,Pd-Mn3O4传感器的响应时间67 s,Pt传感器的响应时间为11 s;而通入100 ppm甲醛气体时,Pd-Mn3O4传感器的响应时间36 s,Pt传感器的响应时间为34 s。Pd-Mn3O4传感器进行低浓度甲醛检测时,响应时间较长,但随着甲醛浓度升高,其响应时间逐渐接近Pt传感器的响应时间。图6(e)为传感器恢复时间。Pd-Mn3O4传感器的恢复时间随甲醛浓度增加没有明显变化,而Pt传感器的恢复时间随甲醛浓度增加明显延长。这是由于Pd-Mn3O4催化剂的抗毒化能力强,受甲醛浓度影响小;而铂黑易受甲醛氧化中间体毒化,因此Pt传感器检测高浓度甲醛时,恢复时间明显延长。由此可见,Pd-Mn3O4传感器在检测高浓度甲醛时具有优势。
图6(f)为Pd-Mn3O4传感器的长期稳定性。测试持续30 d,Pd-Mn3O4传感器响应信号丢失率小于7%,显示出良好稳定性。
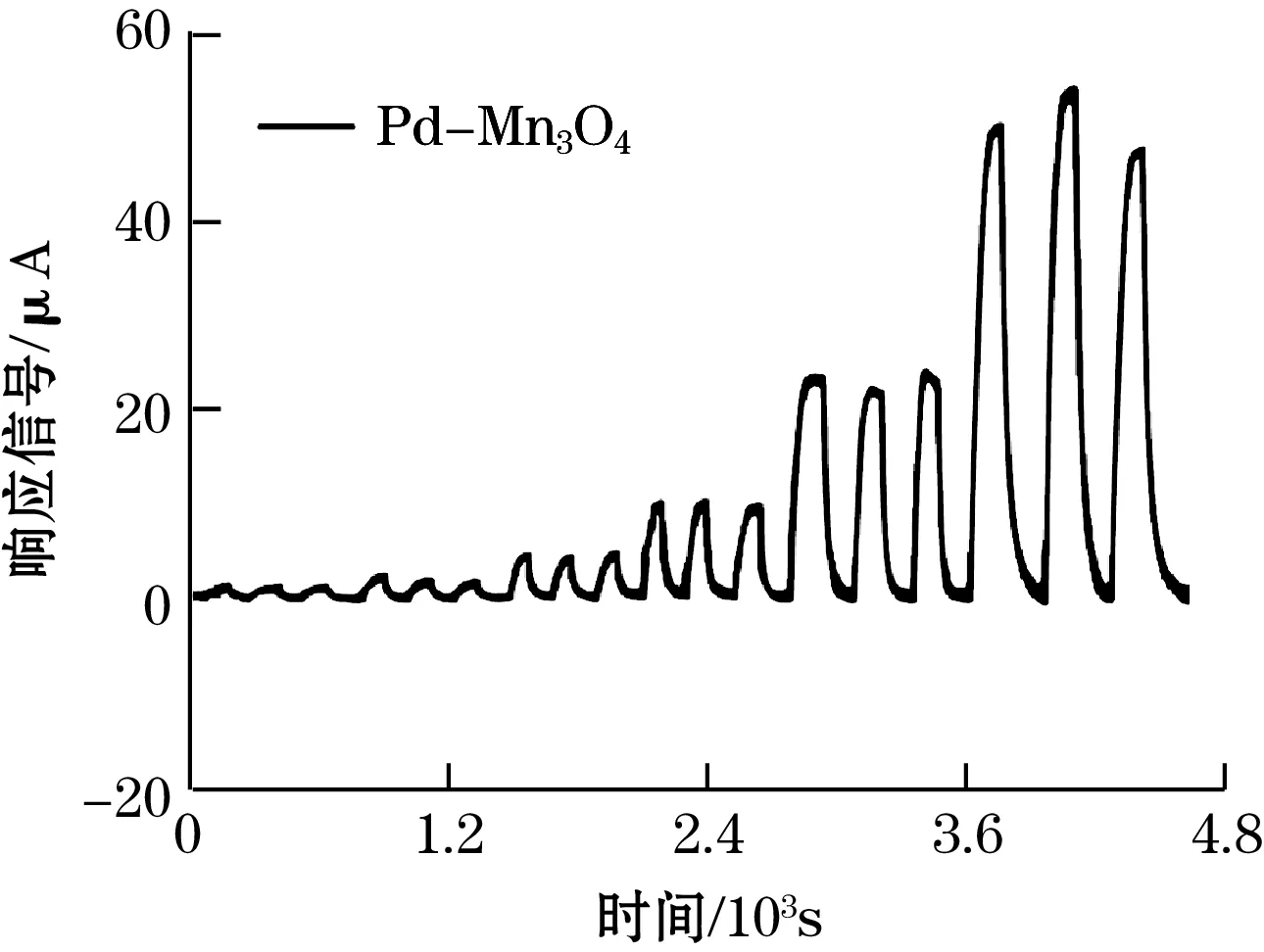
(a)Pd-Mn3O4传感器响应

(b)Pt传感器响应

(c)响应信号线性度
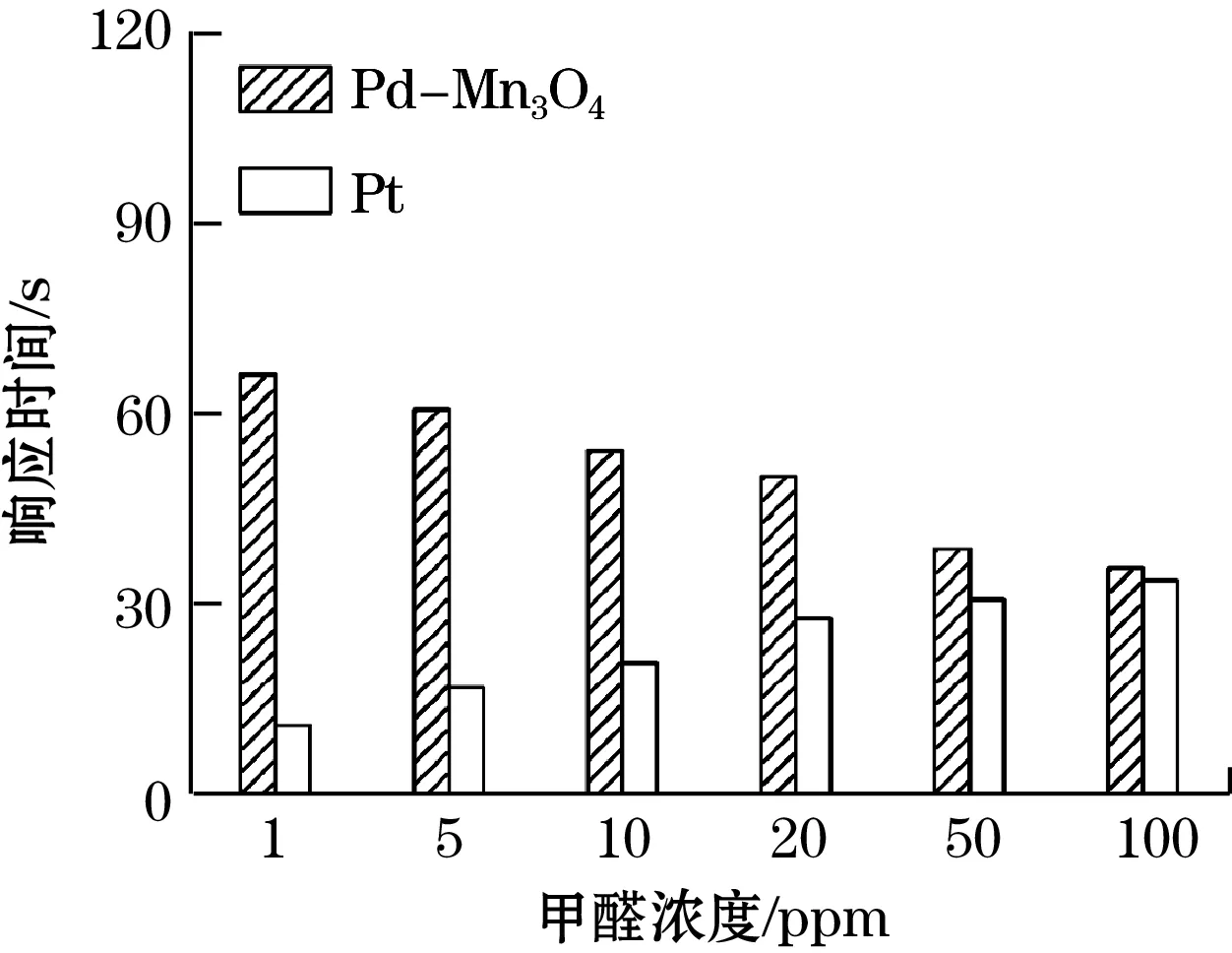
(d)响应时间

(e)恢复时间

(d)Pd-Mn3O4传感器稳定性
在Pd-Mn3O4传感器的气体选择性实验中,测试了100 ppm的干扰气体(一氧化碳、乙醇、硫化氢)。如图7所示,一氧化碳、乙醇和硫化氢的灵敏度分别为19、23、10 nA/ppm。同时,甲醛的灵敏度为490 nA/ppm,约是干扰物的20倍。Pd-Mn3O4传感器对甲醛的高选择性,表明Pd基敏感材料在电化学甲醛传感器中具有巨大应用价值。

图7 传感器选择性测试
3 结束语
本文系统地研究了金属氧化物的掺杂(Mn3O4、 MoO3和SnO)对Pd基敏感材料催化甲醛氧化中活性的影响。电化学测试结果表明氧化物的掺杂提高了Pd对甲醛的电催化氧化性能,Mn3O4的促进效果最为显著。
传感器测试表明,基于Pd-Mn3O4敏感材料的甲醛传感器在检测高浓度甲醛方面具有优势,表现出较强的抗毒化能力。同时显示出良好的选择性,对于甲醛的灵敏度约为干扰气体的20倍。Pd-Mn3O4传感器在甲醛检测方面显示出巨大应用潜力。

