宜肺扶正抗癌汤联合信迪利单抗、培美曲塞治疗晚期非鳞非小细胞肺癌的临床效果
米虽才 陈志明 罗建文

[摘要] 目的 探讨宜肺扶正抗癌汤联合信迪利单抗、培美曲塞治疗晚期非鳞非小细胞肺癌的临床疗效。 方法 选择2019年2月至2020年4月厦门市中医院肿瘤科收治的晚期非鳞非小细胞肺癌患者56例,分为对照组(28例)和观察组(28例),对照组予信迪利单抗联合培美曲塞治疗,观察组加用宜肺扶正抗癌汤治疗。比较两组的治疗疗效,对患者免疫功能、生存质量评分的影响,及药物相关不良事件发生情况。 结果 治疗3个月后,观察组的疾病控制率达到96.43%;客观缓解率为67.86%,显著高于对照组,差异有统计学意义(P<0.05)。观察组患者的CD3+、CD4+、CD4+/CD8+指标水平较治疗前升高,且显著高于对照组;CD8+指标水平降低,且低于对照组,差异有统计学意义(P<0.05)。两组患者在生存质量评分中的生理职能、躯体疼痛方面较治疗前均有所提高,且观察组的获益更加显著,差异有统计學意义(P<0.05)。两组患者均未出现严重的药物相关不良事件,观察组红/白细胞减少、肝肾功能损伤、血小板降低、肺炎不良事件发生率低于对照组,差异有统计学意义(P<0.05)。 结论 宜肺扶正抗癌汤联合信迪利单抗、培美曲塞治疗晚期非鳞非小细胞肺癌的疗效较好,可提高治疗疗效,使患者的免疫功能改善、生存质量提升,并减少药物不良事件的发生。
[关键词] 非小细胞肺癌;宜肺扶正抗癌汤;信迪利单抗;培美曲塞;治疗疗效
[Abstract] Objective To explore the clinical efficacy of Yifei Fuzheng Anti-tumor Decoction combined with Sintilizumab and Pemetrexed in the treatment of advanced non-squamous non-small cell lung cancer. Methods A total of 56 patients admitted to department of oncology, Xiamen Hospital of Traditional Chinese Medicine from February 2019 to April 2020 were divided into the control group(28 cases) and the observation group (28 cases). The control group was treated with sintilimab combined with pemetrexed. The observation group was also treated with Yifei Fuzheng Anti-cancer Decoction. The therapeutic effect of the two groups, the influence on the patient′s immune function, quality of life score, and the occurrence of drug-related adverse events were compared. Results After three months of treatment, the disease control rate of the observation group reached 96.43%. The objective remission rate of the observation group was 67.86%, which was significantly higher than that of the control group(P<0.05). The CD3+, CD4+, CD4+/CD8+ levels of the observation group were higher than before treatment and significantly higher than those of the control group, and the CD8+ levels decreased and were lower than those of the control group(P<0.05). The physiological functions and physical pain in the quality of life scores of the two groups were improved compared with before treatment, and the benefit of the observation group was more significant(P<0.05). There were no drug-related severe adverse events in both groups. The adverse events such as red/white blood cell reduction, liver and kidney function damage, platelet reduction, and pneumonia in the observation group were significant lower than that in the control group(P<0.05). Conclusion Yifei Fuzheng Anti-cancer Decoction combined with sintilizumab and pemetrexed is effective in the treatment of advanced non-squamous non-small cell lung cancer, which can improve the therapeutic effect, improve the patient′s immune function, improve the quality of life, and reduce the adverse drug events.
[Key words] Non-small cell lung cancer; Yifei Fuzheng Anti-tumor Decoction; Sintilimab; Pemetrexed; Therapeutic efficacy
非小细胞肺癌(Non-small cell lung cancer,NSCLC)作为常见的肺癌类型,非鳞非小细胞肺癌(Non-squamous cell non-small cell lung cancer,nsqNSCLC)占其中的绝大部分,此类患者早期诊断的特异性症状较少,大部分患者确诊时为肺癌中晚期,在患者积极配合治疗的前提下,其5年生存率依然较低[1]。近年来,以PD-1/PD-L1抑制剂为代表的免疫检查点抑制剂(Immune checkpoint inhibitors,ICIs)在肺癌治療过程中使部分患者的生存时间得到了明显延长[2-3]。
信迪利单抗是PD-1/PD-L1抑制剂药物之一,目前正在我国进行多项用于NSCLC治疗的临床试验[4]。为最大程度地提升治疗疗效,本研究引入中医药联合信迪利单抗、培美曲塞治疗晚期nsqNSCLC,经临床验证,取得了较为理想的治疗效果,现报道如下。
1 资料与方法
1.1一般资料
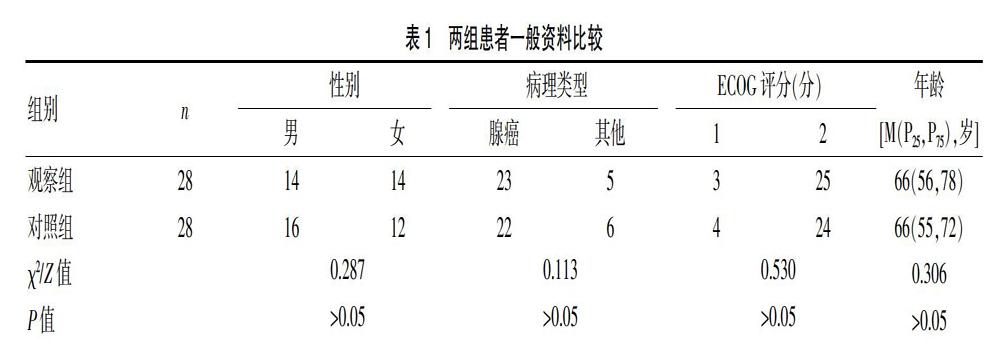
选择2019年2月至2020年4月厦门市中医院肿瘤科收治的晚期nsqNSCLC患者56例为研究对象。纳入标准[5]:①经病理组织学确诊为nsqNSCLC Ⅲb期、Ⅳ期,经基因检测无驱动基因突变,或TKI治疗失败后,且TPS≥1%,生存时间>180 d;②患者或家属知情并同意参与本研究;③完整接受治疗疗程,且治疗依从性较理想,资料保存完整。排除标准:①合并心肝肾等主要器官功能严重障碍;②合并精神类疾病,或存在严重沟通障碍;③入组前有抗肿瘤免疫治疗史或合并自身免疫性疾病等,不适合采用本研究中的治疗方案。本研究经厦门市中医院医学伦理委员会批准。将纳入的患者按照随机数字表法分为观察组28例和对照组28例,两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。
1.2 方法
对照组予信迪利单抗[信达生物制药(苏州)有效公司,批准文号:国药准字S20180016]200 mg,于0.9%氯化钠注射液100 mL中溶解后,于45 min内输液完毕;培美曲塞(德州德药制药有限公司,批准文号:国药准字H20080230)500 mg/m2静脉滴注,D1,每21天为1个周期。持续治疗4个周期(3个月)后观察疗效。
观察组在对照组治疗的基础上予宜肺扶正抗癌汤口服。组方:沙参30 g、细辛3 g、茯苓15 g、半夏15 g、川贝母15 g、百合15 g、百部10 g、蝉蜕10 g、僵蚕10 g、前胡10 g、麦冬15 g、白前10 g、天冬15 g、桑叶10 g、五味子15 g、青皮6 g、陈皮6 g、枸杞子20 g、淫羊藿15 g、苏子20 g、甘草3 g、白花蛇舌草15 g、枳实12 g。常规水煎内服,1剂/d,取汁约250 mL,早晚温服。持续治疗3个月后观察疗效。
1.3 观察指标及评价标准
①比较两组患者的治疗疗效,依据RECIST 1.1目标病灶疗效评价标准判定疗效。其中,完全缓解(CR):全部病灶完全消失,持续时间≥4周,无新病灶出现;部分缓解(PR):目标病灶缩小≥30%,持续时间≥4周,无新病灶出现;病情稳定(SD):非PR/PD;病情进展(PD):目标病灶增加≥20%,且其总和绝对值增加≥5 mm,或出现新病灶。客观缓解率(Objective response rates,ORR)=(CR+PR)例数/总例数×100%,疾病控制率(Disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%[6]。②比较两组患者治疗前后的免疫功能指标。选择在患者治疗前和治疗疗程结束后第1天,晨起采集患者空腹静脉血5 mL,应用流式细胞仪及其配套试剂,严格按照操作说明,于6 h内完成对患者T细胞亚群相关指标的检测。检测得出两组患者的CD3+、CD4+、CD8+、CD4+/CD8+指标水平并做详细记录。③比较两组患者治疗前后的生存质量评分。采用健康调查量表(The MOS item short from health survey,SF-36)进行评价,该量表使用浙江大学医学院翻译的中文版[7]。选取其中的一般健康状况(General health status,GH)、生理职能(Role physical,RP)、躯体疼痛(Body pain,BP)、社会功能(Social function,SF)、精力(Vitality,VT)等维度对患者的生存质量进行评价,为方便对比研究,将标准分统一转化为100分制,得分越高,则患者生存质量越高。④比较患者治疗期间的药物相关不良事件(Adverse drug-related events,AE)发生情况。按照NCI-CTCAE 3.0版标准进行评价和分级,比较两组患者治疗期间红/白细胞减少、血小板降低、皮疹、肺炎、腹泻及结肠炎、肝肾功能损伤、心肌炎、重症肌无力或横纹肌溶解等AE的发生情况。
1.4 统计学方法
应用SPSS 22.0统计学软件进行数据分析,符合正态分布的计量资料用(x±s)表示,采用t检验;不符合正态分布的计量资料用M(QL,QU)表示,采用秩和检验;计数资料用[n(%)]表示,采用χ2检验;多组间比较采用多个样本率(R×C)χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1两组患者治疗疗效比较
随访至2020年8月,两组患者均可客观评价近期的疗效,观察组DCR达到96.43%,高于对照组的92.86%,但差异无统计学意义(P>0.05);观察组OOR为67.86%,显著高于对照组的39.29%,差异有统计学意义(P<0.05)。见表2。
2.2 两组患者治疗前后免疫功能指标变化比较
治疗前两组患者的CD3+、CD4+、CD8+、CD4+/CD8+指标水平比较,差异无统计学意义(P>0.05)。治疗3个月后,观察组患者CD3+、CD4+、CD4+/CD8+指标水平显著高于治疗前,且显著高于对照组;CD8+指标水平低于治疗前,且低于对照组,差异有统计学意义(P<0.05)。治疗3个月后,对照组患者CD4+、CD4+/CD8+指标水平较治疗前显著降低,差异有统计学意义(P<0.001),提示经治疗后患者免疫力明显下降。见表3。
2.3 两组患者生存质量评分比较
治疗前两组患者的生存质量评分比较,差异无统计学意义(P>0.05)。治疗3个月后,观察组患者的生存质量评分在GH、RP、BP、SF、VT维度均较治疗前显著提高,且分值高于对照组;对照组患者的生存质量评分在RP、BP方面较治疗前有所提高,差异有统计学意义(P<0.05)。见表4。
2.4 两组患者治疗期间AE发生情况比较
两组患者均未出现心肌炎、重症肌无力、横纹肌溶解、重度肝肾功能损害、重度血小板减少等严重AE。对照组红/白细胞减少、肝肾功能损伤、血小板降低、肺炎发生率高于观察组,分别为39.29%、25.00%、28.57%、3.57%,差异有统计学意义(P<0.05);两组皮疹、腹泻及结肠炎发生率比较,差异无统计学意义(P>0.05)。治疗期间各种AE经对症处理后均缓解。见表5。
3 讨论
我国的肺癌死亡率在所有恶性肿瘤中居于首位,患者的5年生存率及生存质量均不理想[8]。PD-1抗体彻底改变了NSCLC的治疗格局,成为肺癌患者的新希望。本研究中应用的信迪利单抗是我国最新批准的PD-1/PD-L1抑制剂药物之一,相较于其他同类型药物,其价格具有极大优势。信迪利单抗通过与PD-1结合,抑制其與PD-L1及PD-L2的相互作用,从而阻断导致肿瘤免疫耐受的相关分子通路,再次激活淋巴细胞的抗肿瘤活性,从而杀伤肿瘤[9]。相关研究结果提示,信迪利单抗联合化疗能极大延长患者的生存时间,其AE主要为发热、肺炎、红/白细胞减少、血小板减少、皮疹、肺炎、腹泻及结肠炎、肝肾功能损伤、心肌炎、重症肌无力或横纹肌溶解等,免疫相关AE发生率约为54%[10]。培美曲塞是具有多个靶位点作用的全新抗代谢抗肿瘤药物[11],通过降低叶酸代谢途径相关酶的活性,阻碍细胞核苷酸代谢,从而有效抑制肿瘤。相关研究结果显示,培美曲塞对nsqNSCLC中的大细胞癌及腺癌的治疗效果良好[12-13]。信迪利单抗联合培美曲塞在nsqNSCLC的治疗中应用价值较高,疗效确切。为在此基础上提升治疗疗效,本研究还加用了中药治疗。
中医对肺癌的认识较早,并将其归属于“喘证”“肺积”“咳嗽”等范畴,中医理论认为气血亏损、脏腑虚弱、情志不节是肺癌的病因,其中邪毒侵入是肺癌的直接原因,故针对患者发病的病因病机,采取养阴宜肺、补气扶正、化瘀解毒抗癌的治法,疗效确切[14-15]。现代药理研究结果显示,益气养阴类中药具有免疫调节作用[16-17]。
本研究中采用的宜肺扶正抗癌汤由百合、沙参、百部等20余种中草药组方,其中沙参、麦冬、百合具有清肺养肺和润燥生津的功效,现代药理研究结果显示,此3种中草药可以改善肺癌患者的免疫状况,降低血清TNF-α、IL-6水平,通过调控肿瘤转移过程中黏附、基质降解、VEGFR表达等方面抑制肿瘤转移[18];细辛取其辛散之性,有温肺散寒化饮之力;辅以茯苓健脾渗湿,化饮利水,扶正健脾助运;又佐以五味子敛肺宜肺止咳,且能调节肺司开合之职;半夏对癌细胞的扩散转移有一定的抑制作用;僵蚕、蝉蜕等具有祛风活血散结的作用,能有效控制癌细胞的增殖、复制;而前胡、白前、川贝母、淫羊藿等具有调节免疫系统功能、改善免疫力的作用[19-20];白花蛇舌草的主要功效为清热解毒、消痛散结,研究结果显示,白花蛇舌草乙醇提取物可抑制肿瘤增殖,促进患者机体内单核细胞的增殖并增强NK细胞的杀伤作用[21];桑叶、青皮、陈皮、苏子、枳实配伍应用可以调理气机,宣肺肃肺,理气行气;配合半夏、茯苓等化痰;配伍僵蚕、蝉蜕可入血分、营分以宣邪外出;淫羊藿、枸杞子亦可养肺润肺,健脾益肾等。综上所述,宜肺扶正抗癌汤配伍严谨,治则治法符合肺癌的中医病机,临床疗效确切。
本研究结果显示,在信迪利单抗、培美曲塞治疗的基础上应用宜肺扶正抗癌汤,有助于疗效的提升,表现为观察组DCR达到96.43%,且OOR为67.86%,显著高于对照组的OOR(39.29%)。在肖敬等[22]的研究中,予固摄扶正抗癌汤联合阿法替尼、培美曲塞进行治疗,治疗总有效率达85.00%,与本研究结果一致,体现了联合中药治疗在非小细胞肺癌中的作用。本研究中,对照组治疗3个月后,患者的CD4+、CD4+/CD8+指标水平较治疗前显著降低(P<0.001),提示单纯信迪利单抗联合培美曲塞化疗导致患者部分免疫功能下降;而观察组患者的免疫功能指标CD3+、CD4+、CD8+、CD4+/CD8+均有不同程度的改善,且改善程度明显高于对照组(P<0.05),提示宜肺扶正抗癌汤有调节免疫的作用。在获得理想治疗效果的基础上,两组患者生存质量评分中的RP、BP方面较治疗前均有所提高,提示两组患者经治疗后肿瘤得到了有效控制,肿瘤引起的生理职能障碍及癌性疼痛得到改善,且观察组患者在GH、RP、BP、SF、VT维度的获益较对照组更加显著(P<0.05)。治疗的安全性也是本研究的重点,本研究对患者治疗期间出现的AE进行统计,重点关注G3以上的SAE。研究结果显示,两组患者均未出现心肌炎、重症肌无力、横纹肌溶解、重度肝肾功能损害、重度血小板减少等严重毒副反应。相比较而言,观察组在改善红/白细胞减少、肝肾功能损伤、血小板降低、肺炎发生率方面效果显著(P<0.05);两组发生皮疹、腹泻及结肠炎等AE的情况无明显差异,治疗期间各种AE经对症处理后均可缓解,提示增加宜肺扶正抗癌汤治疗较单纯应用信迪利单抗联合培美曲塞治疗可有效减少化疗的骨髓抑制、免疫性肺炎、肝肾功能损伤等AE,且不会增加AE。本研究结果证实,宜肺扶正抗癌汤对肺癌的治疗有重要作用,能极大地改善患者的免疫调节功能,促进相关免疫治疗疗效的提升。
综上所述,宜肺扶正抗癌汤治疗非小细胞肺癌有较为理想的应用效果,与信迪利单抗、培美曲塞联用,可达到较为理想的治疗效果,能够提高治疗疗效、改善患者的免疫功能及生存质量、减少AE发生,对于延缓肺癌的进展具有重要意义。
[参考文献]
[1] 金建伟,殷珂欣,王青,等.晚期非小细胞肺癌免疫治疗联合化疗研究进展[J].浙江临床医学,2020,22(3):450-453.
[2] 易巧丽,郎梦真,王文哲,等.晚期非小细胞肺癌免疫治疗研究进展[J].中国实用医刊,2019,46(15):119-122.
[3] Cyriac G,Gandhi L.Emerging biomarkers for immune checkpoint inhibition in lung cancer[J].Semin Cancer Biol,2018,52(Pt2):269-277.
[4] 朱丹,李月阳,宋燕青,等.PD-1抑制剂信迪利单抗的临床研究进展[J].中国医院药学杂志,2020,40(1):120-122.
[5] 中华人民共和国国家卫生健康委员会.新型抗肿瘤药物临床应用指导原则(2018年版)[J].肿瘤综合治疗电子杂志,2019,5(1):41.
[6] Eisenhauer EA,Verweij J.11 New response evaluation criteria in solid tumors:Recist guideline version 1.1[J].EJC Suppl,2009,7(2):5-10.
[7] 李鲁,王红妹,沈毅,等.SF-36健康调查量表中文版的研制及其性能测试[J].中华预防医学杂志,2002,36(2):109-112.
[8] 李铭,胡广原,梅齐,等.晚期非小细胞肺癌化疗[J].实用临床医药杂志,2017,21(13):26-28.
[9] Shauang Z,Min Z,Wei W,et al.Preclinical characterization of Sintilimab,A fully human anti-PD-1 therapeutic monoclonal antibody for cancer[J].Antibody Therapeutics,2018,1(2):65-73.
[10] Shi Y,Su H,Song Y,et al.Safety of sintilimab in patients with relapsel or refractory classical Hodgkin lymphoma[J].Lancet Haematol,2019,6(1):e9-e12.
[11] 丛云燕,林忠.培美曲塞联合顺铂方案化疗后行培美曲塞同药维持治疗在晚期肺腺癌患者中的应用[J].中国医药科学,2018,8(4):221-224.
[12] 张厚云,周建华.培美曲塞联合顺铂同步放化疗治疗局部晚期肺腺癌的效果体会[J].临床研究,2018,26(6):100-101.
[13] 廖凌峰.培美曲塞联合顺铂与依托泊苷单药同步放化疗治疗局部晚期老年肺腺癌近期疗效比较[J].中国合理用药探索,2018,15(2):15-17.
[14] 唐振豪,兰聪颖,林丽珠.从肿瘤微环境正常化探讨活血化瘀法及除痰散结法在肿瘤治疗中的机制[J].广州中医药大学学报,2019,36(7):1091-1098.
[15] 程海波,王俊壹,李柳.癌毒病机分类及其在肿瘤临床治疗中的应用[J].中医杂志,2019,60(2):119-122.
[16] 宋洋,方美云,姜凤,等.人参皂苷Rg3促树突状细胞诱导作用的实验研究[J].中华临床医师杂志(电子版),2012,6(8):2120-2123.
[17] 芮冉,焦佩娟,张朝玉,等.提高机体抗肿瘤免疫中药的现代研究[J].吉林中医药,2018,38(3):325-327,338
[18] 冯正权,吴良村,沈敏鹤,等.新加沙参麦冬煎剂抑制肿瘤转移及其作用机制的实验研究[J].医药导报,2006, 25(12):1249-1252.
[19] 刘传锋,丰银平,刘笑静.沙参麦冬汤加减对肺癌恶液质气阴两虚型患者的临床疗效及TNF-α、IL-6的影响[J].中国现代医生,2019,57(28):130-133,137.
[20] 周珂,王晓艳.沙参麦冬汤辅治阴虚型晚期非小细胞肺癌68例临床观察[J].浙江中医杂志,2015,50(5):343-345.
[21] 钱韵旭,赵浩如,高展.白花蛇舌草提取物的体外抗肿瘤活性[J].江苏药学与临床研究,2004,12(4):36-38.
[22] 肖敬,程曉云,张淑平,等.固摄扶正抗癌汤联合阿法替尼、培美曲塞治疗非小细胞肺癌的临床效果观察[J].解放军医药杂志,2019,31(11):20-23.
(收稿日期:2020-09-28)

