葡萄酒泥蛋白质水解制备氨基酸工艺研究
李凤玲,洪诗雨,李梦娟,李 祥
(河南牧业经济学院,河南 郑州 450046)
葡萄酒泥是葡萄酒在酿造过程和陈酿期间产生的沉淀物,据统计每生产100 t的葡萄酒,可形成2.5 t~4 t的葡萄酒泥。葡萄酒泥的主要成分有酵母菌体、多酚类物质、蛋白质、糖类和脂类等物质。目前酒泥的开发利用方式主要是提取酒泥谷胱甘肽[1]、提取酒石酸[2]、提取酚类物质[3]、提取酒泥酵母多糖如甘露聚糖和葡聚糖[4-6]等,对酒泥蛋白质的开发利用研究较少。
酒泥蛋白主要包括酵母菌体蛋白和葡萄蛋白。在葡萄酒成熟和稳定的过程中,在特定的条件下,葡萄酒泥中的酵母会发生自溶,致酵母的细胞膜破裂,细胞中的蛋白酶、核酸酶、葡萄糖水解酶等物质被释放出来,酶的活性增加,导致细胞内的大分子物质被分解为小分子成分[7]。所以酒泥酵母蛋白与一般酵母蛋白质的结构有一定的差别,水解条件也有不同。本实验采用酸水解的方法对葡萄酒酒泥蛋白进行水解,研究葡萄酒泥蛋白酸水解的最适工艺条件,为葡萄酒泥蛋白的进一步开发利用提供参考和依据。
1 材料与方法
1.1 实验材料
葡萄酒泥由河南牧业经济学院酿酒工程实验室提供。
1.2 实验仪器
Pwc214分析天平(武汉艾德衡器有限公司);DHC-9143BS电热鼓风干燥箱(苏州江东精密仪器有限公司);UV1100紫外分光光度计(上海美谱达仪器有限公司);DK-8D水浴锅(上海精宏实验设备有限公司);TG18C高速离心机(江苏凯特实验仪器有限公司);K1100全自动凯氏定氮仪(北京慧龙环科环境仪器有限公司);BCD-529WD1 1HP海尔双开门冰箱(青岛海尔电冰箱总厂);等。
1.3 实验试剂
五水硫酸铜(天津市化工三厂有限公司);18 mol/L硫酸(深圳市安泽科技有限公司);甲基红指示剂(分析纯)、硫酸钾(天津市致远化学试剂有限公司);2%硼酸溶液(江西金诺生物科技有限公司);6 mol/L和12 mol/L盐酸标准溶液(广州和为医药科技有限公司);醋酸溶液(广州臻萃质检技术服务有限公司);酚酞指示剂(南京滴纯生物科技有限公司);氢氧化钠标准溶液(广州市刺水科技有限公司);0.5%茚三酮溶液(上海馨晟试剂有限公司);pH 7的柠檬酸钠缓冲溶液(厦门海标科技有限公司);等。
1.4 葡萄酒泥预处理
1.4.1 除杂
采用加水浸泡的方法,将漂在水面的果皮和果梗等分拣出来。
1.4.2 脱色
精确称取葡萄酒泥50.00 g,按样品与水的比例1∶3加入蒸馏水水洗后放入离心机,10000 r/min转速离心10分钟,经重复水洗、离心,直至葡萄酒泥变为无色。
1.4.3 干燥
将所有酒泥倒入洁净的托盘中,在105 ℃恒温干燥箱中烘至半干,再分别用药匙取出分装到平皿中,烘干至恒重,计算含水量。
1.5 测定方法
1.5.1 葡萄酒泥蛋白质含量的测定
用凯氏定氮法测定葡萄酒泥粗蛋白含量,按照下列公式计算结果。
式中:Y:葡萄酒酒泥蛋白质含量(g/100 g);V:酒泥消耗盐酸的体积(mL);V0:空白消耗盐酸的体积(mL);C:盐酸的浓度(mol/L);m:酒泥的质量(g);0.0140:1.0 mL盐酸标准滴定溶液相当的氮的质量(g)。
1.5.2 酒泥水解液氨基酸含量的测定[8]
1.5.2.1 标准溶液的配制 用分析天平准确称取0.5000 g甘氨酸,用蒸馏水定容至100 mL,即得5.0000 g/L的甘氨酸储备溶液。用移液枪吸取1 mL 5.0000 g/L的甘氨酸储备液于100 mL的容量瓶中,用99 mL缓冲溶液定容,配置成0.0500 g/L的甘氨酸标准溶液。用分析天平称取1.0000 g茚三酮置于200 mL容量瓶中,用丙酮溶液定容至刻度,得到0.5%的茚三酮溶液。
1.5.2.2 标准曲线的绘制 用移液枪分别量取甘氨酸标准溶液0.00 mL、0.50 mL、0.60 mL、0.70 mL、0.80 mL、0.90 mL、1.00 mL于7支试管中并编号,每个容量瓶中分别对应用移液枪加入5.00 mL、4.50 mL、4.40 mL、4.30 mL、4.20 mL、4.10 mL、4.00 mL的pH为7的中性柠檬酸钠缓冲溶液,配成浓度为0.005 g/L、0.006 g/L、0.007 g/L、0.008 g/L、0.009 g/L、0.010 g/L,均加入1 ml的0.5%茚三酮显色剂,于100 ℃水浴半个小时,取出后迅速冷却。此时打开紫外分光光度计预热,冷却后在560 nm处测定,将加入0.00 ml甘氨酸的溶液当作空白值,分别测定另外6个的吸光值。通过测得的吸光值,以甘氨酸的浓度为横坐标,吸光值为纵坐标,应用Excel软件绘制标准曲线和趋势图,得到回归方程为y=188.91x-0.9649(R2=0.997)。
1.6 单因素实验
1.6.1 温度对酒泥蛋白水解度的影响
用分析天平分别称取15份2.0000 g烘干的葡萄酒酒泥,放入圆底烧瓶中,每个烧瓶编号,均加入6.0 mol/L的盐酸溶液20 mL,水解时间均为20 h,设定水解温度为80 ℃、85 ℃、90 ℃、95 ℃、100 ℃,每个温度做3个平行试验,打开水浴锅,设置好温度,将对应温度的烧瓶放置于水浴锅中,摆放好后,在每个烧瓶瓶口处放上一个小漏斗,以免盐酸被蒸干。
待水解时间到,将15个圆底烧瓶取出,迅速降至室温,将水解液全部过滤到对应编号的25.00 mL的容量瓶中,用缓冲溶液定容至刻度处,取滤液5.000 mL(用5.000 mL蒸馏水做空白实验),用移液枪加0.5%茚三酮试剂1.000 mL,在100 ℃水浴10 min,冷却至室温后,测定在560 nm处的吸光值。测得吸光值的数据,根据下列公式计算氨基酸的含量,确定酒泥蛋白盐酸水解的最适温度。
式中Y为水解得到的氨基酸含量(mg/g);m为葡萄酒酒泥测定样品的质量(g);C为根据标准曲线回归方程计算的氨基酸的浓度(mg/mL)。
1.6.2 水解时间对酒泥蛋白水解度的影响
用1.6.1同样的方法取样后,分别加入6.0 mol/L的盐酸溶液20 mL,水解的温度均为90 ℃,水解的时间为12 h、14 h、16 h、18 h、20 h。做酸水解试验,用茚三酮测定氨基氮法测得的吸光值,通过公式计算得出氨基酸的含量,以确定蛋白质酸水解的最适时间。
1.6.3 盐酸浓度对酒泥蛋白水解度的影响
用浓度与物质的量的公式,分别算出用6.0 mol/L、12.0 mol/L的盐酸溶液配制出5.0 mol/L、5.5 mol/L、6.0 mol/L、6.5 mol/L、7.0 mol/L的盐酸溶液需要加蒸馏水的体积,用量筒量取,再将浓盐酸用玻璃棒引流至烧杯中,放至室温,倒入盐酸试剂瓶中备用。
用分析天平称取15份1.0000 g酒泥放入圆底烧瓶中,分别取5.0 mol/L、5.5 mol/L、6.0 mol/L、6.5 mol/L、7.0 mol/L的盐酸溶液20 mL,温度为90 ℃,水解时间为16 h,进行酸水解试验,得出酸水解的最佳浓度。
1.7 葡萄酒泥酸水解正交实验
根据单因素实验的结果,设计正交实验:取最适的点和它左右两边的点作为三因素三水平实验的数据,按照正交实验表2和表3进行实验,三组平行。
2 结果与讨论
2.1 凯氏定氮法测定结果
结果见表1。通过公式计算得出,凯氏定氮法测得的粗蛋白含量为19.26 g/100 g。
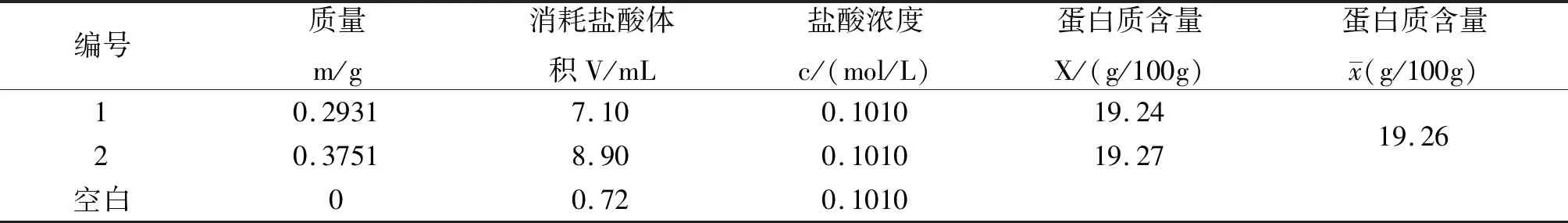
表1 凯氏定氮法结果
2.2 单因素实验结果
2.2.1 温度对水解率的影响
结果见图1。通过图1可以看出,随着温度的升高,氨基酸含量也越来越高,90℃时达最高,随后氨基酸含量下降。说明90 ℃是酒泥蛋白反应的最适温度,氨基酸含量最高(144.58 mg/g),蛋白质水解率达到了75.07%。在80 ℃、85 ℃时比90 ℃时测得的氨基酸含量少,可能是因为在较低温度时,蛋白质并不能完全水解,所以氨基酸得率较低;在95 ℃、100 ℃、105 ℃时,温度升高氨基酸含量却降低,可能是在较高温度时蛋白质水解产物有部分遭到了破坏。
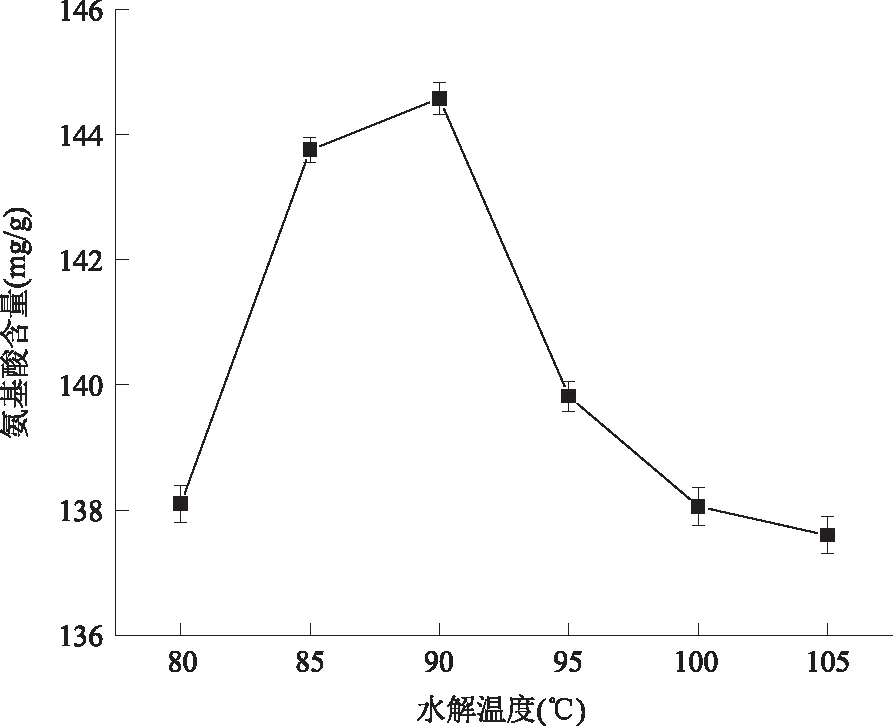
图1 水解温度对氨基酸含量的影响
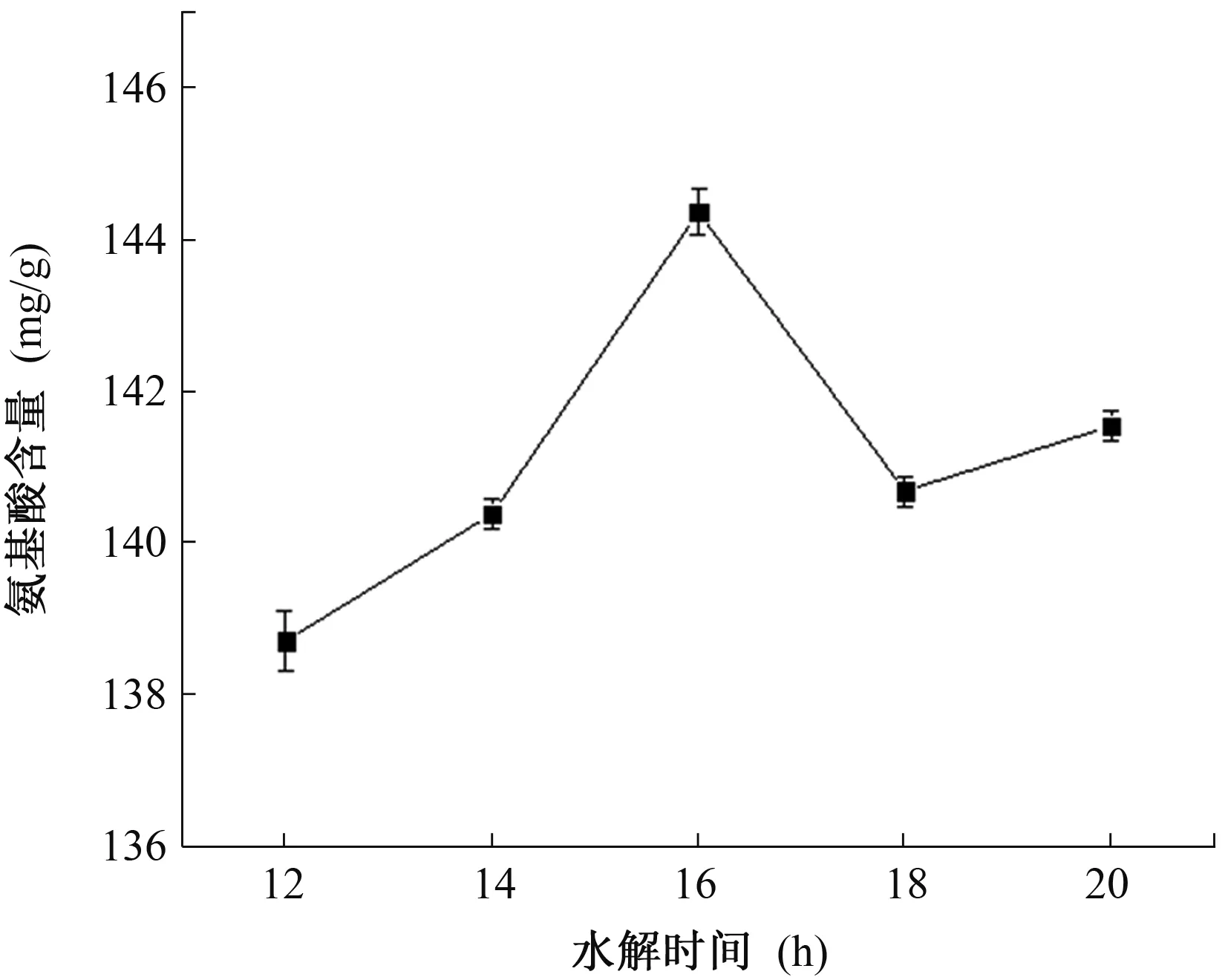
图2 水解时间对氨基酸含量的影响
2.2.2 时间对水解率的影响
结果见图2。通过图2可以看出,水解时间延长,水解得到的氨基酸含量也在增加,水解时间达到16 h后,氨基酸含量不再上升,反而下降,表明酒泥蛋白水解的最佳时间为16 h,氨基酸含量为144.37 mg/g,蛋白质水解率为74.96%。在12 h、14 h时,蛋白质水解成氨基酸的含量较16 h低,可能是因为时间短,蛋白质不能充分水解;在18 h、20 h时,水解的氨基酸含量比16 h低,可能是因为水解时间长导致其他物质也被水解出来或水解出来的氨基酸遭受到一定的破坏所致,在20 h时可以看到比18 h时有略微的上升,但此时斜率已经没有14 h~16 h水解蛋白质的斜率高,所以16 h仍是最佳的水解时间。
2.2.3 盐酸浓度对水解率的影响
结果见图3。由图3可以看出,在盐酸的浓度为6.5 mol/L时,氨基酸含量最高,为146.09 mg/g,蛋白质水解率达到了75.85%。此为酸水解的最适盐酸浓度。氨基酸的含量在盐酸浓度5.0 mol/L、5.5 mol/L、6.0 mol/L时较6.5 mol/L低,可能是因为酸的浓度不够,水解产物不完全;在7.0 mol/L时比6.5 mol/L低,浓度升高,氨基酸含量却下降,可能是因为在酸度过高时,水解得到的氨基酸部分被破坏。
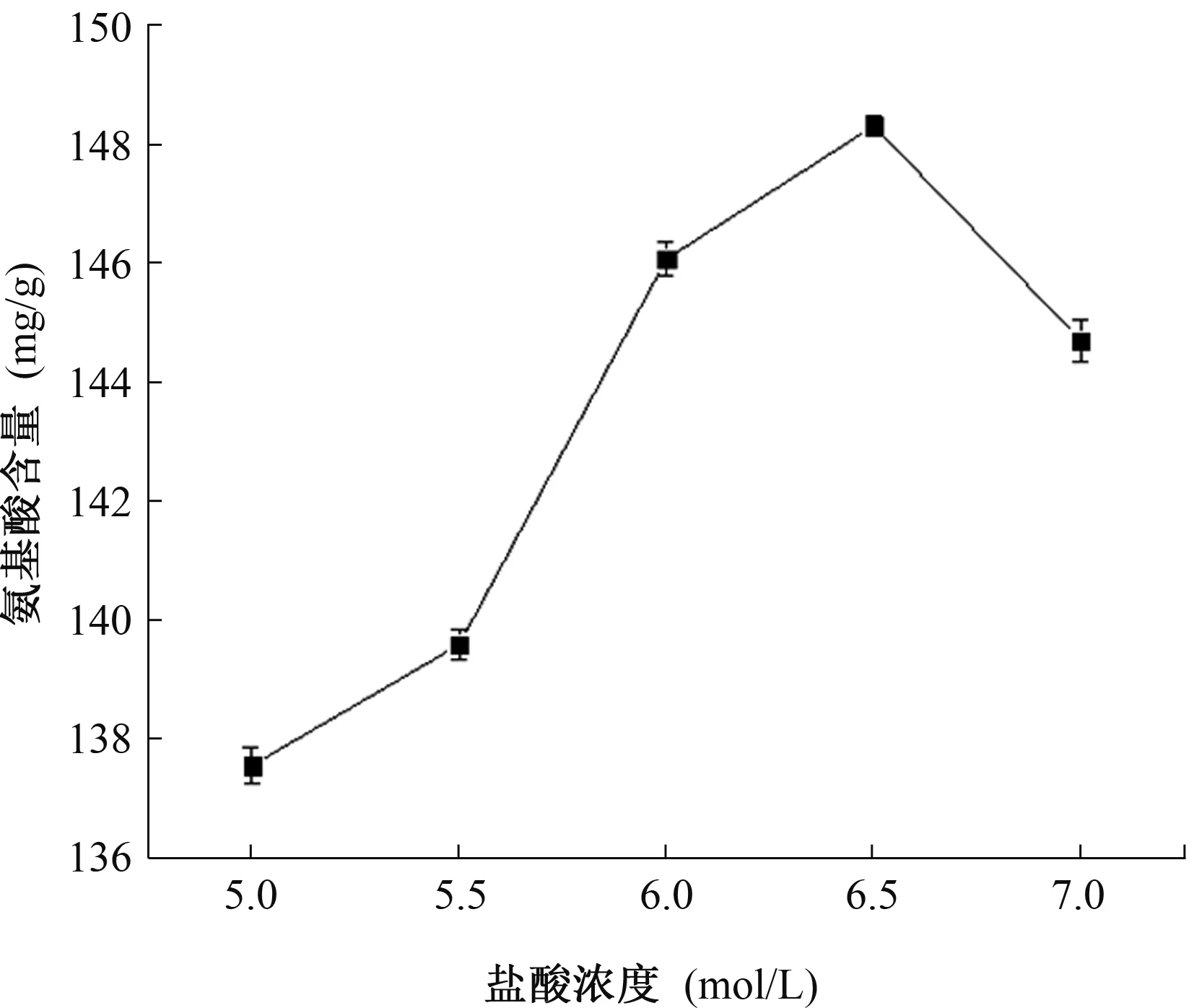
图3 盐酸浓度对氨基酸含量的影响
2.3 正交实验结果
正交实验的因素水平见表2。
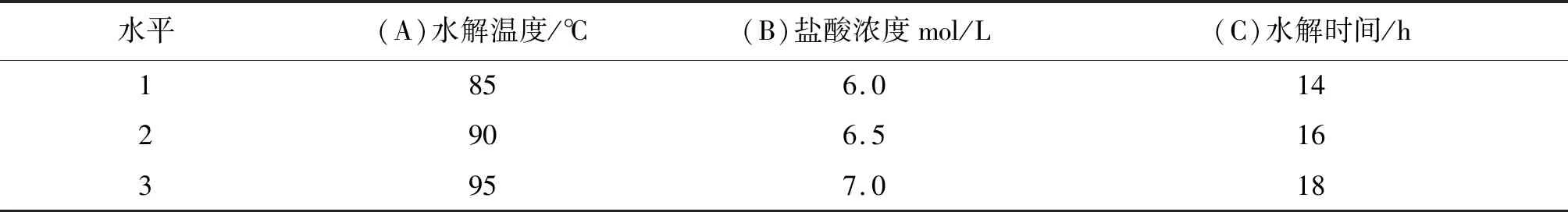
表2 因素水平表
正交实验设计及结果见表3。
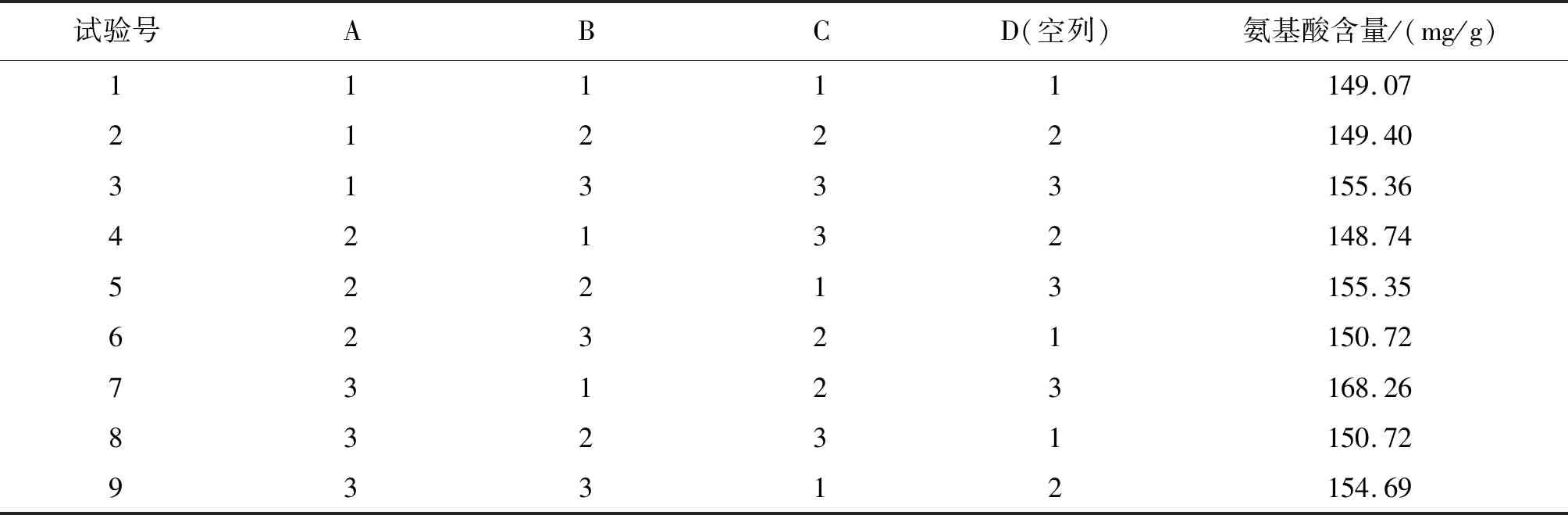
表3 正交设计及结果
正交实验方差分析见表4。

表4 正交实验方差分析
正交实验主体间效应检验见表5。
用SPSS 26数据分析软件对正交实验的结果进行方差分析和主效应检验,从表3、表4、表5的结果可以看出三种因素影响的主次顺序为:水解温度>水解时间>酸的浓度。提取葡萄酒酒泥氨基酸的最优组合为:A3C2B1,即水解的温度为95 ℃,水解的时间为14 h,盐酸的浓度为6.5 mol/L。通过表4和表5可以看出水解的温度和时间对氨基酸水解的影响较为显著。采用最优组合条件,氨基酸产量为168.26 mg/g,水解率达到了87.36%,在此条件下得到的氨基酸含量比正交实验中其他各组的结果都高,证明这个组合即为葡萄酒酒泥氨基酸制备的最佳工艺条件。

表5 正交实验主体间效应检验
3 结论
采用酸水解法水解酒泥蛋白,研究水解温度、时间、酸的浓度三个因素对葡萄酒酒泥蛋白质水解的影响。实验结果表明,酒泥蛋白水解的最适条件为:温度90 ℃、时间16 h、盐酸浓度6.5 mol/L。由正交实验可知,酒泥蛋白水解的最佳条件为:水解温度95 ℃,水解时间14 h,盐酸浓度6.5 mol/L。在此条件下酒泥蛋白水解液的氨基酸含量可达到168.26 mg/g,水解率达到了87.36%。对葡萄酒泥蛋白质其它水解方法的水解条件和水解效果以及葡萄酒泥的开发途径尚待进一步研究与探索。

