QuEChERS-超高效液相色谱-三重四极杆串联质谱法检测保健茶中18种违禁添加药物
甘凝岚,朱晓军,李洁莉,周玮,刘长宇
QuEChERS-超高效液相色谱-三重四极杆串联质谱法检测保健茶中18种违禁添加药物
甘凝岚,朱晓军*,李洁莉,周玮,刘长宇
江苏省产品质量监督检验研究院,江苏 南京 210007
建立了超高效液相色谱-三重四极杆串联质谱同时检测保健茶中西布曲明等18种违禁添加药物的方法。样品经1%甲酸-甲醇溶液超声提取20 min,采用QuEChERS分散固相萃取试剂盒净化,以0.1%甲酸-乙腈溶液为流动相,0.2 mL·min-1流速梯度洗脱,经Agilent ZORBAX Eclipse Plus-C18柱分离,电喷雾离子源正离子扫描,多反应监测模式测定,外标法定量。结果表明,18种违禁添加药物在保健茶基质中的线性良好,相关系数均大于0.999,方法检出限为0.5~5.0 μg·kg-1,方法定量限为2~18 μg·kg-1,RSD为0.5%~5.1%,加标回收率为87.3%~103.8%。运用本方法检测了30批次保健茶样品,其中7批次为阳性样。本方法针对性强、操作简便、准确度高、检测速度快,适用于保健茶中18种违禁添加药物含量的测定,为保健茶的质量控制和安全评价提供科学依据。
超高效液相色谱-三重四极杆串联质谱;QuEChERS;保健茶;违禁药物
保健茶是以普通茶叶为基料,强化某些营养元素或配有适量食药同源或国家规定可以用于保健品的植物类产品,具有保健功能和饮用价值的茶叶再加工产品[1]。随着人们养生意识的不断增强,保健茶已成为保健品市场的新亮点。由于保健茶对健美减肥、降低血压血脂、预防动脉硬化、调节人体新陈代谢、预防三高、抗老防衰等有特殊的保健效果,因此深受广大消费者喜爱。市场需求促进了保健茶产业的迅速发展,目前,国内生产的保健茶已有数百种,产品种类繁多,质量参差不齐,极少数不良商家为牟利,在保健茶中随意添加能快速见效的化学药物来吸引消费者[2-3]。而这些化学药物副作用大,服用时必须严格遵循医嘱,否则长期大量食用会对身体造成严重损害[4-5]。因此,保健茶市场亟需一种快速有效的检测方法来确保保健茶产品的食用安全,促进保健茶产业良好的发展。
QuEChERS(Quick、Easy、Cheap、Effective、Rugged、Safe)方法,是近年来国际上最新发展起来的一种用于农产品检测的快速样品前处理技术,由美国农业部Anastassiades教授等人于2003年开发。该方法最常用于食品中农药残留的检测,一般分为QuEChERS提取试剂盒和净化试剂盒,采用的QuEChERS净化试剂盒是将多种固相吸附剂混合后,达到一次性除去包括脂类、蛋白、着色剂、糖类、有机酸等多种基质干扰物的净化方式,以获得纯净的目标化合物。这种高效的前处理方法现已广泛应用于各种检测领域[6-7]。由于保健茶基质较为复杂,应用QuEChERS试剂盒净化能大大缩短样品前处理时间,有效消除基质干扰,保护检测仪器,提高检测准确度。现今,国内外对检测保健食品违禁添加药物的方法有很多[8-11],而针对保健茶中违禁添加药物检测方法的研究相对较少。据文献报道,常用的检测方法有:薄层色谱法[12-13]、高效液相色谱法[14-16]等,此类方法存在操作复杂、应用范围窄、灵敏度低、准确性差等缺陷;然而已有的色谱-质谱法[17-19]对于保健茶的检测项目较少、检测耗时较长,已经不能满足当前保健茶市场的监管要求。
本试验根据国家市场监管总局对保健食品违禁添加药物的检验要求,针对保健茶中最常添加的减肥类、降血压类、降血脂类、降血糖类、改善睡眠功能类等18种违禁添加药物进行检测[20]。
本研究优化了样品前处理方法,采用QuEChERS试剂盒净化,经超高效液相色谱-三重四极杆质谱(UPLC-MS-MS)进行分析检测。本方法操作简便、灵敏度高、准确性强,从而有效提高保健茶中违禁添加药物的检验效率和定性准确度,为新形势下的保健茶监管提供有效的技术支持。
1 材料与方法
1.1 试验试剂与标准品
试剂:甲醇(分析纯,国药集团)、乙腈(分析纯,国药集团)、甲酸(色谱纯,美国MREAD公司)、甲醇(色谱纯,美国MERCK公司)、乙腈(色谱纯,美国MERCK公司)、超纯水、QuEChERS分散固相萃取试剂盒(5982-0028,美国Agilent公司);18种违禁添加药物标准品信息详见表1。
1.2 试验仪器
本试验所用仪器设备信息见表2。
1.3 试验方法
1.3.1 超高效液相色谱条件
色谱柱:Agilent ZORBAX Eclipse Plus-C18柱,规格100 mm×2.1 mm,3.5 µm;柱温:40℃。流动相:A为0.1%甲酸水溶液,B为乙腈溶液,流动相洗脱梯度为0 min时90%A,7 min时10%A,9 min时保持10%A,9.1 min时90%A,12 min时保持90%A;流速0.2 mL·min-1;进样量2 µL。
1.3.2 三重四极杆质谱参数
离子源:Turbo V电喷雾离子源(ESI);扫描模式:多反应监测(MRM)模式,正离子扫描;气帘气(CUR):12 psi;碰撞气(CAD):12 psi;喷雾电压(IS):5 500 V;离子源温度:600℃。18种化合物的质谱优化信息见表3。

表1 18种违禁添加药物标准品信息

表2 试验所用仪器设备信息

表3 18种药物离子对信息及质谱参数
注:a.定量离子;b.定性离子
Note: a. quantitative ion. b. qualitative ion
1.4 样品处理
1.4.1 标准溶液制备
标准品储备液的配制:将18种违禁添加药物分别称取1~5 mg,至于10 mL容量瓶中,各加入一定量甲醇超声溶解后定容,均配制成质量浓度约为0.1~5 mg·mL-1的单标准品储备液,并保存于–20℃冰箱中。
混合标液的配制:分别吸取0.1~1 mL 18种单标准品储备液于1个50 mL容量瓶中,用甲醇稀释混匀后定容,配置质量浓度为10~100 μg·mL-1的混合标准品溶液,待使用时进一步稀释。
1.4.2 样品的前处理
均质:将茶叶样品彻底粉碎(无可见样品碎片),得到均质样品后称量。
提取:称取均质样品约0.1 g,于50 mL离心管中,加入含1%甲酸的甲醇溶液定容至50 mL,摇匀,在室温下超声提取20 min后,以8 000 r·min-1离心5 min,取上清液待净化。
净化:取上清液2 mL于QuEChERS分散固相萃取试剂盒离心管(含混合试剂粉末)中,盖上盖子,剧烈振摇30 s,以确保上清液和试剂粉末充分接触,样品管以12 000 r·min-1高速离心3 min。取上清液过0.22 μm有机滤膜后待测。
2 结果与分析
2.1 提取试剂的选择
《国家食品安全监督抽检实施细则(2020年版)》(以下简称《细则》)中规定了保健食品中违禁添加药物的检测方法[21-22],这些标准方法在检测不同种违禁添加药物时需采用不同的提取试剂,其中包括三氯甲烷、甲醇、乙腈、50%甲醇溶液、乙酸铵-乙腈混合溶液等。提取试剂种类过多,导致在检测多种违禁添加药物时试验操作繁琐。相关文献资料[23]中,常用甲醇或乙腈作为提取试剂,本研究考虑到检测的化合物多为碱性化合物,在有机溶剂中加入了少量甲酸作为提取试剂。试验研究了甲醇、乙腈、1%甲酸-甲醇溶液对保健茶中18种违禁添加药物同时提取的效果。试验将同一空白保健茶样品分为3份,加入相同浓度的混合标液后,分别用甲醇、乙腈、1%甲酸-甲醇溶液3种溶剂提取,其余前处理步骤按照1.4.2章节进行,根据1.3章节仪器条件检测,比较3种提取试剂的加标回收率(图1)。
试验结果表明,甲醇对18种违禁添加药物提取率高于乙腈,在用1%甲酸-甲醇作为提取剂时18种物质的提取率均高于甲醇和乙腈。试验证明加入少量甲酸有助于提高目标化合物在有机溶剂中的溶解度,因此,试验最终选择1%甲酸-甲醇溶液作为样品提取试剂。
2.2 提取方法的优化
根据《细则》中规定的检测方法[24-25],有些保健食品违禁添加药物的提取方法采用水浴摇床或手动剧烈振荡的方式,还需反复多次提取才能将目标物质提取完全。这样的方法既费时费力,提取效果也很难保证。因此,本试验选用超声提取的方式,在缩短提取时间的同时也提高了目标物质的提取率。参照文献[26],明确了在超声提取10、20、30 min时18种违禁添加药物回收率的情况,从而选出最佳的超声提取时间。对3份同一加标空白样品,采用10、20、30 min时间超声提取,其他前处理方法(1.4.2章节)及仪器条件(1.3章节)不变,考察3个超声提取时间对18种违禁添加药物回收率的影响(图2)。试验结果表明,保健茶样品在超声提取10 min后的目标物质回收率均明显低于20 min和30 min,而样品在超声提取20 min后目标物质的回收率与超声提取30 min无明显差别,即样品在超声20 min后目标物提取已完全。因此,本研究选用20 min为样品超声提取时间。

图1 不同提取溶剂的试验结果
2.3 净化方式优化
按照标准规定的检测保健食品违禁添加药物的方法[27-28]和相关研究文献显示,样品提取液大多经滤纸过滤净化或直接过0.22 μm滤膜待测。由于保健茶基质比较复杂,滤纸对大分子化合物的净化效果不佳,且目标物会较多的吸附在滤纸上造成残留;提取液直接过膜,滤液中依然有较多色素、有机酸等杂质,无法有效降低检测时的基质干扰,影响检测的准确度。净化不完全不仅对目标物检测有影响,也会对检测仪器造成污染,降低仪器灵敏度。本研究采用QuEChERS分散固相萃取试剂盒对保健茶样品进行净化。试剂盒中含有多孔固相萃取吸附剂(PSA,C18,GCB)和MgSO4,其中PSA(Primary secondary amine)能去除有机酸、糖类;GCB(Graphitizing of carbon black)能去除叶绿素等大部分色素;C18(Octadecylsilyl)能去除脂类;MgSO4能去除多余水分。因此,用QuEChERS试剂盒净化能有效降低基质干扰,确保检测准确性。本研究考察了在空白茶叶基质中加入一定浓度的混合标准品溶液,经QuEChERS试剂盒净化后,空白茶叶基质中18种目标化合物的加标回收情况如图3所示。结果表明,空白茶叶样品基质经QuEChERS试剂盒净化后18种药物回收率均较高,该方法能简单、快捷、有效地净化保健茶中的干扰杂质,且不吸附目标化合物。
2.4 18种化合物的质谱信息
将1 µg·mL-1的混合标准溶液进行扫描(Scan)模式,根据18种目标化合物的分子量,确定扫描质量范围,分别找出每种物质的最佳母离子质荷比(Q1)。根据获得的Q1,进行子离子(Q3)的扫描,选择相应较高干扰较少的两个离子对作为定量和定性离子对,分别优化他们的碰撞能量(CE)和去簇电压(DP)。在MRM模式下[29-30],采用正离子扫描,确定18种化合物的出峰时间。18种违禁添加药物的总离子流色谱图如图4所示;各化合物定量离子对MRM离子流色谱图如图5所示。

图2 不同超声提取时间的试验结果

图3 茶叶基质中的18种药物的加标回收率
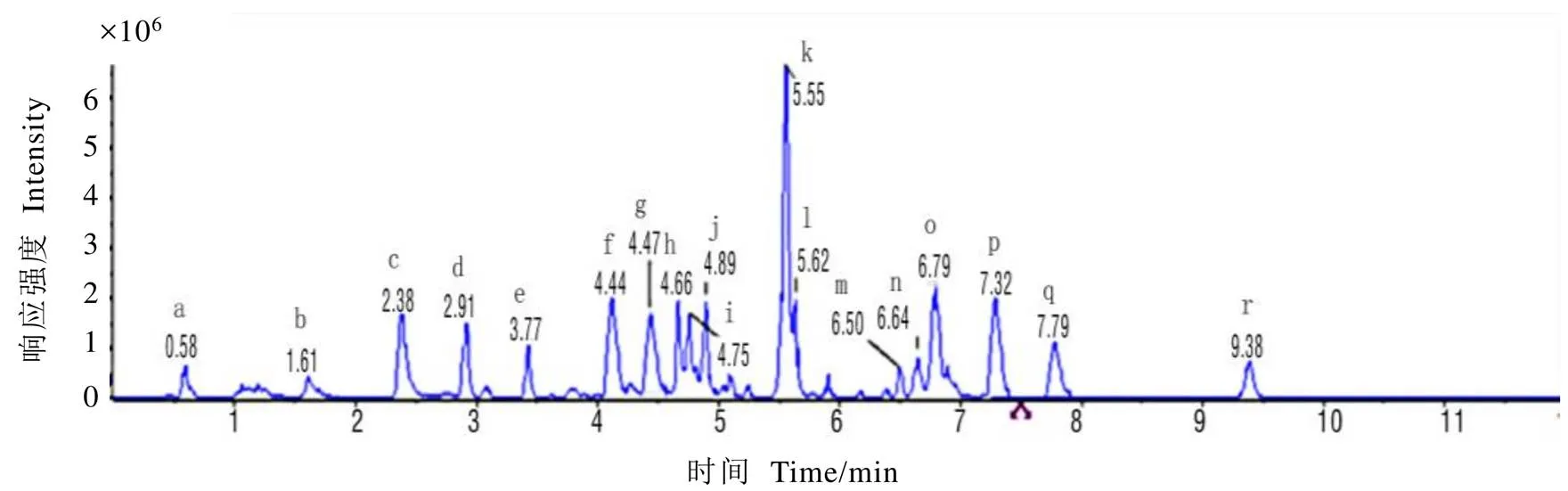
注:a. 盐酸二甲双胍;b. 麻黄碱;c. 盐酸苯乙双胍;d. 褪黑素;e. 哌唑嗪;f. 芬氟拉明;j. 酚酞;h. 阿普唑仑;i. 三唑仑;g. 格列苯脲;k. 瑞格列奈;l. 罗通定;m. 尼莫地平;n. N,N-双去甲基西布曲明;o. N-单去甲基西布曲明;p. 洛伐他汀;q. 辛伐他汀;r. 西布曲明
2.5 标准物质检出限、定量限、线性关系和仪器精密度检测结果
将配制好的混合标准溶液加入空白保健茶样品中,稀释后按照1.3章节条件下的MRM模式进行测定,以各化合物的3倍信噪比(S/N)和10倍信噪比时计算,得到18种违禁添加药物的方法检出限和定量限。将配制好的混合标准溶液,稀释成5个梯度浓度的标准工作液,按照1.3章节方法测定,分别以浓度为横坐标(),峰面积为纵坐标(),绘制标准曲线。选取配制好的标准工作液低、中、高3个梯度浓度,按照1.3章节仪器方法检测,每个梯度溶液平行测定6次,以测得的峰面积计算出相对偏差(RSD),获得18种标准物质的精密度(n=6)。其检出限、定量限、线性范围、标准曲线方程、相关系数见表4。试验结果表明,18种违禁添加药物在其相应的线性范围内,线性相关系数(2)均大于0.999,线性良好。18种目标物质的RSD为0.5%~5.1%,均小于6%,仪器精密度良好。

注:1. 盐酸二甲双胍;2. 麻黄碱;3. 盐酸苯乙双胍;4. 褪黑素;5. 哌唑嗪;6. 芬氟拉明;7. 酚酞;8. 阿普唑仑;9. 三唑仑;10. 格列苯脲;11. 瑞格列奈;12. 罗通定;13. 尼莫地平;14. N,N-双去甲基西布曲明;15. N-单去甲基西布曲明;16. 洛伐他汀;17. 辛伐他汀;18. 西布曲明

表4 18种标准物质检出限、线性范围、标准曲线方程、相关系数
2.6 加标回收试验结果
根据18种化合物的线性范围和样品前处理稀释倍数,在保健茶空白样品中分别加入低、中、高3个浓度梯度的18种混合标准品溶液分别为40、80、200 μg·g-1,每个梯度检测3组平行样品。样品按照1.4.2章节的方法前处理,根据1.3章节仪器方法进行回收率测定,从而计算出18种违禁添加药品的加标回收率(n=3)及相对标准偏差(RSD),结果见表5。试验表明,18种违禁添加药物的回收率为87.3%~103.8%,相对标准偏差(RSD)为1.9%~4.6%,均小于5.0%,方法精密度良好。
2.7 基质效应考察结果
将配制好的混合标准溶液,用甲醇和保健茶空白基质溶液(按1.4.2章节的方法前处理)分别稀释成5个梯度浓度的标准工作液,按1.3章节仪器方法检测,得到18种化合物在甲醇溶液和保健茶空白基质溶液中的标准曲线斜率。采用相对响应值法比较,基质效应Matrix Effect (%)=/×100,其中为溶剂标曲的斜率,基质标曲的斜率[31-32]。计算出18种化合物在茶叶基质中的基质效应(表5)。结果表明,经1.4章节方法前处理后,18种化合物的基质效应为0.88~1.09,基质对化合物的干扰较小。
2.8 稳定性试验结果
将混合标准溶液用保健茶空白基质溶液(按1.4.2章节方法前处理)稀释成质量浓度为20、100、500 μg·kg-1的低、中、高3个浓度梯度,放置于室温环境中,每0、4、8、12、16、24 h按照1.3章节仪器方法各测定一次,18种化合物的每个梯度浓度检测6个时间点,根据测得的6个时间点峰面积的相对标准偏差(RSD),分别得到低、中、高3个浓度梯度的RSD:低浓度为0.5%~4.9%,中浓度为0.7%~4.6%,高浓度为0.2%~4.1%,均小于5%(表6)。试验结果表明,18种混合标准溶液在24 h内稳定。

表5 18种标准物质在茶叶基质中的加标回收率(n=3)

表6 18种化合物保健茶基质标准溶液的稳定性
2.9 样品检测
本研究共检测了市面上常见的保健茶样品30批次,将样品按1.4.1章节方法前处理后根据1.3章节仪器方法进行检测,采用外标法定量。将测得的目标化合物的峰面积与基质标准曲线相对照,得到样品中18种目标化合物的含量。检测结果显示,30批次样品中共检出7批次阳性样品,其中-单去甲基西布曲明、褪黑素、哌唑嗪各检出1批次,含量分别为:310.7、88.8、326.3 μg·g-1;酚酞和盐酸二甲双胍各检出2批次,其中酚酞含量分别为94.8、64.8 μg·g-1,盐酸二甲双胍含量分别为120.6、51.3 μg·g-1。
3 讨论
保健茶种类较多,有减肥类、改善睡眠类、辅助降血压类、辅助降血糖类等,抽检实施细则(2020版)中规定的方法要将保健茶中违禁添加药物进行分类检测,相关文献也较少有针对保健茶中多种类违禁添加药物同时检测的方法。本研究建立了一种能同时检测保健茶中18种违禁添加药物的方法,包括对提取溶剂、提取方法、净化方式和仪器方法的研究。
3.1 提取溶剂的研究
相关标准方法对保健茶中18种化合物分别采用不同溶剂进行提取,造成提取试剂种类过多;文献中常用甲醇或乙腈作为提取溶剂,但没有两种溶剂对18种化合物提取率的比较。本研究考虑到所检测的化合物多为碱性,在有机溶剂中加入少量酸有助于提高溶解度,因此,研究了甲醇、乙腈、1%甲酸-甲醇溶液对保健茶中18种化合物同时提取的效果。本研究结果表明,甲醇提取率高于乙腈,而1%甲酸-甲醇溶液的提取率最高,选择其作为提取试剂有效提高了18种化合物在保健茶中的提取率。
3.2 提取方法的研究
细则中规定的检测方法对保健茶中18种违禁添加药物多采用水浴摇床或手动振荡的方式进行提取,费时费力,且也很难保证提取效果;文献中常用超声提取方式,但未研究合理的提取时间。本方法研究了超声提取10、20 min和30 min对保健茶中18种化合物提取率的影响。试验结果表明,超声提取20 min能在确保18种目标化合物提取效率的同时,进一步缩短试验时间,提高前处理效率。
3.3 净化方式的研究
相关标准及文献方法中,保健茶提取液常用滤纸过滤或直接过0.22 μm滤膜的方式净化。滤纸的净化效果不佳,且目标物残留较多;提取液直接过膜,滤液中依然有较多色素、有机酸等杂质,净化不完全还会对检测仪器造成污染,降低灵敏度。本方法采用含有多孔固相萃取吸附剂的QuEChERS净化试剂盒,能去除保健茶中的有机酸、叶绿素、水分、糖分等杂质。结果表明,经QuEChERS净化试剂盒净化后,保健茶中18种化合物加标回收率均较高,因此,该净化方法在确保目标物不被吸附的同时能有效降低检测时的基质干扰,提高准确度。
3.4 仪器方法建立的研究
按照相关标准方法的要求,保健茶中违禁添加药物的仪器检测,要依次经过薄层色谱筛查、液相定量、液质验证3个步骤,导致方法种类繁多,操作重复性大,结果时效性差;在相关文献中,检测保健茶中违禁添加药物的种类较少,仪器方法耗时较长。本方法采用超高效液相色谱-三重四极杆质谱(UPLC-MS-MS)法,在12 min内可同时对保健茶中18种化合进行定性定量分析,在确保高灵敏度、高准确性的同时,提升检验速度,针对性更强。
本研究建立的方法,具有操作简便、回收率高、稳定性好、准确性强的优势,适用于保健茶中18种违禁添加药物的快速检测,为有效地监管日益扩大的保健茶市场,提供了技术支持和科学保障。
[1] 中华人民共和国国家出入境检验检疫局. 出口保健茶检验通则: SN/T 0797—2016[S]. 北京: 中国标准出版社, 2016. State Entry-Exit Inspection and Quarantine Bureau of the People's Republic of China. General rules for inspection of health tea for export: SN / T 0797-2016 [S]. Beijing: China Standards Press, 2016.
[2] 蒋玉婷, 姜华, 郑健, 等. 保健食品市场现状分析及前景展望[J]. 食品研究与开发, 2013, 34(22): 78-80.Jiang Y T, Jiang H, Zheng J, et al. Health food market analysis and prospects [J]. Food Research and Development, 2013, 34(22): 78-80.
[3] 宁霄, 张伟清, 王钢力, 等. 保健食品中非法添加药物的检测现状及筛查策略研究[J]. 食品安全质量检测学报, 2015, 6(5): 1876-1882.Ning X, Zhang W Q, Wang G L, et al. Detection status and screening strategy of illegally added drugs in healthy food [J]. Journal of Food Safety and Quality, 2015, 6(5): 1876-1882.
[4] 岳琳, 谭有能, 粟芳. 中成药中非法添加化学药物的种类、危害、原因和对策[J]. 全科护理, 2012, 10(15): 1406-1407. Yue L, Tan Y N, Su F. Types, hazards, causes and countermeasures of illegally added chemical drugs in Chinese patent medicines [J]. General Nursing, 2012, 10(15): 1406-1407.
[5] 丁辉. 肥胖与高血脂病关系调查分析[J]. 中国卫生产业, 2017(17): 183-184. Ding H. Investigation and analysis of the relationship between obesity and hyperlipidemia [J]. Chinese Health Industry, 2017(17): 183-184.
[6] 陈林, 温家欣, 吴霞, 等. 改良QuEChERS技术结合液相色谱-串联质谱联用法同时快速检测辣椒制品中14种非法添加工业染料[J]. 食品科学, 2017, 38(8): 296-302. Chen L, Wen J X, Wu X, et al. Rapid simultaneous determination of 14 adulterated industrial dyes in chilli products by a modified QuEChERS method coupled with LC-MS/MS [J]. Food Science, 2017, 38(8): 296-302.
[7] 丁博, 王志元, 谢建军, 等. QuEChERS前处理技术联合液相色谱-四极杆飞行时间质谱法检测保健食品24种违禁降血糖、降血压和降血脂药物[J]. 色谱, 2016, 34(6): 583-590. Ding B, Wang Z Y, Xie J J, et al. Determination of 24 antihyperglycemic,antihypertensive and antihyperlipidemic drugs illegally added in health food samples by liquid chromatography-quadrupoletime of flight mass spectrometry [J]. Chinese Journal of Chromatography, 2016, 34(6): 583-590.
[8] 马祖兵, 孙强, 李小芳, 等. 红曲降脂成分他汀类物质检测方法的研究进展[J]. 中国实验方剂学杂志, 2017, 23(23): 228-234. Ma Z B, Sun Q, Li X F, et al. Detection methods of lipid-reducing statins ingredients from fermentum rubrum [J]. China Journal of Experimental Traditional Medical Formulae, 2017, 23(23): 228-234.
[9] 鲁涓. 液质联用技术在检测中成药及保健食品非法添加中的应用[J]. 海峡药学, 2015, 27(8): 80-82. Lu J. Application of liquid chromatography-mass spectrometry in the detection of illegal addition of Chinese patent medicines and health food [J]. Strait Pharmaceutical Journal, 2015, 27(8): 80-82.
[10] Xu S, Jin P F, Xu W F, et al. Research advances on analytical technologies of illegally adulterated chemical sub-stances in medicines for invigorants [J]. Northwest Pharm J, 2017, 32(5): 677-680.
[11] Li M J, Ma H Y, Gao J L, et al. Rapid screening of nonsteroidal anti-inflammatory drugs illegally added in anti-rheumatic herbal supplements and herbal remedies by portable ion mobility spectrometry [J]. Journal of Pharmaceutical and Biomedical Analysis, 2017, 145: 203-208.
[12] 吴泽君, 刘水平, 郭世明. 减肥食品及保健食品中非法添加化学药物酚酞、盐酸西布曲明的探索性检测[J]. 中国药师, 2011, 14(4): 517-520. Wu Z J, Liu S P, Guo S M. Exploratory detection of chemical drugs phenolphthalein and sibutramine hydrochloride added illegally into slimming food and health food [J]. China Pharmacist, 2011, 14(4): 517-520.
[13] 王铁松, 仝禹, 郑洁, 等. 薄层色谱法快速筛查降脂、降压、止咳平喘类中药制剂中的29 种添加化学药物[J]. 中国药学杂志, 2010, 45(11): 857-861. Wang T S, Tong Y, Zheng J, et al. Detection of 29 adulterations in lipid-regulating, antihypertensive, antitussive and antiasthmatic herbal remedies by TLC [J]. Chinese Pharmaceutical Journal, 2010, 45(11): 857-861.
[14] Yan Q R, Wu W K. Application of ultra performance liquid chromatography in the analysis of prohibited substances,restricted substances and functional ingredients in cosmetics [J]. China Pharm Aff, 2017, 31(1): 74-77.
[15] Guo P Q, Xu X Y, Chen G N, et al. On-line two dimensional liquid chromatography based on skeleton type molecularly imprinted column for selective determination of sulfonylurea additive in Chinese patent medicines or functional foods [J]. Journal of Pharmaceutical and Biomedical Analysis, 2017, 146: 292-301.
[16] 郑勤琴, 项勋, 段纲, 等. 高效液相色谱和超高效液相色谱在药物分析中的应用研究[J]. 上海畜牧兽医通讯, 2017, 2: 57-59. Zheng Q Q, Xiang X, Duan G, et al. Application of high performance liquid chromatography and ultra performance liquid chromatography in drug analysis [J]. Shanghai Journal of Animal Husbandry and Veterinary Medicine, 2017, 2: 57-59.
[17] 张娜. 高效液相色谱-串质谱法在保健食品检测中的应用研究进展[J]. 广东化工, 2016, 43(10): 207-208. Zhang N. Application of the detection in health food by high performance liquid chromatography-mass spectrometry [J]. Guangdong Chemical Industry, 2016, 43(10): 207-208.
[18] Liu F Y, Zhang X F, Li Y Q, et al. Simultaneous screening anddetermination of eight tetracycline antibiotics illegally adulterated inherbal preparations using HPLC-DAD combined with LC-MS-MS [J]. Chromatographia, 2018, 81(2): 303-314.
[19] Huang F, Wu H Q, Huang X L, et al. Simultaneous determination of 17 aphrodisiac chemical drugs illegally added in health products and Chinese patent medicines by high performance liquid chromatography-tandem mass spectrometry [J]. Chin J Chromatogr, 2016, 34(3): 270-278.
[20] 国家市场监督管理总局. 办公室文件: 国家食品安全监督抽检实施细则(2020版)[Z]. (2020-03-04)[2020-05-09].State Administration of Market Supervision and Administration. Office document: Implementation rules for sampling inspection of State Food Safety Supervision (2020 Edition) [Z]. (2020-03-04) [2020-05-09].
[21] 国家食品药品监督管理局. 药品检验补充方法和检验项目批准件(编号2012005): 减肥类中成药和保健食品[Z]. (2012-08-01)[2020-05-09]. State Food and Drug Administration. Approval of supplementary methods and inspection items for drug inspection (No. 2012005): Chinese medicine and health food for weight loss [Z]. (2012-08-01) [2020-05-09].
[22] 国家食品药品监督管理局. 办公室文件(食药监办许[2010]114号): 关于印发保健食品安全风险监测有关检测目录和检测方法的通知[Z]. (2010-11-02)[2020-05-09]. State Food and Drug Administration. Office document (Food and Drug Administration approval No. [2010]114): Notice on the issuance of testing catalogs and testing methods for health food safety risk monitoring [Z]. (2010-11-02) [2020-05-09].
[23] 宫旭, 芦丽, 冯有龙, 曹玲. UPLC-MS/MS法测定减肥降脂通便三类保健食品中添加的37种药物[J]. 药物分析杂志, 2016, 36(5): 918-928. Gong X, Lu L, Feng Y L, Cao L. Determination of 37 drugs illegally added in weight-losing,lipid-lowering and laxative health foods by UPLC-MS/MS [J]. Chinese Journal of Pharmaceutical Analysis, 2016, 36(5): 918-928.
[24] 国家食品药品监督管理局. 药品检验补充方法和检验项目批准件(编号2006004): 治疗肥胖症的中成药[Z]. (2006-03-14) [2020-05-09]. State Food and Drug Administration.Approval of supplementary methods and inspection items for drug inspection (No. 2006004): Chinese patent medicine for treating obesity [Z]. (2006-03-14) [2020-05-09].
[25] 国家食品药品监督管理局. 药品检验补充方法和检验项目批准件(编号2009032): 降压类中成药[Z]. (2009-12-11) [2020-05-09]. State Food and Drug Administration. Approval of supplementary methods and inspection items for drug inspection(No. 2009032): Antihypertensive Chinese patent medicine [Z]. (2009-12-11) [2020-05-09].
[26] 熊爽. 固相萃取-高效液相色谱-串联质谱法同时测定不同基质保健食品中10种减肥药物[J]. 理化检验(化学分册), 2018, 54(2): 142-147. Xiong S. HPLC-MS/MS simultaneous determination of 10 diet drugs in health-care foods of different matrices with solid phase extraction [J]. Physical Testing and Chemical Analysis Part B: Chemical Analgsis, 2018, 54(2): 142-147.
[27] 国家食品药品监督管理局. 药品检验补充检验方法和检验项目批准件(编号2013002): 改善睡眠类中成药和保健食品[Z]. (2013-03-26) [2020-05-09]. State Food and Drug Administration. Approval of supplementary methods and inspection items for drug inspection (No. 2013002): Chinese patent medicine and health food for sleep improvement [Z]. (2013-03-26) [2020-05-09].
[28] 国家食品药品监督管理局. 药品检验补充方法和检验项目批准件(编号2014008): 降压类中成药和辅助降压类保健品[Z]. (2014-04-04)[2020-05-09]. State Food and Drug Administration. Approval of supplementary methods and inspection items for drug inspection(No. 2014008): Antihypertensive Chinese patent medicines and auxiliary antihypertensive health products [Z]. (2014-04-04) [2020-05-09].
[29] 祝伟霞, 张莉, 李睢, 等. 超高效液相色谱-多反应选择离子监测同步在线全扫描质谱技术测定保健品中的类安非他命和匹卡米隆[J]. 色谱, 2016, 34(7): 681-685. Zhu W X, Zhang L, Li S, et al. Determination of-methylphenethylamine and picamilon in health products by ultra performance liquid chromatography-multiple reaction monitoring and online full scan mass spectrometry [J]. Chinese Journal of Chromatography, 2016, 34(7): 681-685.
[30] Paig P, Rodrigues M J E, Correia M, et al. Analysis ofpharmaceutical adulterants in plant food supplements by UHPLC-MS/MS [J]. European Journal of Pharmaceutical Sciences, 2017, 99: 219-227.
[31] Gbylik-Sikorska M, Posyniak A, Sniegocki T, et al. Liquid chromatography-tandem mass spectrometry multiclass method for the determination of antibiotics residues in water samples from water supply systems in food-producing animal farms [J]. Chemosphere, 2015, 119: 8-15.
[32] 杨惠成, 王海鸣, 林绪, 等. 超高效液相色谱-串联质谱法同时测定保健食品中14种功效成分[J]. 现代食品科技, 2018, 34(11): 281-289. Yang H H, Wang H M, Lin X, et al. Simultaneous determination of 14 functional components in health foods by ultra performance liquid chromatography tandem mass spectrometry [J]. Modern Food Science and Technology, 2018, 34(11): 281-289.
Detection of 18 Prohibited Additives in Health-Protecting Tea by QuEChERS Method and Ultra High Performance Liquid Chromatography Triple Quadrupole Tandem Mass Spectrometry
GAN Ninglan, ZHU Xiaojun*, LI Jieli, ZHOU Wei, LIU Changyu
Jiangsu Institute for Product Quality Supervision and Inspection, Nanjing 210007, China
A method for the simultaneous determination of Sibutramine and other 18 prohibited additives in health-protecting tea by ultra high performance liquid chromatography triple quadrupole tandem mass spectrometry (UPLC-MS/MS) was established.Samples were extracted by ultrasonic extraction from 1% formic acid methanol solution for 20 min and purified by QuEChERS dispersive solid-phase extraction kit. The mobile phase was 0.1% formic acid in acetonitrile and 0.2 mL·min-1flow gradient elution was used in Agilent ZORBAX Eclipse Plus-C18column.Electrospray ion source positive ion scanning, multiple reaction monitoring (MRM) mode were determined and external standard method was used for quantification. The results show that the linearity of 18 kinds of illegal additives was good, with the correlation coefficient more than 0.999. The detection limit was 0.5-5.0 μg·kg-1. The quantitative limit of the method was 2-18 μg·kg-1. RSD was 0.5%-5.1% and the recovery rate was 87.3%-103.8%. This method was used to analyze 30 batches of health-protecting tea samples, of which 7 batches were positive samples. This method has strong pertinence,simple operation, high accuracy and fast detection speed. It is suitable for the determination of 18 kinds of forbidden additives in health-protecting tea. This paper also provided a scientific basis for the quality control and safety evaluation of health-protecting tea.
UPLC-MS-MS, QuEChERS, health-protecting tea, contraband drugs
S571.1;O657.63
A
1000-369X(2021)02-237-14
2020-05-09
2020-09-07
国家重点研发计划(2019YFC1605100)
甘凝岚,女,工程师,主要从事食品检测方面的研究,184950171@qq.com。*通信作者:41927970@qq.com
(责任编辑:赵锋)

