硼硅酸盐玻璃固化体蚀变层结构及浸出行为研究
张海洋 吴浪 王宾 姚颖 康泽
(西南科技大学材料科学与工程学院 绵阳 621010)
0 引言
我国玻璃固化工厂处理高放废液(HLLW)采用硼硅酸玻璃,由此产生的高放玻璃固化体需包封在金属容器中进行深地质处置,采用多重屏障系统来限制玻璃固化体中放射性核素与生物圈接触[1-3]。在长期的地质处置过程中很难排除地下水对硼硅酸玻璃固化体的侵蚀,核素的浸出伴随着玻璃固化体蚀变进程。大量研究表明玻璃固化体长期的溶解速率可能与具有微米或纳米级微孔的蚀变层有关,蚀变层的结构是影响核素浸出速 率 的 关 键[4-6]。Ribet等[7]发 现 在 碱 性 溶 液(pH=11.4)中SON68玻璃的溶解速率与蚀变层上的非晶层和结晶矿物相的形成有关。甘学英等[8]采用粉末静态浸泡法(PCT法)研究了硼硅酸盐玻璃固化体的长期蚀变行为,结果表明:Mg、Fe促使了蚀变层页硅酸盐矿物相的形成,从而加速了玻璃的溶解。然而采用短期浸出以及粉末浸泡实验很难揭示玻璃固化体的蚀变进程,关于蚀变层结构随时间变化关系,仍需要进一步深入研究。
目前我国第一座玻璃固化工厂已进入冷调试阶段,不久的将来会生产玻璃固化体,研究玻璃固化体的蚀变行为和抗浸出性能对深地质处置场的安全评价非常重要。本文采用挂片静态浸泡法研究硼硅酸盐玻璃固化体在模拟地下水浸泡364 d的蚀变情况,通过研究蚀变层物相、形貌、成分以及元素浸出随时间变化关系,讨论蚀变层结构对玻璃固化体浸出行为的影响。
1 实验
1.1 样品和浸出剂的制备
1.1.1 样品制备
本实验采用基础玻璃粉和模拟废液混合熔制硼硅酸盐玻璃固化体,废物氧化物包容量为16%,玻璃固化体组成列于表1,其中SO3以NaSO4的形式引入,其他金属氧化物以碳酸盐或硝酸盐的形式引入。首先将基础玻璃原料混合均匀,在1200 ℃熔融2 h后水淬制得基础玻璃。将研磨后的基础玻璃粉与模拟废液在1050 ℃熔制2 h后倒入到预热好的石墨模具中成型,在500 ℃退火1 h随炉冷却至室温。玻璃固化体经打磨抛光制得10 mm×10 mm×10 mm的块状样品,用去离子水和无水乙醇分别超声清洗10 min,在110 ℃下干燥1 h。

表1 硼硅酸盐玻璃固化体组成
1.1.2 模拟地下水的制备
选取我国高放废物处置库北山预选区BS03号钻井地下水[9-10],其成分列于表2。采用实验室自制的去离子水,按照表2所示组成计算称量对应的无机盐先后溶于1L去离子水中,搅拌均匀后密封储存备用。配置的模拟地下水pH为8.10±0.05。

表2 模拟地下水组成
1.2 性能检测
电感耦合等离子体发射光谱仪(ICAP7400,赛默飞世尔科技有限公司,中国)测试浸出液中B、Si的元素浓度;电感耦合等离子体发射光谱-质谱仪(Aiglent1200/7700x,安捷伦科技公司,美国)测试浸出液中U、Cs的元素浓度;X射线衍射仪(X’Pert PRO,帕纳科公司,荷兰)分析玻璃表面物相变化;扫描电子显微镜-X射线能谱仪(TM4000/Oxford IE450X-Max80,日立高新技术公司,日本)分析玻璃样品蚀变层结构变化。
静态浸泡实验参考美国材料与试验协会标准ASTM C1220-2017《放射性废物处置中整体固化块静态浸出的标准试验方法》,S/V=10 m-1,浸出剂采用模拟地下水,在1、3、7、14、28、56、91、182、364 d收集浸出液并且分析元素含量,按照式(1)计算元素归一化浸出率LR:

式中:LRi——元素i 的归一化浸出率,g /(m2·d);
Ci——浸出液中元素i 的浓度,g/m3;
V——浸出液的体积,m3;
fi——玻璃中组分i 的质量分数;
S——溶液中玻璃样品的表面积,m2;
Dt——浸泡时间间隔,d。
2 结果与分析
2.1 蚀变层的物相组成
图1为硼硅酸盐玻璃固化体蚀变层表面的XRD谱。
由图1可知,玻璃样品在模拟地下水浸泡28 d后表面会出现微小的腐蚀孔洞并有少量灰色物质脱落,因其结晶度有限,所以未检测到其衍射峰。浸泡56 d后的玻璃样品已经可以观察到表面蚀变产物的形成,并且有微小的衍射峰存在,表明玻璃样品表面可能存在少量的结晶相。随着浸泡时间的延长,在91 d出现灰白色蚀变层并观察到白色晶体析出,此时玻璃样品表面衍射峰比较明显。在364 d后玻璃样品表面颜色变为黄褐色并且白色晶体增多,已经出现较强的衍射峰。经过分析该衍射峰与BaSO4和CaCO3较为一致。

图 1 玻璃固化体蚀变层表面的XRD谱
2.2 蚀变层的显微结构
玻璃样品蚀变层表面形貌如图2所示。
浸泡28 d后玻璃样品表面出现了腐蚀痕迹,是由于干燥过程中水分的挥发引起表面应力变化出现裂纹及脱落现象[11]。随着浸泡继续进行,56 d的玻璃样品表面基本上已经被侵蚀而水解,出现了明显的蜂窝状页硅酸盐形貌[12](图2(c))。此时玻璃表面孔隙较大且结构疏松,并且这种蜂窝状的结构与玻璃基体结合较弱,在干燥过程中该层会严重开裂并脱落。浸泡91 d后的蚀变层表面形貌已经出现了明显的变化,由蜂窝状转变为短棒状,并且有棱柱状和片状晶体产生。182 d后蚀变层表面形貌不再改变,只是短棒状物质尺寸随着浸泡时间而增加,从而使得该层孔隙减小,364 d后已经形成了较致密的蚀变层。蚀变层晶体的数量随着浸泡的时间而增加,在91 d时蚀变层主要有两种晶体分布。从图3(h)和(i)的EDS分析可知,棱柱状晶体主要元素为Ca、C、O,片状晶体主要元素为Ba、S、O,推测这两种晶体分别为CaCO3和BaSO4晶体,与XRD分析结果一致。

图2 玻璃固化体蚀变层表面形貌
玻璃固化体蚀变层表面(不含晶体)各元素 质量分数随浸泡时间变化如表3所示。

表3 玻璃固化体蚀变层表面元素含量随时间变化(EDS)
浸泡28 d后的玻璃表面Si、Ba等元素含量降低,Fe、Zr元素富集,可能与页硅酸盐二次相在形成时吸纳了Fe、Zr等元素有关[13]。在56 d后Mg、Al所占比重增加,形成了以Mg、Al、Si为主要元素的蜂窝状页硅酸盐二次相,这与Thien等[14]观察到的实验现象一致。此时玻璃样品表面的Na、Ca、Fe、Cs、Ba等元素已经贫化。随着浸泡时间的延长,Si进一步在表面沉积,Al所占比例下降,使得原本的蜂窝状二次相转变为短棒状。91 d后Mg、Si在蚀变层表面所占的比例保持恒定,形成了较稳定的结构,但是表面仍含有较大的孔隙。随着Mg、Si的沉积,短棒状物质尺寸增加,表面变得更加致密,364 d后表面几乎以富Mg硅酸盐为主。
用环氧树脂将玻璃固化体包裹,经切割、打磨、抛光后断面形貌如图3所示。从蚀变层断面形貌可以观察到明显的分层,最外层是由短棒状富镁硅酸盐形成的二次相,在浸泡91 d时其厚度约为5.3 mm,如图3(a)所示。随着Si在玻璃表面沉积,其厚度在182 d增加到6.4 mm,之后二次相厚度基本保持不变。二次相内部是15~25 mm的凝胶层(图3(a)),可以看出凝胶层厚度随着浸泡时间逐渐增加,并呈现出明显的不均匀性,在364 d凝胶层厚度达到了32~51 mm。182 d后二次相厚度已不再发生变化,但是凝胶层厚度仍在增加,可见玻璃的蚀变仍在进行。在凝胶层观察到晶体的析出,通过EDS分析发现其与蚀变层表面分布的片状硫酸钡晶体一致,这种形貌的硫酸钡晶体形成与浸出液中SO42-与玻璃中溶解的Ba2+形 成低饱和度的反应区域有关[15]。
图4为玻璃固化体364 d蚀变层断面的EDS图像。

图3 玻璃固化体蚀变层断面形貌

图4 玻璃固化体浸泡364 d后的断面EDS图像
由图4可以看出,Mg在玻璃基体中含量很少,主要集中在凝胶层和富镁硅酸盐中,Si在表面有些贫化,这表明玻璃表面可能形成了大量的富镁硅酸盐沉淀,阻碍了Si通过蚀变层的迁移[16]。Mg、Na的元素分布能够很好地说明玻璃的非均匀腐蚀。Mg富集的区域中Na基本上已经完全浸出,这与水分子和碱离子的相互扩散有关[17-18]。H+或H2O+扩散到玻璃内部,使得H+取代了与硼氧四面体结合较弱的Na+等碱金属离子,导致了B-O的断裂和Na+的浸出。凝胶层及二次相有层状分布的BaSO4晶体,CaCO3晶体只在表面析出。晶体的形成有两种可能:在玻璃溶解阶段随着离子扩散和沉积使得晶体从玻璃基体向表面生长;也可能是由于浸出液中的元素浓度达到饱和从而在表面沉积或结晶。通过BaSO4和CaCO3分布情况可以认为,CaCO3晶体的形成是由于离子在蚀变层表面沉积结晶,而BaSO4晶体可能是浸出的Ba2+与溶液中大量的SO42-(约1.3 g/L)由成核控制而导致晶体从玻璃基体向表面生长[15,19]。
2.3 玻璃固化体的浸出行为
硼硅酸盐玻璃固化体各元素的归一化浸出率随时间变化如图5所示。
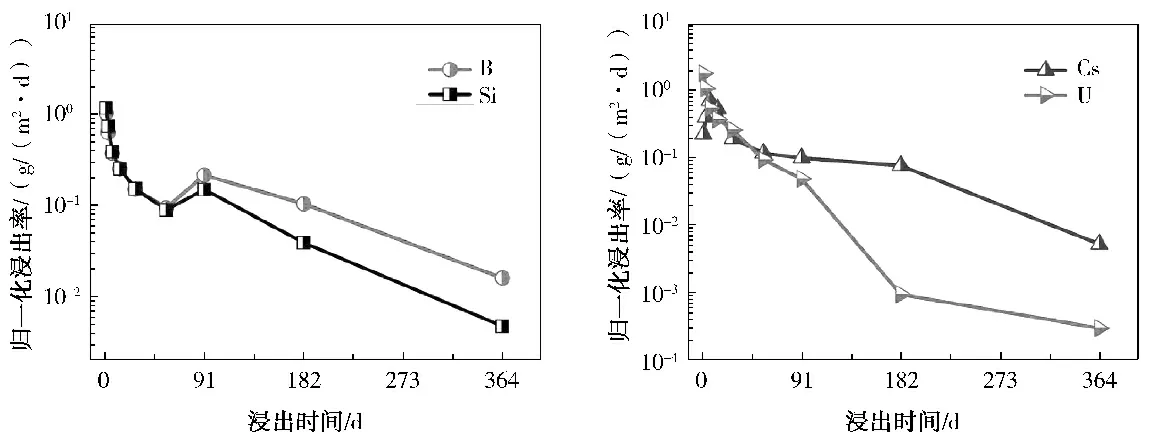
图5 玻璃固化体中B、Si、Cs、U的归一化浸出率
由图5可以看出,Si、B的浸出随时间的变化趋势比较相似,在56 d内Si、B的归一化浸出率相差不大。91 d后Si、B的浸出速率出现反常升高趋势,之后Si、B的浸出快速降低且B的浸出要高于Si,364 d后LRSi(4.76×10-3g /(m2·d))比LRB(1.61×10-2g /(m2·d))低一个数量级。Cs在7 d内快速浸出后不断降低,在56 d后达到了平衡阶段,182 d后Cs的浸出明显下降,这可能和Cs在玻璃表面被吸附有关;U的浸出在91 d后出现了显著下降趋势,之后U的浸出速率不断降低,364 d后的Cs和U的归一化浸出率分别为5.27×10-3g /(m2·d)和9.58×10-4g /(m2·d)。在浸泡初期,玻璃中的Na+等碱金属离子进行离子交换会在玻璃基体表面形成几十纳米厚的水合玻璃层。随着玻璃反应的进行,溶液中离子浓度增加从而降低了玻璃反应亲和力[20]。当浸出液中Si浓度达到一定值,水合玻璃层会逐渐向多孔、无定形的凝胶层转变。随着溶液浓度到达二次相溶解度,浸出液中部分Si会与玻璃中溶解的Mg加上凝胶层中的Al形成蜂窝状页硅酸盐二次相沉淀,此时页硅酸盐中主要以Mg、Al为主,Si只占少部分。二次相的形成降低了溶液浓度,增加了玻璃反应亲和力,并且二次相容易因为表面应力变化产生脱落,导致了玻璃溶解速率增加,因此玻璃固化体56 d后Si、B的元素浸出速率略有上升。可见二次相在形成初期对玻璃样品不具有明显的保护作用[21]。随着溶液中Si浓度的增加,蜂窝状二次相在玻璃表面层层沉积,Si在表面所占比重增加,形成一种富Si保护层从而使得91 d后Si的浸出要低于B。随着浸泡的进行,玻璃表面形成了以Mg、Si为主要元素的短棒状硅酸盐,364 d后该层变得更加致密从而阻碍了玻璃基体与水溶液传质,玻璃中各元素的浸出速率也随之减小。
3 结论
在90 ℃下采用挂片静态浸泡法研究了硼硅酸盐玻璃固化体经模拟地下水侵蚀364 d的蚀变层结构和元素浸出行为,得出结论:
(1)经模拟地下水浸泡56 d后玻璃固化体表面会出现蜂窝状的页硅酸盐,其结构疏松且孔隙较大;91 d后二次相由蜂窝状转变为短棒状形貌并出现了棱柱状CaCO3和片状BaSO4晶体,随着时间进一步延长其结构变得更加致密。
(2)蚀变层主要由富Mg硅酸盐二次相和凝胶层构成,其厚度随着浸泡时间的延长而增加,二次相厚度在182 d后基本保持不变。
(3)蜂窝状页硅酸盐二次相的生成使得Si、B的浸出速率在56 d后略有升高;由于Si的沉积,91 d后蚀变层表面转变为较致密的短棒状富Mg硅酸盐从而使得Si、B的浸出逐渐降低并且Si的浸出速率比B低一个数量级。Cs在7 d内快速浸出后逐渐下降,U的浸出速率总体呈下降趋势,364 d后B、Si、Cs、U的归一化浸出率分别为1.607×10-2,4.761×10-3, 5.265×10-3, 3.022×10-4g /(m2·d)。

