沙美特罗替卡松气雾剂联合辛伐他汀治疗稳定期慢性阻塞性肺疾病患者的临床效果
贺新伟,吴国丽
北京市西城区展览路医院内科,北京 100044
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是指具备气流阻塞特征的慢性支气管炎和(或)肺气肿,以气流不可逆性受限、病情进行性进展为主要特征,发病率和病死率高[1]。COPD患者气流阻塞易致肺动脉压力升高,伴随血液高凝及微血栓形成,导致右心室收缩及舒张功能障碍,血浆脑钠肽(brain natriuretic peptide,BNP)合成分泌增多及血浆内皮素(endothelin-1,ET-1)异常表达[2]。现代医学认为炎症细胞、炎症介质等共同作用于气道,气道慢性炎症可引发支气管平滑肌收缩,炎性反应反复发作会逐渐表现为支气管上皮细胞脱落及坏死[3],由此说明炎性因子在COPD病情进展中发挥一定作用。一直以来临床对COPD治疗以吸入糖皮质激素或长效β受体激动剂为主[4],但现阶段关于沙美特罗替卡松气雾剂联合辛伐他汀对COPD患者的临床疗效、预后效果及其机制的研究尚缺乏统一定论,为此笔者于本文展开临床对照性研究,旨在为COPD患者有效治疗提供依据。
1 资料与方法
1.1 一般资料 选取2019年6月至2020年4月北京市西城区展览路医院收治的80例稳定期COPD患者为研究对象。纳入标准:①符合COPD诊断标准[5];②纳入研究前两周内未使用过治疗COPD的药物;③COPD患者病情稳定,且持续时间≥1个月。排除标准:①有重大肺部手术史;②合并支气管哮喘、急性感染、肿瘤、糖尿病、心脑血管病及肾功能不全等;③妊娠期及哺乳期妇女;④过敏体质,对本研究中所用药物过敏。按随机数表法将患者分为对照组和研究组各40例。对照组中男性18例,女性22例;年龄41~60岁,平均(53.78±4.49)岁;病程1~4年,平均(2.68±1.01)年。研究组中男性20例,女性20例;年龄40~60岁,平均(54.01±4.28)岁;病程1~4年,平均(2.72±1.11)年。两组患者的上述基线资料比较差异均无统计学意义(P>0.05),具有可比性。本研究获得患者及其家属知情同意并签署知情同意书,征得本院医学伦理委员会批准。
1.2 治疗方法 两组患者入院后均进行健康宣教(长期家庭氧疗,积极戒烟、营养支持等);对照组指导患者经鼻吸入沙美特罗替卡松气雾剂(生产企业:Laboratoire GlaxoSmithKline;批准文号:H20140382)50μg/250μg,1吸/次,2次/d。研究组患者在对照组治疗基础上联合辛伐他汀治疗,患者在吸入沙美特罗替卡松气雾剂治疗基础上另口服辛伐他汀片(分包装厂名称:杭州默沙东制药有限公司;批准文号:国药准字J20130181)治疗,20 mg/次,1次/d。两组均持续治疗3个月。
1.3 观察指标与检测(评价)方法 (1)临床疗效:参照《临床疾病诊断依据治愈好转标准》[6]评估疗效,痊愈:临床症状、体征、实验室检查均完全恢复正常,显效:上述三项仍有一项未完全恢复正常,无效:治疗后未达到治愈或显效甚至病情加重。总有效率=(痊愈+显效)/总例数×100%。(2)治疗前后血清炎性因子水平:采用酶联免疫吸附法(奥地利公司提供的型号为Bioelisa ELX-800的酶标仪)检测两组白介素-8(interleukin-8,ΙL-8)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)表达水平,试剂盒由仪器配套,操作严格按照说明书进行。(3)治疗前后ET-1、BNP表达水平:采用酶联免疫吸附法检测ET-1及BNP(仪器为奥地利公司提供的型号为Bioelisa ELX-800的酶标仪),试剂及试剂盒由仪器配套提供,操作严格按照说明书进行。(4)治疗前后肺功能指标:采用肺功能测定仪(型号:CHESTGRAPH HΙ-101)测定并计算用力肺活量(forced vital capacity,FVC)、第1秒用力呼气容积(forced expiratory volume in the first second,FEV1)、最大肺通气量(maximum voluntary ventilation,MVV)分别占预测值的百分比。(5)治疗后预后效果:采用改良英国医学研究理事会呼吸困难指数(modified British medical research council,mMRC)评分和慢性阻塞性肺疾病(COPD)评估测试评分[chronic obstructive pulmonary disease(COPD)assessment test score,CAT]评估患者预后效果,mMRC评分量表包含0~4个等级分为0~4分,CAT评分包含8个项目,总分40分,分值越高表明患者健康状况及生活质量越差,两组于治疗后半年进行评分。(6)治疗后药物安全性。
1.4 统计学方法 应用SPSS19.0统计学软件分析数据,计数资料组间比较采用χ2检验,计量资料符合正态分布,以均数±标准差(±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的治疗效果比较 研究组患者的治疗总有效率为90.0%,明显高于对照组的72.5%,差异有统计学意义(χ2=4.021,P=0.045<0.05),见表1。

表1 两组患者的治疗效果比较(例)
2.2 两组患者治疗前后的血清炎性因子和ET-1、BNP水平比较 治疗后,两组患者的ΙL-8、TNF-α、ET-1、BNP较治疗前明显降低,且研究组明显低于对照组,差异均有统计学意义(P<0.05),见表2。
2.3 两组患者治疗前后的肺功能指标比较 治疗前两组患者的FVC、FEV1、MVV比较差异均无统计学意义(P>0.05);与治疗前比较,治疗后两组患者的FVC、FEV1、MVV明显升高,且研究组升高较对照组更明显,差异均有统计学意义(P<0.05),见表3。
表2 两组患者治疗前后的血清炎性因子和ET-1、BNP水平比较(±s)

表2 两组患者治疗前后的血清炎性因子和ET-1、BNP水平比较(±s)
注:与本组治疗前比较,a P<0.05。
组别研究组对照组t值P值例数40 40治疗前8.78±1.89 8.76±1.90 0.047 0.963治疗后5.16±1.01a 6.01±1.16a 3.495 0.001治疗前0.76±0.29 0.78±0.28 0.314 0.755治疗后0.46±0.19a 0.61±0.22a 3.264 0.002治疗前191.78±42.89 192.76±42.90 0.102 0.919治疗后87.76±13.90a 122.57±23.16a 8.151 0.001治疗前1.23±0.20 1.24±0.19 0.229 0.819治疗后1.06±0.16a 1.16±0.17a 2.709 0.008 ΙL-8(pg/mL) TNF-α(ng/mL) ΙET-1(pg/mL) BNP(ng/mL)
表3 两组患者治疗前后的肺功能指标比较(±s)
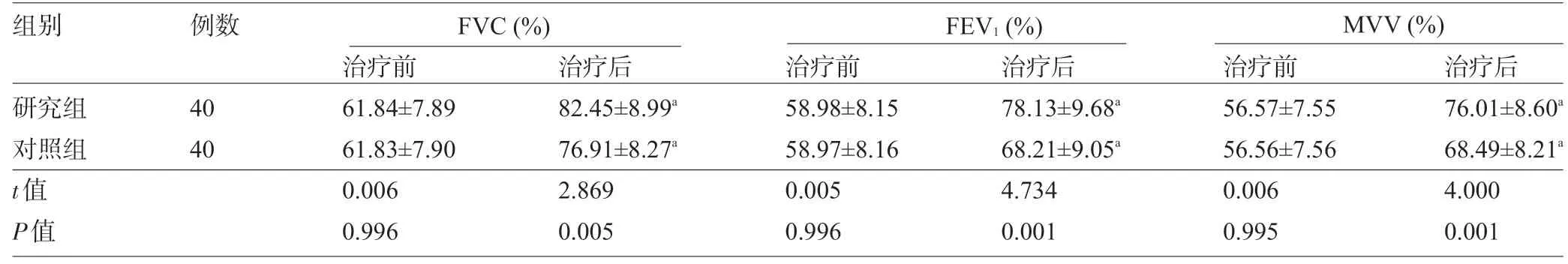
表3 两组患者治疗前后的肺功能指标比较(±s)
注:与本组治疗前比较,a P<0.05。
组别研究组对照组t值P值例数40 40治疗前61.84±7.89 61.83±7.90 0.006 0.996治疗后82.45±8.99a 76.91±8.27a 2.869 0.005治疗前58.98±8.15 58.97±8.16 0.005 0.996治疗后78.13±9.68a 68.21±9.05a 4.734 0.001治疗前56.57±7.55 56.56±7.56 0.006 0.995治疗后76.01±8.60a 68.49±8.21a 4.000 0.001 FVC(%) FEV 1(%) MVV(%)
2.4 两组患者治疗后的预后效果比较 治疗后,两组患者的mMRC、CAT评分较治疗前明显降低,且研究组降低较对照组更明显,差异均有统计学意义(P<0.05),见表4。
表4 两组患者治疗后的预后效果比较(±s,分)

表4 两组患者治疗后的预后效果比较(±s,分)
注:与本组治疗前比较,a P<0.05。
组别研究组对照组t值P值例数40 40治疗前2.58±0.62 2.56±0.62 0.144 0.886治疗后2.01±0.30a 2.17±0.46a 1.843 0.069治疗前25.83±5.36 25.01±5.20 0.694 0.490治疗后15.36±3.56a 20.68±4.17a 6.137 0.001 mMRC CAT
2.5 两组患者治疗后药物安全性比较 治疗后两组患者均未出现严重药物不良反应。研究组患者治疗后出现转氨酶升高2例,皮疹2例,腹痛1例,便秘2例,对照组患者出现关节痛2例,皮疹4例,研究组治疗后药物不良反应发生率为17.50%,与对照组的15.00%比较差异无统计学意义(χ2=0.092,P=0.762>0.05)。
3 讨论
COPD病理性改变主要有气流阻力增加和气道弹性回缩力下降,气流受限呈不完全可逆,发病机制与多种因素共同作用有关。活化上皮细胞产物ΙL-8属于选择性中性粒细胞趋化因子,在COPD炎性细胞的聚集和活化中发挥重要作用[7]。ET-1为临床医师公认的最强血管收缩剂及支气管活性物质,在血管内皮及其他各种组织细胞中广泛存在,ET-1被证实在COPD的发病中发挥重要作用,TNF-α等炎性因子可刺激支气管平滑肌细胞、上皮细胞和肺泡巨噬细胞分泌ET-1,导致气道炎症反应和COPD病情的加重[8]。
研究证实沙美特罗替卡松吸入剂治疗COPD患者可有效降低ET-1表达水平,明显改善患者肺功能,且血管内皮素水平与肺功能存在明显负相关[9];另有研究表明COPD患者常规治疗基础上应用辛伐他汀,可有效改善患者肺功能,考虑沙美特罗替卡松吸入剂联合辛伐他汀在COPD患者治疗中有一定应用价值[10]。而本结果发现研究组总有效率明显高于对照组,治疗后研究组ΙL-8、TNF-α、ET-1、BNP表达水平明显低于对照组,肺功能指标较对照组明显高,初步证实了沙美特罗替卡松气雾吸入剂联合辛伐他汀治疗COPD的临床效果更为理想,说明沙美特罗替卡松气雾吸入剂联合辛伐他汀治疗可有效改善患者肺功能,明显降低肺功能下降速率,有效降低COPD急性加重的风险。
沙美特罗替卡松气雾吸入剂属于一种长效β2受体激动剂,可与支气管和肺组织内β2受体结合,激活腺苷磷酸化酶以促进三磷酸腺苷转化为环磷酸腺苷,明显增加细胞内环磷酸苷含量,有效降低细胞内游离钙离子含量,发挥舒张支气管作用,达到改善患者肺功能的目的[11]。国外学者长达1年的临床研究表明沙美特罗的应用可有效降低重症COPD患者的死亡率[12]。沙美特罗替卡松气雾吸入剂可发挥舒张支气管、减轻气道炎症反应的作用,在减少COPD患者急性发作次数的同时有效减轻患者气道阻塞程度,明显改善患者运动生活质量[13-14]。他汀类药物除了有调脂作用外,同时有明显的抗炎活性、调节细胞凋亡和免疫作用,辛伐他汀在COPD治疗中可有效减缓患者肺功能下降速率,提高其运动耐量[15],由此推测沙美特罗替卡松吸入剂联合辛伐他汀治疗COPD患者可明显提高临床疗效、有效改善患者肺功能,同时明显改善患者预后。
综上所述,沙美特罗替卡松气雾剂联合辛伐他汀治疗稳定期COPD患者,在调节患者炎性因子、ET-1、BNP及改善肺功能和预后方面较单一治疗方案更具优势,值得临床推广应用。

