薏苡仁油自纳米乳化体系的建立及体外释放
易 醒,李 娟,易孜成,罗俊溢,袁弋婷,夏小华,肖小年*
薏苡仁是禾本科的草本植物,为药食同源的原料,其营养价值较高,在健脾祛湿、抗癌、降低血压和免疫调节等方面具有多种作用[1-2]。薏苡仁油(Coix seed oil,CSO)是薏苡仁中的主要生物活性组分,有显著的抗肿瘤作用,主要含有甘油三酯、甘油二酯等成分[3]。目前以CSO 为原料生产的康莱特注射液已广泛运用在肝癌、胃癌等的治疗及辅助治疗[4]。然而,CSO 较差的水溶性、稳定性和口服生物利用度,限制了其在食品及医药领域的使用和发展[5]。目前,对于CSO 制剂,以微乳制剂[6]、纳米粒、脂质体[7]、薏苡仁油酯微胶囊形式居多,鲜有CSO 自乳化体系及其体外释放的相关报道。
自乳化递送系统是由亲脂性或疏水性物质、油相、表面活性剂(Surfactant,SA)和助表面活性剂(Cosurfactant,CoSA)组成,在胃肠道蠕动的内环境条件下,可自发乳化成粒径小于500 nm 的水包油(O/W)型乳剂[8]。根据液滴尺寸大小,自乳化递送系统可分为自纳米乳化递送系统(Self-nanoemulsifying Delivery System,SNEDS) 和自微米乳化递送系统 (Self-microemulsifying Delivery System,SMEDS)[9]。目前研究发现,SNEDS 可解决水难溶性物质在胃肠道内快速分散、溶解与吸收的问题,达到显著提高口服生物利用度,增加在胃肠道的溶出及促进吸收的目的[10],对提高BCS Ⅱ类药物生物利用度有较多帮助。
本文尝试采用伪三元相图及星点设计-效应面优化等方法构建薏苡仁油自纳米乳化体系(CSO-SNEDS),并对其特性进行表征。同时,基于体外释放试验,对CSO-SNEDS 体外释放及动力学进行研究。本研究期望解决CSO 存在的低水溶性问题,并为CSO-SNEDS 体内释放情况的研究与预测提供参考。
1 材料与方法
1.1 原料与试剂
薏苡仁油,广州和博香料有限公司;胰酶、胃蛋白酶、透析袋,上海阿拉丁生化科技股份有限公司;蓖麻油聚氧乙烯醚-35(EL-35),BASF;聚氧乙烯失水山梨醇单油酸酯(Tween80)、聚氧乙烯山梨醇酐棕榈酸酯(Tween40)、聚氧乙烯山梨醇酐单月桂酸酯(Tween20)、蓖麻油聚氧乙烯醚-40(EL-40)、聚乙二醇400(PEG-400)、失水山梨醇单油酸酯 (Span80)、聚氧乙烯山梨醇酐硬脂酸酯(Tween60)、失水山梨醇单月桂酸酯(Span20)、丙二醇、丙三醇,均为分析纯,天津市永大化学试剂有限公司。
1.2 仪器与设备
AED110 电子天平,美国奥豪斯Adventurer 公司;DK-S24 电热恒温水浴锅,上海森信实验仪器有限公司;RH-数显磁力搅拌器,德国IKA 公司;TDL-5-A 低速台式离心机,上海安亭科学仪器厂;T6 紫外可见分光光度计,北京普析通用仪器有限公司;NICOMP380ZL 激光纳米粒度测定仪,英国马尔文粒度分析仪公司;SHA-A 数显恒温水浴振荡器,常州天瑞仪器有限公司。
1.3 试验方法
1.3.1 CSO-SNEDS 的制备过程 准确称取所需量的SA、CoSA 和CSO,置于小烧杯中,在60 ℃下搅拌(250 r/min)约20 min,使其均匀混合,直至形成黄色的澄清黏稠液体。取0.1 mL 的上述制备的混合物至10 mL 蒸馏水中,在37 ℃条件下低速搅拌(100 r/min),考察其自乳化情况。以外观是否澄清透明和自乳化时间为指标,确定该配方能否形成自乳化制剂。
据文献所述,自乳化速率等级可如下所示(表1),其中A、B 级符合试验要求[11]。

表1 自乳化速率等级表Table 1 Self-emulsification rate grade table
1.3.2 CSO 与SA、CoSA 互溶情况考察 将1 mL CSO 分别加入到装有4 mL 不同SA (分别为Tween80、EL-40、EL-35、Tween60、Tween40、Tween20)或不同CoSA(分别为丙三醇、丙二醇、聚乙二醇400)的具塞离心管中,涡旋混匀后,3 500 r/min 离心1 min,若可互溶则继续加入CSO,以出现分层和浑浊为临界指标评估互溶情况。
1.3.3 配方的初步筛选试验
1.3.3.1 单一SA 的筛选 分别以Tween60、EL-35、EL-40 作为SA,按质量比9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9 准确称取SA 与CSO,在不使用CoSA 的情况下,按1.3.1 节进行CSOSNEDS 制备,并考察其自乳化情况。
1.3.3.2 CoSA 的筛选 分别以PEG 400 和丙三醇作为CoSA,固定SA 与CoSA 质量比(Km)为2∶1,按质量比9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9 准确称取SA 与CSO,按1.3.1 节进行CSOSNEDS 制备,并考察其自乳化情况。
1.3.3.3 复合SA 的筛选 选取Tween60、EL-35、EL-40 分别和Span80、Span20 进行复配,复配比例为9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9,CoSA 为丙三醇,固定Km=3∶1,复合SA 与CSO 质量比为9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9,按1.3.1 节进行CSO-SNEDS 制备,并考察其自乳化情况。
1.3.3.4 伪三元相图的绘制 采用初步筛选结果来进行伪三元相图绘制,根据微乳区大小来确定Km范围和最高载油量,具体方法如下:将油相、SA和CoSA 作为伪三元相图的3 个顶点,将SA 与CoSA 按照质量比9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9 的比例混合,再将制得的混合物与油相以质量比9∶1,8∶2,7∶3,6∶4,5∶5,4∶6,3∶7,2∶8,1∶9 的比例混匀,将可形成自微乳点连线成面即得相图。
1.3.4 星点设计-效应面优化法优化配方
1.3.4.1 试验设计 结合伪三元相图的试验结果,选取对自纳米乳化体系影响较显著的油相质量分数(X1,oil%)和Km(X2)作为考察因素,以自乳化时间和透光率作为评价指标。
透光率的测定是由吸光度值换算得出,自乳化时间的测定方法:取0.1 mL CSO-SNEDS 至10 mL 蒸馏水中,在37 ℃条件下低速搅拌 (100 r/min),于0.5,1,1.5,2,2.5,3,3.5,4,5 min 时取样进行吸光度测定,当吸光度值趋于稳定不再改变时,此时自乳化制剂已经乳化完全,即为自乳化时间。
依据星点设计原理拟采用二因素,五水平设计因素水平表,将油相比例控制在10%~22%,Km范围控制在1~5,试验设计如表2所示。
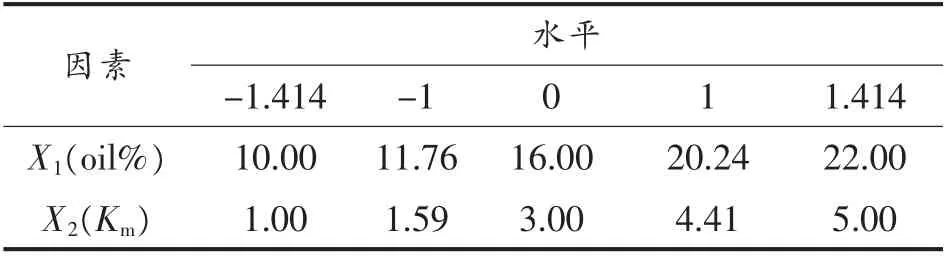
表2 星点设计的因素及水平Table 2 Factors and levels of star point design
1.3.4.2 模型拟合 将试验所得数据采用Design Expert 8.0.6 软件进行处理,以评价指标分别对各因素进行回归分析和数学模型拟合,并绘制效应面三维图。
1.3.4.3 验证试验 采用效应面优化配方,以自乳化时间、透光率作为评价指标,通过比较试验值与效应面预测值之间的差异性进行验证。
1.3.5 CSO-SNEDS 的理化特性表征
1.3.5.1 外观及稀释后的外观 室温下观察最优配方制得的CSO-SNEDS 的外观。然后在温和搅拌下,取1 mL 加入到100 mL 蒸馏水(37 ℃)中,进行分散性试验以考察其自乳化情况。
1.3.5.2 液滴尺寸和ζ-电位 将优化的CSOSNEDS 在恒定磁力低速搅拌下用蒸馏水(1∶100)稀释。使用马尔文粒度仪通过激光散射测定液滴尺寸、多分散性指数(Polydispersity index,PDI)和ζ-电位。测定3 次取平均值。
1.3.5.3 自乳化速率 取0.1 mL 最优配方制得的CSO-SNEDS 加入到装有10 mL 蒸馏水的样品瓶中,在相同条件时,测定在不同温度、转速、稀释倍数下的自乳化时间和体系透光率。
1.3.6 CSO-SNEDS 的体外释放研究
1.3.6.1 反向透析法 人工胃液 (Simulated gastric fluid,SGF)、人工肠液 (Simulated intestinal fluid,SIF)根据2015 版《中国药典》进行配制[12]。
分别移取180 mL 的SIF 于两个锥形瓶中,每个锥形瓶中放入7 个装有2 mL SIF 的透析袋,分别取2.40 g CSO 和同等CSO 含量的SNEDS 于锥形瓶中,并将其置于摇床(37 ℃恒温)中,分别于0.5,1,1.5,2,4,6,8 h 从锥形瓶中取一个透析袋,取样备用。
CSO-SNEDS 在SGF 中释放考察,参照上法操作。
1.3.6.2 释放液的测定 依据先前研究显示[13],甘油三酯是CSO 中的主要成分。本文采用试剂盒法测定透析袋释放介质中甘油三酯含量,取样品2.5 μL 置于酶标板中,加250 μL 工作液,37 ℃孵育10 min 后,用全波长酶标仪测定吸光度,并进行数据分析。
根据公式计算甘油三酯累计释放量:

式中:Mt——甘油三脂累计释放量,mg;Q——甘油三酯累计释放率,%;Ci——第i 次取样时甘油三酯的释放质量浓度,mg/mL;V——第1次取样前的体积,mL;Ci-1——i 时间取样点的前一个取样点时甘油三酯的质量浓度,mg/mL;V样——每次取样对应的体积,mL。
1.3.6.3 体外释放动力学模型的拟合 参照文献[13],选用5 种释放方程对甘油三酯累计释放率进行曲线拟合,根据拟合优度判断体外释放动力学类型。
1.4 数据分析
试验数据采用Origin 2017 软件进行处理。
2 结果与分析
2.1 CSO 与不同SA、CoSA 的互溶情况
根据试验结果,CSO 与SA 的互溶情况:Tween60>EL-35>EL-40>Tween40>Tween80>Tween20,CSO 与CoSA 的互溶情况:PEG400>丙三醇>丙二醇。
CSO 与Tween60、EL-35、EL-40、PEG400 和丙三醇均能很好的相溶,未出现分层或浑浊,因此,选用Tween60、EL-35、EL-40 作为SA,PEG400 和丙三醇作为CoSA 进行试验。
2.2 配方筛选试验结果
选取CSO 溶解度较好的3 种SA 和两种CoSA 进行配方筛选试验,试验结果显示PEG400/EL-35/CSO,丙三醇/EL-35/CSO 体系,Tween60/丙三醇/CSO 体系均可形成CSO-SNEDS,但载油量较低,以Tween60/丙三醇/CSO 体系最佳,载油量可达16%左右。
根据已有研究显示,复合SA 相比于单一SA可形成更稳定的复合凝聚膜,因此更易形成稳定的自纳米乳化体系[14]。因此本试验采用复合SA(Tween60/Span80 或 Tween60/Span20)/丙三醇/CSO 体系进一步进行配方筛选。结果表明,仅Tween60/Span20/丙三醇/CSO 体系可形成CSOSNEDS,其中Tween60/Span20 质量比=9:1。另外,如图1所示,复合SA(Tween60/Span20)/丙三醇=8∶2~5∶5 时,自纳米乳化体系均可形成,且当复合SA(Tween60/Span20)/丙三醇=8∶2 时,体系油相比例最高为18.60%,此时自乳化等级仅为B,因此该体系还需进一步优化。
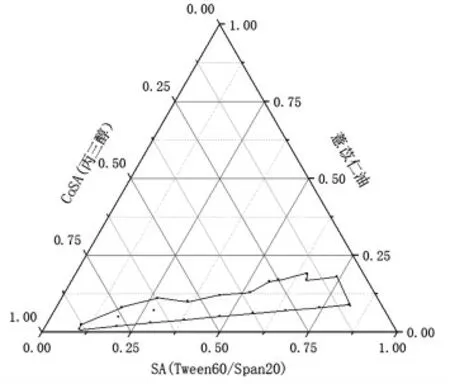
图1 复合SA(Tween60/Span20)/丙三醇/CSO 体系伪三元相图Fig.1 Pseudo-ternary phase diagram of complex surfactant (Tween60/Span20)/glycerol/CSO system
2.3 星点设计-效应面优化法优选配方
2.3.1 模型拟合 采用表2进行星点设计试验,其响应值如表3所示。采用Design Expert 8.0.6软件,对各因素分别进行多元线性、二项式拟合,结果显示二次多项式为最佳方程(表4)。

表3 星点设计表与结果Table 3 Star design table and results

表4 各响应值的回归方程Table 4 Regression equation of each response value
回归方差分析显著性检验表明,Y1和Y2的回归方程的P<0.0001,说明模型回归显著,失拟项不显著(P>0.05),说明该模型具有统计学意义,即自乳化时间和透光率的非线性拟合效果较好,相关系数较高,结果具有统计学意义,可用来进行CSO-SNEDS 的配方优化。
2.3.2 效应面分析 由图2可知,当Km值一定时,随着油相质量分数的增加,自乳化时间延长,油相质量分数在一定范围内时,透光率逐渐上升,当油相质量分数较大时,透光率逐渐下降,不再呈现透明或半透明状态。当油相的质量分数一定时,自乳化时间随Km的增加而增加,透光率呈现先增加后减小的趋势。
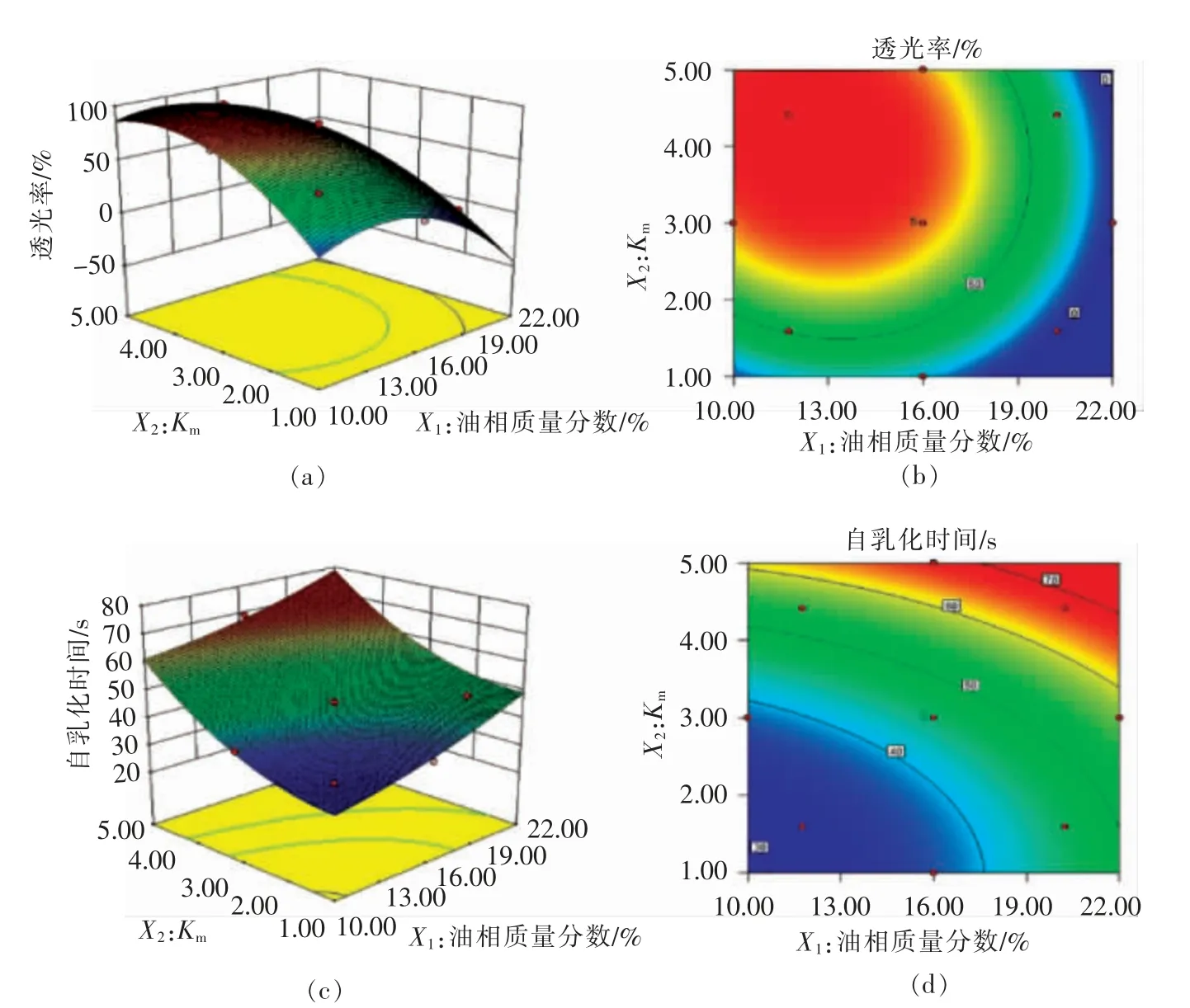
图2 油相质量分数、Km 值对自乳化时间及透光率影响的效应面图及等高线图Fig.2 Effect surface diagram and contour diagram of oil phase mass fraction and Km value on self-emulsification time and light transmittance
2.3.3 效应面估测及最佳验证试验 通过软件的预测分析功能、拟合方程及其三维效应面图综合分析,在试验范围内以载油量(油相质量分数)、自乳化时间和透光率为综合考察指标,结合配方的初步筛选试验,得到最佳配方:油相质量分数为16.11%,Km=3.54,其中油相为薏苡仁油,复合SA为Tween60/Span20=9∶1,CoSA 为丙三醇。根据最优配方制备CSO-SNEDS,考察预测值与实测值的偏差,结果表明,自乳化时间及透光率与预测值之间没有显著差异,表明预测性良好。试验结果见表5。
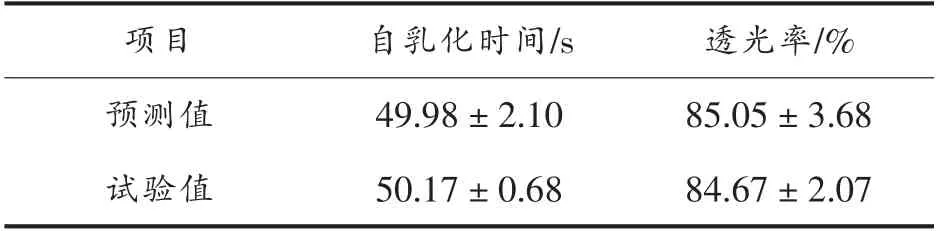
表5 验证配方评价指标的预测值与试验值(n=3)Table 5 Predictive value and experimental value of verified prescription evaluation index (n=3)
2.4 CSO-SNEDS 的理化特性
2.4.1 CSO-SNEDS 外观及液滴尺寸 如图3b所示,CSO-SNEDS 为淡黄色澄清透明体系,将其稀释后可形成微泛蓝光、澄清透明的乳液。另外,SNEDS 粒径大小决定着CSO 溶出速率与溶出度,是影响其在体吸收和生物利用度的重要因素。如图3a 所示,CSO-SNEDS 的平均粒径为47.52 nm(<100 nm),且呈正态分布,符合对纳米乳的理想要求[15]。
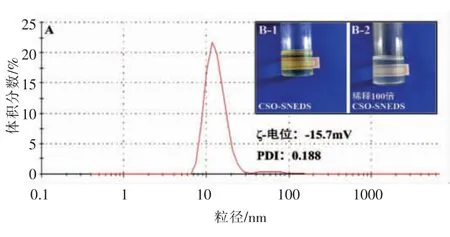
图3 CSO-SNEDS 的粒径分布(A)及外观(B)Fig.3 Particle size distribution (A) and appearance (B)of CSO-SNEDS
2.4.2 自乳化速率 由表6可知,转速和温度对自乳化时间的影响很大,对透光率影响较小,而稀释倍数对自乳化时间的影响较小,对透光率影响较大。随着转速的增大,CSO-SNEDS 的自乳化时间减小,透光率增加。自乳化时间随着温度的升高明显缩短,可能是由于温度较高时,增加了各分子间的碰撞,从而降低油水界面间的界面能,有利于形成乳剂。
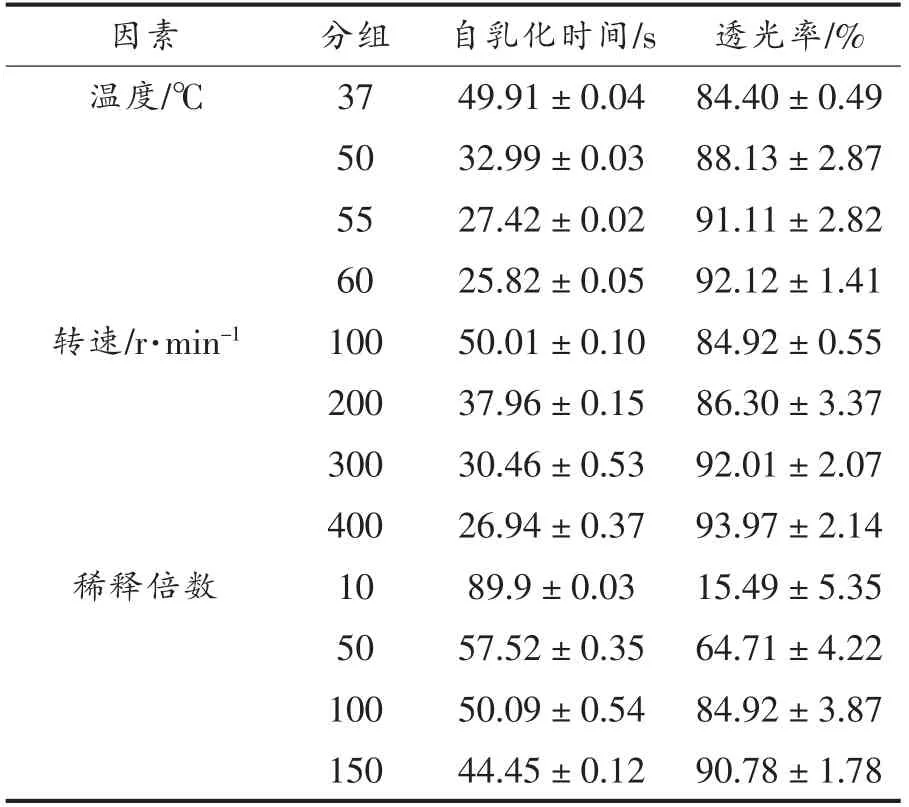
表6 自乳化速率体外评价Table 6 In vitro evaluation of self-emulsification efficiency
2.5 CSO-SNEDS 体外释放及动力学
体外释放度是评价纳米制剂质量的重要指标[16],采用反向透析法对CSO 及其SNEDS 的体外释放性进行评估。由图4可知,SNEDS 显著提高了CSO 在SIF 与SGF 中的累计释放量,8 h 后分别为2.98 倍与9.54 倍。CSO 不易溶于人工消化液,多漂浮于表面,不利于甘油三酯的扩散,而CSOSNEDS 为粒径较小的O/W 体系,其可于消化液中均匀分散并更大程度被释放[17],这可能是SNEDS提高CSO 体外释放量的最主要原因。另外,CSO与CSO-SNEDS 在SIF 中的释放量均高于SGF,这可能是由于弱酸性的CSO 更易溶解于碱性SIF 而引起的[18]。
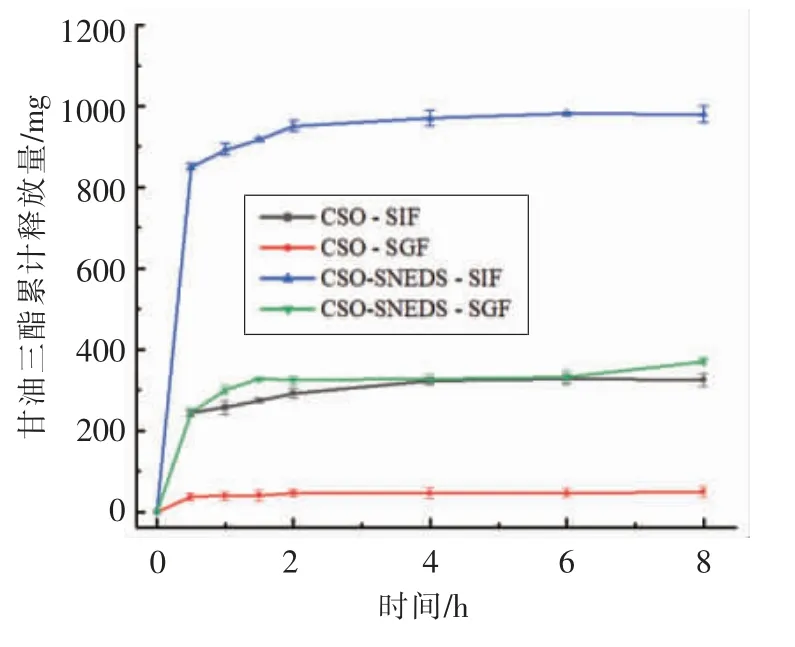
图4 CSO-SNEDS 在体外释放模型中的释放情况Fig.4 Release of CSO-SNEDS in vitro model
将CSO-SNEDS 在两种人工消化液中的累计释放率分别用5 种方程进行释放动力学拟合[13],拟合结果如表7所示。Ritger-Peppas 方程的拟合优度更高,其在人工肠液与胃液中的释放拟合系数分别为0.731 和0.912,可较好地描述CSO-SNEDS在消化液中的释放规律。另外,对于Ritger-Peppas方程来说,n(释放指数)是用来表征释放机制的特征参数,如果0.45

表7 CSO-SNEDS 在SGF 与SIF 中的体外释放动力学拟合结果Table 7 Results of in vitro release kinetics of CSO-SNEDS in SGF and SIF
3 结论
本文以CSO 作为油相,通过配方筛选试验及伪三元相图的绘制结果,成功构建了以Tween60/Span20/丙三醇/CSO 为体系的CSO-SNEDS。同时,使用星点设计-效应面法,以透光率、自乳化时间为评价指标,通过模型效应面图及模型拟合确定了各组分比例,即油相质量分数为16.11%,Km值为3.54,其中复合SA 为Tween60/Span20=9∶1,CoSA 为丙三醇。优化所得CSO-SNEDS 载油量较高,外观为黄色澄清液体,稀释后稳定性较好。体外释放结果表明,SNEDS 中CSO 的体外释放量显著提升,其体外释放动力学均符合Ritger-Peppas方程,且符合Fick 扩散机制。

