尿素14C胶囊中55Fe分析方法研究
马莉娜,宋丽娟,杨永刚,王亚东,马 彦,戴雄新
(中国辐射防护研究院,山西 太原 030006)
幽门螺旋杆菌(Hp)是目前所知能在人体胃酸中生存的唯一微生物种类。Hp感染能引发多种胃病,在2017年世界卫生组织国际癌症研究机构公布的致癌物清单中Hp被列为一类致癌物。目前,14C尿素呼吸试验是Hp感染检测的有效方式。尿素14C胶囊的初始14C原料通过中子辐照高纯氮化铝(AlN)靶获得[1-2],为保证药品的放射性纯度,需分析AlN靶原料经辐照后可能产生的放射性杂质核素及其放射性活度。《美国药典》[3]《中国药典》2015 年[4]均未给出详细可行的尿素14C胶囊中放射性杂质核素的检验方法。因此,需建立实际可行的尿素14C胶囊中放射性杂质核素的检验方法,确保药品质量。
高纯AlN靶中Fe、Co元素的最高含量分别可达到1 500 ppm及600 ppm[5]。Fe、Co等杂质元素被中子活化生成55Fe、60Co等放射性核素,其母体54Fe和59Co热中子吸收截面较大,55Fe(t1/2=2.74 a)和60Co(t1/2=52 711 a)半衰期长,因此,55Fe和60Co是最有可能引起14C标记尿素原料药的放射性核纯度超标的主要杂质核素。60Co为高能β-γ核素,较易通过γ能谱、液闪或Cerenkov计数测量来检验[6-7],而55Fe是电子俘获衰变核素,其发射的低能俄歇电子及X射线的探测效率低,易被屏蔽而难以检测。对55Fe最灵敏的检测手段是液闪计数,但其液闪能谱处于极低能区[8-11],14C为纯β放射性核素,最大能量为156 keV[12],能谱处于较高能区,完全覆盖活度很低的55Fe 能谱,因此检测14C标记尿素样品中低活度的55Fe需首先将高活度14C从样品中完全分离,才能进行55Fe的液闪测量。本工作拟建立尿素14C胶囊中放射性杂质核素55Fe分析方法,并对方法进行验证,以满足尿素14C胶囊生产中的质控需求。
1 实验
1.1 主要试剂和仪器
55Fe标准溶液比活度为59 kBq/g,美国国家标准技术研究所(NIST);14C标准淬灭源、Hisafe闪烁液,美国Perkin Elmer;浓HCl、六水合三氯化铁,市售分析纯。
Hidex-300SL液体闪烁计数器(LSC),芬兰Hidex;X射线荧光光谱分析仪、Milli-Q Reference超纯水机系统,美国默克;XS-205分析天平,分度值为0.1 mg,美国梅特勒。
1.2 胶囊样品中55Fe的化学分离及测量流程
胶囊样品中55Fe的化学分离及测量流程示于图1。具体过程如下。
1) 将AGMP-1强碱性阴离子交换树脂在高纯水中浸泡1 h,将浸泡好的树脂装入2 mL树脂柱中,加入5 mL 9 mol/L HCl平衡树脂。
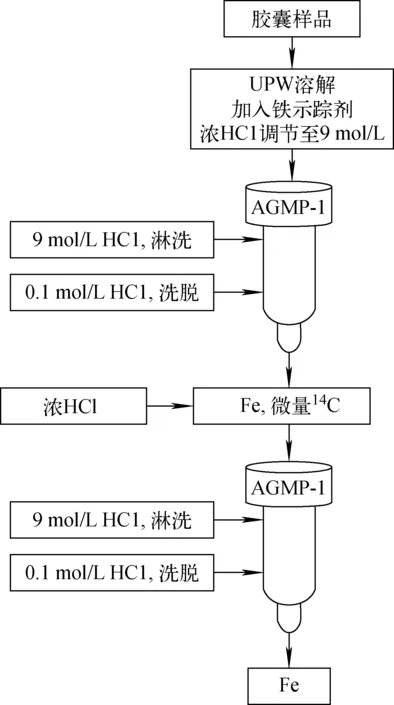
图1 尿素14C胶囊中55Fe的放化分析流程Fig.1 Flow diagram of radioanalytical procedure for determination of 55Fe in urea 14C capsule
2) 取1粒胶囊样品和2 mL高纯水加入50 mL离心管中,60 ℃水浴加热至胶囊溶解后加入5 mg稳定铁示踪剂和10 mL 12 mol/L HCl,混合均匀。
3) 将第2步所得胶囊溶解液通过树脂柱,再用10 mL 9 mol/L HCl以1 mL/min的流速淋洗树脂柱,之后用3 mL 0.1 mol/L HCl将铁洗脱至50 mL离心管中。在离心管中加入10 mL 12 mol/L HCl,混合均匀,再次通过树脂柱,样品全部流出后,用10 mL 9 mol/L HCl以1 mL/min的流速淋洗树脂柱,最后用3 mL 0.1 mol/L HCl将铁洗脱至20 mL聚乙烯(PE)闪烁瓶中。在闪烁瓶中加入0.6 mL 15 mol/L H3PO4、1 mL水和14 mL Hisafe闪烁液,避光放置12 h,采用LSC测量并计算55Fe的活度。
1.3 铁标准工作曲线
称取0.970 5 g分析纯级六水合三氯化铁于20 mL PE液闪瓶中,再加入0.1 mol/L HCl配置成10 mg/g的稳定铁溶液。准确称取0.2、0.3、0.4、0.5、0.6、0.7、0.8 g浓度为10 mg/g的Fe3+溶液于系列20 mL PE闪烁瓶中,用0.1 mol/L HCl定量至3.000 0 g,混合均匀后,用X射线荧光光谱仪(XRF)测量其浓度,绘制铁的标准曲线。

图2 XRF测量的Fe3+标准曲线Fig.2 Standard curve of Fe3+ by XRF
1.4 14C活度测量
1) 尿素14C胶囊中14C活度测量
取1粒胶囊样品,转移至50 mL离心管中,加入2 mL高纯水,60 ℃水浴加热至胶囊溶解,取出0.2 g,转移至20 mL聚乙烯闪烁瓶中,加入1 mL高纯水和14 mL Hisafe闪烁液,混合均匀,采用LSC测量并计算胶囊中的14C活度。
2) 纯化后样品中14C活度测量
在纯化后的洗脱液中加入14 mL Hisafe闪烁液,混合均匀,避光放置12 h后,采用LSC测量并计算样品中14C的活度。
1.5 14C及55Fe液闪测量效率校正
1)14C液闪测量效率校准
取系列14C标准淬灭源,用LSC测量计数,测量时间为5 min。由式(1)计算每个淬灭源的14C测量效率ε14C。
(1)
其中:Am为14C淬灭源的活度测量值,Bq;Ae为14C淬灭源的活度理论值,Bq;Di为14C样品两管符合计数;D0为空白两管符合计数;t为测量时间,s;
样品的三管、两管符合计数比(TDCR)计算公式如下:
(2)
其中:Ti为样品三管符合计数;T0为空白三管符合计数。
14C的测量效率与TDCR的关系曲线如图3所示,分析窗口为5~650道。
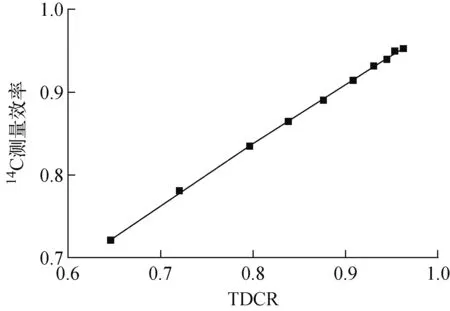
图3 14C的TDCR-LSC效率校正曲线Fig.3 TDCR-LSC efficiency correction curve of 14C
2)55Fe液闪测量效率校准曲线
LSC测量55Fe时选择的分析窗口为20~250道,淬灭校正曲线表达式如式(3)[8]所示。
ε55Fe=1.53TDCR0.91
(3)
1.6 流程验证
在尿素14C胶囊样品中,加入已知活度的标准55Fe,按照1.2节所述流程分离后,测量胶囊样品中55Fe的活度,验证流程的准确性。
2 方法的建立与验证
2.1 方法建立
55Fe的分离纯化可采用阴离子交换树脂、TRU树脂、溶剂萃取等手段[8,13]。阴离子交换树脂对铁有良好的选择性以及较高的吸附容量,铁离子与9 mol/L HCl生成阴离子络合物吸附在阴离子树脂柱上[8-9],而碳不会吸附在阴离子树脂柱上,可用适当的淋洗剂将其从树脂柱上洗脱,从而达到分离纯化的目的。测量尿素14C胶囊样品中的55Fe时需将14C完全去除,胶囊中14C活度在μCi级,远高于55Fe的活度,此外,55Fe淋洗液中含有高活度14C,不能直接排放,需在淋洗过程中考虑将淋洗液最小化,以方便放射性废物的后续处理。已报道的文献中,55Fe纯化时,每个样品淋洗液的体积超过60 mL[8-9],会生成大量放射性废液,因此需对方法进行改进。
将样品按1.2节溶解并调节酸度后,通过2 mL AGMP-1树脂柱,再用10 mL 9 mol/L HCl淋洗14C、0.1 mol/LHCl洗脱55Fe后测量,样品中14C残余量可达到30 Bq,会显著干扰55Fe的测量。将洗脱后的样品用12 mol/L HCl调至9 mol/L,再次通过2 mL AGMP-1树脂柱,用10 mL 9 mol/L HCl淋洗,淋洗液的测量结果示于图4。由图4可知,14C低于检测限(0.1 Bq),其测量谱与空白样品无差异。以上结果表明,采用AGMP-1树脂柱2次纯化可有效除去样品中的高活度干扰核素14C,并将淋洗液的体积减小至20 mL,有利于放射性废物的储存与处理。
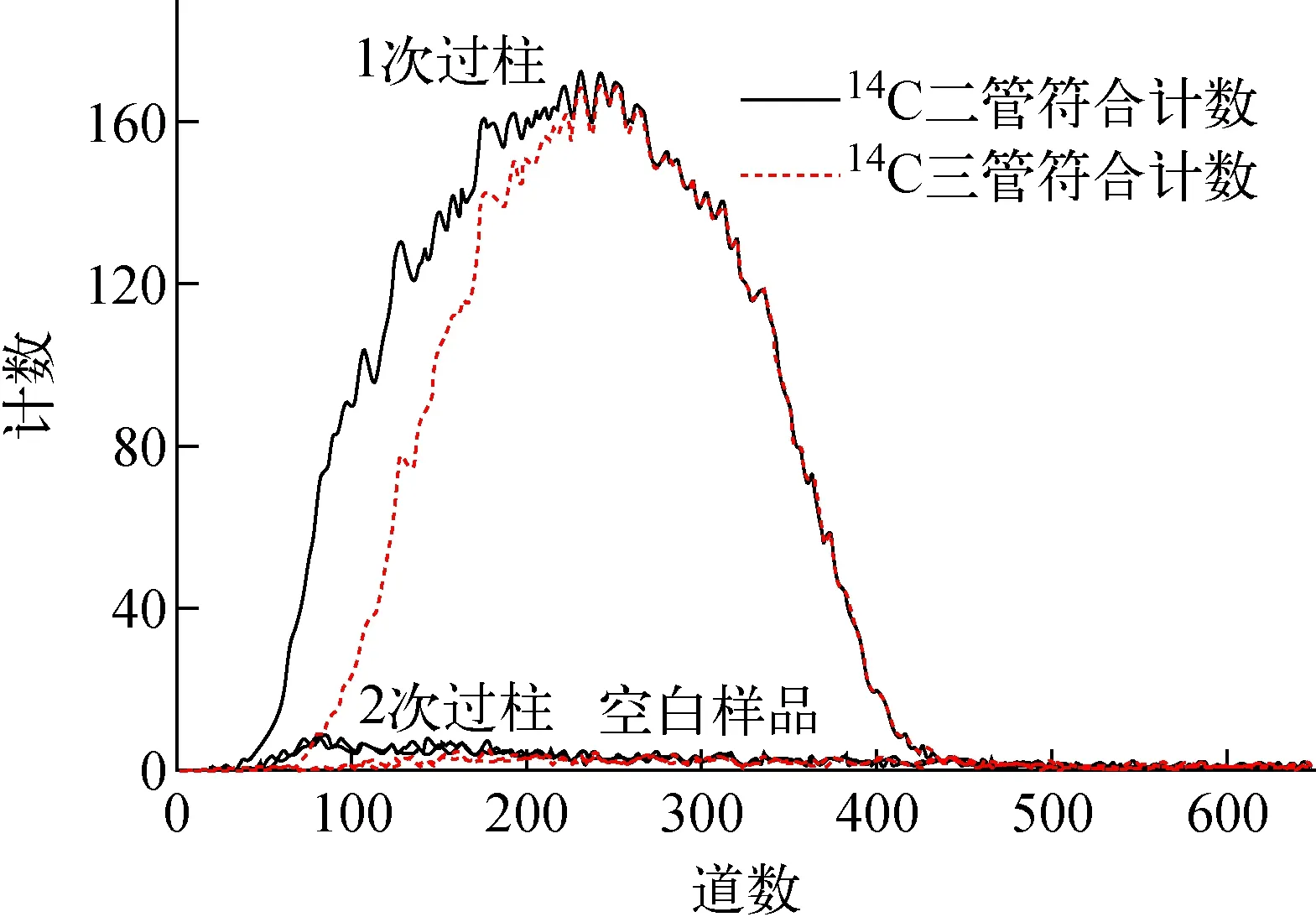
图4 AGMP-1树脂柱2次纯化后的胶囊样品与空白样品的14C液闪测量谱Fig.4 Liquid scintillation spectra of 14C in capsule sample after purified twice by AGMP-1 resin column and blank sample
2.2 尿素14C胶囊中放射性杂质55Fe核纯度限值估算
根据药品制剂中<1 mg 的单个杂质按1%或5 μg(取最小值)的质控限度要求[14],可限定其中任意一种放射性杂质核素所造成的辐射剂量(即待积有效剂量,CED)不高于尿素胶囊中14C 本身所致剂量的1%,即:
(4)
式中:CEDI为放射性杂质核素的待积有效剂量;CED14C为14C的待积有效剂量;DCFI为放射性杂质核素的剂量系数;DCF14C为14C的剂量系数;AI为胶囊样品中放射性杂质核素的活度;A14C为胶囊样品中14C的活度。据此,可推导出式(5)用以估算尿素14C胶囊的放射性核纯度(RP14C):
(5)
根据式(5)可限定尿素14C胶囊中放射性杂质核素的纯度。根据AlN靶中杂质元素的含量、中子反应截面、辐照时间及冷却时间估算,尿素14C胶囊中最主要的放射性杂质核素为55Fe和60Co。尿素14C胶囊中主要杂质的放射性核纯度计算结果列于表1。由表1可看出,放射性核纯度限值要求最高的杂质核素是60Co,假设所有的杂质都是食入剂量系数最大的60Co时,计算得到尿素14C胶囊制剂的放射性核纯度要求为99.83%。本工作取99.9%作为尿素14C胶囊制剂的放射性核纯度要求,相应地单个放射性杂质核素55Fe的限值要求为0.1%。

表1 尿素14C胶囊中14C及主要杂质核素的放射性核纯度估算结果Table 1 Estimation result of radionuclide purity of main impurity nuclide in urea 14C capsule
2.3 55Fe分析方法验证
尿素14C胶囊样品中55Fe活度的测定属于杂质核素的限量检查。根据药典2015年版[4]中“药品质量标准分析方法验证指导原则”,杂质限度测定方法的验证指标包括专属性、检测限和耐用性。
1) 专属性
尿素胶囊中14C活度约为3.7×104Bq,远高于胶囊样品中可能存在的55Fe的放射性活度,是测量55Fe最主要的干扰核素,14C的去污效果是影响方法专属性最主要的因素。本实验测量4批次胶囊样品中14C的初始活度,并根据式(6)计算流程对14C的去污因子(DF)。
(6)
式中:Q14C,0为初始样品中14C的活度,Bq;Q14C为纯化后样品中14C的活度,Bq;QFe,0为初始样品中加入的稳定铁的质量,mg;QFe为纯化后样品中稳定铁的质量,mg;RFe为铁的回收率(RFe=QFe/QFe,0)。
14C及55Fe的检测限(MDA)由式(7)[16]计算:
(7)
式中:k为包含因子,取值1.645(置信度为95%);B为液闪测量时空白样品的二管符合计数;f为用于液闪测量的样品质量与放化分离得到的样品质量的比值;ε为液闪计数器的测量效率。
4批次胶囊样品中14C的初始活度、纯化后活度及流程对14C的去污因子列于表2。由表2可见,纯化后14C活度均低于MDA,去污因子均>3×105,可见本方法可高效分离样品中的高活度干扰核素14C。因此,可认为本方法对尿素14C胶囊中55Fe的测量具有很强的专属性。

表2 不同批次尿素14C胶囊样品纯化后14C去污因子Table 2 14C decontamination factor of different batches of urea 14C capsule after purification
2) 耐用性
样品溶解、过柱、淋洗步骤中由于人为操作所造成的损失,均可由回收率进行校正,以确保方法的耐用性。流程开始时在尿素14C胶囊样品中加入稳定铁作为示踪剂,流程结束后,用XRF测量接入PE闪烁瓶中样品的稳定铁含量,每个样品测量3 min,计算样品浓度及回收率,结果列于表2。由表2可见,铁的回收率在57%~67%之间,回收率较低的样品可能是由于样品在多次上样、转移的过程中沾在容器壁上造成的损失。
3) 检测限
根据2.2节,胶囊样品中55Fe的放射性核纯度限值低于0.1%,14C的活度约为3.7×104Bq,故胶囊中若能准确测得37 Bq的55Fe,即可说明本工作建立的分离测量流程完全适用于胶囊样品中55Fe的测量。
在4个批次的尿素14C胶囊样品中分别加入约30 Bq和3 Bq的55Fe放射性标准溶液,按1.2节所示流程分离后,测量样品中55Fe的活度,结果列于表3,可见测量值与标称值的相对偏差小于±10%。

表3 加标样品的测量结果Table 3 Measurement result of spiked sample
胶囊样品加标前后的液闪测量谱示于图5。从图5可看出,采用55Fe分析流程分离纯化后的加标样品,55Fe 的信号明显可见,依据该谱图即可判断胶囊样品中是否含有高于核纯度限值的55Fe。

图5 加入标准55Fe样品与空白样品的液闪测量谱Fig.5 Liquid scintillation spectra of spiked standard 55Fe sample and blank sample
3 实际胶囊样品中55Fe的测量
按本文所建立流程测定上海某医药公司生产的4批次尿素14C胶囊的平行样品,结果列于表4。从表4可知,4批次样品均未检测到高于55Fe 检测限(0.4 Bq)的信号,满足55Fe放射性核纯度小于0.1%的质控要求。这主要是由于辐照后AlN靶需经过一系列化学转化合成流程最终制备成14C标记的尿素,这些化学转化及合成工艺对14C中的放射性核素杂质有极高效的分离效果。

表4 尿素14C胶囊样品中55Fe的测量结果Table 4 Measurement resultof 55Fe in urea 14C capsule
4 结论
1) 本工作计算了尿素14C胶囊样品杂质核素55Fe的限值,建立了尿素14C胶囊样品中55Fe活度测定方法:胶囊样品溶解后,采用AGMP-1阴离子交换树脂对其进行2次分离纯化,再用液体闪烁计数器测量55Fe的活度。
2) 验证了方法的专属性、耐用性和检测限。
3) 实际尿素14C胶囊实测结果表明,本文所建方法满足55Fe放射性核纯度小于0.1%的质控要求。

