50 W功率射频消融生物学效应的在体心脏实验研究
余凌祺 蒋晨阳
心房颤动(下称房颤)是临床上最常见的一种心律失常;而导管消融术是治疗房颤的常规有效手段,近年来在各房颤指南中的推荐级别越来越高[1-2]。射频能量是房颤导管消融最常用的一种能量,主要通过导管头端将射频电流转化为热能并释放到靶点的心肌组织,通过热损伤引起凝固性坏死,从而阻断异常的电活动、电传导。虽然房颤射频消融技术在不断进步,但仍存在引起邻近器官损害和心包压塞的风险[3-5]。传统的房颤射频消融治疗多采用25~35 W功率。近年来陆续有关于高功率房颤消融的报道,提示可有效治疗房颤[6-7]。除有效性外,高功率短时间主要通过阻抗热损伤心肌细胞,对邻近组织的损伤可能减少[8-10],但国内关于高功率消融的生物学效应研究较为少见。消融指数(ablationindex,AI)是目前量化组织消融损伤较为准确的指标,它是基于射频功率、消融持续时间和接触力等参数计算的,与预测消融损伤大小、实际靶点深度及宽度均有很好的相关性[11-13]。传统功率消融持续时间较长,而50 W高功率射频消融可以缩短消融持续时间,减少手术时间,但其生物学效应尚未明确。因此,本研究拟通过动物在体射频消融实验作一探讨,现将结果报道如下。
1 材料和方法
1.1 动物和仪器 体重约40 kg的健康成年雄性实验猪4头,由浙江大学医学院附属邵逸夫医院动物实验中心提供。标准的市售压力感知冷盐水灌注导管(Thermocool Smart TouchTMCatheter)、三维电生理标测系统(CARTO3)均购自美国强生Biosense Webster公司。本实验经浙江大学医学院附属邵逸夫医院动物伦理委员会审查通过。
1.2 消融手术 实验猪注射盐酸替来他明盐酸唑拉西泮(规格:50 mg/mL,批号:7VU4A,法国维克有限公司)麻醉,固定四肢,给予气管插管正压机械通气,持续监测肢体导联心电图。待完全麻醉后,于左侧第4肋间开胸,心包开窗悬挂,充分暴露心脏,0.9%氯化钠溶液灌注心包腔。直视下将消融导管置于心室外膜面进行消融,冷盐水灌注流速17~30 L/min。按消融功率不同分为两组,即50 W组、35 W组,其中50 W组接触压力控制在5~15 g,35 W组接触压力控制在5~25 g。两组在不同AI值(500、400、350)指导下完成消融心外膜损伤。
1.3 观察指标 实验猪经安乐死处理后,取心脏活检,核对各消融点位置,直视下消融灶呈圆形,沿最大直径切入每个灶的中心,使用数字精密游标卡尺测量每个消融损伤表面最大直径及最大深度,见图1。
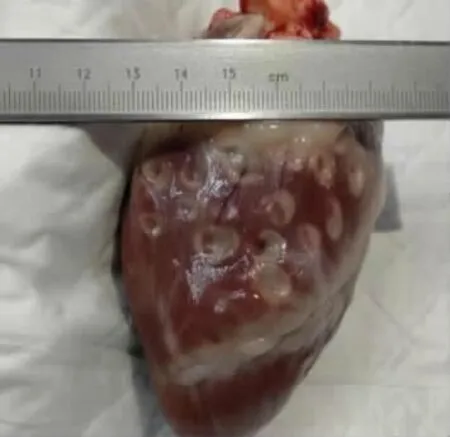
图1 消融后实验猪心脏外观与测量
1.4 统计学处理 采用SPSS 22.0统计软件。计量资料以表示,两组间比较采用两独立样本t检验;组内不同AI值指导下相关指标比较采用单因素方差分析,两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2 结果
心室外膜消融共产生66个消融损伤,其中50 W组不同AI值(500、400、350)指导下消融分别产生11、12、12个损伤点,35 W组分别产生11、10、10个损伤点;在所有消融点中,未发现有POP或焦痂产生。在50或30W功率下,消融损伤表面最大直径、最大深度及消融持续时间均随AI值增加而增加,差异均有统计学意义(均P<0.05)。在AI=500、400的指导下消融,50 W组产生的消融损伤表面最大直径均大于35 W组,最大深度均小于35 W组,消融持续时间均短于35 W组,差异均有统计学意义(均P<0.05);在AI=350的指导下消融,50 W组产生的消融损伤表面最大直径、最大深度均大于35 W组,消融持续时间短于35 W组,差异均有统计学意义(均P<0.05),见表1和图2-3。
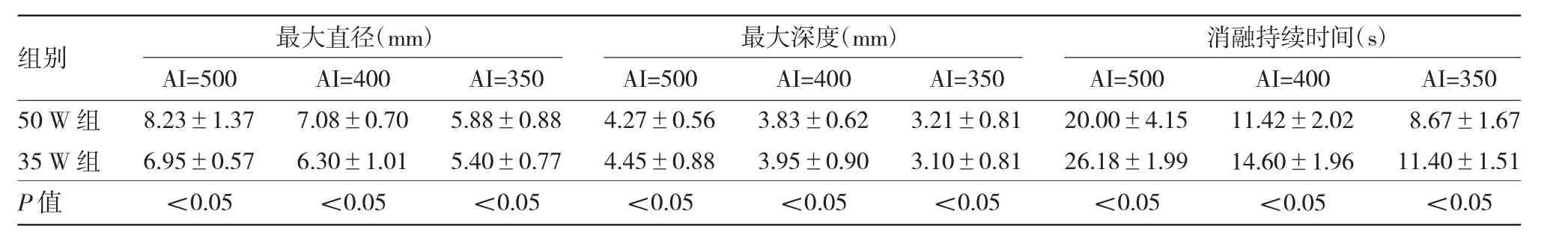
表1 50 W组与35 W组在不同消融指数(AI)值指导下消融产生的消融损伤表面最大直径、最大深度及消融持续时间比较
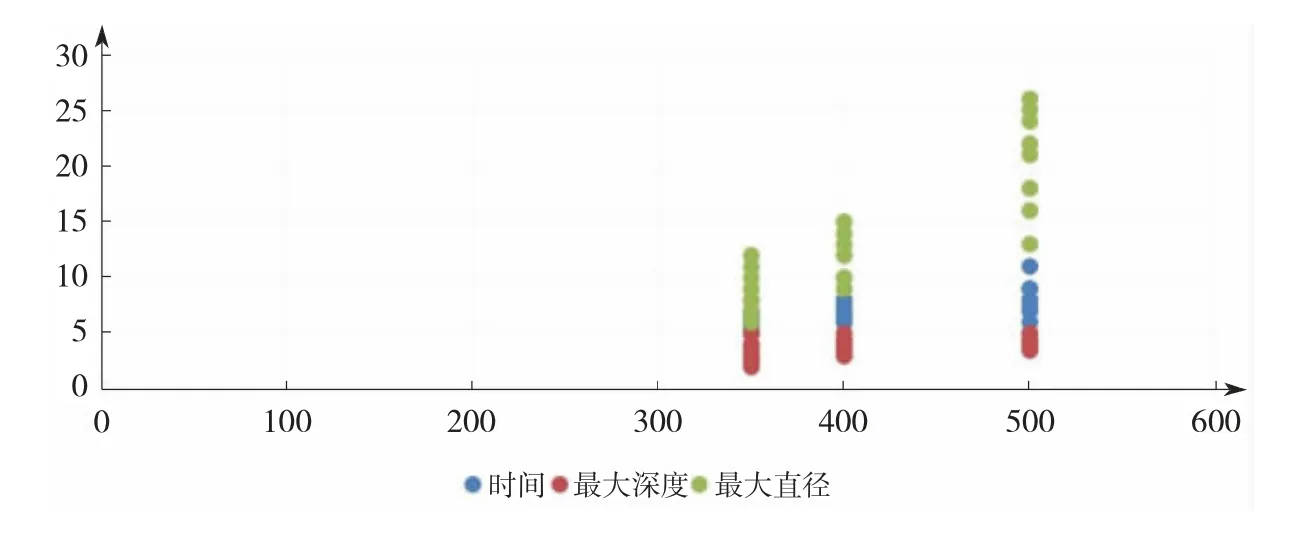
图2 50 W组在不同消融指数(AI)值指导下消融产生的消融损伤表面最大直径、最大深度及消融持续时间比较
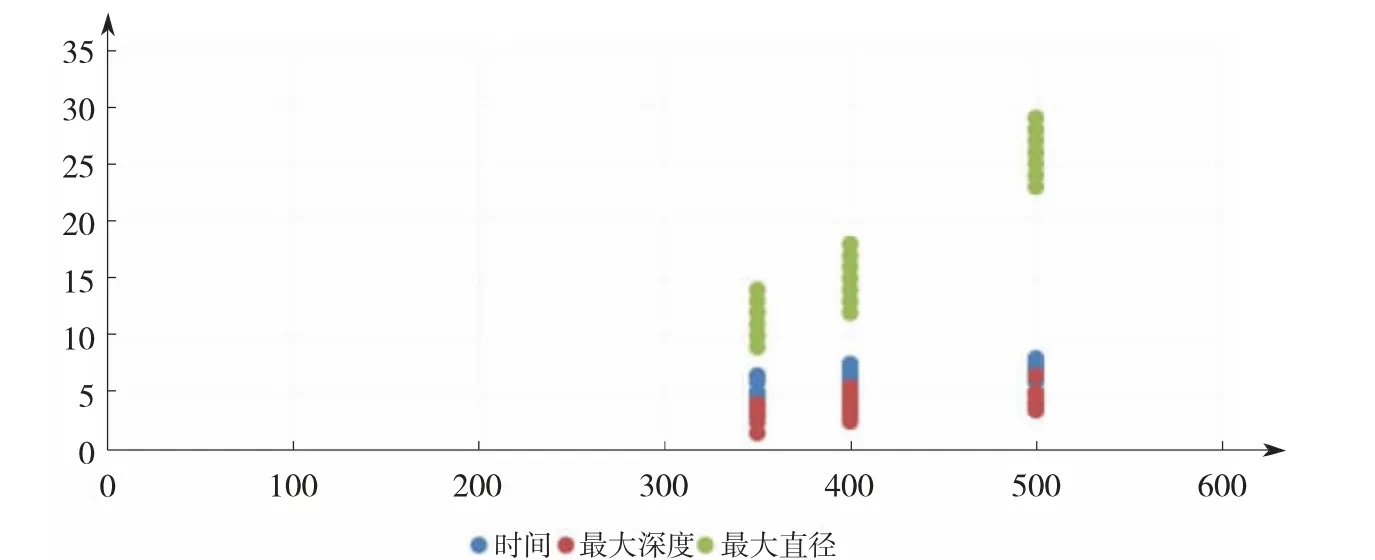
图3 35 W组在不同消融指数(AI)值指导下消融产生的消融损伤表面最大直径、最大深度及消融持续时间比较
3 讨论
AI是衡量消融损伤大小的量化指标。既往动物实验功率多采用25~45 W,目前尚缺少50 W的研究数据[14]。故本研究在不同AI值指导下消融,比较功率50 W与35 W所致的消融损伤灶大小,当AI值相等时,50 W组消融损伤表面最大直径较35 W组大,最大深度较小,消融持续时间较短;而在相同功率(50或30 W)下,消融损伤表面最大直径、最大深度及消融持续时间均随AI值增加而增加。从射频消融原理分析,射频损伤有两个机制[15-16]:(1)直接电阻热引起的损伤,发生在消融导管头端的局部组织内(心肌贴靠电极处),导管-组织界面电阻热引起表层组织立即加热升温,局部温度>50℃,导致心肌细胞凝固性坏死等不可逆损伤。功率越高,产生的阻抗热在组织内的作用越强;(2)被动的传导热,电阻抗热向周围组织传导产生,并传导至较深的组织层。热传导是消融致邻近器官损伤的主要因素,可能导致心脏邻近器官如食管和膈神经等的损伤。热传导与消融时间成正比,消融持续时间越长,热传导的损伤越深。在射频消融过程中,局部电阻热会在数秒内达到峰值,即射频消融第一阶段主要通过电阻热损伤靶心肌组织,接着阻抗热向邻近组织传导。本研究结果显示,在35 W设置下进行射频消融,消融持续时间较长,传导性加热增加,周围组织被加热;而50 W功率短时间消融,高功率能量产生更大阻抗热,由于消融持续时间较短,限制了热量的进一步传导,减少传导热。
Bourier等[17]利用计算机模型和组织实验表明,高功率短时间消融时最大的病变增长出现在射频能量输送的前10 s内。本研究结果显示,50 W/350 AI、35 W/350 AI消融持续时间分别为(8.67±1.67)、(11.40±1.51)s。在50、35 W消融功率下,AI=350的损伤深度主要由电阻热产生,而传导热较少,阻抗热的消融损伤大小主要与功率有关,功率越大则消融灶越大。因此,在AI=350的指导下射频消融,50 W组消融损伤表面最大深度大于35 W组。Beinart等[18]通过对肺静脉隔离患者的心脏CT扫描发现,左心房壁厚度为(1.89±0.45)mm;后壁是整个左心房较薄区域,厚度为(1.43±0.44)mm,其中后壁上方最薄;二尖瓣峡部、左心房嵴部及左心房中上部较其他区域厚,厚度分别为(2.05±0.47)、(2.10±0.63)、(2.15±0.47)mm。Nakamura等[19]报道阵发性房颤患者左心房壁厚度平均为2.4 mm,而慢性房颤患者为2.1 mm,窦性心律患者为1.9 mm。据先前解剖和影像学研究报道,食管位于左心房后方5 mm处,与最薄区域特别接近。传统的射频消融持续时间为20~30 s,在30 s时,平均病变深度为7.25 mm。使用传统功率射频消融可能存在食管损伤的风险,进而导致心房食管瘘等[20-24]。Bhaskaran等[25]在绵羊模型体内及体外消融实验中,以50 W功率消融5 s,产生的病变深度平均为2.3 mm,所有病变(肌小梁除外)都是透壁的。高功率短时间消融可导致更大的病变直径和更小的病变深度,缩小的病变仍可以在平均厚度为2 mm的心肌中达到透壁的消融效果。
另外,心房内消融中导管接触压力、消融持续时间与消融安全性密切相关。压力过大、消融持续时间过长,会增加心肌穿孔、邻近组织损伤等风险[26]。心房食管瘘是房颤消融的严重并发症之一,其发生率较低(0.015%~0.2%),但致死率极高[27-28]。有研究尝试各种方法保护食管避免损伤,如对食管消融前和消融时进行成像、预防性的食管黏膜保护、对食管管腔温度进行监测、限制后壁的消融能量、食管隔热等,但结果并不一致[29-30]。食管损伤的发生和食管与消融靶点的距离有关,减少后壁消融压力有助于避免食管损伤。本实验数据提示,50 W功率短时间消融,可以在相对低的接触压力情况下,更快地达到类似大小的消融损伤灶,宽度更大,深度更小,提示功率50 W左心房后壁消融可能有助于减少对食管的损伤。最近研究提示,当左后房壁的接触力值限制在<20 g时,可避免食管损伤的风险[31]。另外,接触压力过高可能增加手术并发症的风险,如心脏压塞、蒸汽爆裂、导管尖端碳化、食管损伤等[4-5]。
综上所述,在相同AI值指导下消融,50 W较35 W产生的消融损伤表面最大直径更大,最大深度更小(AI=350除外);相同功率下,消融损伤表面最大直径及最大深度随AI值增加而增加。本研究也存在一定的局限性,如在全麻直视下对猪心室外膜进行消融,而心外膜没有红细胞,消融导管头端无焦痂产生,与临床上心内膜消融环境可能有所区别等。