疏水低共熔溶剂萃取金属离子研究进展
张鹤鹏, 陈金清
(江西理工大学材料冶金化学学部,江西 赣州341000)
2003 年 Abbott 等发现氯化胆碱(熔点=302 ℃)与尿素(熔点=133 ℃)2∶1(摩尔比,下同)的混合物在室温下为液体且具有独特的溶剂性质,将这种室温液体混合物称为低共熔溶剂(deep eutectic solvent,DES)[1]。DES 可以定义为2 种或2 种以上纯化合物(即,氢键受体和氢键供体)形成的混合物,通过混合熵、范德华相互作用和氢键作用使其熔点远低于单个组分的熔点的室温液体[2-3]。 DES 具有与离子液体相似的理化性质,例如蒸气压低、液体范围宽、导电性、增溶性好等[4-5]。 通过改变混合物的组成、比例和含水量可以对DES 的理化性质进行调整,在催化、燃油脱硫、药物释放、活性物质的提取、有机合成、金属氧化物的浸出与金属电沉积等领域具有广泛应用[6-10]。 例如,Tran 等利用DES 能溶解氧化物的特性,将氯化胆碱与乙二醇组成DES 用于废弃锂离子正极材料的浸出[11]。Hammond等利用DES 具有催化功能的特性,使用氯化胆碱与尿素组成的DES 催化合成纳米二氧化铈[12]。
氯化胆碱和尿素是报道最早的DES, 也是近年来研究最多的一种DES[13]。后续在此基础上又开发了由氯化胆碱、甜菜碱、四烷基季铵(膦)盐等为氢键受体(Hydrogen Bond Acceptor,HBA),由醇、酸和酰胺为 HBD 组成的 DES[14]。 早期报道的DES,由于起始组分亲水且内部氢键的增溶作用,可与水混溶,只能应用于非水介质且难以循环[15]。2015 年,Van Osch 等以季铵盐为HBA,癸酸为HBD 设计了一类DES,其在水中的溶解度可以低至11 mg/g[16]。 疏水DES 的引入扩展了DES 运用范围,在萃取分离的各个领域获得了广泛关注[17-19]。疏水DES 对金属离子的萃取于2016 年首次报道。 Tereshatov 等以四庚基氯化铵或薄荷醇为HBA, 羧酸为HBD 设计了4 种疏水DES用于从盐酸体系中萃取铟[20]。 由于DES 与离子液体一样具有可设计性;且制备工艺更加简单,原料来源更广[21-22]。国内外关于萃取金属离子的疏水DES 报道迅速增加。 本文概述了2016 年以来用于萃取分离金属离子的疏水DES 结构设计现状, 分析了疏水DES理化性质与其组成的关系, 介绍了近年来疏水DES萃取金属离子的研究进展, 总结了目前疏水DES 用于工业分离过程存在的问题, 展望了疏水DES 用于金属萃取分离的未来研究方向。
1 疏水DES 分子结构
DES 制备过程不需要溶剂,也不需要发生传统意义上的反应。 最常用的制备方法为将一定摩尔比的HBA 和HBD 在惰性气氛下加热搅拌, 直到形成均匀的液体。 液体在室温下保存24 h 未有固体析出,表明DES 已制备成功[23]。 DES 在制备过程中不会发生化学反应,与组成DES 的起始组分相比,只有分子间作用力的改变。核磁共振光谱仪和红外光谱仪检测表明,组成DES 后,HBA 或HBD 分子内的氢键消失或减弱,HBA 和HBD 分子间的氢键形成并占主导地位[16,24-27]。
在DES 的其它萃取领域,已有3 组分DES 用于萃取的报导[28-29]。但萃取金属离子的疏水DES 仍由单一HBA 和单一HBD 2 种组分组成。 DES 组分中,HBA 与HBD 需根据物质的酸度系数pKa值的大小判断。 pKa大的组分作为HBA,pKa小的组分作为HBD。 表1 列出了一些已被设计用于金属离子萃取的疏水DES 组分的结构与熔点。 如表1 所列,用于萃取金属离子的疏水DES,起始组分熔点均小于100 ℃,且多数含有能与金属离子配位的官能团。 常见疏水DES 的组合包括:

表1 用于金属离子萃取DES 组分的结构与熔点Table 1 Structure and melting point of components of DES used for metal ion extraction
1)以叔胺或烷基季铵(膦)盐为 HBA,羧酸为HBD[20-21,25,27,30-31];
2)以三辛基氧化膦为HBA,醇或酚为HBD[32-34];
3)以醇或酚为 HBA,羧酸为 HBD[20,35-36]。
此外,HBA 与HBD 之间通过酸度差异也能形成DES[21,37]。例如,辛酸、壬酸、癸酸和月桂酸以一定比例混合可以形成DES[26]。 三辛基氧化膦与β-二酮类化合物之间也可以组成DES(图1)[24]。

图1 三辛基氧化膦(TOPO)与噻吩甲酰三氟丙酮(HTTA)混合后形成的DES[24]Fig. 1 DES formed by the mixture of trioctyl phosphine oxide (TOPO) and thiophenoyl trifluoroacetone(HTTA)
2 疏水DES 理化性质
疏水DES 是一种新型的溶剂, 分析其理化性质能更直观地了解疏水DES。 表2 列举了一些用于萃取金属离子的疏水DES 的常见理化性质。 疏水DES在萃取的同时充当稀释剂与萃取剂,在液-液萃取的工业规模应用中,稀释剂和萃取剂的密度,黏度,疏水性是溶剂与萃取剂选择的关键因素。黏度大不利于有机相和水相的传质;有机相与水相密度相近会导致分相困难; 有机相疏水性不强不仅会使萃取剂流失,而且会污染萃取后的水相[19,38]。
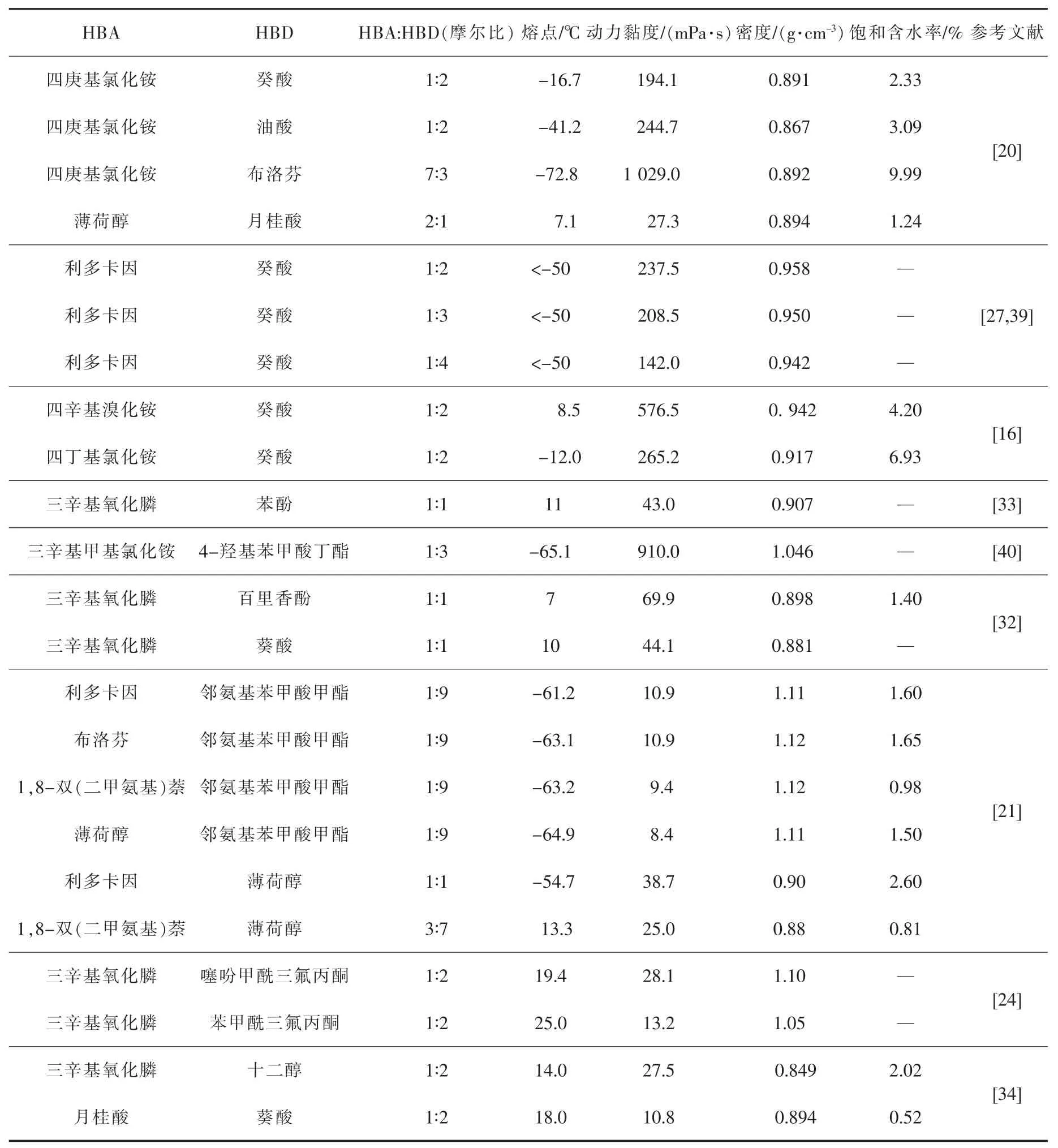
表2 用于萃取金属离子的疏水DES 的常见理化性质Table 2 Common physicochemical properties of hydrophobic DES for extraction of metal ions
疏水DES 的密度与分子的堆积及其组分之间的相互作用有关,但存在显著的规律。例如,三辛基氧化膦和苯酚组成的DES 密度介于单一组分之间, 密度大组分相对含量增加,密度变大[33]。 由三辛基甲基氯化铵与4-羟基苯甲酸酯组成的DES 随着4-羟基苯甲酸酯相对含量的增加,密度变大[40]。 薄荷醇与饱和脂肪酸组成的DES 密度随着一元羧酸烷基链的增加而降低,与一元羧酸的密度变化规律相同[41]。 季铵盐与癸酸组成的DES 密度随季铵烷基链长度的增加而减小,密度大小依次为:四丁基氯化铵:癸酸>四庚基氯化铵:癸酸>四辛基氯化铵:癸酸[16]。 温度上升会使DES 的密度呈线性下降[16,33,39]。 此外,由于 DES 具有一定的吸水能力,在与水预饱和后,DES 的密度会向水的密度偏移[26,39]。
疏水DES 的黏度不仅取决于HBD 和HBA 的自身的化学性质,HBD 和HBA 之间的氢键强度也会对黏度产生影响[42]。 例如,百里香酚与饱和脂肪酸的共晶混合物的黏度介于纯组分的黏度之间[41]。 利多卡因和癸酸组成的DES 黏度随癸酸相对含量增加而减小[27]。组成DES 的烷基链越短,黏度越低[26,41]。 叔胺或季铵盐与羧酸形成的DES,由于其内部的静电相互作用强,空隙体积小, 离子尺寸大, 往往具有较高的黏度(142~1 029 mPs·s)[7]。需要指出的是,同一 HBA 与不同HBD 在固定摩尔比下的黏度没有直接的正相关关系。 DES 黏度随温度变化明显,温度的升高导致黏度的大幅下降[20,26,33]。 DES 吸水后黏度下降[21,31]。
疏水DES 的疏水性能可以通过HBD 和HBA 结构及组成进行推测,主要可以分为3 种类型。 第1 类是由季胺(膦)盐和羧酸组成的疏水DES,由于内部存在离子型氢键,其在水中的溶解度会大于单一组分的溶解度[16,20,25]。 第 2 类是由叔胺为 HBA 组成的 DES,由于叔胺在酸性条件下会质子化,在萃取金属后叔胺会转移到水相中[21,27,30]。剩余的DES 可以归于第3 类。这类DES 内部通过非离子型氢键结合, 使这类DES溶解度会小于单一组分的溶解度。 例如,三辛基氧化膦和苯酚组成的DES 后, 三辛基氧化膦的溶解度由0.15 g/L 下降至0 g/L, 苯酚的溶解度由88 g/L 下降至1 g/L[33]。百里香酚和饱和脂肪酸组成疏水DES 后,百里香酚的在水中的溶解度下降了一个数量级[41]。
3 疏水DES 用于金属离子的萃取
疏水DES 在金属离子萃取领域的发展迅速,已被用于分离提取各种金属离子。按照主要发挥萃取作用的组分结构来划分,用于萃取金属离子的疏水DES主要有4 种类型:第1 类是由四烷基季铵(膦)盐为主要萃取组分的DES;第2 类是由叔胺为主要萃取组分的DES;第3 类是以羧酸为主要萃取组分的DES;第4 类是以三辛基氧化膦为主要萃取组分的DES。
3.1 季胺(膦)盐型DES
三辛基甲基氯化铵和三己基十四烷基氯化膦是性能优异季铵(膦)离子液体,通过阴离子交换可提取金属含氧酸根阴离子 (TcO4-,ReO4-,HCrO4-,HV2O5-和 HWO4-等), 或者利用金属阳离子在高盐(Fe3+,Re3+,In3+,Zn2+,Cu2+,Co2+,Mn2+,Fe2+,VO2+)体系具有阴离子化的特性,可与溶液中的阴离子(Cl-,NO3-,SO42-)形成络阴离子被季铵(膦)离子液体萃取[43]。两者的结构如图 2 所示。 季胺(膦)盐型DES 具有和季铵(膦)离子液体相似的官能团,已被用于从水溶液中萃取各种金属含氧酸根阴离子与金属络阴离子。

图2 季铵(膦)离子液体的分子结构Fig. 2 Molecular structure of quaternary ammonium (phosphine) ionic liquid
Tereshatov 等报道了3 种疏水DES 从盐酸体系萃取In(Ⅲ)的方法,四庚基氯化铵:布洛芬(代表HBA:HBD,下同)(7∶3),四庚基氯化铵:油酸(1∶2),四庚基氯化铵:癸酸(1∶2)3 种 DES 对 In(Ⅲ)的萃取能力分别为四庚基氯化铵:布洛芬(7∶3)>四庚基氯化铵∶油酸(1∶2)≈四庚基氯化铵:癸酸(1∶2)。 在水相 HCl 浓度为6 mol/L,3 种疏水DES 均可以完全提取 In (Ⅲ)。DES 萃取铟的机理主要是因为离子对的形成,萃取机理如式(1)所示。 负载 In(Ⅲ)的 DES 相用 0.1 mol/L 二乙烯三胺五乙酸,可成功反萃取至水相[20]。
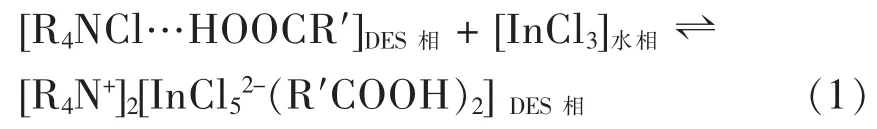
Phelps 等开发了三己基十四烷基氯化膦: 癸酸(1∶2),四辛基溴化铵:癸酸(1∶2),四辛基溴化铵:己酸(1∶2)3 种疏水 DES 从水溶液中萃取痕量99mTcO4-。 在水相初始pH 值为5 时,3 种DES 均可以在含有大量Cl-,NO3-,HCO3-,H2PO4-,SO42-的体系中定量(>99%)去除99mTcO4-,但负载99mTcO4-的 DES 再生比较困难[25]。其萃取机理如式(2)所示。

Ruggeri 等演示了四丁基氯化铵: 癸酸 (1∶2)的DES 从水介质中萃取Cr(Ⅵ),在弱酸性条件下,疏水DES 可以将水溶液中的Cr(Ⅵ)去除至0.3 mg/L 以下,提取的 Cr(Ⅵ)在 DES 相中会自动被还原为 Cr(Ⅲ),萃取其他金属如铜(Ⅱ)和镍(Ⅱ)会导致DES 的胶凝[31]。Shi 等研究了三辛基甲基氯化铵:4-羟基苯甲酸丁酯(1∶1)的 DES 用于从废水中去除 Cr(Ⅵ),水溶液中离子强度的增加会使Cr(Ⅵ)萃取效率降低,影响次序依 次为 NO3->Cl->SO42-[40]。 DES 可 以 在 金 属 离 子(Cd2+、Cu2+)与有机化合物((C6H10O5)n、C6H12O6·H2O)共存浓度为Cr(Ⅵ)的2 000 倍时选择性提取Cr(Ⅵ)。选择性萃取的原理为在酸性条件下Cr (Ⅵ) 主要以HCrO4-形式存在,HCrO4-与三辛基甲基氯化铵中的N+(R3R)通过静电相互作用使Cr (Ⅵ)从水相中转移到 DES 相中[31]。 季铵(膦)盐型 DES 提取 Cr(Ⅵ)的机理如式(3)所示:

Chen 等使用四丁基氯化铵:油酸(1:3)与 TBP 协同萃取 Li(I),在 DES 添加量为 30%,相比=1、氨水为1.5 mol/L 的较优萃取条件下,协同萃取体系对Li+单次萃取率可达 76.8%,βLi/Na值为 20.5。Li(I)和 DES 之间的阳离子交换以及Li(I)与TBP 之间膦氧键的配位作用导致了 Li(I)的选择性萃取。 使用 1 mol/L 的盐酸可以反萃97%的锂,有机相循环使用5 次,萃取效率仍在60%以上[44]。
与季铵(膦)离子液体相比,季胺(膦)盐型DES 在黏度上表现出更优异的性能。 298.15 K 下季胺(膦)盐型 DES 黏度在 194.1~1 029 mPa·s 之间, 而未稀释的三辛基甲基氯化铵和三己基十四烷基氯化膦离子液体的黏度分别为 2 391.4 mPa·s 与 2 729.1 mPa·s[45-46]。季胺(膦)盐型DES 与季铵(膦)离子液体对金属含氧酸根离子具有一致的萃取规律, 对水合能较小的金属含氧酸根阴离子均表现出高萃取能力。对于高盐体系下金属阳离子的萃取,季胺(膦)盐型DES 的萃取能力明显偏弱。 四庚基氯化铵和羧酸组成的DES 需在6 mol/L HCl 体系才能完全提取In(Ⅲ),而季铵(膦)离子液体在2 mol/L HCl 条件下即可完全提取In(Ⅲ)。 多数季胺(膦)盐型 DES 的稳定性较差,四辛基溴化铵:癸酸(1∶2),四辛基溴化铵:己酸(1∶2)在萃取99mTcO4-后会有固体析出;四丁基氯化铵:癸酸(1∶2)在萃取铜(Ⅱ)和镍(Ⅱ)后DES 会胶凝;四丁基氯化铵:油酸(1∶3)在碱性条件下会与 Li(I)进行阳离子交换,四丁基氯化铵会进入水相。
根据不同的萃取机理,季铵(膦)离子液体的反萃有多种方式。可用的反萃试剂包括水,酸和碱,其中碱是最有效的反萃试剂[47-50]。 多数金属含氧酸根阴离子与季铵(膦)类化合物的稳定常数大,需用强碱进行反萃。 季胺(膦)盐型 DES 的反萃受 HBA 的限制,以羧酸为HBA 的季胺(膦)盐 DES 在强碱性下结构可能受到破坏。 季铵(膦)离子液体提取金属络阴离子后,一般使用水或者稀酸进行反萃,三己基十四烷基氯化膦萃取In(Ⅲ)后可通过0.1 mol/L 盐酸完全反萃[51]。而四庚基氯化铵:油酸(1∶2)在萃取 In(Ⅲ)后使用0.2 mol/L 盐酸反萃率仅有25%。 就目前而言, 季胺(膦)盐型DES 相比与季铵(膦)离子液体在金属离子萃取领域并无的优势。
3.2 叔胺型DES 用于金属离子萃取
N235 是工业上常用的叔胺萃取剂, 其主要成分为三辛癸烷基叔胺。与季铵(膦)离子液体类似,N235在酸化后可萃取各种含氧酸根阴离子和金属络阴离子[52-55]。 由 N235 与 P507 的协同萃取体系,还可用于无皂化提取稀土[56-57]。 不同于N235,以利多卡因和1,8-双(二甲氨基)萘为 HBA 的叔胺型 DES 不具备在酸性体系萃取金属的能力。根据Edgecomb 等的研究,利多卡因:邻氨基苯甲酸甲酯(1∶9),利多卡因:薄荷醇(1∶1),1,8-双(二甲氨基)萘:邻氨基苯甲酸甲酯(1∶9),1,8-双(二甲氨基)萘:薄荷醇(3∶7)4 种 DES 的HBA 在酸性条件下都会大量进入水相。 水相平衡pH<4 时,4 种 DES 的 HBA 在水相中的溶解度均大于0.3 mol/L[21]。 目前叔胺型DES 的开发主要围绕如何提升叔胺型DES 的疏水性能, 并附带了一些对金属离子萃取的测试。
Van Osch 等研究了利多卡因: 癸酸组成的DES从水溶液中萃取过渡金属和碱金属。 利多卡因:癸酸可在自然pH 条件下萃取水溶液中的Co (Ⅱ),Fe (Ⅱ),Mn(Ⅱ),Ni(Ⅱ),Zn(Ⅱ)与 Cu(Ⅱ),但对碱金属 Na(I),K(I)和 Li(I)的萃取效果较差,DES 中利多卡因的相对含量越高,对金属离子的萃取能力越强[27]。 其萃取机理与N235 和P507 的非皂化协同萃取类似, 利多卡因夺取了癸酸的氢离子使癸酸的萃取能力变强,在萃取金属离子后,质子化的利多卡因会和金属离子发生阳离子交换转移到水相中。 Ola 和Matsumoto 将利多卡因:癸酸(2∶1)溶于正庚烷进行了进一步研究,在初始 pH 值为 1.5,Fe(Ⅲ)和 Mn(Ⅱ)均为 0.01 mol/L时,通过调节有机相中的DES 浓度,可以依次从溶液中分离 Fe(Ⅲ)和 Mn(Ⅱ)[30]。 但仍未解决利多卡因在提取金属后进入水相的问题。 基于利多卡因:癸酸组成的DES 其萃取实质如式(4)所示:

Edgecomb 等基于活性药物和食品级成分开发出4 种的疏水性和低黏度DES 用于萃取In (Ⅲ)。利多卡因:邻氨基苯甲酸甲酯(1∶9),利多卡因:薄荷醇(1∶1),1,8-双(二甲氨基)萘:邻氨基苯甲酸甲酯(1:9),1,8-双(二甲氨基)萘:薄荷醇(3∶7),4 种 DES均能实现高效的In (Ⅲ)提取,在提取In (Ⅲ)后,DES 中的 HBA 仍会进入水相[21]。 作者对 DES 萃取In(Ⅲ)的机理推测如式(5):
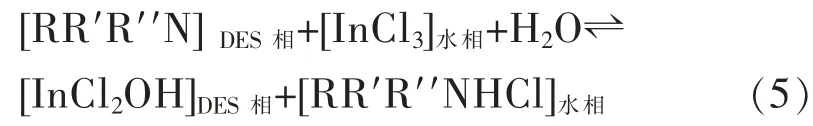
叔胺型DES 的开发还处在早期阶段, 研究人员做过很多尝试。 通过更换HBA 或HBD 的结构,或将其溶于有机溶剂中以减少叔胺质子化后的损失。但均未取得突破性的进展。即使在中性的萃取环境中,在提取金属离子后叔胺型DES 中的HBA 仍会进入水相。 就目前而言,叔胺类DES 还不适合进行金属离子的萃取。
3.3 羧酸型DES 用于金属离子萃取
目前,工业上常用的羧酸类萃取剂包括环烷酸和叔碳酸(versatic 10)。 环烷酸广泛用于稀土料液中铝的去除和钇的提纯[58-59]。 versatic 10 是红土镍矿硫酸浸出液的钴镍提取的特效萃取剂[60]。 长链脂肪酸(碳链大于10)熔点高,油溶性差,在工业上不适合做萃取剂。羧酸型DES 的出现解决了长链脂肪酸油溶性差和熔点高的问题。 且羧酸型DES 的起始原料绿色环保,价格低廉,生物相容性好,具有较好的商业化前景。
Tereshatov 等研究了薄荷醇:月桂酸(2∶1)的 DES对 In(Ⅲ)的萃取。 DES 对 In(Ⅲ)的萃取率随 pH 值的升高而增加,与癸酸在煤油中萃取In(Ⅲ)的规律一致[20]。马尚文等研究了不同碳数双脂肪酸疏水DES的合成, 并考察了其对水溶液中铜离子的萃取效能。当月桂酸与癸酸物质的量比为1∶2 时,可以在室温下组成DES。将其用于含铜废水处理,在相比为1,水相pH 值为 4.1~4.7,铜离子浓度为 10 mg/L,震荡时间为60 min 时,对铜离子的去除率可达93.24%[61]。
陈倩文开发了薄荷醇:癸酸(1∶1)、薄荷醇:油酸(1∶1)、百里酚:癸酸(1∶1)和百里酚:油酸(1∶1)4 种 DES,并用于从含钍放射性废渣浸出液中回收Th(IV)。 4 种DES 对 Th 的萃取能力强弱依次为百里酚:癸酸(1∶1)>百里酚:油酸(1∶1)>薄荷醇:癸酸(1:1)>薄荷醇:油酸(1∶1)。 在水相初始 pH 值为 3,相比为 1,平衡时间为 10 min 条件下,使用百里香酚:癸酸(1∶1)从含钍放射性废渣模拟浸出液中萃取分离 Th (Ⅳ)/REEs(Ⅲ),经单级萃取-洗涤-反萃后,Th(Ⅳ)最终的回收率为96.4%,纯度为94.2%,萃余液中Th(Ⅳ)的浓度低于 2 mg/L,Th(IV)/REEs(Ⅲ)的分离系数达到3 223[35]。
Schaeffer 等研究了以薄荷醇/百里香酚和饱和脂肪酸 (链长分别为 8,10,12,14,16 和 18) 组成疏水DES 对过渡金属离子的萃取能力。 DES 对过渡金属离子的萃取能力随脂肪酸链长增加而减弱, 随脂肪酸相对含量增加而增加。 水相加入 0.1 mol/L 的Na2SO4可使DES 的萃取效率提高10%。百里香酚:葵酸(3∶7)的 DES 对过渡金属 Fe(Ⅱ)、Cu(Ⅱ)和 Fe(Ⅲ)具有较好的萃取能力,对 Cr(Ⅲ)、Mn(Ⅱ)、Co(Ⅱ)和Ni(Ⅱ)的萃取能力不佳(图 3)。 在 pH=4.9,T=20℃,相比=1 时,对 Cu(Ⅱ)/Co(Ⅱ)和 Cu(Ⅱ)/Ni(Ⅱ)的分离系数分别达到 500 和 154。 使用 0.1 mol/L 硫酸反萃Cu(Ⅱ)可以再生 DES[36]。

图3 百里香酚:葵酸(3∶7)的DES 对常见金属的萃取[36]Fig. 3 Extraction of common metals by DES of thyme:truvic acid(3∶7)[36]
Ni 等使用月桂酸:葵酸(2∶1)的 DES 对废 SmCo 磁体浸出液中的 Cu(Ⅱ)、Co(Ⅱ)进行了分离。 对 Co(Ⅱ)含量为21.90 g/L、Cu(Ⅱ)含量为2.51g/L 的浸出液进行单级萃取,并对负载有机相进行三级洗涤和反萃。Co(Ⅱ)、Cu(Ⅱ)纯度均可达到 98.50%以上。 Co(Ⅱ)、Cu(Ⅱ)的回收率分别为 99%、96.47%。 月桂酸:葵酸(2∶1)萃取铜的机理为阳离子交换,通过调节水相的pH 可以选择性的萃取或者反萃金属离子。 疏水DES中没有与铜配位的部分起溶剂的作用[34]。
羧酸型DES 对金属离子的萃取机理可以定义如式(6):
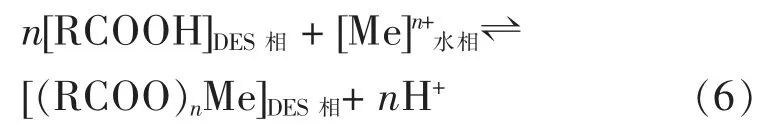
羧酸型DES 具有优异理化性质。黏度低,与水的密度相差大,疏水性能强,可以很好的萃取以及反萃金属离子,具有优异的循环性能,但熔点仍偏高。 与常规萃取体系相比, 羧酸型DES 可看成一种无稀释剂的协萃体系, 其萃取能力与起始组分羧酸酸性和含量直接相关, 内部的氢键降低其对某些金属离子的萃取动力学和萃取能力。 羧酸型DES 内部的氢键作用对萃取能力的影响明显强于羧酸酸性对萃取能力的影响,预计通过改变HBD 的结构,可调节羧酸型DES 对不同金属的选择性。 目前羧酸型DES 对金属分离的研究集中在一些易于分离的金属离子,无法充分发挥DES 的选择性和可设计性, 应加深对性质相近金属的分离研究。
3.4 三辛基氧化膦型DES 用于金属离子萃取
三辛基氧化膦是美国氰胺公司开发的一种中性膦氧类萃取剂。其P=O(磷酰基)基团电子云密度大,萃取能力强,对镧系元素,锕系元素,贵金属,三价铁和六价铬等金属离子具有较好的配位能力[62-65]。在常规液液萃取中,三辛基氧化膦常作为协萃剂,与β-二酮类萃取剂组成的协萃体系可在中性条件下萃取锂[66]。但三辛基氧化膦在烃类溶剂中的溶解度相对较低, 其萃取效率受溶解度的限制。 将三辛基氧化膦与HBD 液化组成DES 可以充分发挥三辛基氧化膦萃取效率。
Gilmore 等报道了三辛基氧化膦:苯酚(1:1)的疏水 DES 用于萃取铀酰离子(UO22+)。 DES 相中三辛基氧化膦的浓度为1.875 mol/L, 远大于三辛基氧化膦在煤油中的溶解度。 在硝酸浓度为0.01~1 mol/L 时,使用三辛基氧化膦:苯酚(1∶1)的 DES 均可以使水相中的UO22+从250 mg/L 降低至0.5 mg/L 以下。通过红外光谱分析和紫外光谱分析表明, 苯酚的存在不参与UO22+的络合萃取, 在萃取过程中只起到液化三辛基氧化膦的作用[33]。
Schaeffer 等研究了三辛基氧化膦与百里香酚/癸酸组成的疏水DES 在盐酸体系分离铂族金属和常见过渡金属的能力。 2 种DES 对金属离子的选择性与内部氢键强度有关。 三辛基氧化膦:百里香酚(1∶1)内部氢键强度大于三辛基氧化膦: 癸酸(1∶1)内部氢键强度,因此表现出更好的选择性与更低的萃取能力。在盐酸浓度为2 mol/L 时,2 种DES 都对金属的萃取强弱规律均为 Pt(Ⅳ)≈Fe(Ⅲ)>Pd(Ⅱ)>>Cr(Ⅲ)≈Cu(Ⅱ)≈Co(Ⅱ)≈Ni(Ⅱ),Pd(Ⅱ)与 Cr(Ⅲ)、Cu(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)之间的分系数均大于 100[32]。
Ni 等基于三辛基氧化膦:十二醇(1∶2)设计一个流程用于选择性回收废SmCo 磁体盐酸浸出液中的Sm(Ⅲ)与 Fe(Ⅲ)。 浸出液中分别含 10.05 g/L Fe(Ⅲ)、21.93 g/L Co(Ⅱ)、2.58 g/L Cu(Ⅱ)和 9.87 g/L Sm(Ⅲ),在相比为4,通过两级逆流萃取,可以优先萃取超过99%的 Fe(Ⅲ)和 Sm(Ⅲ),仅 0.16%的 Co(Ⅱ)和2.89%的 Cu(Ⅱ)被共萃取。 负载 Fe(Ⅲ)和 Sm(Ⅲ)的DES 相用1.5 mol 草酸反萃,可分别得到高纯草酸铁溶溶液和草酸衫沉淀。 所开发的DES 对Sm (Ⅲ)与Fe(Ⅲ)的饱和负载量超过 18 g/L(图 4),且在 5 次循环使用过程中DES 的性能未发生变化[34]。

图4 三辛基氧化膦:十二醇(1∶2)饱和负载Fe(Ⅲ)和Sm(Ⅲ)后DES 的外观变化[34]Fig. 4 Trioctyl phosphine oxide: dodecanol (1∶2)saturated loading Fe(Ⅲ) and Sm(Ⅲ) on the appearance of DES[34]
三辛基氧化膦型DES 对金属阳离子的萃取机理如式(7)所示:

Hanada 等研究中性膦类萃取剂与β-二酮类萃取剂组成的协同DES 用于萃取Li(I),三辛基氧化膦与苯甲酰三氟丙酮在摩尔比为1∶2 时可在室温下组成 DES。 DES 对 Li(I)的饱和负载量达到 4.4 g/L,是常规锂萃取体系的2 倍以上。 通过调节溶液的pH 值可以从盐湖卤水中选择性萃取 Li(I),Li (I)与 Na(I)的分离系数达到2 000。 使用HCl 溶液可从DES 相中反萃90%以上的 Li(I),DES 在 5 个循环内使用对Li(I)的萃取和反萃未发生变化。与三辛基氧化膦与苯甲酰三氟丙酮在煤油中的协萃体系相比, 由于协同DES不含稀释剂,DES 相中萃取剂的浓度更高, 萃取能力也相应更高,但对 Li (I)与 Na(I)选择性会稍有降低[24]。
三辛基氧化膦型DES 的综合性能与羧酸类DES类似,同样具有低黏度,强疏水性以及较高的熔点。 对金属离子的萃取和反萃性能与三辛基氧化膦在稀释剂中的性能一致。不同三辛基氧化膦型DES 的特点是内部氢键的强度的不同。 三辛基氧化膦:百里香酚和三辛基氧化膦: 癸酸这2 种DES 内部表现出强的氢键相互作用, 当DES 组分中三辛基氧化膦的摩尔分数低于0.3 时对Pd(Ⅱ)没有萃取能力。 由于内部氢键的影响,在盐酸浓度为0.05 mol/L 和1mol/L 时三辛基氧化膦:百里香酚(1∶1)与三辛基氧化膦: 癸酸(1∶1)这 2 种 DES对Fe(Ⅲ)的萃取次序发生了变化,会优先萃取Pt(Ⅳ)和Pd(Ⅱ)。 三辛基氧化膦:十二醇和三辛基氧化膦:苯甲酰三氟丙酮这2 类DES 中的氢键相互作用比较弱,在萃取时未有明显的抑制现象。 DES 内部的氢键对金属离子具有明显反协同作用,可以继续深入研究。
4 结论与展望
疏水DES 用于金属离子的萃取分离研究已经有5 年时间,虽然还在起步阶段,但已在金属离子的萃取分离方面展现了良好工业应用前景,有很大的潜力取代传统的稀释剂和萃取剂。通过改变HBA 与HBD的组成,可以调节对特定金属离子的选择性。 与传统液萃取体系相比, 疏水DES 可同时充当稀释剂与萃取剂,不仅具有较大的负载能力,且对环境造成的影响比较小。 但笔者认为疏水DES 用于实际运用还有一些关键问题需深入研究:
1) 疏水DES 自身的理化性质已有很多的数据,但疏水DES 负载金属以后的理化性质和相变化性质报道的很少。 由于疏水DES 在萃取过程中同时充当稀释剂和萃取剂, 在与金属离子结合以后DES 相的成分发生了很大的变化,其负载金属以后的理化性质可能会变化很大。 应当加强对疏水DES 萃取金属后理化性质的表征。
2) 疏水DES 的机理应该需要更深入的研究。 大多数研究侧重于分析DES 中发挥萃取作用的成分与金属离子的作用机制,但对另一组分对过程萃取的影响分析的很少。研究非萃取组分对萃取过程的影响可能有助于更好的设计疏水DES。
3) 疏水DES 理化性质还有待改进。 季胺盐型DES 大多都水溶性大, 黏度大, 虽然具有极佳的选择性,但萃取多数金属离子都难以反萃。叔胺盐型的DES在萃取过程中的流失会使DES 结构受到破坏,难以循环使用。 基于羧酸或者三辛基氧化膦为主要萃取组分的疏水DES 选择性好,可循环使用,但DES 的熔点仍偏高。 对DES 结构的设计应该进一步加强。
4) 羧酸型DES 目前测试还是一些比较容易分离的金属,未充分展示的DES 的选择性与可设计性。 对工业上某些性质相近金属分离研究应当继续加强。

