超疏水性铜镍涂层的结构和耐蚀性
贺春林,杨锡芃,于济豪,朱明臻,杨 杰,池坪礁,马国峰,宋贵宏
(1.沈阳大学 辽宁省先进材料制备技术重点实验室,辽宁 沈阳 110044;2.沈阳工业大学 材料科学与工程学院,辽宁 沈阳 110870)
铜镍合金具有优良的导热性、导电性,良好的力学和加工性能,被广泛应用于工业制造的各个领域[1].当铜镍合金在海洋及大气环境中使用时,会发生不同程度的腐蚀破坏,导致铜镍材料或零部件的使用性能下降,甚至造成安全事故及经济损失.金属涂层技术是改善金属材料耐蚀性的有效手段之一,目前,超疏水涂层由于具有良好的耐腐蚀性和独特的自清洁性,在材料保护领域受到了广泛关注,在金属材料表面覆盖超疏水性涂层已成为一种十分有效的金属保护方法[2].
制备超疏水涂层需要具备2个重要条件,即超疏水涂层的粗糙表面微观结构及较低的表面自由能.通常,制备超疏水表面所使用的技术分为2类:①在具有一定疏水性材料表面制备微纳米粗糙结构;②在粗糙的微纳米结构表面,使用低表面能物质进行修饰[3].近年来出现了多种超疏水表面的制备方法,如刻蚀法、化学沉积法、一步浸泡法、电化学沉积法、溶胶-凝胶法以及阳极氧化法等[4-9].Wang等[10]用磷酸刻蚀黄铜,使黄铜表面逐渐粗化,再通过十八烷酸对刻蚀后的黄铜表面进行修饰,最终获得了超疏水性黄铜表面.Liu等[11]在肉豆蔻酸中浸泡铜10 d后,铜的表面出现了花瓣状形貌的薄片,所制样品接触角为155°,呈超疏水特性.Xi等[12]将钛、铁、镍、铝、锌和铜分别作为阴极,将铜作为阳极,以十四烷酸为电解液,由于铜易与十四烷酸分子发生反应,成功获得了具有微纳米结构的微簇表面,所得样品不仅对蒸馏水表现出超疏水性,还对碳酸钠、氯化钠溶液以及强酸、强碱溶液等腐蚀性更强的液体均表现出超疏水性.Hou等[13]在干燥箱中放入锌,获得了纳米氧化锌薄膜,再通过低表面能物质十八烷基硫醇修饰,使样品获得了超疏水性.
电沉积法是制备金属超疏水涂层的主要方法之一,具有反应条件温和、工艺简单、所需设备便宜以及环境污染小等优点[14].铜镍合金是一种重要的耐海水腐蚀合金,但目前,尚鲜见电沉积法制备超疏水性铜镍合金涂层的研究报道.本文通过直流电镀工艺先在304钢板上制备一层铜镍合金涂层,再通过硬脂酸对涂层进行修饰,获得了具有疏水性和超疏水性的铜镍涂层,并比较了2类涂层的表面结构和耐蚀性.采用扫描电镜和电化学技术对涂层进行表征,结果表明,适当地延长疏水化处理时间,可使铜镍涂层呈现出超疏水性,以及更好的耐3.5%(质量分数)NaCl水溶液腐蚀性能,表现出良好的应用前景.
1 实验材料与方法
1.1 阴极和阳极材料
阴极基体为线切割的20 mm×20 mm×1 mm的304钢板,阳极基体为线切割的20 mm×30 mm×3 mm的B30铜合金,购于沈阳有色金属加工有限公司.
1.2 电镀液
铜镍涂层的电镀液由25 g·L-1五水合硫酸铜(CuSO4·5H2O)、70 g·L-1二水合柠檬酸三钠(C6H5O7Na3·2H2O)、70 g·L-1六水合硫酸镍(NiSO4·6H2O)和0.3 g·L-1十二烷基硫酸钠(C12H25SO4Na)组成.用磁力搅拌器将电镀液充分搅拌直至完全溶解后,再用2 mol·L-1的NaOH水溶液将电镀液的pH值调至6.所有化学试剂均为分析纯,购于国药集团化学试剂有限公司.
1.3 涂层制备
首先,对线切割成尺寸为20 mm×20 mm×1 mm的304钢板薄片依次用400#、800#、1200#和1500#砂纸进行打磨,再用金相抛光机将基体表面抛光成镜面,最后用无水乙醇和丙酮对基体薄片进行仔细清洗,经冷风吹干后备用.电镀前,将基体放入5 mol·L-1的硫酸中进行30 s的刻蚀处理,以便去除基体表面的氧化物,同时使基体表面形成微小的沟壑,以增加镀层与基体表面之间的膜基结合力[15].电镀实验在装有电镀液的1 000 mL烧杯中进行,阴极和阳极基体平行放置于烧杯两侧,采用直流电源,电镀的电流密度为12.5 mA·cm-2,电镀液温度为45 ℃,机械搅拌1 h.Cu-Ni电镀层制备完成后,将镀件放入由硬脂酸和无水乙醇配置的硬脂酸乙醇溶液中进行不同时间疏水化处理后取出,用冷风吹干后放入干燥箱中备用.
1.4 表面形貌分析
采用日立S-4800场发射扫描电子显微镜及附带的能谱仪(FESEM/EDS)表征样品的微观形貌,FESEM的加速电压为2~5 kV.
1.5 接触角测试
先用微注射器将体积为10 μL的蒸馏水滴在样品表面,再用接触角测试仪测试样品表面的接触角.每个样品选取3处不同的区域进行测试,测试结果取3次实验的平均值.
1.6 电化学腐蚀实验
采用电化学阻抗谱(EIS)和极化曲线技术测试涂层在质量分数为3.5%的NaCl溶液中的耐蚀性.实验设备为上海辰华仪器有限公司生产的CHI 604E电化学分析仪,采用三电极体系,所制备样品为工作电极(非测试部分用可剥性阻镀胶封闭),饱和甘汞电极为参比电极,石墨为辅助电极.EIS测试是在开路电位(Eocp)下进行,实验所用的正弦波振幅为5 mV,扫描频率为105~10-2Hz.极化曲线测试的电位扫描范围相对于Eocp为-250~250 mV,电位扫描速率为0.5 mV·s-1.实验结束后,用ZSimpWin软件对EIS进行拟合,对极化曲线进行Tafel拟合,得到相关电化学数据.
2 结果与讨论
2.1 涂层微结构
在直流电流密度为12.5 mA·cm-2,电镀液pH值为6,电镀温度为45 ℃条件下电沉积铜镍涂层,未经疏水化处理(0 h)和疏水化处理6、9、12 h条件下获得的铜镍涂层FESEM形貌如图1(a)~图1(d)所示.从图中可以看到,未经疏水化处理的铜镍涂层表面呈现团簇状,由微纳米尺度的细小颗粒聚集而成的较大颗粒组成[16],颗粒间可见少量微孔和缝隙(图1(a)),这种具有微观粗糙结构的表面,是制备超疏水性表面的重要前提.经疏水化处理后,铜镍涂层表面伴有半透明的花瓣状形貌薄片.随着疏水化处理时间的延长,涂层表面花瓣状形貌薄片的数量有所增加,薄片也变得更加挺立(图1(b)~图1(d)).0和12 h疏水化处理时间下所制样品的EDS能谱分析结果如图1(e)和图1(f)所示.由图1(e)可知,未经疏水化处理的电镀层含C、O、Cu和Ni,相应元素的原子百分比分别为37.46%、22.04%、5.19%和34.36%.由图1(f)确定疏水化处理12 h涂层所含元素C、O、Cu和Ni的原子百分比分别为75.63%、3.39%、0.36%和20.63%,这说明该超疏水铜镍涂层表面形成的花瓣状薄片与低表面能物质硬脂酸铜所含元素一致[17].疏水化处理导致铜镍涂层表面C原子百分比增加,是由于铜镍涂层表面出现了更多的具有花瓣状形貌的硬脂酸铜薄片,硬脂酸铜中的有机官能团增加了涂层表面的碳原子百分比[17].

图1 不同疏水化处理时间下涂层的FESEM/EDSFig.1 FESEM/EDS images of the coatings with different hydrophobic treatment times
图2为水滴在未经疏水化处理(0 h)及疏水化处理6、9和12 h的涂层上的表面形态,测得的接触角分别为84.15°、120.82°、138.14°和152.15°.可见,涂层与水滴的接触角随疏水处理时间的延长而增大.当时间达到12 h时,所得涂层的接触角大于150°,表现出超疏水性[11].这是因为,增加疏水处理时间,可使涂层表面的低表面能花瓣状形貌薄片数量逐渐增多,密度逐渐增加,进而增大了涂层表面的粗糙度(见图1(b)~图1(d));而涂层上面的低表面能花瓣状形貌薄片,提升了液滴下截留空气的能力,使得样品与水滴的接触角增大,涂层表面的疏水性提高.

图2 水滴在不同疏水化处理时间涂层上的表面形态Fig.2 Surface morphology of the coatings prepared with different hydrophobic treatment times
2.2 涂层电化学腐蚀行为
图3为不同疏水化处理时间所制备样品在质量分数为3.5% 的NaCl溶液中的动电位极化曲线,表1为经Tafel拟合所获得的腐蚀电流密度(Icorr)和腐蚀电位(Ecorr)数值.其中,铜镍涂层样品制备条件为:电镀电流密度12.5 mA·cm-2,电镀液pH值为6,电镀温度45 ℃,疏水化处理时间为0、6、9和12 h.
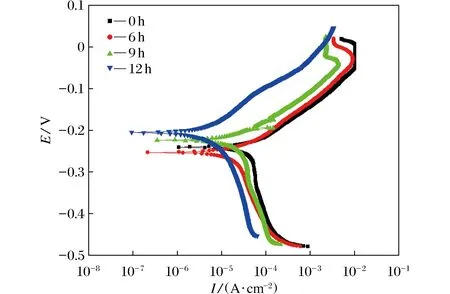
图3 不同疏水化处理时间下涂层的动电位极化曲线Fig.3 Potentiodynamic polarization curves of the coatings with different hydrophobic treatment times

表1 不同疏水化处理时间下涂层的极化曲线Tafel拟合结果Table 1 Tafel fitting results of polarization curves of the coatings with different hydrophobic treatment times
由表1可见,疏水化处理时间由0 h增至12 h,样品的腐蚀电流密度由25.10 μA·cm-2降到3.41 μA·cm-2,腐蚀电位从-241 mV升高到-204 mV.通常,腐蚀电流密度越小,涂层的腐蚀速度就越慢,意味着涂层的耐腐蚀性能也就越好;腐蚀电位越高,涂层的惰性就越大,意味着涂层越不易与腐蚀介质发生腐蚀反应[15].与6 h疏水化处理的样品相比,疏水化处理12 h的铜镍涂层表面形成了更多的低表面能的花瓣状薄片,使涂层表面由疏水性转变为超疏水性,从而明显增强了涂层表面对NaCl溶液的阻隔作用,大幅减少了NaCl溶液(Na+和Cl-)与铜镍涂层的接触面积,使涂层腐蚀电流密度降低,耐蚀性大幅改善.
除极化曲线外,电化学阻抗图谱也是研究涂层/金属体系腐蚀行为的有效方法[15].图4(a)~图4(c)为不同疏水化处理时间下铜镍涂层在质量分数为3.5%的NaCl溶液中浸泡5 h后的电化学阻抗图(EIS).由图4(a)可知,不同疏水化处理时间下样品的EIS曲线明显不同.0 h、6 h的EIS在高频和低频区表现为2个容抗弧,容抗弧曲率半径较小,表明阻抗较小.9 h、12 h的EIS形状相似,在高频区为一曲率半径较大的容抗弧,中低频区为近半圆容抗弧,低频区尾部出现了实部收缩.容抗弧半径与电荷转移电阻的大小成正相关,容抗弧的半径越大,该涂层的电荷转移电阻越大,涂层的耐蚀性越好.由图可知,随疏水化处理时间延长,EIS容抗弧半径明显增大,所以,疏水化处理12 h的涂层对基体有更好的保护作用.

图4 不同疏水化处理时间下涂层的电化学阻抗谱及等效电路Fig.4 Electrochemical impedance spectra and their equivalent circuit of the coatings with different hydrophobic treatment times
图4(b)给出了经不同时间疏水化处理的铜镍涂层的阻抗模值|Z|与频率f之间的关系,可见,随疏水化处理时间延长,涂层的|Z|值明显增大.与疏水化处理0 h涂层相比,疏水化处理12 h涂层的|Z|值大约增加1~2个数量级,这说明,增加疏水化处理时间,有利于改善超疏水性铜镍涂层的耐腐蚀性.由图4(c)可见,不同疏水化处理时间下涂层均呈现2个容抗弧,且增加疏水化处理时间,相位角最大值增大,表明涂层的保护作用增强.
为进一步解析图4的EIS谱图,采用图4(d)的等效电路模型对EIS进行了拟合,获得的相关电化学参数如表2所示,其中Rs为溶液电阻,数值在3.679~7.328 Ω·cm2之间.由表2可见,对应涂层和基体表面双电层的常相位角元件Q的指数参量n1和n2(0 表2 不同疏水化处理时间下涂层的电化学阻抗谱拟合结果Table 2 Fitting results of EIS of the coatings with different hydrophobic treatment times 具有花瓣状形貌薄片的硬脂酸铜超疏水层是一种隔绝层,通过阻止和延缓腐蚀介质由涂层孔隙向涂层/基体界面的扩散,达到保护基体金属免受腐蚀的目的.图5为超疏水铜镍涂层在质量分数为3.5%的NaCl溶液中浸泡不同时间的电化学阻抗谱.从图5(a)中可以看到,浸泡9 h、15 h和21 h的涂层均呈现出2个容抗弧,低频区的容抗弧半径随浸泡时间的增加不断增大,表明耐蚀性逐渐增强. 图5 不同浸泡时间下超疏水涂层电化学阻抗谱Fig.5 EIS of superhydrophobic coatings under different immersion times 分析超疏水性涂层的奈奎斯特图(图4(a)和图5(a))可知,浸泡5 h、9 h的EIS在低频区尾部发生了实部收缩的现象,这是由于超疏水层的结构本身具有孔隙,腐蚀介质通过孔隙渗透到超疏水性铜镍涂层底部与基体间的界面,于是腐蚀介质和涂层在界面处发生电化学反应,导致样品在低频区的极化电阻减小.相对于图4(a)中浸泡5 h的EIS,浸泡9 h的EIS极化电阻仍有较明显的增大.当浸泡时间延长到15 h后,样品EIS低频区尾部的实部收缩现象趋于消失.在阻抗模值|Z|和频率f的波特图(图5(b))中,随浸泡时间增加,EIS曲线(0.2~400 Hz之间)逐渐朝低频方向移动,在最低频0.01 Hz处的阻抗模值|Z|逐渐增大.图5的EIS对应的等效电路如图4(d)所示,表3为不同浸泡时间下超疏水涂层的电化学阻抗谱拟合结果.从表3可见,随着浸泡时间的延长,铜镍涂层的双电层电容Q1逐渐减小,指数参量n1逐渐增大,而基体电荷转移电阻Rct则逐渐增大,指数参量n2缓慢减小.浸泡21 h后的铜镍涂层的常相位角元件表现为纯电容(n1=1),Rct达最大值25 850 Ω·cm2.所以,随着浸泡时间的增加,超疏水性涂层的耐蚀性不断增大,是由于腐蚀介质与涂层发生反应,腐蚀产物不仅减缓了涂层表面的腐蚀反应,同时涂层/基体界面处的腐蚀产物还会堵塞涂层中的孔隙,进而阻碍腐蚀介质向界面扩散,减缓界面处的腐蚀进程,增强对基体的保护作用. 表3 不同浸泡时间下超疏水涂层的电化学阻抗谱拟合结果Table 3 Fitting results of EIS of superhydrophobic coatings under different immersion times 1)通过直流电镀后再疏水化处理的方法,在304不锈钢基体上制备了超疏水性铜镍涂层,发现涂层的表面形貌和润湿性与疏水化处理时间密切相关.当疏水化处理时间从6 h延长到12 h时,涂层表面硬脂酸铜薄片数量增加,与水滴间的接触角由120.82°增加到152.15°,呈现出由疏水性向超疏水性转变. 2)极化曲线和电化学阻抗谱实验结果表明,增加疏水化处理时间,可改善涂层在质量分数为3.5%的NaCl溶液中的耐蚀性.疏水处理12 h的涂层具有最佳的耐蚀性,这与该涂层超疏水性表面结构和特性有关. 3)在质量分数为3.5% 的NaCl溶液中浸泡5~21 h的超疏水涂层,随着浸泡时间延长,EIS低频区尾部实部收缩逐渐消失,极化电阻增大,涂层耐蚀性逐渐改善.
2.3 超疏水涂层EIS随时间的变化


3 结 论

