电场作用下P掺杂硅烯选择性吸附CH4的第一性原理计算
霍英菲, 黄珍霞, 王军凯, 王雪晴, 胡前库, 周爱国
(1.河南理工大学 材料科学与工程学院, 焦作 454003; 2. 河南理工大学 化学化工学院, 焦作 454003)
1 引 言
在如今煤矿生产过程中,甲烷(CH4)堆积造成的煤矿爆炸仍在全球范围内造成重大人员伤亡[1]. 开发低成本,高选择性的甲烷传感器以实时,连续地监测煤矿中的甲烷浓度至关重要. 目前已经开发出基于各种传感机制的甲烷传感器,例如金属氧化物型,催化燃烧型,非分散红外(NDIR)吸收光谱型[2-5]等. 金属氧化物方法基于在高温下与甲烷反应引起的金属氧化物(即氧化锡)的电导率变化[6]. 由于甲烷非常稳定,因此操作温度通常高于400 ℃,以实现正常的灵敏性[7,8]. 催化燃烧型甲烷传感器通过使用加热的催化元素(通常为钯)燃烧甲烷来运行[4]. 对甲烷的选择性是通过利用两种贵金属(如钯和铂)的不同催化活性来实现的[9]. 也可以通过测量近红外(IR)或中红外波段中甲烷的吸收光谱来检测甲烷. 中红外方法比近红外方法更灵敏,但需要大而昂贵的红外传感器冷却设备[2,10]. 甲烷的红外吸收也可以使用光声法检测. 在这种方法中,甲烷分子吸收特定波长的IR并将其转换为声音信号,然后通过麦克风或其他类型的振动传感器对其进行检测[11,12]. 即使光声甲烷传感器非常灵敏,但整个系统是复杂且昂贵的. 而基于气体分子吸附和脱附所引起的具体物理量相对变化的薄膜型气敏传感技术,使得快速响应和低成本的甲烷检测传感器得以发展,使传感器的性能得到较大的提升. 此类型气敏型传感器的性能高度依赖于传感材料的类型、比表面积和微观结构,因此,开发具有高比表面积以及良好传感能力的新型材料是非常必要的.
硅烯,是一种类似于石墨烯的单原子二维层状材料[13],早在1994年就被Takeda等[14]在理论上预测出来,并于2010年在实验中被合成出来,此后便引起了越来越多学者们的关注. 特别是由于硅烯具有的弯曲六角形蜂巢结构,使其可以通过简单的方法来调节电子性质,例如通过施加电场[15],或通过有机功能化[16]. 更高的表面反应性能和带隙调节功能让硅烯作为气体传感装置[17,18]的候选材料成为可能.
到目前为止,已经有部分学者研究了硅烯对一些气体的吸附. Hu等[19]发现硅烯对NH3、NO和NO2都有较强的吸附能力. 电荷从硅烯转移到分子中,导致硅烯的p型掺杂,使得硅烯的狄拉克点处有可调的带隙开口. Gurel等[20]通过研究发现通过克服一个相对较小的能量障碍,H2、O2可以在硅烯空位处解离,H2O分子对硅烯是惰性的,而OH分子则吸附在空位上,具有显著的结合能. 然而硅烯对甲烷气体的敏感性能尚无人研究.
此外,目前对石墨烯气敏性能的研究结果表明,纯石墨烯对多数气体的吸附较弱,无法作为气体敏感探测材料. 然而采用过渡金属/非金属掺杂后的石墨烯通常具有优越的气体敏感性能. 例如,掺杂Al的石墨烯作为一种新型传感器用于检测HF气体[21],掺杂镓的石墨烯能够有效吸附有毒气体NO2[22],硼和硫掺杂的石墨烯可以作为NO、NO2等污染气体的良好传感器[23]等等. 那么掺杂硅烯是否具有更加优越的气敏性能呢?经联机检索,目前对掺杂硅烯作为气敏材料的研究仍然较少. 相关研究还表明,外加电场通常可以提升二维材料的吸附性能[24,25],进而实现对有害气体的探测和捕捉. 并且与其他方法相比,外加电场在实际应用中具有许多优势,例如清洁、易于实现方向和强度的调节等等. 其中,Zhang等[26]的研究中介绍到在钛修饰的石墨烯表面施加电场可大大增强与氢分子的相互作用. Zhang等[27]指出通过对Li修饰的Stone-Wales缺陷石墨烯进行外部电场调控,可简单地实现H2分子的吸附或脱附. Guo等[28]发现二氧化碳能够通过外部电场的控制在h-BN上被高效地捕获和释放.
基于此,本文采用第一性原理计算首先研究了纯硅烯及掺杂硅烯对甲烷气体的吸附性能. 在此基础上,研究了加电场对纯/掺杂硅烯对甲烷气体的选择性吸附和捕获性能的影响.
2 计算方法
文中所有计算均采用Materials-Studio8.0软件中基于密度泛函理论的DMol3软件包[29,30],电子和电子相互作用的交换关联能函数采用的是广义梯度近似(GGA)的PBE交换关联泛函[31],轨道占据参数采用0.005 Ha. 布里渊区的特殊点积分使用Monkhorst-Pack方法[32]. 自洽场(SCF)计算收敛标准为电子密度变化小于1×10-6Ha,能量的收敛标准为1×10-5Ha,Hellmann-Feynman原子收敛判据为每个原子受力不大于2×10-3Ha/Å,最大位移为 5×10-3nm.
我们的计算模型如图1(a)和(b)所示,为含50个Si原子的5×5×1硅烯超晶胞,其真空层厚度为30 Å.
为了定量描述气体分子在纯硅烯表面以及P掺杂硅烯表面的吸附强度,我们用吸附能Ead来定义:
Ead=Egas+silicene-(Esilicene+Egas)
(1)
Ead=Egas+P-doped silicene-(EP-doped silicene+Egas)
(2)
其中,Esilicene、EP-doped silicene、Egas、Egas+silicene以及Egas+P-doped silicene分别代表纯硅烯、P掺杂硅烯、单个小气体分子、整个纯硅烯吸附体系以及P掺杂硅烯吸附体系的能量. 根据公式(1)、(2)中Ead的定义,Ead数值越负,吸附作用越强. 采用Mulliken方法[33]来分析衬底与吸附物之间的电荷转移.
图1 硅烯晶胞的结构模型图Fig. 1 Structural model diagrams of silicene cell
3 结果与讨论
3.1 无外加电场条件下,甲烷在纯硅烯表面的吸附
首先研究了纯硅烯对甲烷气体分子的吸附行为,考虑了甲烷分子的不同吸附位点和取向. 图2为甲烷分子的3种可能取向模型,一个氢原子垂直硅烯表面朝下(a),两个氢原子所在平面平行于硅烯表面(b),一个氢原子垂直硅烯表面朝上(c). 可能的吸附位点分别是硅原子上方的顶位点(T),Si-Si键中心位置上方的桥位点(B),六边形中心位置上方的空穴位点(H). 图3为9种结构优化后的吸附构型示意图,对应的吸附能计算结果如表1所示. 可以看出,吸附能变化范围为-0.011 eV到-0.079 eV. 该结果表明,在纯硅烯表面,无论甲烷是何种取向,吸附在何种位置,吸附都比较弱,即纯硅烯不适合作为甲烷的吸附材料.
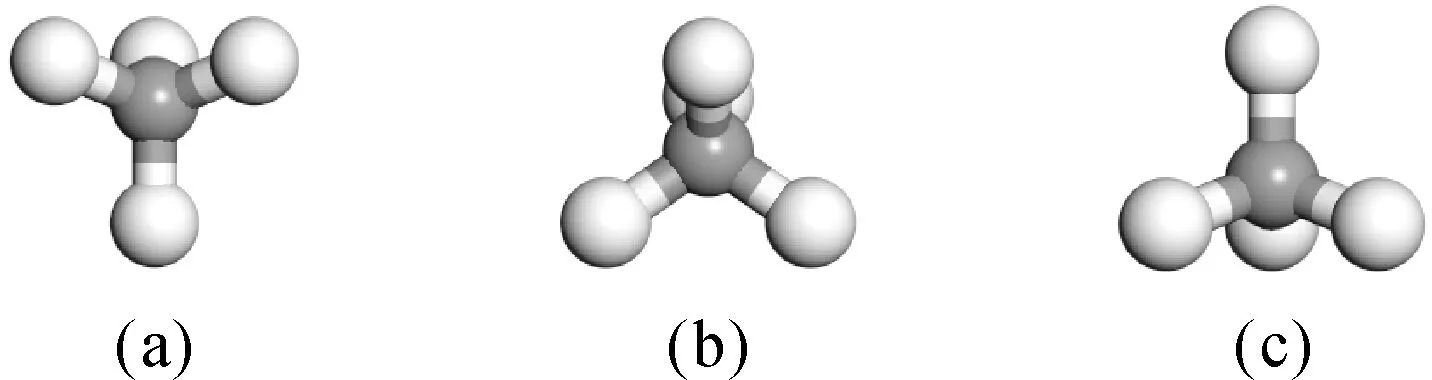
图2 甲烷分子的初始吸附构型在硅烯上的不同取向: (a) 一个氢原子垂直硅烯表面朝下,(b) 两个氢原子所在平面平行于硅烯表面,(c) 一个氢原子垂直硅烯表面朝上Fig. 2 The initial adsorption configurations of methane molecules on the silicene have different orientations: (a) one hydrogen atom is perpendicular to the silicene face downwards, (b) two hydrogen atoms are parallel to the silicene face, (c) one hydrogen atom is perpendicular to the surface of the silicene

图3 优化后不同取向的甲烷吸附在硅烯表面不同位点的结构,其中T、B、H分别代表三个吸附位点:(T)硅原子上方的顶位点、(B)Si-Si键中心位置上方的桥位点、(H)六边形中心位置上方的空穴位点Fig. 3 The optimized structure of methane with different orientations adsorbed on the surface of silicene. T, B and H represent three adsorption sites: (T) the top site above the silicene atom, (B) the bridge site above the Si-Si bond center, (H) the hole site above the hexagon center

表1 在没有外加电场的情况下,优化后不同取向的甲烷在纯硅烯表面的吸附能
3.2 外加电场对甲烷/氧气在纯硅烯表面吸附的影响
为了增强纯硅烯对甲烷分子的吸附能力,在纯硅烯对甲烷的吸附体系上加入了范围为0.000 au到0.010 au的垂直电场(沿z轴方向),吸附能的变化如图4所示. 结果表明,随着电场强度从0.000 au增大到0.010 au,纯硅烯对甲烷的吸附能越来越大,当电场强度为0.010 au时,其吸附能达到-1.878 eV. 因此在外加电场的作用下,纯硅烯能够有效地吸附甲烷.

图4 电场强度为0.000 ~ 0.010 au时,硅烯对甲烷的吸附能Fig. 4 Adsorption energies of CH4 on silicene with the electric fields from 0.000 to 0.010 au
同时计算了同样条件下纯硅烯对氧气的吸附能,如图5所示. 结果表明,纯硅烯对氧气的吸附能同样也在随着电场强度的增大而增大,最大吸附能达到-6.910 eV. 综合以上结果可以看出,施加外加电场确实提高了甲烷在硅烯表面的吸附,但是同时也提高了氧气在硅烯表面的吸附,表明外加电场下纯硅烯不具有选择吸附性. 因此即使在外加电场的作用下,纯硅烯仍然不能作为甲烷气体的吸附材料.
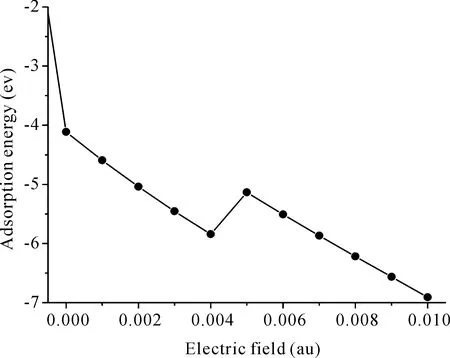
图5 电场强度为0.000 ~ 0.010 au时,硅烯对氧气的吸附能Fig. 5 Adsorption energies of O2 on silicene with the electric fields from 0.000 to 0.010 au
3.3 甲烷在磷掺杂硅烯表面吸附
计算了无外加电场情况下,磷掺杂硅烯对甲烷的吸附能,结果如表2所示. 磷掺杂硅烯对三种不同构型的甲烷分子的吸附能分别为-0.071 eV,-0.069 eV,-0.084 eV. 这表明在无外加电场条件下,磷掺杂硅烯对甲烷的吸附能很小,依旧不能用于有效捕获甲烷.

表2 甲烷在磷掺杂硅烯表面的吸附能
3.4 外加电场对甲烷在磷掺杂硅烯表面的影响
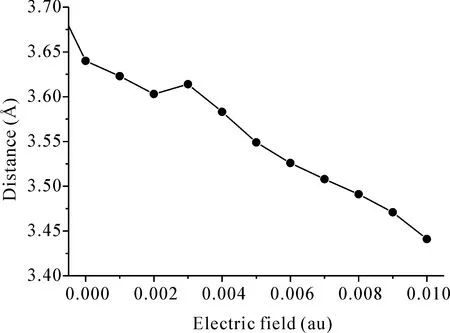
研究了外加电场条件下磷掺杂硅烯对CH4的吸附能力,电场强度为0.000 au到0.010 au的垂直电场(沿z轴方向). 随着电场强度的变化,CH4与P掺杂硅烯之间的结合距离、电荷转移以及吸附能的变化曲线,如图6所示. 1)从图6(a)中可以看出随着电场强度的增加,CH4与P掺杂硅烯之间的结合距离有所减小,更具体地说,当外加电场为0.010 au时,CH4与P掺杂硅烯之间的距离为2.866 Å,比电场强度为0.000 au的时候缩短了0.322 Å,表明磷掺杂硅烯对CH4有吸附作用,且随着电场强度的增加,吸附作用越强. 2) CH4分子的电荷转移幅度从图6(b)可见,随着电场强度的从0.000 au增加0.010 au,CH4分子所带电荷从-0.051 e增加到-0.092 e(‘-’表示获得电子),进一步表明该过程中吸附作用增强. 3) 计算得出的吸附能如图6(c)所示,当电场强度从0.000 au变为0.010 au时,P掺杂硅烯对CH4的吸附能从-0.087 eV增加到-1.842 eV,吸附能增加了1.229 eV,吸附能数值越负,说明吸附作用越强.

(a) 磷掺杂硅烯与甲烷的距离
这些结果都清楚地表明,当电场强度增加到0.010 au时,CH4与P掺杂硅烯之间的相互作用会逐渐增大. 当施加0.010 au的电场时,CH4分子进一步接近P掺杂硅烯表面. 此时,从P掺杂硅烯到CH4分子的电荷转移约为0.021 e. 据先前的研究可知,当吸附能小于-0.50 eV时,气体小分子可以被固体表面有效捕获. 这意味着P掺杂硅烯在外加正电场下可以有效捕获CH4.
3.5 电场作用下其他气体分子在磷掺杂硅烯表面的吸附
煤层气中主要包括甲烷、氮气以及氧气等气体,其中甲烷占30-50%,氧气大约占10%,剩余气体主要为氮气. 因此要提高P掺杂硅烯的选择性,首先必须排除N2和O2的干扰. 首先研究了外加电场条件下P掺杂硅烯对O2的吸附性能. 图7的结果表明,随着外加电场强度从0.000 au增加到0.010 au,P掺杂硅烯与O2之间的结合距离(图7a)从3.234 Å减小到2.643 Å,O2的电荷从-0.1690 e变化为0.4949 e(图7b),对应的吸附能从0.564 eV逐渐变为-0.180 eV(图7c),改变幅度为0.744 eV. 在同样外加电场条件下,CH4的吸附能增加幅度为1.756 eV,两者之间有较大差距. 说明P掺杂硅烯对氧气吸附较弱,不会对甲烷吸附造成干扰. 之后研究了同样条件下,N2在P掺杂硅烯上的吸附性能,结果如图8所示. 从中可以发现,P掺杂硅烯对N2的吸附性能与O2类似,都是随着外加电场强度的增大,其结合距离和电荷逐渐降低,对应的吸附能逐渐增大,但整个过程中吸附能从-0.065 eV到-0.125 eV,仅增加了0.06 eV,变化非常微弱,相比于CH4的吸附能增加值(1.756 eV)有较大差距. 因此,在外加正电场条件下,P掺杂硅烯对N2同样不敏感.

(a) 磷掺杂硅烯与氧气的距离
(a) 磷掺杂硅烯与氮气的距离
由于空气湿度因素对气敏材料的稳定性有较大的影响,因此P掺杂硅烯还要排除H2O的干扰. 研究了在同样条件下P掺杂硅烯对H2O的吸附性能,结果如图9,随着外加电场强度从0.000 au增加到0.010 au,P掺杂硅烯与H2O的结合距离变化曲线如图9(a)所示,随着电场强度的增加,结合距离增加. 具体而言,结合距离从3.302 Å增加到3.326 Å,此气体分子在P掺杂硅烯吸附现象与前面介绍的CH4、O2和N2气体分子在P掺杂硅烯吸附现象相反. 此外,随着电场强度的增加,H2O分子的电荷变化幅度不明显,吸附能从-0.062 eV降低到0.018 eV(图9c),说明P掺杂硅烯对H2O是排斥作用. 综上所述,在外加电场作用下P掺杂硅烯可选择性地从氮气、氧气以及水蒸气中选择性捕获CH4分子,有望成为 CH4气体的捕获材料.
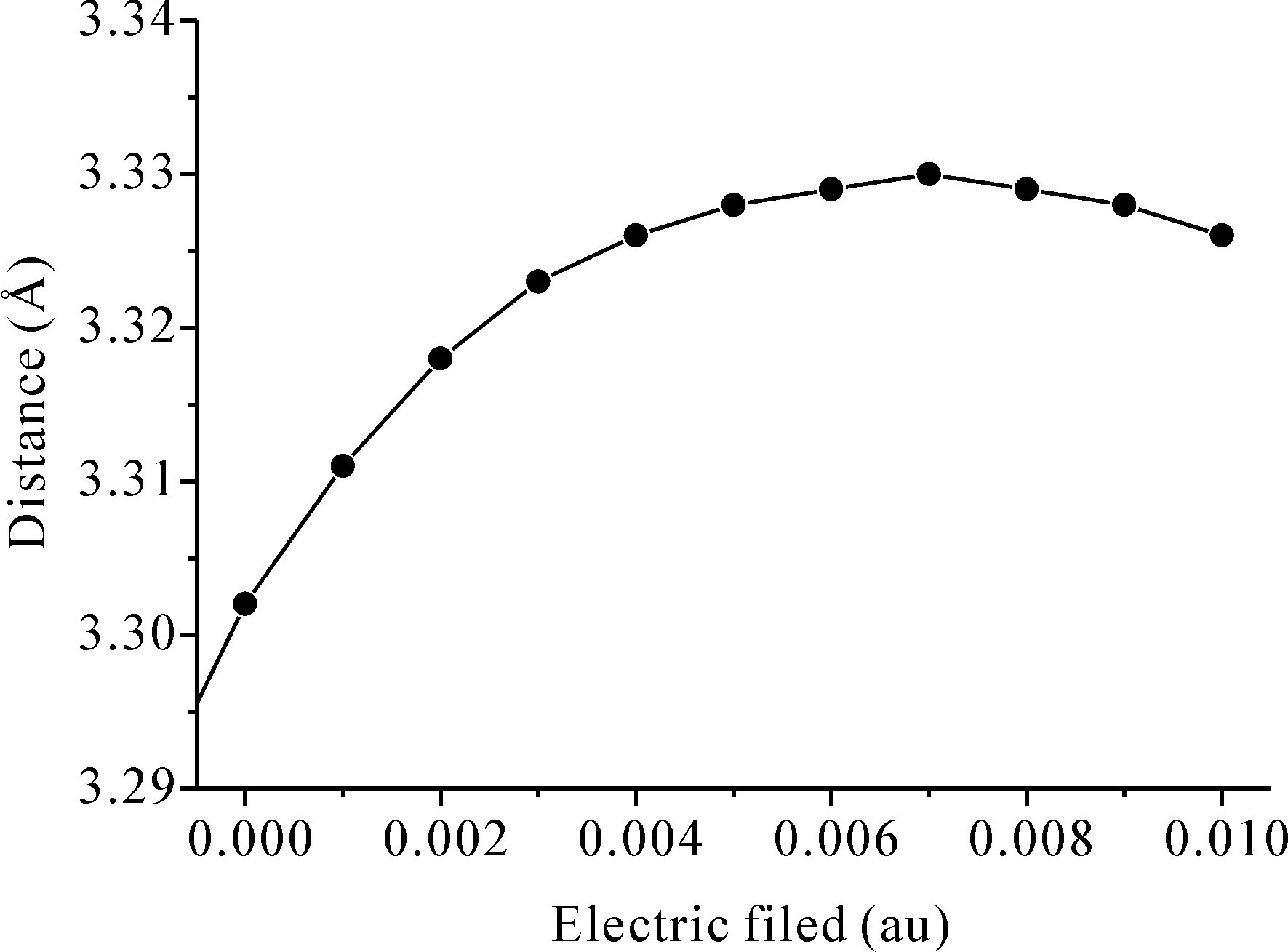
(a) 磷掺杂硅烯与水分子的距离
4 结 论
采用第一原理计算研究了P掺杂硅烯对CH4的吸附性能. 得到的主要结论如下:
(1)无外加电场时,P掺杂硅烯对CH4仅有微弱的吸附作用. 当施加外加电场时,甲烷与P掺杂硅烯之间吸附距离随电场强度的增加而逐渐减小,并伴随大量电荷转移,吸附从物理吸附转化为化学吸附. 当外电场被移除时,P掺杂硅烯与甲烷分子之间则为微弱的物理吸附,甲烷分子很容易实现脱附.
(2) 通过控制电场强度,P掺杂硅烯能够从O2、N2、H2O的混合气体中选择性捕获CH4分子. 因此,P掺杂硅烯可作为一种高选择性的CH4吸附、捕获材料,其选择性程度可通过外加电场强度进行控制.

