二氯N-哌啶二苯并环庚烯类杀鼠剂的合成及生效研究
陈锋,张鑫野,赵国书
(东北大学,辽宁 沈阳 110004)
鼠类威胁着世界范围内的粮食生产[1-3],它们是许多传染病的媒介[4-5]。目前第二代抗凝血杀鼠剂,例如溴敌隆、氯丙二醇二酮、氯地那非和氟可马 芬[6-7],由于强毒性,被广泛使用。但这些产品对老鼠的毒性增强的同时还对非靶向生物的存在潜在毒性[8-9]。近年来,第二代抗凝血杀鼠剂的广泛使用已导致在许多人类饲养的动物[11]和野生动物体内出现抗凝血灭鼠剂[10-13],同时老鼠抗药性也在增强[13-14]。N-哌啶-10,11-二氢-5H-二苯并[a,d]环庚烯是一种对大鼠具有高选择性的灭鼠剂,但由于相对较低的毒性而使其使用受到限制[15]。最近,笔者制备了该杀鼠剂的单氯衍生物(在苯并环庚烯部分的苯环上取代)[16]。氯的添加显著增加了灭鼠剂对褐家鼠的毒性,同时对小白鼠保持低毒性。但是,该化合物尚无适合的工业生产的合成途径。本文使用简单方法合成了二氯代N-环庚烯灭鼠剂,并测试了其效果。
1 材料与方法
1.1 试剂和仪器
DF-101S 集热式恒温加热磁力搅拌器,郑州长城科工贸有限公司;BS200S-WEI 型电子天平,上海海康电子仪器厂;WS70-1 型红外线快速干燥器,上海锦屏仪器仪表有限公司通州分公司;DZ-2BC 型真空干燥箱,天津市泰斯特仪器有限公司;三用紫外分析仪,杭州齐威仪器有限公司;电动搅拌器,金坛市科析仪器有限公司;旋转蒸发仪,郑州长城科工贸有限公司;循环水式多用真空泵,郑州长城科工贸有限公司;DHT 型搅拌调温电热套,山东鄄城光明仪器有限公司;红外光谱仪,英国Perking Elmer 的Spectrum One 红外光谱仪,固体样品采用KCl 压片;核磁共振仪(1H NMR 和13C NMR),瑞士 Cluker 公司的 RX-300 核磁共振仪,使用DMSO 作为溶剂和TMS 作为内标;Q10TA 差示扫描量热仪(DSC),美国Instruments 公司。所有试剂均为商业购买分析纯试剂,并直接使用。
1.2 合成方法
1.2.1 5-氧代-10,11-二氢-5H-二苯并[a,d]环庚烯基-3,7-二磺酸(M1)的合成
在搅拌下,用将二苯并环庚酮(20.00 g,96.15 mmol)和浓硫酸(98%,48.00 g,489 mmol)缓慢加入到三口烧瓶中,并将温度升至140 ℃并保持3.0 h。然后将冷却的溶液用CaCO3中和,并在真空下将其体积减少至50 mL。加入浓盐酸150 mL,过滤得到的沉淀,得到白色固体,将其在60 ℃下真空干燥。熔点221.5 ℃;产量24.87 g,产率70.29%。IR(KCl,cm-1):3 428、3 069、2 960~2 860、1 453、1 695、1 640~1 492、1 210、1 133~1 062、1 014、885、838 cm-1。
1.2.2 1,9-二氯-5-氧代10,11-二氢-5H-二苯并[a,d]环庚烯基-3,7-二磺酸(M2)的合成
将M1(20.00 g,54.30 mmol)溶解在去离子水(50 mL)中。然后将溶液倒入250 mL 的三口烧瓶中,加入8 g 浓盐酸,加入催化量Al3+。搅拌加热至60 ℃后,缓慢滴加入40 g 次氯酸钠溶液 ( 质量分数为5% ),7 h 滴加完,滴加过程中补充4 g 浓盐酸。此时反应体系中,溶液呈黄色。反应完成后向烧瓶中加入过量浓盐酸至无气体产生。将反应体系减压蒸馏至20 mL,转移至烧杯中,缓慢滴加10 mL 浓盐酸,滴加过程中有白色沉淀析出。抽滤,保留白色固体并于60 ℃时真空烘干。熔程231.2~234.4℃,产量21.79 g,产率76.19`%。IR(KCl,cm-1):3 439、3 067、2 928~2 861、1 694、1 604、1 448、1 213、1 134、1 066、1 015、835、692、590 cm-1。
1.2.3 1,9-二氯-5-氧-10,11-二氢-5H-二苯并[a,d]环庚烯(M3)的合成
将M2(20.00 g,37.94 mmol)溶解在去离子水(50 mL)中,加入草酸溶液(30 g,98%),并通过减压过滤回收得到的沉淀,得到黄色固体,将其在125 ℃干燥20 h 以除去过量的草酸。将干燥的黄色固体溶解在硫酸(60 g 的50%溶液)中,并在120 ℃下回流30 h。用碳酸钠溶液将pH 调节至7以沉淀目标产物。IR(KCl,cm-1):3 072、2 922~2 863、1 700、1 642~1 494、1 457、922、841、699、593 cm-1。
1.2.4 1,9-二氯-5-羟基-10,11-二氢-5H-二苯并[a,d][7]环戊烯(M4)的合成
将M3(5.00 g,13.66 mmol)溶于三口烧瓶中的无水乙醇(20 mL)中,在4.0 h 内将NaBH4(固体,1.25 g,33.25 mmol)分批加入保持在50 ℃的搅拌溶液中。当烧瓶中出现大量白色固体时,反应终止,无法进行搅拌。过滤固体,并保留滤液。减压除去固体中的残余溶剂,然后将其用10%稀盐酸处理以除去未反应的NaBH4。用适当量的甲苯萃取产物,然后将其减压除去,得到目标物质。通过向残留的乙醇滤液(含未反应的M3)中再添加NaBH4来重复此过程,以确保底物的完全反应。合并的目标产物用去离子水洗涤并减压过滤,得到白色固体。熔程191.2~194.3 ℃,产量4.88 g,产率97.31%。IR(KCl,cm-1):3 321、3 068、2 989~2 822、1 598、1 495、1 455、1 481、1 357、1 041、844、789、610、575 cm-1。
1.2.5 1,9-二氯-5-氯-10,11-二氢-5H-二苯并[a,d]环庚烯(M5)的合成
将M4(4.00 g,10.78 mmol)溶解于水饱和的甲苯中,并倒入装有恒压滴液漏斗的三口烧瓶中,缓慢加入SOCl2(6.00g,50.42 mmol),并将混合物在回流下加热至80 ℃ 保温4.0 h。当白烟停止逸出时终止反应,并在减压下除去过量的SOCl2和甲苯。过滤得到白色固体。熔程 153.2~156.7 ℃,产量3.96 g,产率94.22%。IR(KCl,cm-1):3 021、2 929、2 886、1 636、1 593、1 446、1 480、743、632、586 cm-1。
1.2.6 1,9-二氯-5-(1-哌啶)-10,11-二氢-5H-二苯并[a,d]环庚烯(R1)的合成及表征
在冰浴下的三口烧瓶中,将 M5(3.96 g,10.24 mmol)溶解在甲苯中,通过恒压滴液漏斗缓慢加入溶解在甲苯(4.00 g,42.41 mmol)中的六氢吡啶(2.50 g,29.36 mmol),并使反应进行20 min。减压除去未反应的六氢吡啶。将稀盐酸滴加到烧瓶中,直到观察到分离为止。保留水相,并使用碳酸钠和氢氧化钠的混合溶液将pH 调节至8~10,以获得沉淀物。过滤沉淀,用去离子水洗涤并干燥,得到白色产物。熔点171.7~174.6 ℃,产量3.26 g,产率82.74%。
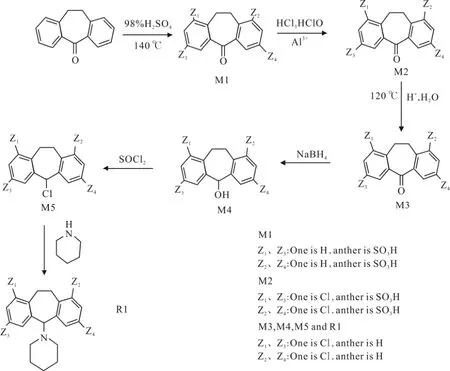
图1 R1 的合成路线
分离R1 并通过柱色谱法(硅胶柱;洗脱液为乙酸乙酯∶二氯甲烷=3∶1)纯化,得到单独的异构体P4、P5、P6,其通过NMR 进行表征。R1 中P4、P5、P6 的相对量为4∶2∶1.4。
P4:1H NMR (DMSO 0.05% v/v TMS, 300 MHz)δ7.52 (2H, d,J= 9.0 Hz), 7.22 (2H, d,J= 9.0 Hz), 7.17 (2H, q,J= 14.2 Hz), 5.19 (1H, s), 2.88-2.90 (4H t,J= 7.1 Hz), 2.45 (4H, q,J= 7.1 Hz), 1.5 (4H, m,J= 14.2 Hz), 1.38 (2H t,J= 14.2 Hz).13C NMR (DMSO, 75 MHz)δ145.7, 136.0, 130.1, 127.2, 125.0, 123.2, 65.2, 54.2, 28.1, 26.2, 24.5。
P5:1H NMR(DMSO with 0.05%v/vTMS,300 MHz)δ7.76 (1H, d,J= 9.0 Hz), 7.52 (1H, d,J= 9.0 Hz), 7.17-7.22 (3H, m), 7.39 (1H, s,J= 1.5 Hz), 5.19 (1H, s), 2.86-2.90 (4H t,J= 7.1 Hz), 2.45 (4H, q,J= 7.1 Hz), 1.5 (4H, m,J= 14.2 Hz), 1.38 (2H t,J= 14.2 Hz)。13C NMR (DMSO, 75MHz)δ145.7, 136.0, 135.4, 132.9, 130.4, 130.1, 1127.2, 125.0, 123.2, 120.8, 118.9, 65.2, 54.2, 30.7, 28.8, 26.2, 24.5。
P6:1H NMR (DMSO 0.05% v/v TMS, 300 MHz)δ7.74 (2H, d,J= 9.0 Hz), 7.36 (2H, s,J= 1.5 Hz), 7.15 (2H, d,J= 15.0 Hz), 5.19 (1H, s), 2.87-2.91 (4H, t,J= 7.1 Hz), 2.44 (4H, q,J= 7.1 Hz), 1.51 (4H, m,J= 14.2 Hz), 1.38 (2H, t,J= 14.2 Hz)。13C NMR (DMSO 75M Hz)δ145.7, 135.4, 132.9, 130.4, 1127.2, 120.8, 118.9, 65.2, 54.2, 31.4, 26.2, 25.3。
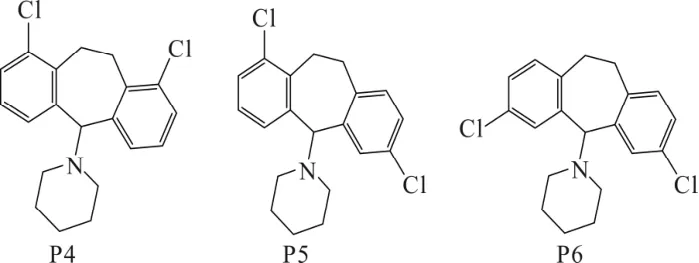
图2 异构体的结构
1.3 生物活性测定
在无选择和选择实验中,将化合物R1、P4、P5、P6 用作实验室制备的灭鼠剂诱饵(所有质量分数均为0.005%)。目标动物为从沈阳捕获的健康成年褐家鼠,并经实验室繁育(150~300 天,150~200 g)和进行实验比较的非目标动物是昆明的一个封闭小组获得的小白鼠(28~30 天,体重18~22 g)。
1.3.1 杀鼠剂的摄食系数测定
杀鼠剂的摄食系数由实验室的诱饵接受测试确定[17]。用全麦和玉米油(2.5%)和细砂糖(5%)制备试验诱饵;加入P4、P5、P6、R1 的水溶液,使每个诱饵的质量分数为0.005%;没有添加药物的小麦饵用作空白。将每种测试诱饵提供给10 只褐家鼠(5 只雄性和5 只雌性,雌性未怀孕,随机选择)。将所有大鼠关在笼子里,提供足量的水。将含有空白诱饵的盆放置在测试环境中,并在测试前正常喂养大鼠7 天。在测试的第一天,提供包含空白和活性成分的干净的食物,并定期更换它们的放置位置,使大鼠自由选择。2 天后,记录死亡数(死亡率)和食物消耗。摄食系数为毒饵消耗与空白饵料消耗之比。
1.3.2 口服LD50的测定
LD50是一种药物的急性毒性的量度。该剂量可能导致50%的受试动物死亡。实验动物如下:小白鼠雌雄比例1∶1(雌性未怀孕);褐家鼠雄雌比例1∶1(雌性未怀孕)。
将相同物种的实验动物平均分为5 组,每组包括10 只不同性别和体重的动物。通过口服管饲法1~2 s 内施用不同质量分数的杀鼠剂溶液(1.0 mL,相应地用水稀释)。LD50 和RSD 根据式(1)和 式(2)[18]计算:
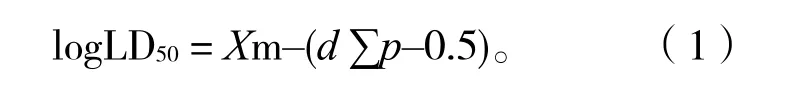
式中:Xm—最大剂量的对数;
d—两个相邻组之间剂量对数的差;
p—每组小鼠的死亡率。

式中:g—每组小鼠的存活率,用十进制表示;
n—每组小鼠的数量。
LD50为平均值±1.96×RSD(95%置信水平)。
1.3.3 现场测试
试验前采用粉迹法测鼠密度。通过现场调查,选择沈阳市区内居民区3 个编号为A、B、C 和粮食仓库3 个编号为D、E、F 为试验现场,A 和D 投放R1、B 和E 投放溴敌隆,C 和F 作为对照区。同类型场所环境条件相似,且半年内未开展过灭鼠,用粉迹法测定鼠密度超过 20% 以上,现场可发现新鲜鼠粪等鼠迹和较多鼠洞甚至活鼠。试验前后均采用《病媒生物密度监测方法鼠类》[19]中的粉迹法进行密度测定。在有鼠活动的试验现场的室内每15 m2布毒饵2 堆,室外沿墙基每间隔5 m 布放一堆,每堆50 g,次日检查,发现有鼠盗食毒饵的,按照吃多少补多少,吃完加倍投放的原则饱和投放,并检查周围是否出现老鼠尸体,统计出现老鼠尸体的数量,连续投放5 d。对照区按同样方法投放无毒基饵。投药灭鼠后的第21 天进行灭后鼠密度调查,计算灭鼠率及校正灭鼠率计算方法按《农药登记用杀鼠剂防治家栖鼠类药效试验方法及评价》[20]中的公式计算。
2 结果与讨论
2.1 杀鼠剂的适口性
表1 显示了使用褐家鼠对同分异构体P4、P5、P6 和异构体混合物R1 进行的灭鼠诱饵试验获得的摄食系数测量值以及单氯代R 的数据。
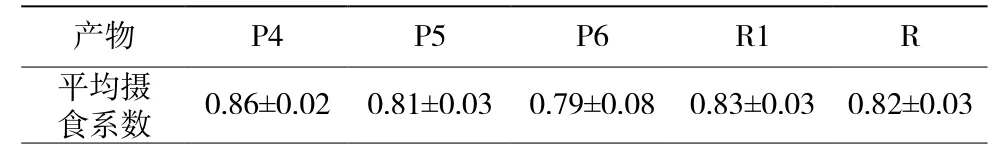
表1 1%产物的适口性数据
对于含1%P4、P5、P6 的诱饵,有100%死亡率,平均摄食系数为0.86~0.79,表明毒饵适口性好(> 0.3,p>0 .05)。同样,R1 的杀灭率也为100%,平均摄食系数(0.84,p> 0.05)也显示出良好的适口性。
2.2 LD50测量结果
通过式(1)和式(2)确定了 P4、P5、P6、R1 对褐家鼠的口服LD50,结果见表2 并且同时列出了单溴代R 的数据。P4 的LD50为2.82 mg·kg-1,P5的LD50为3.02 mg·kg-1,对褐家鼠的毒性较高,而R1 的LD50为2.92 mg·kg-1,介于P4 和P5 的值之间。P6 的LD50为95.50 mg·kg-1,毒性较低。同时还测得了对小白鼠的口服LD50,如表3 所示。结果表明,R1 对小白鼠的LD50为741.31 mg·kg-1,毒性较低。

表2 产物对褐家鼠的LD50数据

表3 产物对小白鼠的LD50数据
2.3 现场试验结果
表4 显示,R1 和溴敌隆对褐家鼠的平均校正杀伤率均> 85%。使用R1 时,大多数褐家鼠的死亡发生在食用诱饵后2 小时至4 小时,而使用溴敌隆的最大死亡率发生在5-7 天后。

表4 R1 和溴敌隆的现场杀灭测试结果
2.4 讨论
适口性和LD50测试结果表明,异构体对褐家鼠的毒性顺序为P4> P5 >> P6。可以通过氯原子与哌啶部分的接近来解释,这可能由于空间位阻而影响其功能(参见图2)。当两个Cl 原子位于Z1 和Z2位置(P4)时,哌啶基团不存在空间位阻,并且其活性不会降低。在异构体P5(Z1=Z4=Cl)中,Z4处的Cl 导致哌啶基团的部分空间位阻,其活性减弱。在异构体P6(Z3=Z4=Cl)中,哌啶基在空间上受到两个Cl 原子的阻碍,因此杀鼠剂的活性显着降低。因此,可以将这3 种异构体的毒性分级为P4> P5 >> P6。R1 对褐家鼠的LD50 介于P4 和P5之间,是因为其组成异构体P4、P5、P6 的含量比例为4∶2∶1。因此,R1 的急性毒性由P4 决定,表明R1 可以直接使用,无需分离异构体。同时R1对小白鼠的LD50 测试结果表明其对非目标生物的毒性很低,具有高选择性。
与单氯N-哌啶二苯并庚烯灭鼠剂相比,二氯代杀鼠剂的毒性显着提高。使用二苯并环庚酮的3,7-磺化合成氯化二氯杀鼠剂,然后将氯原子引导至苯并庚烯部分的目标1,9-位置(见图1)。不需要将产品分离的合成方法通常是更方便的工业生产的方法。尽管二氯代杀鼠剂有更多合成步骤,但产物(R1)只有3 种异构体(见图2),其中两个具有高毒性(P4、P5),不需要分离。而单氯杀鼠剂合成产率低且需要分离4 种异构体。因此R1 的合成方法更方便用于工业生产。
3 结 论
使用简单的合成方法,以二苯并环庚酮为起始原料以高产率制备了新型抗凝血灭鼠剂R1 的异构体混合物,并使用物理和光谱技术对中间体和产物进行了表征。急性毒性和现场试验的结果表明,R1对大鼠是一种有效且高度选择性的灭鼠剂,并且更适合于工业生产。

