EAACI与WAO严重过敏反应指南药物急救管理解读及证据分析
张紫薇,骆兵,葛卫红,汪小海
(1.南京大学医学院附属鼓楼医院药学部,南京 210008;2.中国药科大学基础医学与临床药学学院,南京 210009;3.南京大学医学院附属泰康仙林鼓楼医院麻醉科,南京 210008)
世界过敏组织(World Allergy Organization,WAO)于2011年发表了首篇严重过敏反应评估和管理指南[1](《World Allergy Organization Guidelines for the Assessment and Management of Anaphylaxis》),并于近期根据最新的证据发布了WAO严重过敏反应指导意见2020(《World Allergy Organization Anaphylaxis Guidance 2020》),下称“WAO指南”[2]。欧洲变态反应与临床免疫学会(European Academy of Allergy and Clinical Immunology,EAACI)于2014年发布了严重过敏反应指南(《Anaphylaxis:guidelines from the European Academy of Allergy and Clinical Immunology》,简称EAACI指南)[3]。此前,一项针对国内外现有严重过敏反应诊疗指南的质量评价研究[4]表明,EAACI指南的总体质量最高。本研究就EAACI指南和WAO指南急救管理部分内容进行解读,对比分析两部指南中应用肾上腺素、抗组胺药物、糖皮质激素、肾上腺素能β2受体激动药等急救药物管理有关的引文证据来源、类型和质量,并探讨最新的研究证据,以期了解严重过敏反应急救管理的规范用药及研究进展。
1 EAACI指南和WAO指南的基本特征
见表1。
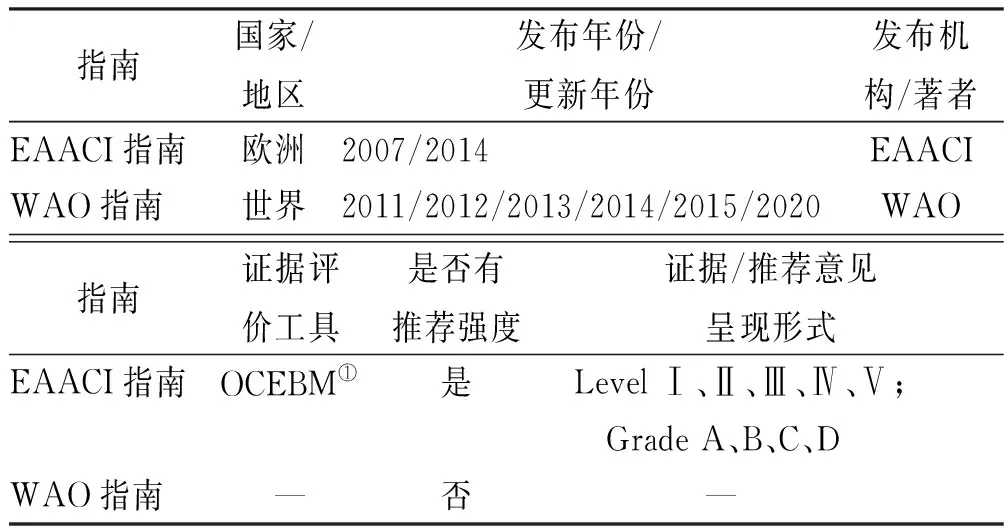
表1 EAACI指南与WAO指南基本特征
2 肾上腺素的应用
2.1作用机制 肾上腺素通过激动α1受体,收缩周围血管,从而逆转低血压和黏膜水肿;激动β1受体,增加心脏收缩力度和速度,从而逆转低血压;激动β2受体,逆转支气管收缩并减少炎性递质释放[5]。
2.2两部指南均支持将肾上腺素作为一线用药 国际上关于严重过敏反应的指南一致认为,肾上腺素是过敏反应的首选药物,同时也是减少住院和死亡人数的唯一药物,用于过敏反应的一线治疗[2-3,6]。LONG等[7]评估了急诊临床医师关于过敏反应诊断和管理的关键循证更新,强调了肾上腺素作为一线治疗药物的地位;英国复苏委员会(Resuscitation Council UK,RCUK)过敏反应小组也证实了须将肾上腺素作为治疗过敏性休克的一线干预措施[8]。
对于过敏反应患者,肾上腺素没有绝对禁忌证,所有过敏反应患者必须使用肾上腺素,该药也可用于可能发展为过敏反应的潜在患者,EAACI指南将此建议作为C级推荐。EAACI指南指出,快速识别过敏反应、早期肌内注射肾上腺素与提高生存率有关。而近期一项描述性研究指出,虽然大多数儿科医生将肾上腺素视为一线药物,但近半数医生未能识别和正确处理过敏反应[9]。因此,提高医疗人员和患者对肾上腺素重要性的认识与依从性十分必要。WAO指南指出,肾上腺素的时间依赖性和浓度依赖性药理作用已在体外人血管平滑肌细胞模型中得到证实。SUNDQUIST等[10]研究表明,与就诊后使用肾上腺素相比,就诊前立即使用肾上腺素治疗可降低住院可能性,且缩短住院时间。WAO指南指出,在过敏反应初始治疗中,注射肾上腺素的证据基础强于抗组胺药和糖皮质激素,并强调了迅速进行初始治疗以防止症状加重的重要性[1]。最近,一项在加拿大进行的队列研究表明,早期使用肾上腺素可降低患者接受≥2剂肾上腺素治疗的可能性[11]。
2.3肾上腺素给药途径的异同
2.3.1两部指南均支持肾上腺素肌内注射给药 EAACI指南和WAO指南均推荐肾上腺素通过肌内注射到大腿中部外侧,EAACI指南将此给药途径作为B级推荐(I类证据)。其证据来源于SIMONS等[12-13]开展的2项临床对照试验,其中一项试验指出,患儿在肌内注射后(8±2) min肾上腺素达到峰浓度,明显短于皮下注射后[(34±14) min],儿童皮下注射肾上腺素的建议是基于临床经验,实际应根据皮下注射时肾上腺素吸收延迟的情况重新评估,证据支持肌内注射法[12]。另一项试验研究了年轻男性2个不同部位(股外侧肌或上臂三角肌)肌内注射或皮下注射相同剂量(0.3 mg,0.3 mL)肾上腺素后平均血浆肾上腺素浓度与时间的关系。结果发现与三角肌相比,股外侧肌对肾上腺素吸收更好,血浆肾上腺素达峰时间更短,建议成人过敏反应初始治疗首选股外侧肌肌内注射肾上腺素[13]。尽管证据被评估为低确定性,但根据肾上腺素肌内注射给药便利性和安全性,以及目前临床和非临床对肌内注射途径的接受程度,RUCK过敏反应小组强烈推荐肾上腺素肌内注射给药途径[8]。
2.3.2肌内注射安全性的证据差异 肾上腺素肌内注射的安全性问题,EAACI指南指出,尽管患者可能出现短暂的脸色苍白、心悸和头痛,但肌内注射肾上腺素安全性非常好。EAACI指南对此未给出明确证据来源,而WAO指南引文证据支持肌内注射肾上腺素的耐受性良好。LIEBERMAN等[14]指出,静脉推注肾上腺素(与肌内注射剂量相当)与增加不良事件的风险有关。尽管肾上腺素最佳剂量药动学和药效学数据有限,但在过敏反应中正确使用肾上腺素具有良好的安全性和有效性。
2.3.3关于其他给药途径的建议 关于肾上腺素给药途径,EAACI指南提出不建议对过敏反应患者使用皮下或吸入性肾上腺素。近期一项关于肾上腺素药动学的研究指出,肌内注射可达到更高血浆肾上腺素水平,因此不推荐皮下注射给药[15]。WAO指南不建议将静脉途径用于过敏反应初始治疗,如需使用静脉途径,应由临床工作者使用静脉输注泵进行静脉输注。尽管国际指南建议在所有情况下将肌内注射肾上腺素用于过敏反应一线治疗,但最新一项对与过敏反应相关心脏骤停的高级生命支持指南的综述指出,如果心脏骤停即将发生或已经发生,则需要静脉推注肾上腺素[16]。
2.4肾上腺素给药剂量异同
2.4.1肾上腺素肌内注射给药剂量比较 通常用于过敏性休克的肾上腺素浓度为1 mg·mL-1,如果仅有浓度0.1 mg·mL-1肾上腺素,则需进行大剂量多部位注射[5]。EAACI指南引文证据支持肾上腺素肌内注射应使用1:1000肾上腺素(1 mg·mL-1),剂量为0.01 mL·kg-1(最大单次剂量为0.5 mg),相当于10 μg·kg-1,这个剂量可以短时间(每5~10 min)重复,直到患者病情稳定;如果静脉注射肾上腺素,建议剂量为0.1 μg·kg-1·min-1,此证据来源缺乏可靠性,推荐等级低。WAO指南推荐肌内注射肾上腺素给药剂量为0.01 mg·kg-1的1:1000(1 mg·mL-1)溶液,成人最大剂量为0.5 mg,儿童和青少年最大剂量为0.3 mg,这是基于美国食品药品管理局批准的肾上腺素标准剂量和给药途径[17],此建议是根据肾上腺素的其他用途推断出来的。RCUK过敏反应工作组的综述纳入的3项随机对照试验[18-20]比较了肌内注射不同剂量肾上腺素的药动学过程,研究发现较高剂量肾上腺素吸收更好,但对过敏反应患者临床反应的影响尚不清楚。虽然有关肾上腺素剂量证据可靠性较低,但鉴于这些剂量已在全球广泛使用了几十年,该工作组强烈推荐以上给药剂量[8]。
2.4.2肾上腺素自动注射器给药剂量比较 目前肾上腺素自动注射器(epinephrine autoinjector,EAI)有两种固定剂量,即EpiPen Jr(0.15 mg)或EpiPen(0.3 mg)。EAACI指南推荐体质量7.5~25 kg患者应接受EpiPen Jr,体质量25~30 kg应使用EpiPen。一项随机试验针对存在过敏风险的儿童使用EpiPen Jr或EpiPen进行研究,结果发现后者可显著提高收缩压,但不良反应更多,固定剂量肾上腺素有助于过敏反应患儿在院外完成更精确给药[18]。WAO指南指出,使用EpiPen Jr或EpiPen无法给体质量<15 kg或体质量15~30 kg儿童提供精确的剂量(0.01 mg·kg-1)。根据研究数据,推荐将0.15 mg规格的EAI用于体质量10~25 kg儿童,0.3 mg规格EAI用于体质量≥25 kg儿童,但在临床决策中必须考虑特定临床情况[21]。EAI剂量随着年龄增长而变化,幼儿可能受益于较小剂量,肥胖成年人可能受益于较大剂量[5]。一项关于肾上腺素安全性和药动学的研究指出,与0.3 mg相比,0.5 mg剂量组血浆肾上腺素峰值更高(P=0.01),曲线下面积更大(P<0.05),具有更有利的药动学和药效学特征,且不会导致更高全身不良反应发生率事件[19]。虽然使用EAI初始给药更方便快速,但应通过注射器给药以提供最佳剂量[8]。
2.5重复肌内注射肾上腺素的必要性 EAACI指南指出需要重复肌内注射肾上腺素的患者可从中受益,当患者对肌内注射≥2次剂量的肾上腺素反应不足时,应由重症监护室和急诊医生进行输液和心电监护,推荐等级为D级(IV类证据);需要重复剂量肾上腺素的患者应至少间隔5 min,此建议主要基于专家共识,仍缺乏充足的研究证据支持,推荐等级为D级。WAO指南推荐,根据过敏反应的严重程度和患者初次注射肾上腺素的反应,可每5~15 min重复注射,大多数患者对肌内注射1或2剂肾上腺素有反应,有时需要大于2剂。关于重复肌内注射肾上腺素的时间间隔,近期一项药动学研究给出了证据支持。研究表明,肌内注射后肾上腺素吸收遵循双相曲线,初始峰值出现在5~10 min内[15],而在过敏反应患者对肾上腺素没有反应的情况下等待超过5 min的原因尚不清楚[8]。关于重复肌内注射肾上腺素的合理性,一项系统评价和荟萃分析表明,大多数患者对重复剂量的肾上腺素有反应,只有2.2%(95%CI1.1%~4.1%)患者对重复剂量肾上腺素无反应[22]。
3 抗组胺药物的应用
3.1作用机制 H1抗组胺药(如静脉注射氯苯那敏或苯海拉明、口服西替利嗪)通过拮抗H1受体,减轻皮肤和黏膜症状(如瘙痒、潮红、荨麻疹、打喷嚏和鼻漏等),由于其不能防止或缓解气流阻塞,故不能代替肾上腺素用于挽救患者生命[1]。
3.2EAACI指南推荐抗组胺药物作为三线用药 EAACI指南指出,口服H1和H2抗组胺药可以缓解皮肤过敏症状,并将此建议作为B级推荐(I类证据),同时推荐作为过敏反应的三线用药。一项关于评估西咪替丁(H2抗组胺药)和苯海拉明(H1抗组胺药)单独和联合治疗急性过敏反应效果的研究表明,治疗急性过敏反应引起的瘙痒,苯海拉明比西咪替丁更有效,而联合用药没有更多益处;治疗急性荨麻疹,联合用药比单用苯海拉明更有效[23]。基于以上研究,EAACI指南指出,联用H1和H2抗组胺药可能比单用H1抗组胺药更有益。
3.3WAO指南推荐抗组胺药物作为二线用药 WAO指南推荐将抗组胺药作为治疗过敏反应的二线药物,证据源于荨麻疹的治疗方案,使用二线药物可能延迟一线药物肾上腺素的及时注射[1]。WILEY等[24]研究发现,入院前使用抗组胺药与延迟就诊有关,可能导致肾上腺素给药延迟和发病率增加。一项在加拿大进行的队列研究指出,H1抗组胺药在过敏反应治疗中的作用有限,但有助于缓解皮肤症状,入院前使用肾上腺素和抗组胺药物可能减少≥2剂肾上腺素的使用[11]。WAO指南指出,仍需要高质量随机对照试验来研究抗组胺药物在急性过敏反应中的作用。
3.4两部指南均支持抗组胺药物口服给药 EAACI指南与WAO指南所引用的病例报告表明,静脉注射抗组胺药可能引起低血压,这可能与给药速度有关,因此仅建议口服H1和H2抗组胺药缓解皮肤过敏性症状。该建议是基于一项关于肠外抗组胺药异丙嗪所致过敏性低血压研究的结果,该研究强调了肠外抗组胺药的潜在风险[25]。WAO指南引用的一项队列研究表明,鉴于第二代抗组胺药起效较快且不良反应较小,建议联用第二代抗组胺药和肾上腺素,避免静脉注射第一代抗组胺药[11]。
4 糖皮质激素的应用
4.1作用机制 糖皮质激素(静脉注射氢化可的松或甲泼尼龙、口服泼尼松或泼尼松龙)可关闭许多促炎蛋白活化基因编码的转录,需几小时才能起效,通常用于预防和缓解长期或双相过敏反应[1]。
4.2EAACI指南推荐糖皮质激素作为三线用药 EAACI指南指出,全身性糖皮质激素可用于降低晚期呼吸系统症状的风险,大剂量雾化吸入糖皮质激素可能有利于改善上呼吸道阻塞症状(V类证据);一线和二线治疗结束后,可将糖皮质激素作为过敏反应的三线用药;高剂量雾化吸入布地奈德可能有助于治疗气道水肿,建议用于伴有喘鸣的患者,此建议推荐等级为D级。
4.3WAO指南推荐糖皮质激素作为二线用药 WAO指南推荐将糖皮质激素作为过敏反应的二线用药,并指出糖皮质激素的给药剂量源于急性哮喘治疗方案,给药途径取决于发作的严重程度[1]。口服或静脉注射糖皮质激素可以预防延迟性过敏反应症状,尤其是在伴有哮喘或双相反应患者中,但这尚未得到证实。Cochrane系统评价未发现任何关于糖皮质激素在过敏反应中的有效性证据。WAO指南指出,目前关于糖皮质激素在过敏反应中的使用存在争议,越来越多的证据表明糖皮质激素可能在过敏反应急救中没有益处,甚至可能有害。CAMPBELL等[26]指出,缺乏可靠的证据支持在过敏反应中常规使用糖皮质激素,RCUK过敏反应工作组明确建议不常规使用糖皮质激素治疗过敏反应[8]。LIYANAGE等[27]的系统评价指出,根据现有数据,糖皮质激素可能有益,而且尚无证据表明在过敏反应紧急治疗中使用糖皮质激素会产生不良后果。目前仍需进一步研究来阐明糖皮质激素治疗是否能减少过敏反应中双相反应的发生。
5 肾上腺素能β2受体激动剂的应用
EAACI指南推荐应吸入短效β2受体激动剂以减轻过敏反应患者支气管收缩症状,推荐等级为D级(V类证据);轻度喘息初期可能仅使用吸入的短效β2受体激动剂进行治疗,如5 min内没有反应,应给予肌内注射肾上腺素,此建议推荐等级为D级。WAO指南指出,在有过敏反应和支气管狭窄症状的患者中,可给予吸入短效β2受体激动剂,但若存在持续症状,吸入或雾化给药的支气管扩张剂不能替代肌内肾上腺素的重复给药。证据基础源于急性哮喘的治疗方案,尚无相关研究证据支持。
6 其他药物的应用
EAACI指南和WAO指南指出,胰高血糖素肠外给药可治疗对肾上腺素无反应的过敏患者,特别是服用β受体阻断药的患者,此建议推荐等级为D级。证据基于一项回顾性研究[28],该研究指出,当所有其他公认的治疗都失败时,胰高血糖素肠外给药可能对服用常规β受体阻断药过敏性休克患者有益,但临床证据源于病例报告,因而证据质量有限。
7 讨论
严重过敏反应是临床紧急情况,严重时可能危及患者生命,通常基于临床症状和体征来诊断,过敏测试通常有助于准确识别触发因素。其严重程度评分系统对患者的治疗决策意义重大,但目前国际上对其尚未达成共识。本文对2014年EAACI指南和2020年WAO指南中严重过敏反应药物急救管理部分内容进行解读,列举了引文证据内容与证据水平,真实反馈了指南建议的推荐等级和证据来源,并对当前最新研究证据进行了补充分析。
7.1两部指南内容和形式的差异 EAACI指南全面阐述和讨论了严重过敏反应的定义、危险因素、临床症状、诊断标准、鉴别诊断、治疗、预防、长期管理和教育培训,推荐将肾上腺素能β2受体激动剂作为过敏反应的二线用药,抗组胺药物和糖皮质激素作为三线用药。WAO指南关注严重过敏反应的触发和协同因素、诊断、治疗、出院后管理和预防,特别强调了初始基础治疗及肾上腺素的使用,并将肾上腺素能β2受体激动剂、抗组胺药和糖皮质激素均作为二线用药。在EAACI和WAO两部指南中,EAACI指南以推荐意见的形式给出建议,列举了明确的证据等级和推荐强度,其推荐强度基于证据质量,并权衡利弊而形成,而WAO指南并未提及,推荐意见不明晰。
7.2缺乏高质量研究证据 两部指南一致认为,肌内注射肾上腺素是过敏反应的一线干预措施,但目前仍缺乏强有力的研究评估其有效性[29]。关于肾上腺素的给药方案,需要药动学研究以确定最佳给药剂量和给药间隔,并加强肾上腺素其他给药途径的相关研究。EAACI指南和WAO指南二线和三线用药的证据基础仍有待加强,仍需随机对照研究来评估全身性糖皮质激素在预防迟发型过敏反应的有效性,关于联用抗组胺药是否能改善过敏反应患者呼吸或心血管功能的随机对照研究有待补充。关于过敏反应文献的系统综述表明该领域缺乏高质量的证据支持当前的治疗决策,循证证据仍有待补充[29],应对现实环境中有过敏反应风险患者进行大规模前瞻性队列研究,以便更清楚地了解与每个因素相关的风险大小[30],以使患者获益。
7.3两部指南对我国指南制订的启示 国内外医疗条件和卫生意识等方面均存在较大差异,国外指南在国内的适用性仍待验证,国内对于严重过敏反应急救用药的管理有待加强,对肾上腺素作为一线用药的重要性仍缺乏认识,应明确肾上腺素的给药时机、给药途径和给药剂量,并提高二三线用药合理性。目前国内对于严重过敏反应的认识严重不足,《严重过敏反应急救指南》尚未正式发布,仅刊出了该指南关于严重过敏反应诊断、救治和救治后管理的26条推荐意见[31],并确定了需要纳入的临床问题与结局指标[32]。由于各国医疗资源存在差异,医护人员根据现有指南与共识进行的临床决策,以及患者对疾病的认知有所不同,因此,应关注国外指南的推荐意见是否适合本国国情,重点考虑该领域最佳证据在严重过敏反应急救过程中的应用,制订适合我国国情的严重过敏反应救治指南有利于该疾病的管理。此外,国外随机对照试验、系统评价和Meta分析研究相较于国内范围更广,国内应加强相关研究以弥补不足。
总之,EAACI指南和最新版WAO指南在严重过敏反应急救管理方案中的引文证据均支持将肾上腺素作为一线用药,而对于抗组胺药、肾上腺素能β2受体激动剂和糖皮质激素推荐意见有所不同。指南间存在的分歧仍需通过进一步的研究来解决,高质量的研究证据则需要更多的大规模前瞻性队列研究加以补充。

