负载ZnO的赤泥吸附剂对刚果红的吸附试验研究
乔春蕾,殷 悦,徐高扬,许玉星,刘长青
(青岛理工大学 环境与市政工程学院,山东 青岛 266033)
纺织、印染工业每年排放大量染料废水[1]。染料本身结构稳定,难生物降解,进入水体后会对生态环境产生一定影响[2-3],因此,染料废水需处理后才能排放。刚果红(CR)是一种联苯胺阴离子偶氮染料,分子式为C32H22N6Na2O6S2,目前用于去除或降解刚果红的研究受到关注[4]。
吸附法因操作简单、常用于处理染料废水,但吸附剂的吸附效果和成本是制约该方法的瓶颈问题之一。赤泥(RM)是生产氧化铝过程中的碱性废渣,其中含有大量Fe2O3、Al2O3,且具有高比表面积,其对废水处理有很好的效果,适于作为吸附剂载体进行资源化利用。
氧化锌(ZnO)成本低,化学稳定性好,对环境无害,因有大量官能团而常常被用作吸附剂[5-6]。氧化锌的等电点(IEP)为9.3~9.8[7],在中性pH下具有正电荷,对阴离子染料刚果红有较好的吸附潜力。但ZnO纳米粒子在水溶液中易于聚集[8],不利于扩散。利用多孔材料负载ZnO可以提高ZnO纳米粒子的比表面积和聚集电阻[9],还会增加多孔材料的吸附位点,提高吸附能力。为此,研究了在赤泥表面原位沉淀Zn2+,再经过煅烧使生成ZnO,充分利用赤泥的碱性和高比表面积,扩大ZnO与溶液的接触面积,从而提高ZnO吸附能力,以期为印染废水的处理及赤泥的资源化利用提供一种新思路。
1 试验部分
1.1 仪器与试剂
试剂:赤泥(RM),粒度<100目,山东省滨州市魏桥电解铝厂;Zn(Ac)2·2H2O、NaOH、HCl,国药集团化学试剂有限公司,分析纯;刚果红,国药集团化学试剂有限公司。
仪器:分析天平,磁力搅拌器,电热鼓风干燥箱,pH计,便携式分光光度计DR2800,恒温振荡器,马弗炉,傅里叶变换红外光谱仪,扫描电子显微镜,布鲁克X射线能谱仪,X射线衍射仪。
1.2 RM-ZnO及ZnO的制备
RM-ZnO的制备:取2 g干燥赤泥,在250 mL纯净水中静置12 h充分释放碱性后,磁力搅拌同时分别将用5 mL纯净水溶解的0.2、0.4、0.8 g Zn(Ac)2·2H2O缓慢加入其中;同时,用5 mol/L的NaOH溶液调pH至10以上,室温下搅拌1 h,之后静置沉淀,过滤,洗涤,沉淀物于80 ℃下烘干,在马弗炉中于400 ℃下焙烧2 h,分别得到RM-ZnO-1、RM-ZnO-2、RM-ZnO-3。
ZnO的制备:将0.1 mol的Zn(Ac)2·2H2O溶于50 mL纯净水中,再缓慢加入0.5 mol/L NaOH溶液中,磁力搅拌1 h,之后步骤同RM-ZnO制备。
1.3 材料表征
采用扫描电子显微镜(SEM,蔡司,Sigma 300)测定表面形貌,采用布鲁克X射线能谱仪(EDS)进行面扫描和光谱分析元素组成,采用X射线衍射仪(XRD,日本理学,Smartlab)测定物质组成,采用傅里叶变换红外光谱仪(FT-IR,PE,Frontier FT-MIR)测定官能团种类和化学键。
1.4 吸附试验
首先配制刚果红储备液(1.0 g/L),之后稀释储备液至不同浓度。吸附试验在玻璃试管中进行。刚果红溶液25 mL,加入一定质量吸附剂,于180 r/min转速下恒温振荡一定时间,之后在4 000 r/min速度下离心分离5 min。取上清液于λmax=497 nm处测定吸光度。用0.1 mol/L的HCl和NaOH溶液调刚果红溶液pH。
为了试验数据的准确性,每组试验设置3个平行样品。
1.5 数据处理
刚果红吸附量计算公式为
(1)
刚果红去除率计算公式为
(2)
式中:qe—平衡吸附量,mg/g;r—去除率,%;ρ0—初始刚果红质量浓度,mg/L;ρe—吸附平衡时刚果红质量浓度,mg/L;ρt—吸附t时间时刚果红质量浓度,mg/L;m—吸附剂质量,g;V—刚果红溶液体积,L。
1.6 动力学模型
为了解释吸附机制,对试验数据进行准一级动力学模型、准二级动力学模型、颗粒内扩散模型拟合。模型分别见式(3)~(5):
lg(qe-qt)=lgqe-k1t;
(3)
(4)
(5)
式中:qe—平衡吸附量,mg/g;qt—吸附t时间时的吸附量,mg/g;t—吸附时间,h;k1—准一级吸附速率常数,h-1;k2—准二级动力学常数,g/(mg·h);ki—颗粒内扩散常数,mg/(g·h1/2);I—与边界层反应相关的常数,mg/g。
1.7 等温吸附模型
Langmuir、Freundlich等温吸附模型分别见式(6)、(7):
(6)
(7)
式中:qm—吸附剂最大吸附量,mg/g;kL—Langmuir平衡常数,L/mg;kF—Freundlich分布系数,mg1-1/n·L1/n·g-1;n—Freundlich常数。
Langmuir等温吸附模型假设吸附剂表面是均匀的[10-12],描述了吸附质在吸附剂表面形成单层吸附,吸附位点间无相互作用,只要吸附位点没有被完全占据,吸附质浓度会影响吸附量[13]。Freundlich等温吸附模型描述了非均质表面的多层吸附,认为非均质表面的活性位点具有能量分布不均一现象,并伴有被吸附分子之间的相互作用[13-14]。
2 试验结果与讨论
2.1 材料表征
2.1.1 形貌及元素组成分析
ZnO和RM-ZnO-2的SEM图像及RM-ZnO-2部分区域EDS扫描元素映射图像如图1所示。

图1 ZnO(a)和RM-ZnO-2(b、c)的SEM图像及RM-ZnO-2的EDS元素图像(d~h)
由图1(a)、(b)看出,ZnO与RM-ZnO-2的形貌有很大不同:ZnO为很薄的片状结构,并有团聚;而RM-ZnO-2的表面有一些不规则形状凸起。由图1(c)、(e)、(g)、(h)看出:这些凸起部分含有Al、Fe、Si元素,说明这部分是赤泥本身的形貌组成部分;凸起部分也有Zn元素,且与Al、Fe、Si元素有相同轮廓,说明ZnO分布在赤泥表面,并非自聚集。RM-ZnO-2表面看不到ZnO的片状结构,可能是因为赤泥表面上所负载的ZnO纳米颗粒较小,不易被观察到,这也说明复合材料中赤泥会阻止ZnO团聚。
2.1.2 晶体形态分析(XRD)
ZnO、RM、RM-ZnO-2的XRD结果如图2所示。
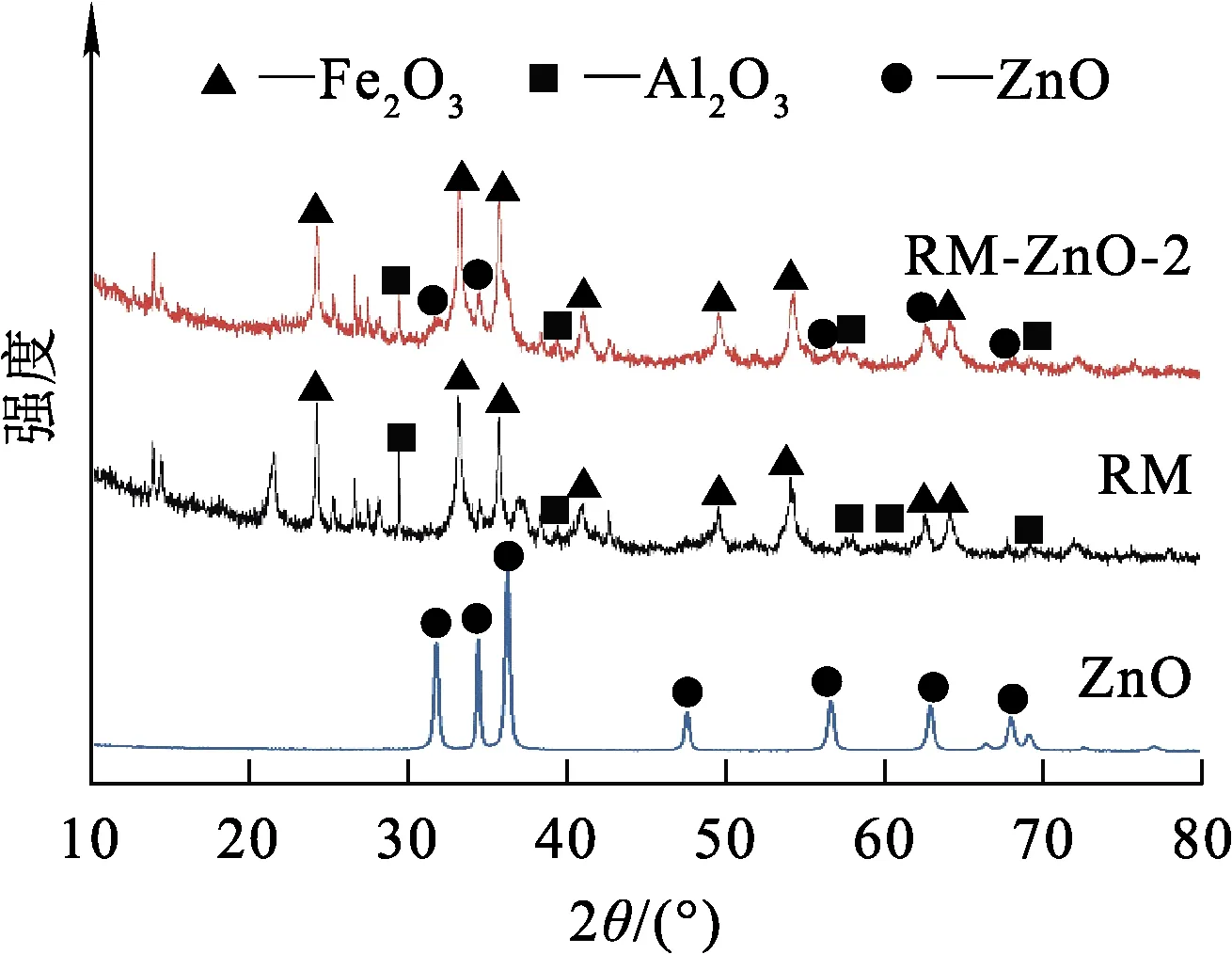
图2 RM-ZnO-2、RM和ZnO的XRD表征结果
由图2看出:ZnO在2θ为31.76°、34.40°、36.26°、47.54°、56.56°、62.84°、67.94°附近出现ZnO特征峰;RM-ZnO-2图谱上也有ZnO特征峰,说明ZnO被成功负载到RM表面;RM-ZnO-2图谱中的ZnO特征峰比纯ZnO的更宽,说明RM-ZnO-2中的ZnO粒径更小[15],这与SEM分析结果一致,且RM-ZnO-2中的部分ZnO特征峰未检测出,说明RM-ZnO-2上的ZnO是无定型且高度分散的[16]。
2.1.3 官能团及化学键分析

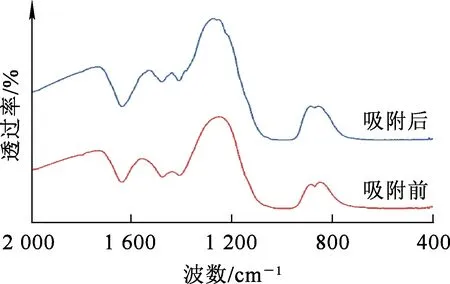
图3 RM-ZnO-2吸附刚果红前、后的FT-IR光谱
2.2 RM与ZnO配比对吸附的影响
试验条件:溶液中初始刚果红质量浓度50 mg/L,溶液体积25 mL,溶液pH为初始时的6.5,RM-ZnO-2投加量0.5 g/L,温度25 ℃,搅拌速度180 r/min,吸附时间8 h。RM与ZnO配比对RM-ZnO吸附刚果红的影响试验结果如图4所示。
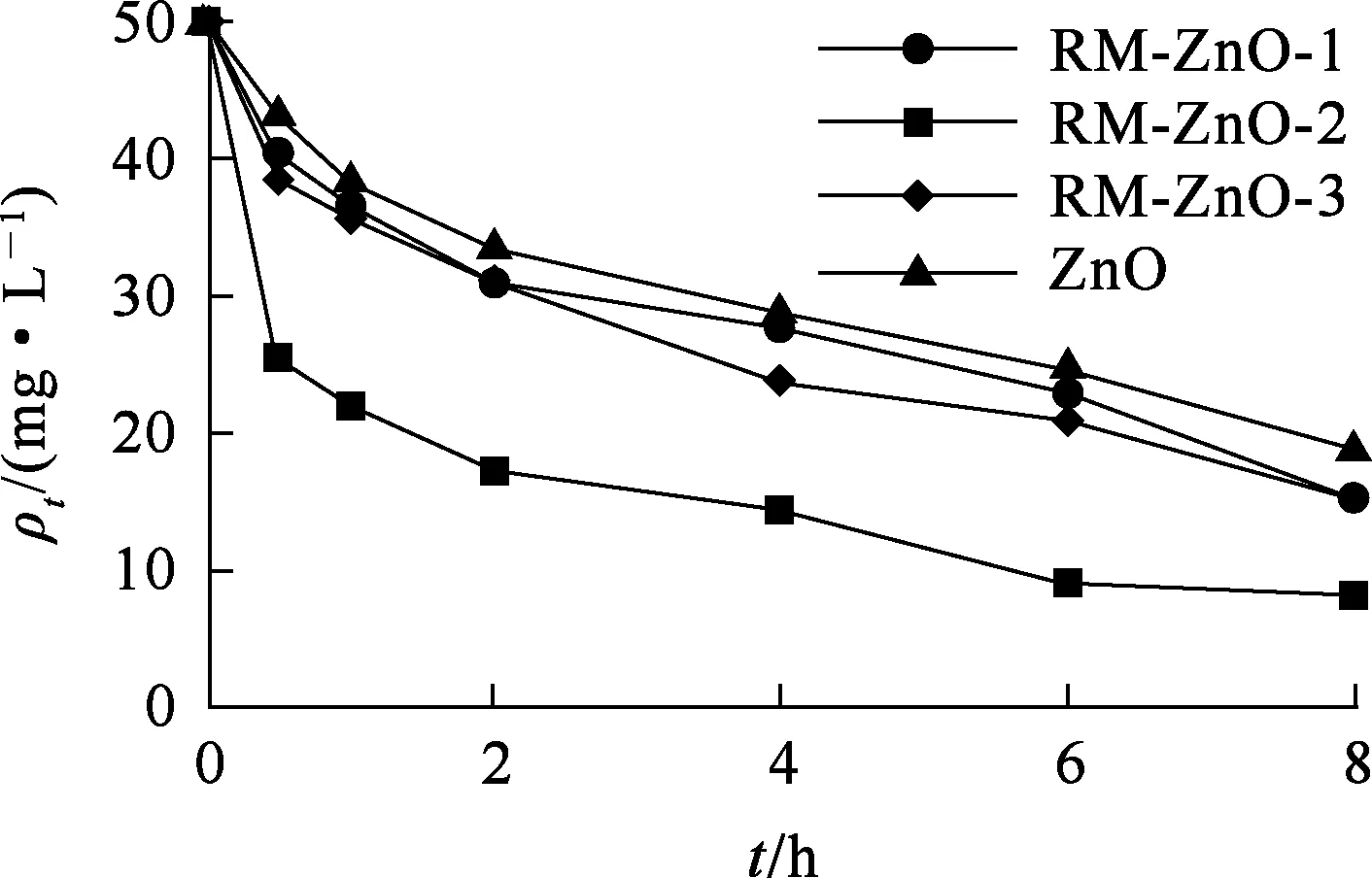
图4 不同配比的RM-ZnO和纯ZnO对刚果红的吸附曲线
由图4看出:相同条件下,RM-ZnO的吸附效果优于纯ZnO的吸附效果。这是因为RM上的ZnO没有聚集现象,吸附位点不会相互遮盖,并且RM本身对刚果红也有一定吸附能力[17]。图4表明:RM-ZnO-1、RM-ZnO-3的吸附能力均弱于RM-ZnO-2的吸附能力,因为RM-ZnO-1表面负载的ZnO数量较少,有效位点少;而RM-ZnO-3表面负载的ZnO的量过多,导致比表面积减小。后续试验中,均选用RM-ZnO-2作吸附剂。
2.3 溶液pH对吸附的影响
试验条件:溶液中初始刚果红质量浓度50 mg/L,溶液体积25 mL,RM-ZnO-2投加量0.5 g/L,温度25 ℃,振荡速度180 r/min,吸附时间8 h。溶液pH对RM-ZnO-2吸附刚果红的影响试验结果如图5所示。
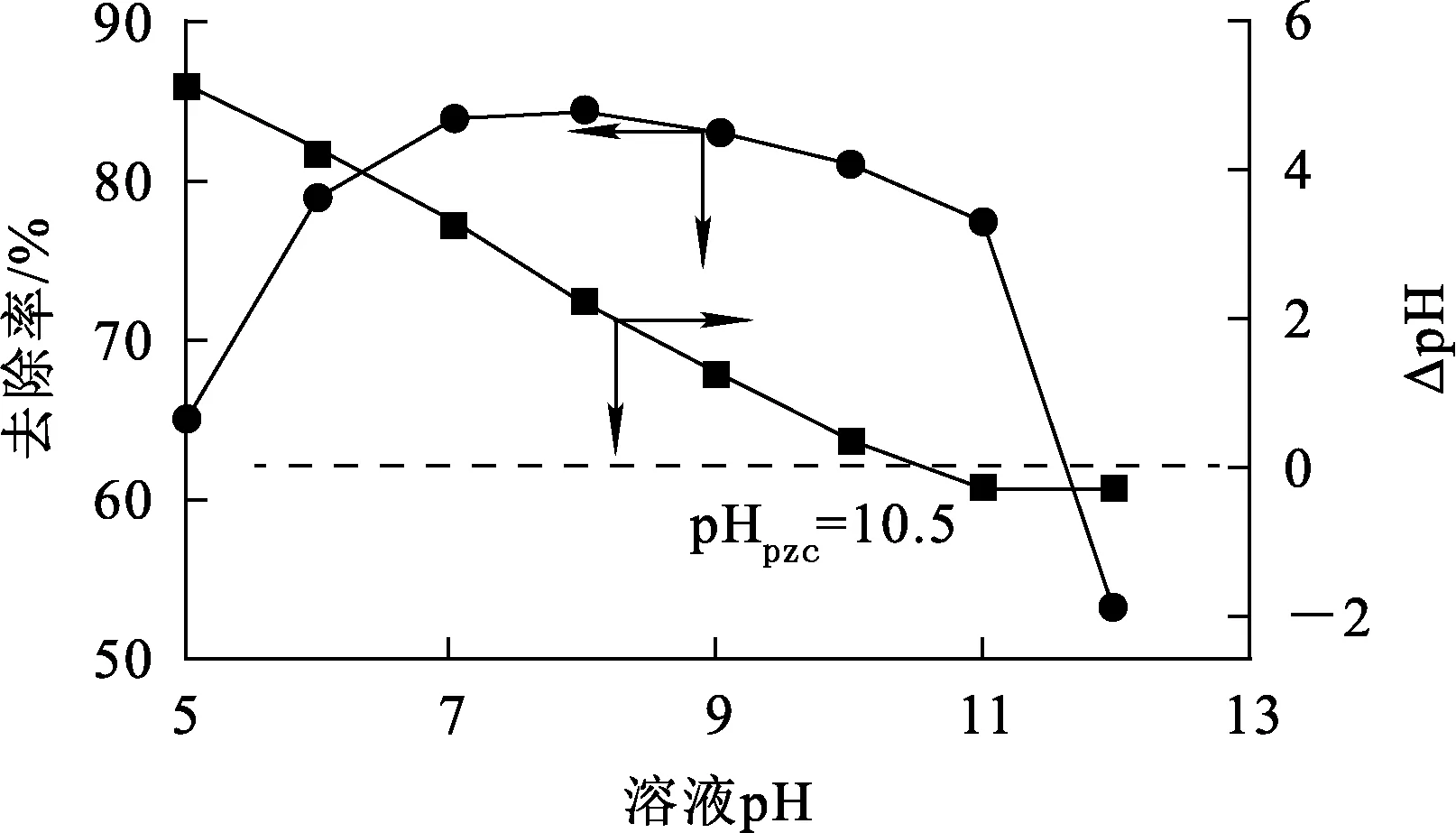
图5 溶液pH对RM-ZnO吸附刚果红的影响
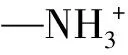
pH对RM-ZnO吸附刚果红有很大影响,说明吸附过程中存在静电作用;而在pH=12时依然能达50%的吸附能力,说明除静电作用外还有其他吸附机制[18]。溶液初始pH=6.5时吸附效果良好,所以后续试验均在初始pH条件下进行,溶液pH不必调整。
2.4 吸附动力学分析
在温度25 ℃、RM-ZnO-2投加量0.5 g/L条件下,溶液中刚果红质量浓度分别为50、100、200 mg/L,吸附时间对RM-ZnO-2吸附刚果红的影响试验结果如图6(a)所示。图6(b)~(d)分别为准一级动力学模型、准二级动力学模型和颗粒内扩散模型对该试验数据的线性拟合结果,拟合相关参数见表1。
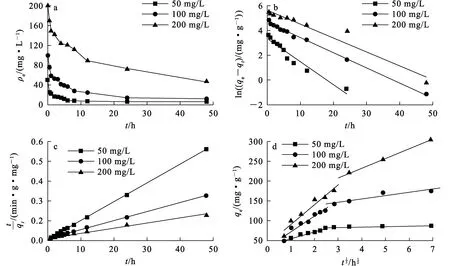
图6 吸附时间对RM-ZnO-2吸附刚果红的影响(a)及准一级(b)、准二级(c)、颗粒内扩散吸附模型(d)的拟合曲线
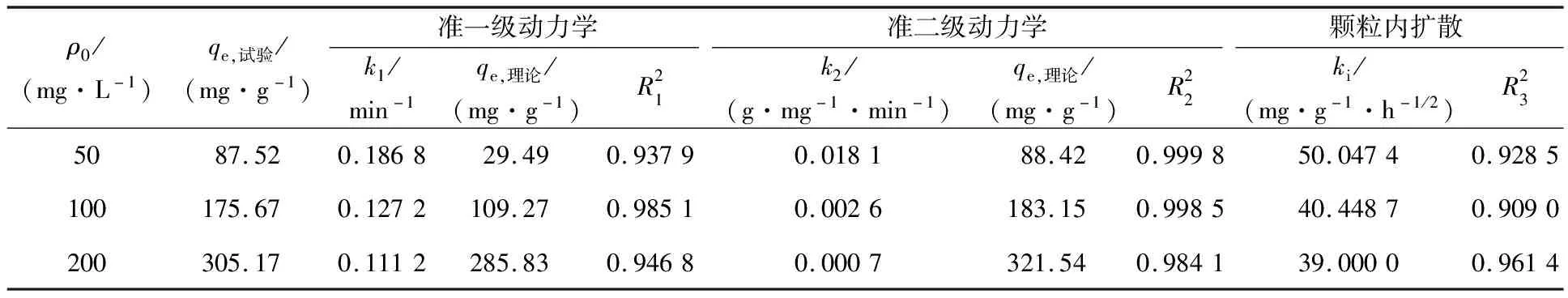
表1 准一级、准二级、颗粒内扩散吸附模型动力学拟合参数
由图6(a)看出:曲线整体趋于平滑且连续,说明刚果红分子可能在RM-ZnO-2表面形成单层覆盖[20]。最初的10 h内,刚果红浓度降低非常快,这主要是RM-ZnO-2有大量吸附位点,且溶液中的刚果红与RM-ZnO-2上的刚果红浓度差较大,吸附驱动力较大,使得反应速率较快[21];而随吸附进行,溶液中刚果红浓度降低速度变慢,因为RM-ZnO-2表面大量吸附位点被占据,而溶液中刚果红浓度降低,RM-ZnO-2表面的刚果红浓度却增大,吸附驱动力减小,甚至液相和固相上的刚果红分子产生排斥,使得吸附速率逐渐变小;也因为排斥力的存在,导致RM-ZnO-2表面的剩余空位无法被刚果红完全占据,从而刚果红分子不会被完全吸附[14]。另外,图6(a)中,刚果红浓度较低时,达到平衡所需时间短,刚果红去除率高,而刚果红浓度较高时,达到平衡所需时间较长,刚果红去除率低。这是因为高浓度溶液中刚果红分子多,分子间竞争力较大[22],而低浓度溶液中刚果红分子间竞争力较小,更有利于吸附。
准二级动力学模型拟合曲线与试验数据更匹配,且相关系数更接近1,说明吸附过程更符合准二级动力学模型,吸附过程受化学反应控制,吸附机制涉及电子共享或电子转移[8]。图6(d)中线性部分有两段,说明不止一种动力学机制参与刚果红吸附过程:第一段线性斜率较大,受物理吸附和化学吸附所控制,为表面吸附;第二段线性斜率较小,受颗粒内扩散效应和化学吸附所控制。
2.5 等温吸附模型拟合
分别在25、35、45 ℃下对不同浓度刚果红溶液吸附至平衡,RM-ZnO-2投加量0.5 g/L,分别对不同温度下的吸附数据进行等温吸附模型拟合,拟合曲线如图7所示,拟合参数见表2。
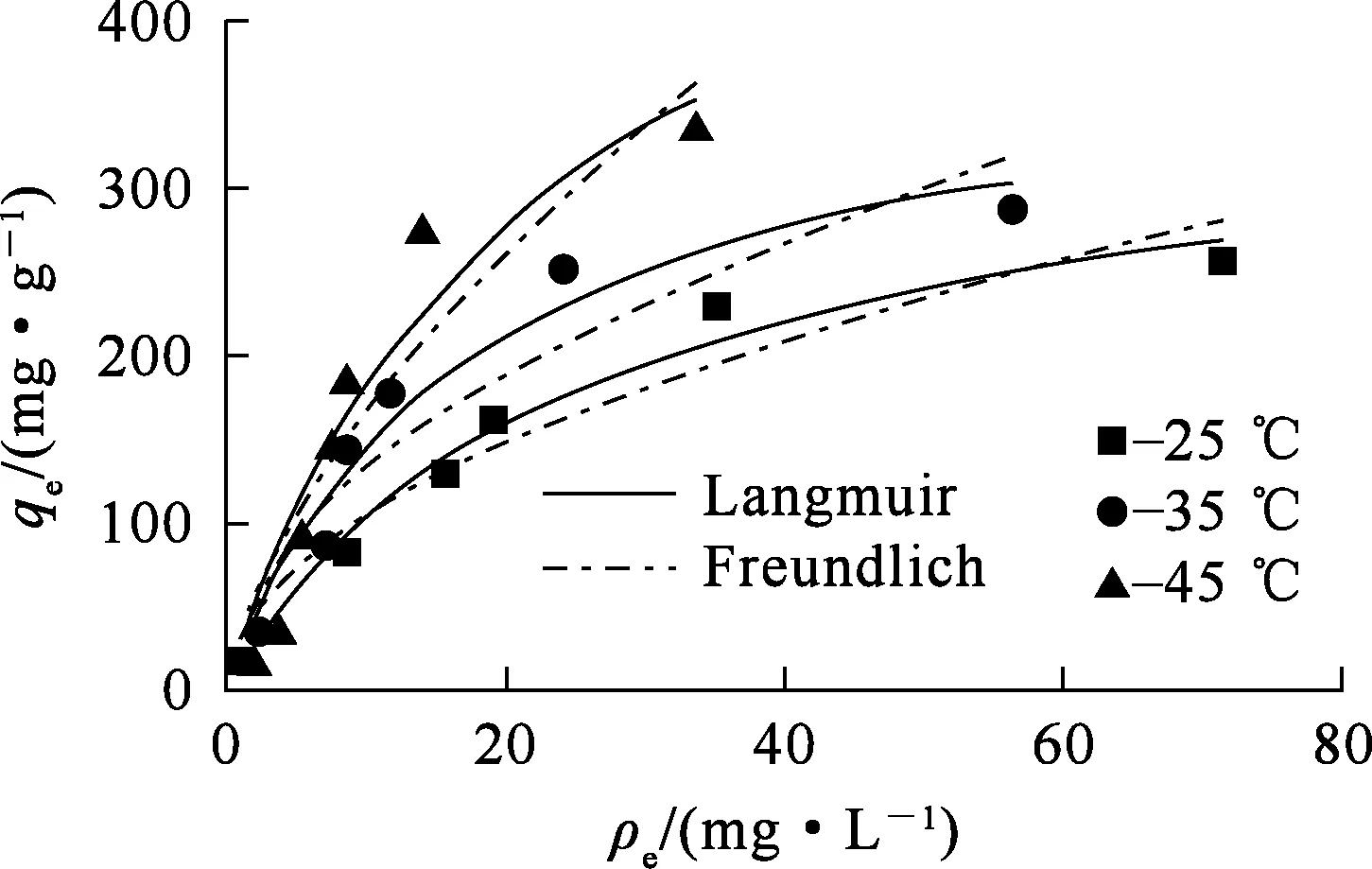
图7 等温吸附拟合曲线
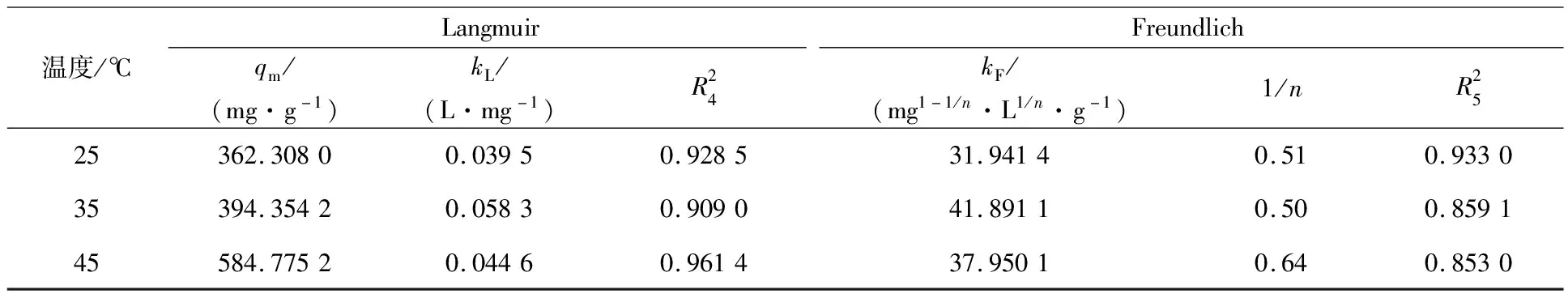
表2 Langmuir和Freundlich等温吸附拟合参数
由图7看出:RM-ZnO-2对刚果红的吸附量随温度升高而增大。这可能有以下原因:随温度升高,溶液黏度降低,刚果红分子扩散速率提高,更多的刚果红分子获得能量与RM-ZnO-2表面活性位点相接触[23-24];温度升高会增加结合位点数,可以吸附更多刚果红分子[23];升温可能会使RM-ZnO-2内部产生膨胀效应,有利于大的刚果红分子更好地渗透到颗粒内部。一般来说,放热过程意味着存在物理反应或化学反应,而吸热过程则归因于化学反应[25]。RM-ZnO-2对刚果红的吸附过程中吸热,说明吸附过程中存在化学吸附反应。
由表2看出,不同温度下,Langmuir模型的相关系数均大于Freundlich模型的相关系数。由此得出,RM-ZnO-2对刚果红的吸附过程更符合Langmuir等温吸附模型,说明吸附过程为均匀单层吸附,吸附位点之间没有相互作用。这与前面的结论一致。
2.6 吸附机制分析
吸附过程受溶液pH影响,可以推测,吸附过程中存在静电相互作用,可能是刚果红上去质子化的磺酸基和RM-ZnO上质子化后的氧原子产生了静电吸引,也就是存在物理吸附;而由FT-IR分析结果可知,RM-ZnO上的锌原子可能与刚果红上的磺酸基团发生配位效应,即存在化学吸附;动力学分析结果表明,准二级动力学模型对该吸附过程拟合的更好,说明吸附过程以化学吸附为主、物理吸附为辅。除此之外,可能还存在微弱的氢键作用,如偶极—偶极氢键和吉田氢键[18],如图8所示,其中,M指吸附剂中的金属原子。
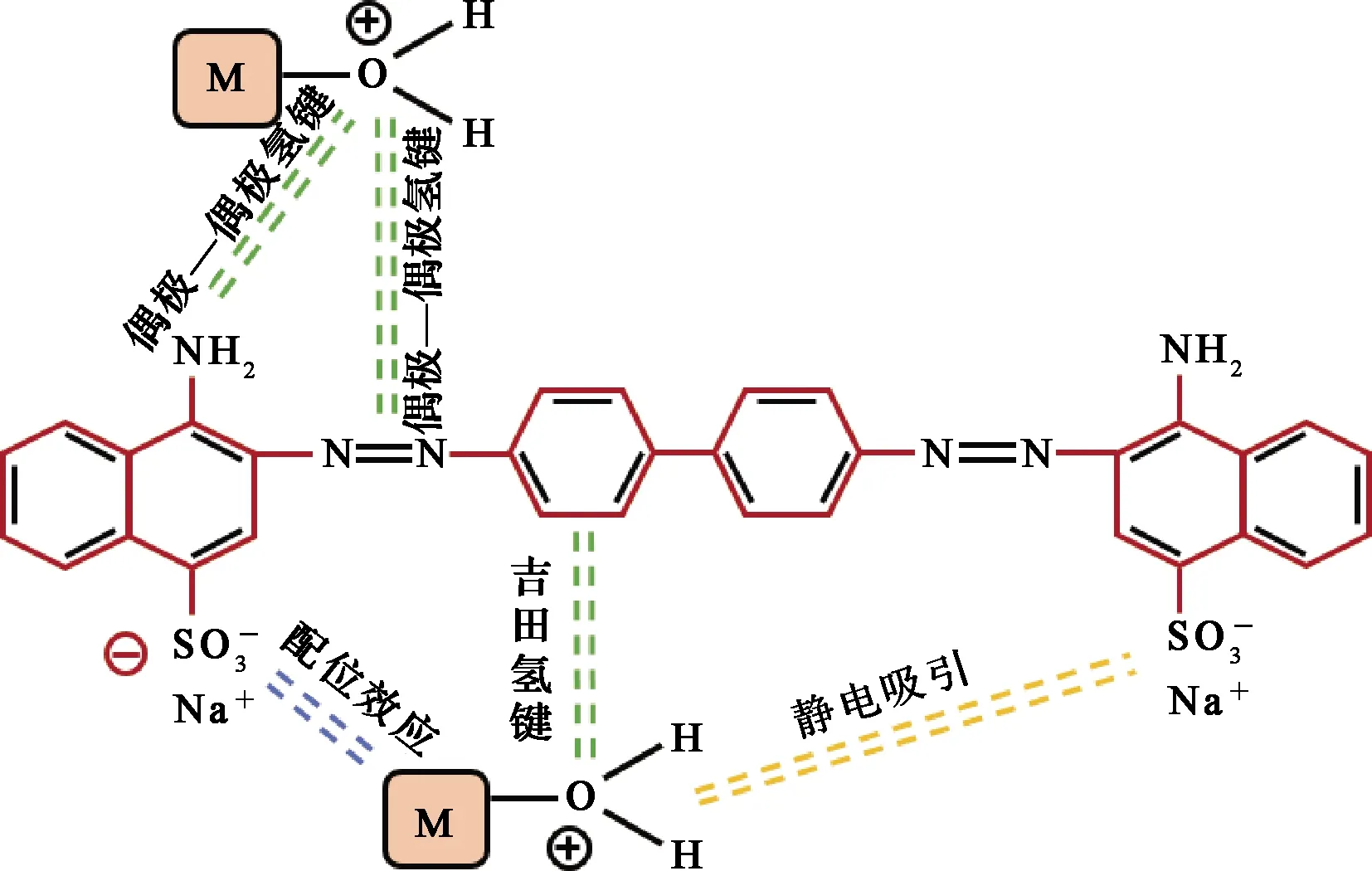
图8 吸附机制示意
3 结论
常温、中性条件下,RM-ZnO对溶液中的刚果红有较好的吸附去除效果,平衡吸附量为305.17 mg/g,吸附效果优于纯ZnO的吸附效果;且碱性赤泥是一种工业废弃物,价廉易得,用其制备吸附剂可以实现以废治废并很好地用于染料废水的处理。
RM-ZnO对刚果红的吸附过程涉及2个阶段:第1阶段为边界层扩散阶段,因为RM-ZnO表面有大量吸附位点,对刚果红分子吸附速度较快,此阶段主要为物理吸附协同化学吸附;第2阶段为颗粒内扩散阶段,刚果红分子进入RM-ZnO颗粒内部,此时吸附过程缓慢且吸附速率受颗粒内扩散和化学作用控制。总体上,吸附反应以化学吸附为主、物理吸附为辅;刚果红上的磺酸基和RM-ZnO上的锌原子发生配位,刚果红上去质子化的磺酸基和RM-ZnO上质子化后的氧原子产生静电引力,进而实现吸附。

