石杉碱甲二元醇质体温敏凝胶大鼠鼻腔给药药动学及脑靶向性研究
陈筱瑜, 冯连晶, 黄庆德*, 冯玉天娇
(1.福建卫生职业技术学院药学院,福建 福州 350101;2.福建中医药大学药学院,福建 福州 350122)
石杉碱甲是从民间草药千层塔(蛇足石杉)中分离得到的一种石松类生物碱,为有效的、竞争性的、可逆性的乙酰胆碱酯酶(AChE)抑制剂[1],常用于增强阿尔茨海默患者记忆功能[2-3],目前上市的相关制剂有片剂、胶囊剂、注射剂(肌内),但它们均缺乏脑选择性,导致其不良反应发生会随剂量增大而增加。鼻腔给药是目前比较理想的脑靶向给药途径,其特点是吸收快,生物利用度高,可避免首过效应,而且使用方便[4-6]。
醇质体由磷脂(2%~5%)、乙醇(20%~50%)、水组成,是一种多层囊泡结构,其双分子层流动性较高,易于变形可穿透皮肤(黏膜)屏障。宋艳丽等[7]将栀子苷制成醇质体,发现它对猪鼻腔黏膜的单位面积渗透量是普通脂质体的2.17倍,水溶液的11.03倍,而且基本无鼻黏膜纤毛毒性。二元醇质体是用混合醇(乙醇、丙二醇)替换醇质体中的乙醇,与普通醇质体比较可减少了乙醇用量,防止药物泄露,避免醇质体的聚集,增加制剂稳定性,降低对皮肤(黏膜)刺激性,在一定程度上也增加了药物透皮(黏膜)吸收效果[8-10]。本实验在前期报道的基础上,制备石杉碱甲二元醇质体温敏凝胶及石杉碱甲温敏凝胶,对其大鼠鼻腔给药药动学及脑靶向性进行初步研究,评价二元醇质体技术对该成分鼻腔给药生物利用度及脑靶向性的影响,以期为该剂型今后开发利用提供实验数据。
1 材料
1.1 仪器 ACQUITY UPLC®TOD system超高效液相串联质谱仪、ACQUITY UPLC®BEH C18超高效液相色谱柱(美国Waters公司);MPLR-702恒温磁力搅拌器(常州市金坛大地自动化仪器厂);BT100-1F蠕动泵(保定兰格恒流泵有限公司);FA2004N电子天平(万分之一,上海精密科学仪器有限公司);XS205电子天平[十万分之一,梅特勒-托利多仪器(上海)有限公司];Centrifuge 5418高速离心机(德国Eppendorf公司);VXH-3微型涡旋混合器(上海跃进医疗器械厂);HAC-20-034浓缩氮吹仪(天津市恒奥科技发展有限公司)。
1.2 试剂与药物 石杉碱甲对照品(上海源叶生物科技有限公司,批号H29D8J51963,纯度≥98%);石杉碱甲原料药(西安普莱特生物工程有限公司,批号HA20191102,纯度99%)。大豆卵磷脂[艾伟拓(上海)医药科技有限公司,批号SY-SI-190602];吐温-80(上海源叶生物科技有限公司,批号Z17D9Y77731);泊洛沙姆407(批号GNC21922B)、泊洛沙姆188(批号GNC10821B)(德国BASF公司)。石杉碱甲注射剂(海南灵康制药有限公司,批号200601102);苯海拉明对照品(上海至吉生化科技有限公司,批号B111310D5);乌拉坦(合肥巴斯夫生物科技有限公司,批号BSF200509)。乙酸乙酯(分析纯,四川西陇科学有限公司);生理盐水(江西科伦药业有限公司,批号B20050701);甲酸、水、甲醇(色谱纯,德国Merck公司)。
1.3 动物 SD大鼠,清洁级,雄性,体质量(200±20)g,购于吴氏实验动物贸易有限公司,动物生产许可证号SCXK(闵)2016-0002,饲养条件为温度(22±2)℃、相对湿度(50±5)%,保持室内自然通风,自由饮食进水,实验前在上述环境下适应7 d。清洁级医学实验动物环境设施由福建中医药大学动物中心提供。
2 方法与结果
2.1 石杉碱甲二元醇质体温敏凝胶制备 量取22.5 mL二元醇相(乙醇-丙二醇=1∶1),置于锥形瓶中,加入50 mg石杉碱甲、1.8 g大豆卵磷脂、0.15 g聚山梨酯-80,密闭搅拌20 min至完全溶解,在温度30 ℃、搅拌速度700 r/min条件下,将27.5 mL超纯水以1 mL/min速度缓慢加到二元醇相中,持续搅拌90 min至室温,得到二元醇质体[平均包封率为(94.05±0.22)%,平均粒径为(260.1±5.7)nm,Zeta电位为(-20.9±0.3)mV]。称取11.5 g P-407、2.5 g P-188,置于烧杯中,加入50 mL纯化水使其完全润湿,置于4 ℃冰箱中,得到澄清、无团块、分散均匀的空白温敏凝胶溶液,将其置于烧杯中,放入冰水浴,加入等量二元醇质体,搅拌20 min即得,在4 ℃下保存。同法制备石杉碱甲温敏凝胶(不加二元醇质体,改加石杉碱甲溶液)。该制剂外观为乳白色黏稠液体,具有一定流动性;当升温至胶凝温度时,二元醇质体温敏凝胶发生胶凝,呈凝胶状,不具有流动性,pH值为7.01±0.04,少量2%磷钨酸负染后在透射电子显微镜下观察其形态,见图1,可知其形态规整,呈球形或类球形。

图1 石杉碱甲二元醇质体温敏凝胶透射电镜图(×50 000)Fig.1 Transmission electron microscopic image for ther-mosensitive gel binary ethosomes of huperzine A(×50 000)
2.2 UPLC-MS/MS测定大鼠血浆及脑组织中石杉碱甲含量 参考文献[11-13]报道。
2.2.1 色谱条件 ACQUITY UPLC®BEH C18色谱柱(100 mm×2.1 mm,1.7 μm);流动相水(含0.1%甲酸)-甲醇,梯度洗脱(0~1.5 min,52∶48;1.5~3.0 min,52∶48~25∶75;3.0~3.1 min,25∶75~52∶48;3.1~5.0 min,52∶48);体积流量0.3 mL/min;柱温45 ℃;进样量2 μL。
2.2.2 质谱条件 离子模式ESI+;扫描模式MRM;离子源温度150 ℃;去溶剂温度500 ℃;锥孔气体积流量150 L/h;去溶剂气体积流量800 L/h;碰撞气体积流量0.25 mL/min;石杉碱甲m/z243.33~134.15,内标(苯海拉明)m/z256.17~167.20;锥孔电压石杉碱甲30 V,内标30 V;碰撞能量石杉碱甲25 V,内标18 V。
2.2.3 空白血浆、脑组织溶液制备 大鼠禁食不禁水12 h,腹腔注射20%乌拉坦(0.7 mL/100 g)麻醉,腹主动脉取血,置于肝素钠抗凝的EP管中,4 000 r/min离心15 min后分离得到血浆,在-20 ℃下冷冻保存备用。取血后大鼠立即处死,断头,剪开头盖骨,取出脑组织,去除血管,吸干表面血液并用生理盐水冲洗,精密称定质量后置于匀浆器中,加入生理盐水(2 mL/g)匀浆5 min,4 000 r/min离心15 min,取上清液,在-20 ℃下冷冻保存。
2.2.4 对照品、内标溶液制备 精密称取石杉碱甲对照品、内标适量,置于50 mL量瓶中,50%甲醇溶解稀释,即得(质量浓度分别为46、50 μg/mL),置于4 ℃冰箱中保存备用。
2.2.5 样品前处理
2.2.5.1 血浆 取大鼠血浆100 μL,精密加入100 μL内标溶液,混匀,加入3 mL乙酸乙酯,涡旋混合2 min,4 000 r/min离心15 min,取上层有机相至另一试管中,40 ℃氮气吹干,残留物加入100 μL 50%甲醇复溶,涡旋混合,14 000 r/min离心10 min,取上清液,即得。
2.2.5.2 脑组织 取大鼠脑组织上清液100 μL,精密加入100 μL内标溶液,混匀,加入3 mL乙酸乙酯,涡旋混合2 min,4 000 r/min离心15 min,取上层有机相至另一试管中,40 ℃氮气吹干,残留物加入100 μL 50%甲醇复溶,涡旋混合,14 000 r/min离心10 min,取上清液,即得。
2.2.6 专属性试验 取空白血浆或脑组织、空白血浆或脑组织+对照品+内标、给药后血浆或脑组织+内标适量,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定,结果见图2。由此可知,空白血浆、脑组织中的内源性物质不干扰测定,表明该方法专属性良好。
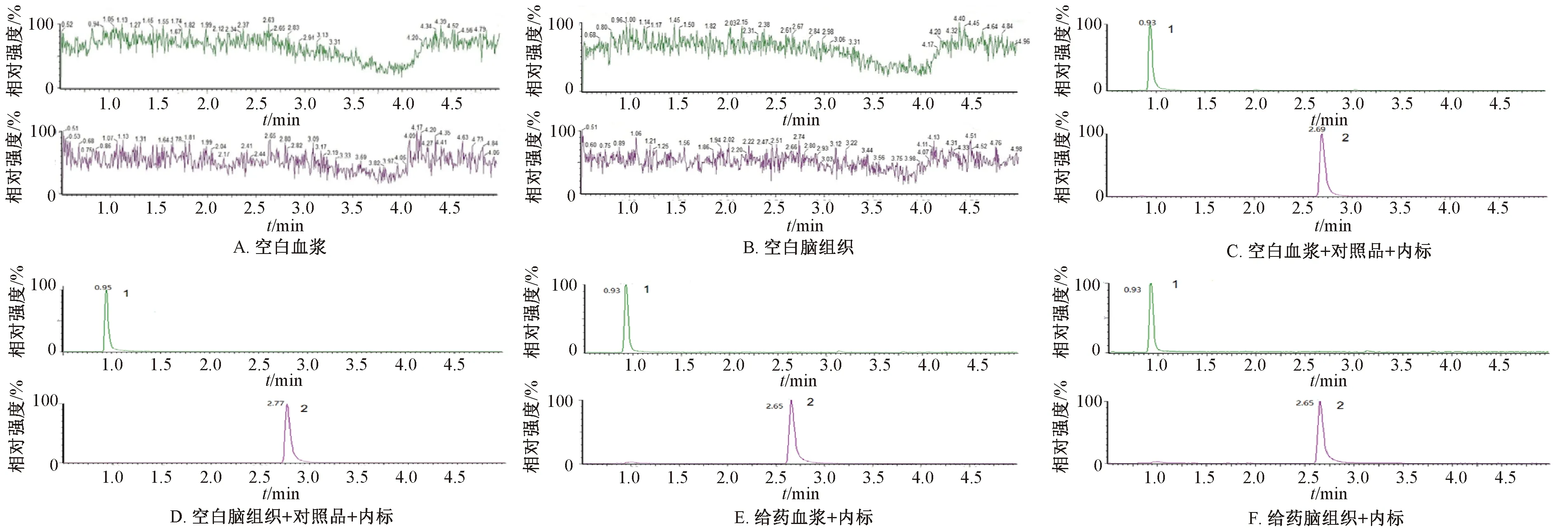
1.石杉碱甲 2.内标(苯海拉明)1.huperzine A 2.internal standard (diphenhydramine)图2 石杉碱甲MRM色谱图Fig.2 MRM chromatograms of huperzine A
2.2.7 线性关系考察 精密吸取石杉碱甲对照品溶液适量,50%甲醇稀释至0.023、0.575、5.75、23、69、138、230、253 ng/mL,分别精密吸取100 μL至EP管中,氮气吹干,加入500 μL空白血浆或脑组织,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定。以石杉碱甲质量浓度为横坐标(X),石杉碱甲、内标峰面积比值为纵坐标(Y)进行回归,得石杉碱甲在大鼠血浆、脑组织中的方程分别为Y=0.008 8X+0.014(R2=0.999 4)、Y=0.009 2X-0.045 2(R2=0.997 8),分别在0.023~253、0.023~230 ng/mL范围内呈良好的线性关系,定量限为0.023 ng/mL。
2.2.8 精密度试验 精密吸取“2.2.7”项下5.75、23、69 ng/mL对照品溶液各5份,每份100 μL,置于EP管中,氮气吹干,加入500 μL大鼠空白血浆或脑组织混匀,按“2.2.5”项下方法处理,同一天在“2.2.1”“2.2.2”项条件下进样测定6次,测得日内精密度RSD分别为1.56%~3.04%、2.03%~3.53%;连续5 d,测得日间精密度RSD分别为2.57%~4.08%、2.57%~5.24%,符合生物样品测定要求。
2.2.9 稳定性试验 精密吸取“2.2.7”项下5.75、23、69 ng/mL对照品溶液各100 μL,置于EP管中,氮气吹干,加入500 μL大鼠空白血浆或脑组织混匀,室温放置24 h,分别在-20 ℃冰箱中放置7 d、1周内反复冻融3次,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定。结果,血浆、脑组织在不同条件下石杉碱甲含量RSD分别小于5.0%、6.0%,表明血浆、脑组织样品稳定性良好。
2.2.10 方法回收率试验 精密吸取“2.2.7”项下5.75、23、69 ng/mL对照品溶液各5份,每份100 μL,置于EP管中,氮气吹干,加入500 μL大鼠空白血浆或脑组织混匀,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定,测得实测浓度,计算方法回收率。结果,血浆方法回收率分别为98.43%、93.42%、93.43%,RSD分别为12.83%、4.75%、1.82%;脑组织方法回收率分别为100.13%、109.13%、96.58%,RSD分别为6.07%、4.64%、2.14%,均符合相关要求。
2.2.11 提取回收率试验 精密吸取“2.2.7”项下5.75、23、69 ng/mL对照品溶液各5份,每份100 μL,置于EP管中,氮气吹干,加入500 μL大鼠空白血浆或脑组织混匀,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定,计算石杉碱甲、内标峰面积比值A;以甲醇代替空白血浆或脑组织,同法制备质量浓度相同的对照品溶液,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定,计算石杉碱甲、内标峰面积比值B,计算提取回收率,公式为提取回收率=(A/B)×100%。结果,血浆提取回收率分别为95.88%、92.20%、90.86%,RSD分别为4.63%、0.37%、4.04%;脑组织提取回收率分别为98.23%、108.10%、93.94%,RSD分别为2.18%、8.40%、2.24%,均符合相关要求。
2.2.12 基质效应 精密吸取“2.2.7”项下5.75、23、69 ng/mL对照品溶液及内标溶液各5份,每份100 μL,按“2.2.5”项下方法处理,在“2.2.1”“2.2.2”项条件下进样测定,计算石杉碱甲含量C;取大鼠空白血浆或脑组织100 μL,按“2.2.5”项下方法处理,将上述质量浓度的对照品、内标溶液加到处理好的上清液中,40 ℃氮气吹干,残留物加入100 μL 50%甲醇复溶,涡旋混合,14 000 r/min离心5 min,取20 μL上清液,在“2.2.1”“2.2.2”项条件下进样测定,计算石杉碱甲含量D,计算基质效应,公式为基质效应=(D/C)×100%。结果,基质效应为90.92%~102.17%。
2.3 鼻腔给药药动学与脑靶向性研究
2.3.1 分组、给药与采血 155只大鼠随机分为3组,其中鼻腔给药组(二元醇质体温敏凝胶、温敏凝胶)各50只,静脉给药组(石杉碱甲注射剂)55只,给药前12 h禁食不禁水。
鼻腔给药组大鼠腹腔注射20%乌拉坦(0.7 mL/100 g)麻醉,仰卧,固定头部和四肢,打开颈部,暴露食管,结扎食道以防止药液流失,采用平头微量注射器分别鼻腔给药二元醇质体温敏凝胶、温敏凝胶各60 μL(含石杉碱甲30 μg),给药后立即捏住鼻子以确保温敏凝胶快速胶凝,于给药后5、15、30、45 min及1.0、2.0、4.0、8.0、12.0、24.0 h,按“2.2.3”项下方法采集血浆、脑组织,按“2.2.5”项下方法处理,待测。
静脉给药组大鼠腹腔注射20%乌拉坦(0.7 mL/100 g)麻醉后,尾静脉注射石杉碱甲注射剂(200 μg/mL)0.15 mL,于给药后2、5、15、30、45 min及1.0、2.0、4.0、8.0、12.0、24.0 h,按“2.2.3”项下方法采集血浆、脑组织,按“2.2.5”项下方法处理。

3 结果
大鼠血浆、脑组织中石杉碱甲浓度-时间曲线分别见图3~4,主要药动学参数见表1,脑靶向性评价结果见表2。由此可知,二元醇质体温敏凝胶鼻腔给药后脑组织AUC0~t分别是温敏凝胶鼻腔、静脉给药的1.36、1.24倍,差异具有统计学意义(P<0.01),其DTE、DTP分别比后者高24.45%、16.77%,其中前者为133.58%,即具有一定的脑靶向性。
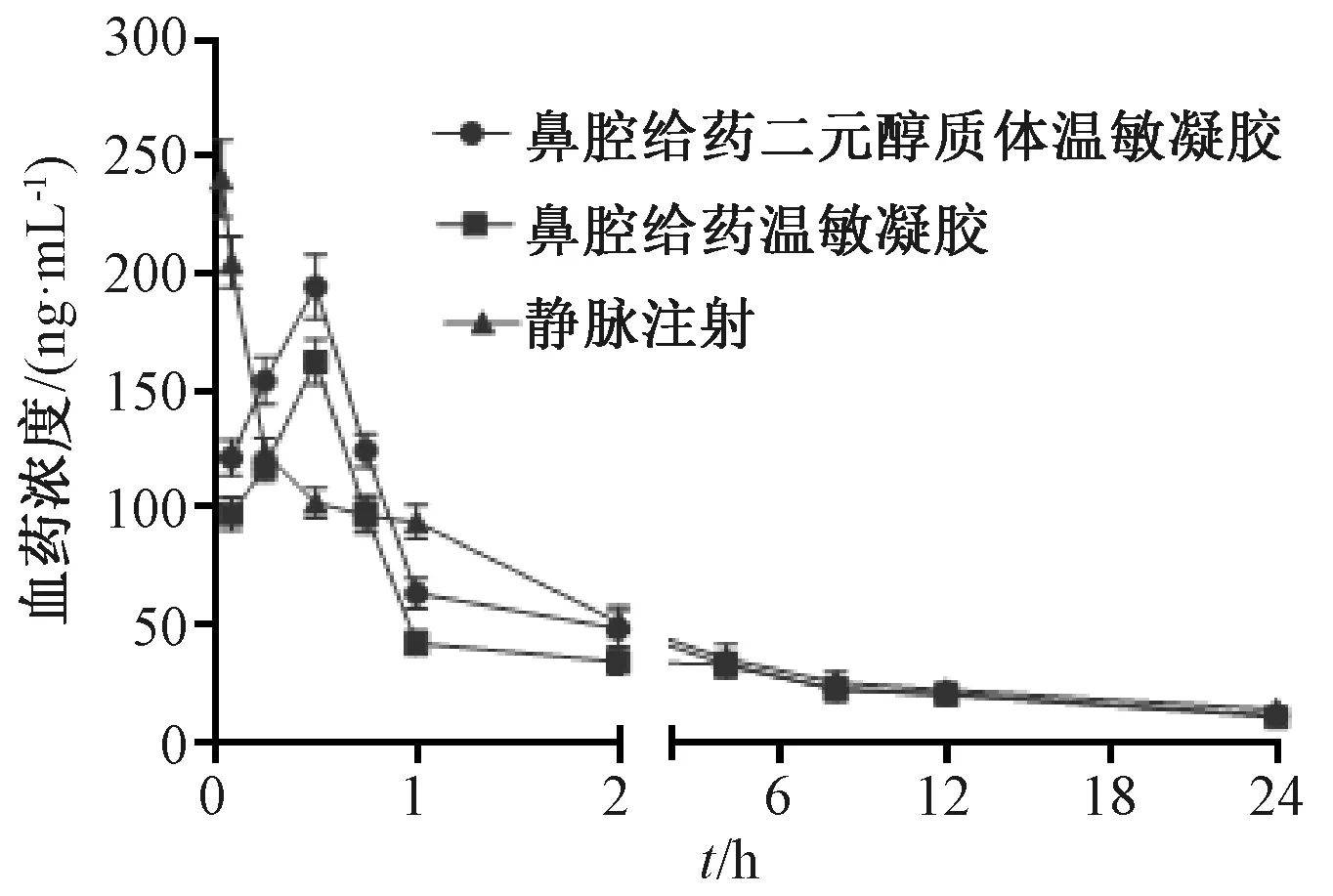
图3 大鼠血浆中石杉碱甲浓度-时间曲线(n=5)Fig.3 Concentration-time curves for huperzine A in rat plasma(n=5)
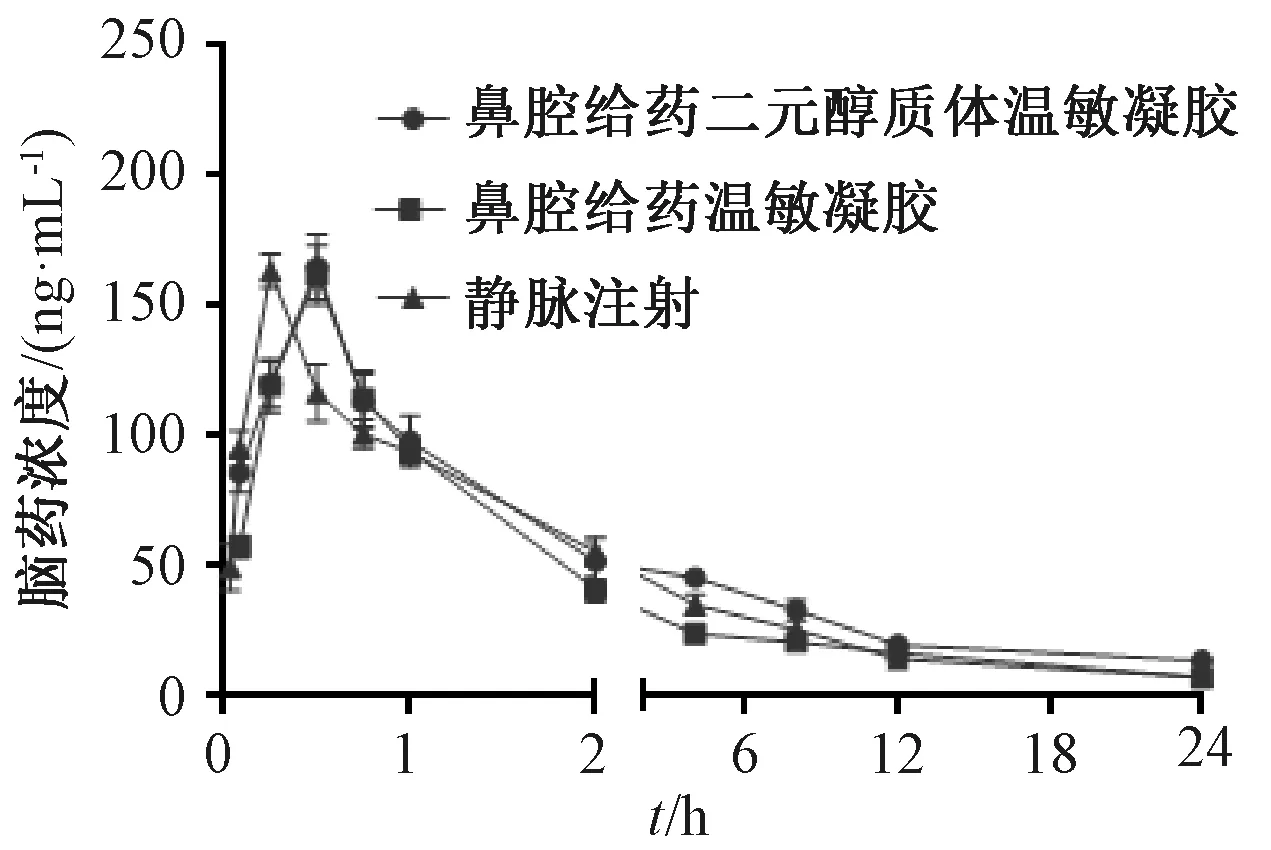
图4 大鼠脑组织中石杉碱甲浓度-时间曲线(n=5)Fig.4 Concentration-time curves for huperzine A in rat brain tissue(n=5)
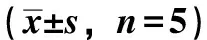
表1 石杉碱甲主要药动学参数
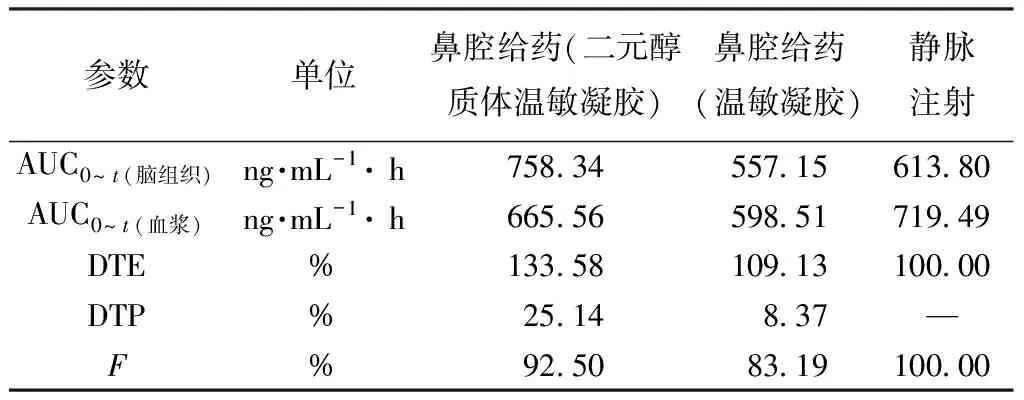
表2 石杉碱甲脑靶向性评价结果
4 讨论
通过比较鼻腔给药与静脉给药的AUCbrain/AUCplasma值可初步判断药物脑靶向性[16],如果无鼻-脑通路,则前者该数值应小于后者,本实验发现,石杉碱甲二元醇质体温敏凝胶及其温敏凝胶药物鼻腔给药后该数值分别为1.14、0.93,均大于静脉给药的0.85,表示药物经鼻腔给药具有一定脑靶向性;石杉碱甲二元醇质体温敏凝胶鼻腔给药在脑组织中的AUC0~t、MRT0~t显著高于其温敏凝胶鼻腔给药、注射剂静脉给药,表明其平均滞留时间更长;石杉碱甲二元醇质体温敏凝胶鼻腔给药后DTE、DTP均大于其温敏凝胶,表明该剂型可增加经鼻给药脑靶向性,但程度并不明显。文献[17]报道,石杉碱甲脂溶性(表观油/水分配系数)取决于介质的pH,在pH≥6.5时较强,由于温敏凝胶pH为7.0,故在鼻腔环境条件下该成分具有较强的脂溶性,可获得良好的鼻腔黏膜吸收,它通过鼻腔黏膜吸收进入血液循环后,再透过血脑屏障而进入脑组织比例较大,而通过鼻-脑通路吸收进入脑组织的药物所占比例则变小,可能是导致其DTE、DTP数值增加程度不大的原因。
研究表明,不易吸收的药物(如蛋白质、多肽等)鼻腔给药后,更易表现出脑靶向性[18]。本实验虽然未设置灌胃给药组,但文献[19]报道,石杉碱甲原位凝胶鼻腔给药后脑组织AUC0~6 h分别为同剂量静脉注射、灌胃给药的1.3、2.3倍,tmax较灌胃给药明显缩短,表明石杉碱甲鼻腔给药的脑靶向性强于口服给药。
5 结论
本实验研究了石杉碱甲二元醇质体温敏凝胶及其温敏凝胶经大鼠鼻腔给药后的体内药动学,并对其脑靶向性进行评价。结果表明,二元醇质体温敏凝胶脑靶向性效果更优,表明将石杉碱甲制成该剂型后可增加其经鼻给药脑靶向性。

