二氟双草酸磷酸锂的合成及其与石墨半电池的适配性研究
王 洁,蔡海峰,宋林虎,王 鹏,张宁霜,李世友*
(1.兰州理工大学 石油化工学院,甘肃 兰州 730050;2.甘肃省低碳能源化工重点实验室,甘肃 兰州 730050;3.甘肃省锂离子电池电解液材料工程实验室,甘肃 兰州 730050)
六氟磷酸锂(LiPF6)是当前锂离子电池中应用最为广泛的锂盐,其主要制备方法有气固反应法、有机溶剂法、离子交换法和氟化氢溶剂法[1]。目前国内外主要采用氟化氢溶剂法制备LiPF6,此工艺是将LiF4溶于无水氟化氢中制备出均相LiF4溶液,再将PF5气体引入到LiF4溶液中,PF5与LiF4反应生成LiPF6。该方法反应容易发生,可大规模生产,是目前比较成熟的LiPF6生产工艺路线[2]。LiPF6在有水或高温的情况下容易发生分解,从而影响产品的纯度,因此在LiPF6的生产工艺中,对设备及反应条件的控制较为严格。
由于传统工艺中HF 存在危险性,部分企业和科研机构已经开始了对以气固反应法、有机溶剂法为主的工艺技术路线的研究,以满足绿色化工的发展要求[3]。对于LiPF6的研究重点已经转移到了新型合成工艺路线的研发,以满足我国锂离子电池行业发展需求[4]。
二氟双草酸磷酸锂(LiDFBOP)是一种新型锂盐,其作为电解液的添加剂,能够有效改善电池正负极表面的钝化膜结构,提升LiPF6电解液在高温循环中的稳定性[5-8]。目前,二氟双草酸磷酸锂的开发处于科研探索阶段,其研究能够推动国内锂电新能源产业的发展[9]。本研究首先合成了LiDFBOP,并对其在石墨半电池中的应用进行研究。
1 实验部分
所用试剂纯度均为电池级,除特别注明外均未作进一步处理。
1.1 LiDFBOP 的合成
(1)在手套箱内称取30 g 双(三甲基硅)草酸酯和20 g LiPF6于两口烧瓶中,加入80 mL 碳酸酯,在手套箱里密封取出[10];
(2) 将两口烧瓶的两口分别加上干燥装置和液封装置,置于油浴锅中反应,油浴温度为75 ℃,反应时间为27 h。
(3)将充分反应的液体过滤,滤液用二氯甲烷进行重结晶、减压过滤,得到白色固体LiDFBOP。
1.2 合成产品LiDFBOP 的纯度滴定
(1)KMnO4溶液标定时通常使用草酸(H2C2O4)为基准,KMnO4和H2C2O4的反应方程式如下:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2+8H2O
滴定时的温度可以控制在70 ℃~80 ℃,不应该低于60 ℃。否则反应过程中的速度会很慢,但若温度过高,草酸会被分解。
(2)称取1.6 g KMnO4固体,置于500 mL 烧杯中,加入蒸馏水500 mL 溶解。加热到沸腾并保持15 min,随时添加蒸馏水补充至500 mL。冷却后,于暗处停留数天(最多为2~3 d),再使用微孔玻璃漏斗或玻璃棉过滤,以去除MnO2沉淀。将滤液存于干净的褐色瓶中,摇匀。
(3) 准确称取在130 ℃烘干的Na2C2O40.15~0.20 g,置于250 mL 锥形瓶中,加入蒸馏水40 mL及3 mol·L-1的H2SO410 mL,加热到75 ℃~80 ℃,立刻使用待标定的KMnO4溶液将其滴定到溶液显示出粉红色,并且30 s 内不发生褪色,即为滴定终点。
(4)根据称取Na2C2O4的品质及耗用KMnO4溶液的体积,计算出KMnO4标准水溶液中的浓度。
(5)通过三次平行滴定,经计算可知产品纯度为95.79%。
1.3 LiDFBOP 的表征分析
图1和图2分别是合成LiDFBOP的核磁共振19F谱和31P谱图。图1中,在峰位约为-61ppm和-59 ppm时,出现了目标产品LiDFBOP 的特征峰,峰位约为-81 ppm 时出现了杂质峰。图2 中,在峰位约为-146 ppm、-142 ppm 和-138 ppm 时,出现了目标产品LiDFBOP 的特征峰,峰位约为-16 ppm 时出现了杂质峰,主要杂质为四氟草酸磷酸锂。
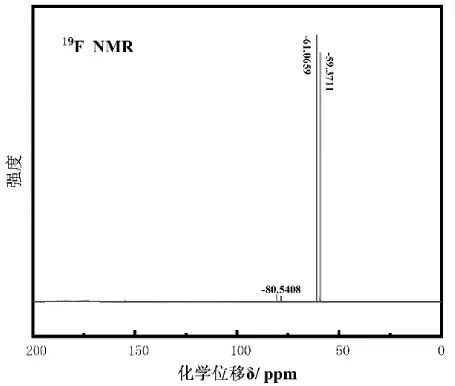
图1 合成LiDFBOP 的核磁19F 谱图表征
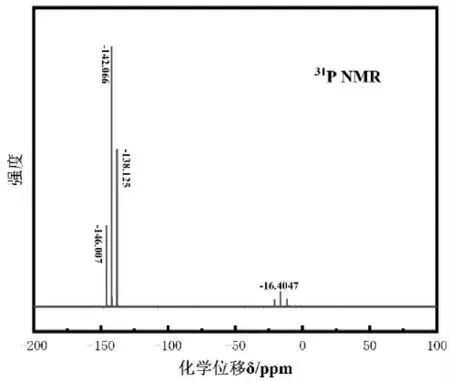
图2 合成LiDFBOP 的核磁31P 谱图表征
1.4 电解液的配制
在本实验中,将制备的高纯度LiDFBOP 作为添加剂以及主盐分别配制电解液,以测定加入LiDFBOP 后对负极电化学性能的改善作用,并研究LiDFBOP 作为电解液主盐在高温环境的性能。
电解液的配制是本次实验极其重要的一部分,具体的配制步骤为:用1 mol/L 的LiPF6-EC/DEC(体积比1:1)的电解液作为标准,并将其标记为STD。待充满氩气的手套箱中的水、氧含量均控制在0.1 ppm 以下,将合成的LiDFBOP 作为添加剂按1 wt%加入STD 电解液中,标记为STD+LiDFBOP。其次将合成的LiDFBOP 作为主盐添加到EC/DEC(体积比1:1)溶剂中,配制为1 mol/L的LiDFBOP-EC/DEC 电解液体系,标记为LiDFBOP-EC/DEC。
1.5 电化学性能测试
电池的循环性能采用CT2001A 型电池测试仪(武汉市蓝电电子有限公司)进行测试,本次测试充放电的电压范围为0~2 V[11]。其他电化学测试均在电化学工作站上进行[12-13]。
2 结果与讨论
2.1 电导率性能测试
图3 表示在25 ℃和55 ℃下STD 电解液、LiDFBOP-EC/DEC 电解液和STD+LiDFBOP 电解液的离子电导率。由图3 可知,在25 ℃和55 ℃下,LiDFBOP 作为主盐时电解液的电导率较低,分别为4.9 mS·cm-1和6.5 mS·cm-1;LiDFBOP 作为添加剂的电解液离子电导率较高,分别为5.8 mS·cm-1和7.8 mS·cm-1。说明LiDFBOP 作为添加剂时电解液的离子电导率得到了提升,而LiDFBOP 作为主盐的电解液电导率与STD 电解液相比较差。

图3 25 ℃与55 ℃下三种电解液的离子电导率
2.2 电化学性能测试
图4 为STD 电解液、LiDFBOP-EC/DEC 电解液和STD+LiDFBOP 电解液首次循环充放电曲线。由图4 可知,LiDFBOP-EC/DEC 电解液的首次放电比容量为602.8 mAh·g-1,充电比容量为318.7 mAh·g-1;STD 电解液的首次放电比容量为528.5mAh·g-1,充电比容量为348.2 mAh·g-1;LiDFBOP 作为添加剂的电解液的首次放电比容量为574.5 mAh·g-1,充电比容量为327.5 mAh·g-1;即LiDFBOP-EC/DEC 电解液的首效为52.82%,STD 电解液的首效为65.91%,STD+LiDFBOP 电解液的首效为60.12%。也可以看出在高温(55 ℃)环境下LiDFBOP 的嵌锂电位较高(2.3 V 左右),LiDFBOP 作为添加剂和LiPF6电解液的嵌锂电位较低(1 V 左右)。

图4 三种电解液体系在高温环境下的首次充放电曲线
图5 是在55 ℃高温环境下三种电解液前100周循环的比容量,在倍率为1.0 C 的情况下,STD电解液的比容量明显低于STD+LiDFBOP 电解液的比容量,但高于LiDFBOP-EC/DEC 电解液的比容量。STD+LiDFBOP、STD 和LiDFBOP-EC/DEC体系在1.0 C 首周比容量分别为331.6 mAh·g-1、315.8 mAh·g-1和276.9 mAh·g-1,经过循环100 周后分别为324.2 mAh·g-1、305.17 mAh·g-1和266.8 mAh·g-1,其容量的保持率分别为97.77%、97.25%和96.35%。表明含有LiDFBOP 添加剂的电解液在高温循环性能方面要优于标准LiPF6电解液和LiDFBOP 主盐体系的电解液。
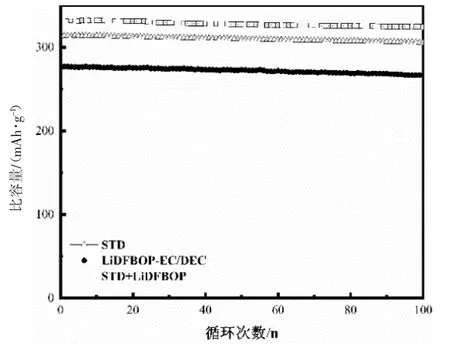
图5 三种电解液100 周循环的比容量
图6 为在55 ℃高温环境下三种电解液前100 周循环的库仑效率曲线图(1.0 C 倍率)。从图6 可以看出,三种电解液首周的循环均没有超过100%,STD+LiDFBOP、STD 和LiDFBOP-EC/DEC体系电解液库仑效率分别为98.96%、98.7%和97.80%。首周循环库仑效率较低的原因是电解液的氧化分解产生一层初始保护膜,随着电池不断循环,SEI 膜自我修复生长,电解液的氧化分解也逐渐被抑制。在经历了几个循环之后,三种不同电解液组成的半电池的库仑效率逐渐接近100%。通过对比三种电解液的库仑效率曲线,可以看出LiDFBOP-EC/DEC 体系电解液的库仑效率在不同的循环次数下波动最大,STD 体系次之,STD+LiDFBOP 体系的波动较小,在循环的过程中其库仑效率的稳定性也更为优良。通过对比,表明在高温环境下STD+LiDFBOP 体系比STD 体系锂离子电池的库仑效率更加稳定,而STD 体系要比LiDFBOP-EC/DEC 体系更优。

图6 三种电解液100 周循环的库仑效率
图7 是三种电解液在高温下的平台比容量随放电电流变化的倍率性能。含有三个体系电解液的电池在不同倍率下均循环5 次,循环倍率分别为0.1 C、0.2 C、0.5 C、1.0 C、2.0 C 和5.0 C,再调回到0.2 C。从图7 中可以看出,LiDFBOP-EC/DEC 电解液的容量低于标准STD 电解液的容量,而STD+LiDFBOP 电解液容量要高于STD 体系。并且在提高电流时,可以看到STD 电解液的容量衰减程度也要高于STD+LiDFBOP 电解液,低于LiDFBOP-EC/DEC 电解液。当将各个电池的倍率都从5.0 C 调回0.2 C 后,STD+LiDFBOP、STD 和LiDFBOP-EC/DEC 体系的电池容量分别回到初始0.2 C 的99.1%、98.2%和98.8%。由此可以看出,在高温环境下LiDFBOP 作添加剂不仅提高了电池容量,还能够稳定电极体系,提高了Li+的扩散速度。

图7 三种电解液在不同倍率下的比容量
图8 和图9 是在电化学工作站下测得的三种电解液所组装的电池在循环100 个周期后的交流阻抗谱图。交流阻抗谱图主要由高频区的半圆与低频区的斜线组成,在高频区,半圆部分主要代表锂离子在电极面的转移,中频区的半圆表示电荷转移的过程,位于低频区的斜线则表示锂离子从电解液中扩散到锂离子电池材料内部的过程。从图8 可以看出,在高频区,LiDFBOP-EC/DEC 体系电解液的半圆最大,STD+LiDFBOP 体系电解液的半圆最小。即LiDFBOP-EC/DEC 体系电解液的阻抗最大,锂离子在电解液中扩散通过SEI 膜的迁移最差;STD+LiDFBOP 体系电解液的阻抗最小,锂离子在电解液中扩散通过SEI 膜的迁移最好。从图9 可以看出,100 个循环后,高频区的半圆较循环前的半圆小,即循环后锂离子在电解液中扩散通过SEI 膜的迁移变得更加稳定。则STD+LiDFBOP 的电解液构成的半电池性能表现更加稳定,锂离子的扩散速率得到很大的提升,导电性能增加,电解液的电阻降低,而LiDFBOP-EC/DEC体系电解液在这些方面较差。

图8 三种电解液在循环前的交流阻抗谱图

图9 三种电解液在100 个循环后的交流阻抗谱图
2.3 极片表征
图10 是天然石墨在不同放大倍数下的扫描电镜图片。其中,图10(a)~(a2)是在LiDFBOPEC/DEC 电解液体系循环后的电池极片,在放大1000 倍时,其表面形貌存在较多的凸起圆球,有较多颗粒;放大至5000~10000 倍后,其粒径分布分散,主要以球形结构为主,比较疏松。图10(b)~(b2)是在标准电解液体系循环后的电池极片,在放大1000 倍时,其表面形貌存在较少的孔隙,表现的排布较为规整;放大至5000~10000 倍后,颗粒分布较为聚集,表面凸起的圆球较少,粒径较小。图10(c)~(c2)是STD+LiDFBOP 电解液体系在循环后的电池极片,在放大1000 倍时,其表面形貌存在少量的孔隙,排布很规整;放大至5000~10000 倍后,也看不出颗粒的存在,只能看到少量凸起的圆球,粒径较为聚集,粒径较为均匀。对比之下,在加入LiDFBOP 作为添加剂后,电池极片表面形貌最为规整,粒径较均匀。

图10 石墨极片在不同电解液中循环后的扫描电镜
3 结论
本文研究了新型锂盐LiDFBOP 的合成,并将合成产品应用于AG/Li 半电池。结果表明,LiDFBOP 作为主盐时,并不能有效提升石墨半电池的高温性能,而其作为添加剂时,能明显改善高温下石墨半电池的循环和倍率性能。通过扫描电镜分析,LiDFBOP 能有效提升界面的稳定性。这为今后LiDFBOP 的应用研究提供了新的思路。

