生物电子等排体双环[1.1.1]戊烷(BCP)在药物设计中的应用
黄 雨,张寅生
(正大天晴药业集团股份有限公司,江苏省抗病毒靶向药物研究重点实验室,南京 211100)
生物电子等排是指将化合物结构中的某些原子或基团,用其外层电子总数相等(同价)或在体积、形状、构象、电子分布、脂水分配系数、pKa,化学反应性和氢键形成能力等重要参数上存在相似性的原子或基团进行替换,从而产生新化合物的一种方法[1]。它是药物结构优化中一种非常有效的策略。随着药物化学和有机化学的发展,越来越多经典和非经典生物电子等排体被运用到新药的设计中,并取得了显著的成果。然而,面对日益狭小的专利保护空间,药物化学家们不得不寻求一些结构新颖的、具有潜在生物活性的生物电子等排体来改善化合物的性质[2]。正是在这样的背景之下,具有三维立体结构的双环[1. 1. 1]戊烷(BCP)因其弱亲脂性、增强电负性等理化性质,备受药物化学家的青睐。为此,本文综述了BCP 在药物设计中的应用,以便于给药物研发人员提供参考。
1 双环[1. 1. 1]戊烷(BCP)在药物设计中的应用
近年来,BCP作为生物电子等排体在药物设计中已经得到了广泛的应用。其应用主要分为3类[3]:(1)作为1,4-二取代苯环的生物电子等排体;(2)作为1,2-二取代炔基的生物电子等排体;(3)作为叔丁基等空间位阻较大的基团的生物电子等排体。其主要作用是改善化合物的溶解度、代谢稳定性及生物活性,同时,可突破专利,当然也可作为新颖的结构片段运用到新药设计中(图1)。
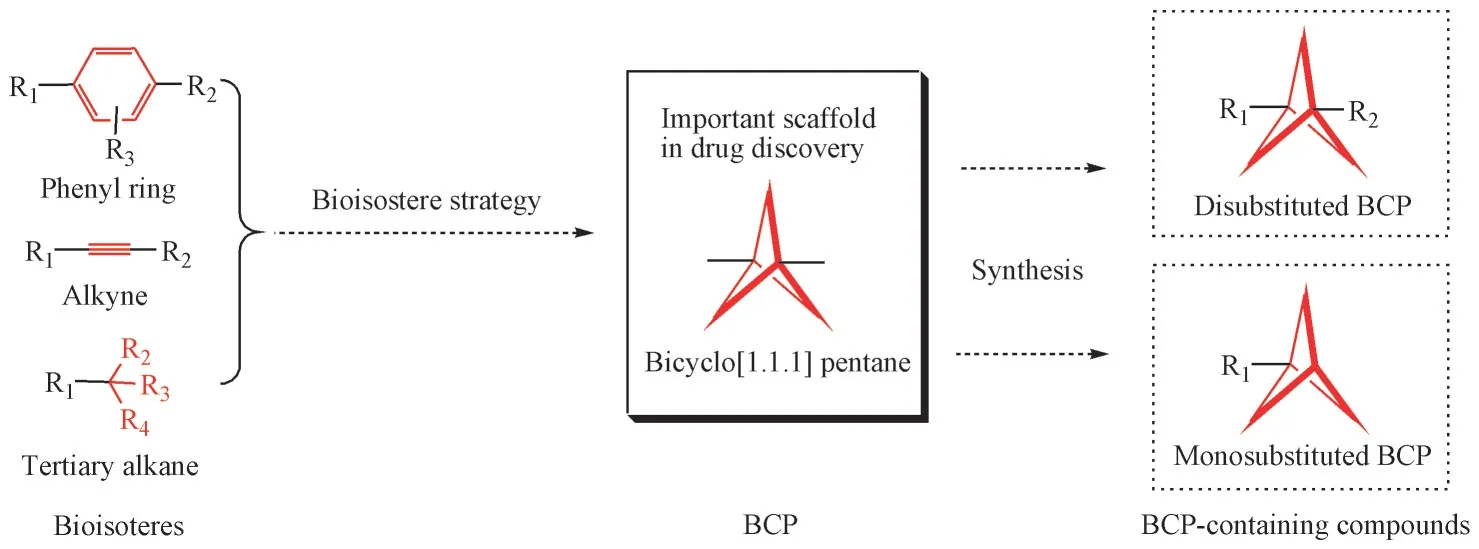
Figure 1 Application and classification of bicyclo [1. 1. 1] pentane (BCP) as a bioisostere in drug design
1. 1 BCP 作为1,4-二取代苯环的生物电子等排体在药物设计中的应用
苯环是有机化学中最基本的结构元素之一,并且广泛的存在于各种生物活性分子及天然产物当中。然而,随着分子结构中苯环数目的增加,其水溶性变差,毒性也随之增加[4]。所以,近年来药物化学家们倾向于以饱和的生物电子等排体来代替苯环,以期获得生物活性更好或者理化性质更佳的药物活性分子[5]。其中,BCP 因其与1,4-二取代的苯环具有很多相似的空间结构特征(图2),在近年来备受关注。
1996 年,Pellicciari 等[6]首次用BCP 代替苯环应用于代谢型谷氨酸受体拮抗剂的结构改造当中(图3)。化合物1 是已知的代谢型谷氨酸受体1选择性拮抗剂,为了探究苯环在该分子中的构效关系,研究者以BCP 替代苯环成功合成了化合物2。活性数据表明BCP 结构的替换,增强了化合物的活性并且保持了其选择性(mGluR1a,IC50= 25 μmol/L;mGluR2,IC50>300 μmol/L;mGluR4a,IC50>300 μmol/L)。

Figure 2 Comparison between BCP skeleton and 1, 4-disubstituted benzene ring
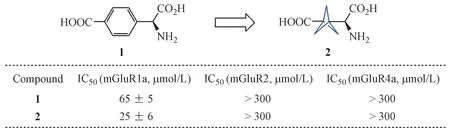
Figure 3 Comparison between compound 1 and 2
2006 年,Pellicciari 课题组又成功地将BCP 结构应用于选择性代谢型谷氨酸受体激动剂的结构优化中[7](图4)。从活性数据可以看出,苯环的替换提高了化合物对于mGluR4 受体的选择性(mGluR4,EC50= 4. 2 μmol/L;mGluR6,EC50= 66 μmol/L;mGluR7,EC50>1 000 μmol/L)。上述BCP代替苯环应用实例(1 & 2,3 & 4)说明苯环并不是活性必需基团,只是起到连接两个药效团的作用,而BCP 作为连接链,使得二侧的取代基之间的距离缩短,可能使得两边的活性基团处于更佳的与受体mGluR1a 或者mGluR4 的结合位置,从而使化合物的活性和选择性得到提高。
2012 年,Stepan 等[8]创造性地以BCP 结构替换已知γ-分泌酶抑制剂5(BMS-708163)中的氟苯,从而得到化合物6(图5)。实验数据显示,化合物6具有更强的生物活性、更低的亲脂性以及更好的水溶性和代谢稳定性。最为重要的一点是,该化合物具有一定的结构新颖性,并开创了突破制药公司关于含苯生物活性分子专利的先例。此后,含有BCP 结构的衍生物越来越多地被包含在相关专利中。

Figure 4 Comparison between compound 3 and 4

Figure 5 Comparison between compound 5 and 6
伊马替尼是治疗白血病的一个“明星”药物。2016 年,Nicolaou 等[9]试图以BCP 结构替换伊马替尼(7)结构中的对位双取代苯环,以期获得结构新颖的药物实体分子(图6)。与伊马替尼相比,化合物8具有较低的亲脂性、较高的水溶性和代谢稳定性。然而,化合物8对于ABL1 酶的抑制活性却显著低于伊马替尼(ABL1 激酶,IC50>1 μmol/L)。推测其活性降低的原因可能是:(1)连接链的长度缩短,哌嗪环上的氮原子与受体结合位点的距离变长;(2)伊马替尼中的对位双取代苯环不仅起到一个连接链的作用,而且会与蛋白产生一定的π-π相互作用并对活性产生影响,而BCP 不具备π-π相互作用。

Figure 6 Comparison between compound 7 and 8
2016 年,研究人员应用BCP 结构对Wtn 抑制剂9进行结构改造[10](图7)。实验结果显示,化合物10 基本丧失了活性(IC50>50 nmol/L)。这表明化合物9 中的苯环结构参与到了蛋白与受体的相互作用当中,可能是活性必须基团。
Darapladib(11)是一种有效的治疗动脉粥样硬化的脂蛋白相关磷脂酶A2(Lp-PLA2)抑制剂,目前正处于临床试验阶段。2017 年,Measom 等[11]采用BCP 骨架替换苯环的策略,对Darapladib 进行结构优化(图8)。研究数据表明,化合物12 相比于Darapladib,仍旧保持了良好的生物活性,并且水溶性得到了显著的提升,但是其亲脂性却出乎意外的增加了。生物活性保持说明BCP 可以代替苯环起到连接链的作用,而亲脂性的增加说明整体化学环境决定了分子的理化性质。
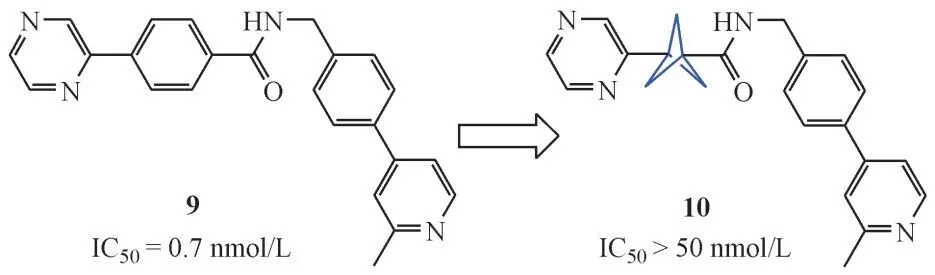
Figure 7 Comparison between compound 9 and 10

Figure 8 Comparison between compound 11 and 12
白藜芦醇(13)是一种具有抗氧化、抗糖尿病和抗肿瘤活性的天然产物。然而其生物利用度太差,特别是在口服吸收之后,血药浓度很低。为了改善白藜芦醇的药代动力学特征,Goh等[12]尝试以BCP 骨架替换白藜芦醇中的苯环结构(图9)。研究数据显示,与白藜芦醇相比,化合物14在保留了相当的抗肿瘤活性的同时,其水溶性增强了40倍,并且具有较低的亲脂性和良好的代谢稳定性。此外,在经过口服吸收之后,化合物14所能够达到的血药浓度也显著高于白藜芦醇。对于一些相对分子质量较小的化合物,芳香环对化合物的理化性质影响较大,BCP替换白藜芦醇中的苯环能够达到增强分子水溶性的目的。
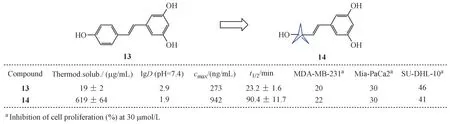
Figure 9 Comparison between compound 13 and 14
吲哚胺2,3-双加氧酶1(IDO1)是色氨酸代谢的关键酶,其在多种肿瘤细胞中过度表达,是肿瘤免疫治疗的一个重要靶点。近年来,IDO1 抑制剂的研究得到了广泛关注。其中默克公司的科学家通过高通量筛选的方法得到了一个活性优异的苗头化合物15。然而由于苯甲酰胺易于水解,导致化合物15代谢稳定性较差。为此,Pu 等[13]采用了多种改造策略进行结构优化,最终发现以BCP 骨架替换中心苯环可以有效地避免酰胺键的水解,从而提高其代谢稳定性(图10)。与此同时,化合物16也保留了良好的生物活性和选择性。这项研究结果说明BCP 可以代替苯环起到连接链的作用,同时,BCP 代替可以获得空间位阻较大的脂肪酰胺,使不易被水解代谢。
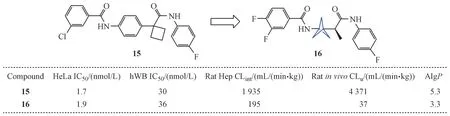
Figure 10 Comparison between compound 15 and 16
当用饱和的烷基作为生物电子等排体取代生物活性化合物中的苯环时,需要考虑下列几个因素。首先,这种替代物有可能增加化合物的代谢稳定性和水溶性。例如,含有苯酚和苯胺的衍生物在体内因易被细胞色素P450快速氧化成1,4-苯醌,因而被认为代谢稳定性差[14]。而用脂肪族连接体则可以避免这种方式降解,因此更稳定。另一方面,由于苯衍生物在晶格中的π堆积,其水溶性较差[15]。用BCP 或立方烷取代苯环,通过破坏π堆积可增加化合物的溶解度,而双环[2. 2. 2]辛烷骨架取代苯环对化合物水溶性的影响并不明显。
2017年,Auberson等[16]报道了3种可替代苯环的生物电子等排体:BCP、立方烷(cubane)和双环[2. 2. 2]辛烷(BCO),并对它们的理化性质进行了综合比较,重点分析了化合物中的C-C 距离、基于人工膜上色谱疏水指数所反映的非特异性结合力以及它们在水中的溶解度(图11)。从几何角度看,立方烷和双环[2. 2. 2]辛烷中的连接原子之间的距离与对位取代苯中的连接原子之间的距离非常相似,而BCP 中的连接原子之间的距离比对位取代苯中的连接原子小约35%,并显著降低非特异性结合,不过BCP 取代芳香环可使溶解度提高至少约50 倍。双环[2. 2. 2]辛烷的结构替换导致分子更加亲脂,并且在非特异性结合或溶解度方面没有表现出优势,而立方烷的替换即显示了这两个参数上的改进。研究者认为,BCP 和立方烷是两种较好的对位取代苯环的生物电子等排体。
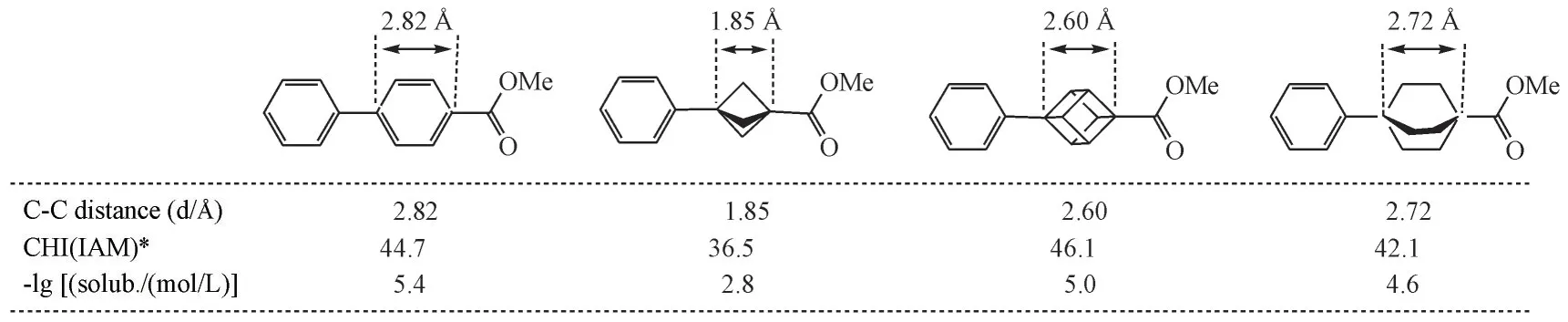
Figure 11 Comparison between benzene ring, BCP, cubane and BCO
虽然用饱和的烷基取代生物活性分子中的苯环对活性和选择性的影响很难预测(图12),但有两种简化的情形是可能预测的:(1)被取代的苯环纯粹作为构象刚性连接片段,将两个取代基保持在彼此很好的确定距离上(图12-A,12-C),使两个取代基与受体结合。在这种情况下,起作用的关键因素是连接片断的长度。例如,用立方烷或双环[2. 2. 2]辛烷取代苯环,有可能保持类似的活性水平。因为相比之下这3 个连接物中的C-C 距离与苯环最相似(2. 82 Åvs2. 60 Åvs2. 72 Å)。另一方面,如果生物活性化合物中取代基之间的较短距离更适合于受体结合囊,则可以观察到甚至增加的活性。(2)在第二种情况下,苯环起到两种作用:作为刚性间隔基来保持取代基间的距离和特定的芳基-蛋白质相互作用(图12-B)。后者可包括:(i)苯环与精氨酸和赖氨酸残基质子化氨基的阳离子-π相互作用;(ii)苯环与蛋白质中苯丙氨酸、色氨酸、酪氨酸和组氨酸残基的π-π相互作用;(iii)其他弱偶极-π相互作用[17]。在这种情况下,事实上,用任何饱和连接物替换生物活性化合物中的苯环将大大降低其活性,如在化合物8和10的饱和类似物中观察到的那样。
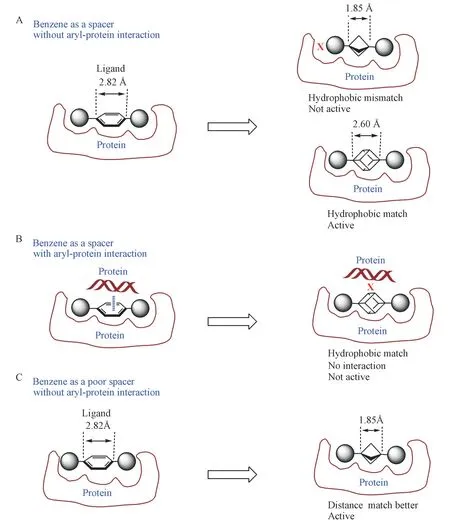
Figure 12 Effect of substituting benzene with saturated alkyl on activity and selectivity in bioactive molecule
1. 2 BCP 作为1,2-二取代炔基的生物电子等排体在药物设计中的应用
BCP作为炔基的生物电子等排体也有应用,因为炔基比苯环的长度更接近BCP。 2017 年,Makarov 等[18]首次尝试用BCP 结构替换炔基的策略,对已上市药物Tazarotene(17)进行结构改造(图13)。药代动力学研究及理化性质检测发现,化合物18 在pKa 和非特异性吸附等性质上与Tazarotene非常接近。

Figure 13 Comparison between compound 17 and 18
1. 3 BCP作为叔丁基的生物电子等排体在药物设计中的应用
叔丁基是药物分子中一种常见的空间位阻较大的取代基,然而当向感兴趣的分子骨架中引入叔丁基时却往往会使化合物的脂溶性提高以及代谢稳定性降低[19]。为了解决这一问题,科学家们发现了多种叔丁基的生物电子等排体,其中由于BCP的结构新颖性和亲脂性降低而备受关注。
1993 年,Barbachyn 等[20]首次应用BCP 骨架来替换叔丁基(图14)。BMY-40062(20)是已上市药物环丙沙星(19)的结构类似物,其杀菌活性得到了较大提升,但是没有能够克服环丙沙星所带来的耐药性。所以研究者在BMY-40062 的结构基础上对其进行结构优化,并创造性地以BCP 结构来替换叔丁基得到了U-87947E(21)。实验数据显示,U-87947E的抗菌活性要优于环丙沙星,并且对于耐环丙沙星的金黄色葡萄球菌有很强的抑制作用。

Figure 14 Design of compound 21
2015 年,Westphal 等[19]分别用BCP 骨架替换已上市药物Bosentan(22)和Vercirnon(24)结构中的叔丁基,并系统性的研究了化合物改造前后在物理化学性质、药代动力学性质和生物活性上产生的变化(图15)。研究数据表明,在结构上,BCP骨架的体积要小于叔丁基。当以BCP 替换叔丁基之后,化合物亲脂性降低,其他理化性质也会得到一定的改善。

Figure 15 Comparison between compound 22 & 23, 24 & 25
1. 4 BCP 作为新颖的结构片段在药物设计中的应用
辉瑞公司通过高通量筛选发现了一类新的热休克蛋白90(Hsp90)拮抗剂,并对其进行了构效研究[21]。值得引起注意的是结构中含有BCP 大体积酰胺取代基。含有BCP胺基片段的化合物26显示出对细胞色素P450 的抑制作用,但也观察到不必要的脱靶效应,对动物肿瘤模型试验表明该化合物具有显著的抗肿瘤疗效以及其他令人满意的成药特性。应用相同的设计理念,BCP 片段已经被引入到JAK 抑制剂27[22]、RIPK1 抑制剂28[23]、RET抑制剂29[24]、DLK 抑制剂30[25]、Ikaros 和Aiolos 的降解剂31[26]等创新药物分子中(图16)。上述活性分子已作为瑟法隆(Cephalon)、辉瑞、百时美施贵宝、药明康德等国内外制药公司在研的先导化合物。

Figure 16 Examples of novel bioactive compounds with a BCP moiety
2 结语与讨论
到目前为止,BCP骨架作为1,4-二取代苯环的生物电子等排体的应用最为广泛。而其作为炔基和叔丁基的生物电子等排体的应用却屈指可数,所以在未来还有很多研究的空间。总体而言,将BCP 引入药物分子当中可以极大地提高化合物的被动渗透性、水溶性和代谢稳定性等。但是对于生物活性而言,还需要综合考虑替换基团的具体作用。
近年来,BCP 作为1,4-二取代苯环、1,2-二取代炔基和叔丁基的生物电子等排体在药物设计中已经得到了广泛的应用。越来越多的化合物专利中,已经将该结构纳入了保护的范围。与此同时,BCP衍生物合成方法的开发也如火如荼地进行着,并已经取得了非常显著的进展。可以预见,随着时间的沉淀,会有含BCP 结构的药物成功上市并造福人类。

