罗沙司他减轻小鼠心肌缺血再灌注损伤的作用和机制研究
姚金东 王妮妮 刘亚然

【摘要】 目的:研究罗沙司他减轻小鼠心肌缺血再灌注损伤的作用和机制。方法:选取20只雄性C57BL/6小鼠,随机分为生理盐水组和罗沙司他组,每组10只。生理盐水组腹腔注射生理盐水,罗沙司他组腹腔注射罗沙司他。结扎冠状动脉左前降支45 min,再灌注3 h。记录小鼠心肌梗死面积;检测小鼠血浆中肌酸激酶(CK)、乳酸脱氢酶(LDH)水平;TUNEL检测小鼠心肌细胞凋亡;免疫印迹检测小鼠心肌组织中低氧诱导因子-1α(HIF-1α)表达;实时定量PCR检测小鼠心肌组织中Ddit4和Ndufa4l2的mRNA表达。结果:与生理盐水组比较,罗沙司他组可明显减小小鼠心肌梗死面积,降低血浆心肌酶水平,减轻心肌细胞凋亡,上调心肌组织中HIF-1α、Ddit4 mRNA和Ndufa4l2 mRNA的表达水平(P<0.05)。结论:罗沙司他可通过上调HIF-1α和低氧反应基因Ddit4和Ndufa4l2的表达,减轻实验小鼠的心肌缺血再灌注损伤。
【关键词】 罗沙司他 心肌缺血再灌注损伤 低氧诱导因子 凋亡
Study on the Effect and Mechanism of Roxadustat in Alleviating Myocardial Ischemia Reperfusion Injury in Mice/YAO Jindong, WANG Nini, LIU Yaran. //Medical Innovation of China, 2022, 19(08): 0-019
[Abstract] Objective: To study the effect and mechanism of Roxadustat in alleviating on myocardial ischemia reperfusion injury in mice. Method: A total of 20 male C57BL/6 mice were randomly divided into normal saline group and Roxadustat group, 10 mice in each group. The normal saline group was intraperitoneally injected with normal saline, and the Roxadustat group was intraperitoneally injected with Roxadustat. The left anterior descending coronary artery was ligated for 45 min and reperfusion for 3 h. The area of myocardial infarction in mice was recorded; and the levels of creatine kinase (CK) and lactate dehydrogenase (LDH) in plasma were detected; TUNEL was used to detect myocardial cell apoptosis in mice; Western blotting was used to detect the expression of hypoxia-inducible factor-1α (HIF-1α) in mice myocardium; the mRNA expressions of Ddit4 and Ndufa4l2 in mice myocardium were detected by real-time PCR. Result: Compared with the normal saline group, Roxadustat group could significantly reduce the myocardial infarction area, reduce the level of plasma myocardial enzymes, reduce cardiomyocyte apoptosis and up-regulate the expression levels HIF-1α, Ddit4 mRNA, Ndufa4l2 mRNA in myocardial tissue (P<0.05). Conclusion: Roxadustat alleviates myocardial ischemia reperfusion injury in mice by up-regulating the expression of HIF-1α and hypoxia response genes Ddit4 and Ndufa4l2.
[Key words] Roxadustat Myocardial ischemia reperfusion injury Hypoxic-inducible factor Apoptosis
First-author’s address: Panjin Liaoyou Gem Flower Hospital, Liaoning Province, Panjin 124000, China
doi:10.3969/j.issn.1674-4985.2022.08.004
早期再灌注是心肌梗死發生后缩小梗死面积、维持心功能最有效的治疗方法,然而,缺血性心脏病仍然是导致心力衰竭的主要原因[1]。为进一步改善心血管疾病的预后,亟须探究缺血性心脏病管理新的方法和新策略。缺血预处理已被证实是预防缺血/再灌注损伤的有效方法。为在药理学上实现缺血预处理,已有研究报道了一些潜在的可介导缺血预处理的药物,如腺苷、蛋白激酶C、阿片受体和活性氧等[2]。此外,多项研究表明,抑制脯氨酸羟化酶结构域蛋白或过表达低氧诱导因子-1α(HIF-1α)可显著减轻缺血性损伤[3-4]。作为缺氧诱导型应激反应基因,DNA损伤诱导转录物4(Ddit4)和Ndufa4l2是HIF-1α的直接靶基因,其与细胞压力应激、凋亡、自噬等生命进程息息相关[5]。
先前的研究报道脯氨酸羟化酶抑制剂能够上调红细胞生成素并促进肝脏中红细胞产生,随后开发了第一类脯氨酸羟化酶抑制剂——罗沙司他[6]。罗沙司他可稳定提高促红细胞生成素和血红蛋白水平,用于模拟缺氧的自然反应,最初被用于治疗慢性肾病患者的贫血[7]。然而,罗沙司他对心肌缺血/再灌注损伤的治疗效果仍有待充分阐明。因此,在本研究中,笔者建立心肌缺血小鼠模型,再灌注后观察罗沙司他对小鼠心梗面积和HIF-1α信号通路和低氧反应基因的影响,探讨罗沙司他预处理是否能保护小鼠心肌缺血再灌注损伤,以及其潜在的机制。现报道如下。
1 材料与方法
1.1 主要试剂和仪器 罗沙司他[阿斯利康(中国)],DMSO(上海科昊生物工程),伊文思蓝、TTC染色剂(美国Sigma公司),血浆肌酸激酶(CK)和乳酸脱氢酶(LDH)检测试剂盒(南京建成生物工程研究所),TUNEL检测试剂盒(上海碧云天),HIF-1α抗体(#36169,美国CST公司)。
1.2 实验动物分组及小鼠心肌缺血再灌注模型制备 于2019年6月-2020年9月进行实验。选取20只12周龄雄性C57BL/6小鼠,体重20~26 g,随机分为两组,每组10只。3 h后,所有小鼠手术区域备皮消毒,行异氟醚(生产厂家:河北一品制药股份有限公司,批准文号:国药准字H19980141,规格:100 mL)麻醉,于胸骨左侧第3、4肋间剪开皮肤,逐层钝性分离皮下组织、肌肉,打开胸腔,用开胸器撑开肋间、充分暴露心脏,剪开心包,在体视显微镜下仔细辨认,可见在心耳下缘或左侧出现一条粉红色血管即为左冠状动脉的前降支,开胸后迅速结扎冠状动脉左前降支,45 min后解开结扎,结扎冠状动脉的前降支后看到左心室前壁心肌变白,局部收缩运动受限,左心耳充盈胀满,心电图见ST段持续弓背抬高,表明心肌缺血再灌注模型成功。3 h后静脉取血1 mL,处理小鼠以进行后续实验。对照组腹腔注射生理盐水,罗沙司他组腹腔注射罗沙司他(溶于DMSO溶液)[生产厂家:珐博进(中国)医药技术开发有限公司,批准文号:国药准字H20180024,规格:50 mg]25 mg/kg。
1.3 伊文思蓝/TTC染色 各组小鼠再灌注3 h后,从右侧颈内静脉注入1%伊文思蓝。小鼠唇染蓝后,剪下心脏,剔除心房,-80 ℃速冻,切片。平行房室沟将左室切成1.5~2.0 mm厚切片。放入2%的TTC染液中小心避光浸染,30 ℃避光孵育30 min,并随时观察样本颜色变化。随后,切片置于10%中性福尔马林中固定24 h。用生理盐水冲洗组织表面多余的染色液,拍照记录各组小鼠心肌梗死面积。
1.4 血浆中心肌酶水平检测 再灌注3 h后,小鼠静脉取血1 mL,分别按说明书用血浆CK和LDH检测试剂盒检测小鼠血浆中CK和LDH水平。
1.5 心肌细胞凋亡检测 再灌注3 h后,取小鼠心肌组织,4%多聚甲醛固定,石蜡包埋,切厚度为3~4 μm的组织切片。按照说明书操作进行TUNEL染色。小鼠正常心肌细胞呈蓝色荧光,凋亡心肌呈红色。分别取3个不同的视野,荧光显微镜下计数TUNEL染色阳性的小鼠心肌细胞数量。
1.6 免疫印迹 再灌注3 h后,摘取小鼠心脏,RIPA裂解液冰上裂解,4 ℃ 12 000 r离心5 min,取上清,加SDS上样缓冲液100 ℃变性10 min后,即得心肌组织蛋白。行SDS-PAGE电泳、转膜,BSA封闭1 h,孵育一抗(HIF-1α、GAPDH)4 ℃过夜,漂洗后孵育二抗4 ℃约4 h,ECL增强化学发光法显影,凝胶成像系统检测各组小鼠心肌组织中相关蛋白的相对含量。
1.7 实时荧光定量PCR 用Trizol试剂提取小鼠心肌中的总RNA,反转录为cDNA后,以GAPDH为内参,SYBR法进行实时荧光定量PCR扩增,各基因相对表达量用2-ΔΔCt表示。引物序列為:
(1) GAPDH。 F,5’-GGCACAGTCAAGGCTAGAATG-3’,R,5’-ATGGTGGTGAAGACGCCAGTA-3’。(2)Ddit4:F,5’-TGGACAGCAGCAACAGTGG-3’;R,5’-TGCATCAGGTTGGCACACAG-3’。(3)Ndufa4l2:F,5’-CTGGGACAAGATGGCAGGAAC-3’;R,5’-GGGCAAGTCGCAGCAAGTAGA-3’。
1.8 统计学处理 采用GraphPad Prism 7.0软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
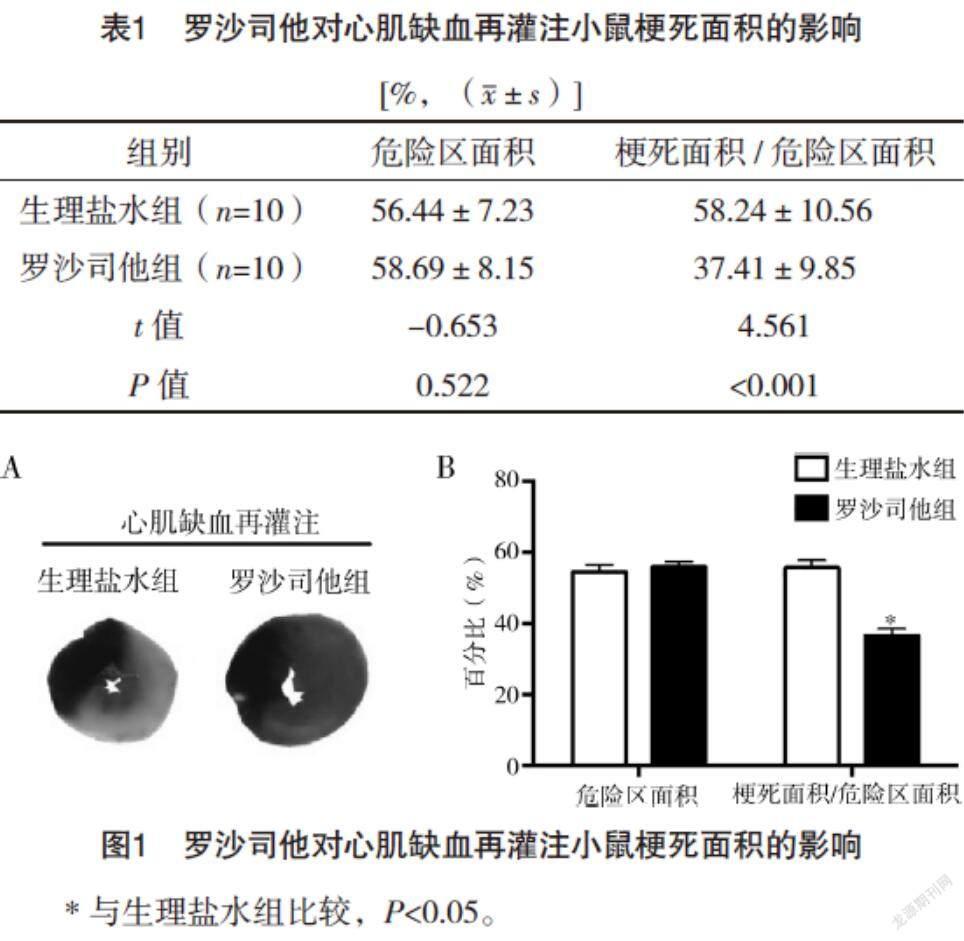
2.1 罗沙司他对心肌缺血再灌注小鼠梗死面积的影响 在小鼠冠状动脉左前降支结扎术后3 h给予罗沙司他腹腔注射25 mg/kg,与生理盐水组相比,再灌注3 h后,罗沙司他可显著诱发小鼠对心肌缺血再灌注损伤的抵抗,表现为小鼠心肌梗死面积缩小(未染色区域);再灌注3 h后,两组危险区面积比较,差异无统计学意义(P>0.05);罗沙司他组心肌梗死面积/危险区面积百分比较生理盐水组显著下降(P<0.05)。见表1、图1。
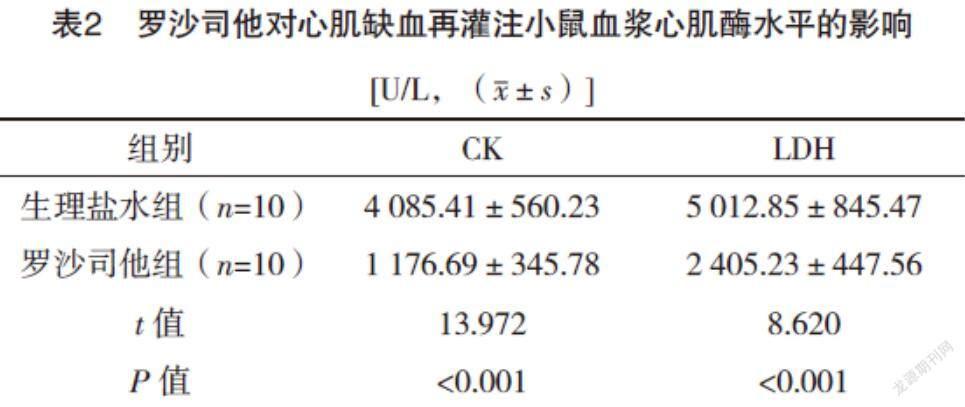
2.2 罗沙司他对心肌缺血再灌注小鼠血浆心肌酶水平的影响 小鼠行心肌缺血再灌注后,与生理盐水组相比,罗沙司他组小鼠血浆CK、LDH的水平均显著下降(P<0.05),见表2。
2.3 罗沙司他对心肌缺血再灌注小鼠心肌细胞凋亡的影响 小鼠行心肌缺血再灌注后,与生理盐水组小鼠心肌中TUNEL阳性细胞数(214.37±20.65)/mm2相比,罗沙司他组(96.45±11.94)/mm2显著减少(t=-15.633,P<0.001),见图2。
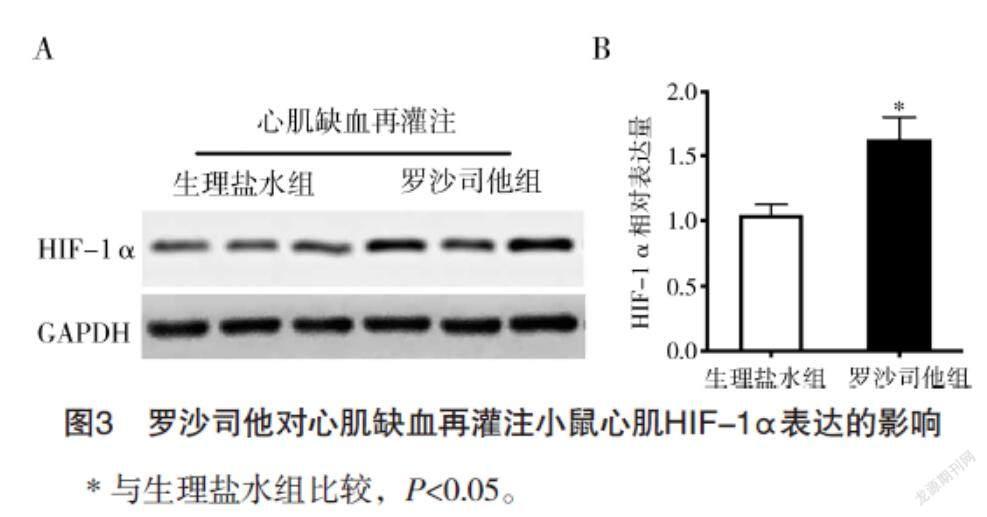
2.4 罗沙司他对心肌缺血再灌注小鼠心肌HIF-1α表达的影响 与生理盐水组小鼠心肌中HIF-1α的表达水平(1.14±0.10)相比,罗沙司他组(1.62±0.25)显著升高(t=5.637,P<0.001),见图3。
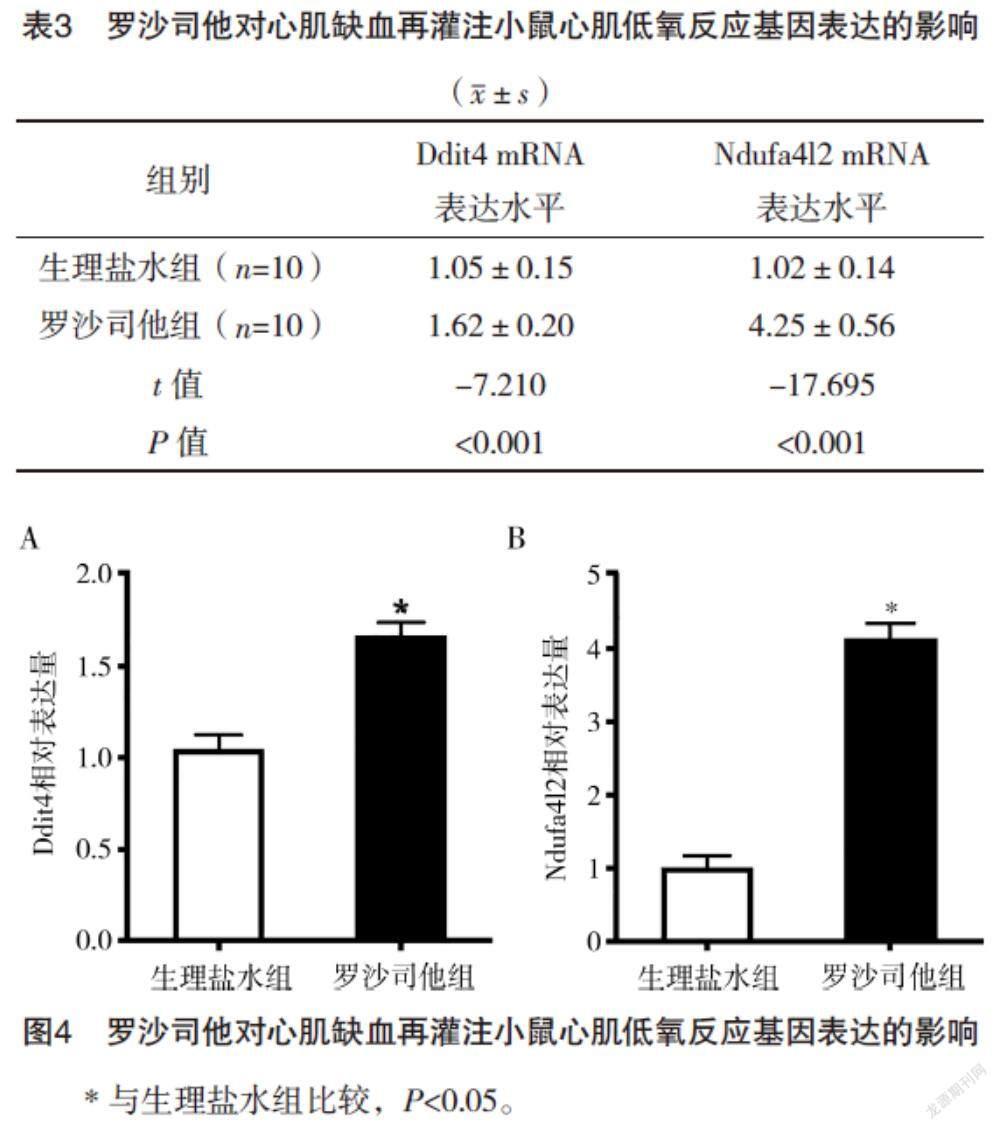
2.5 罗沙司他对心肌缺血再灌注小鼠心肌低氧反应基因表达的影响 结果显示,与生理盐水组相比,罗沙司他组小鼠心肌中Ddit4和Ndufa4l2的mRNA表达水平均显著升高(P<0.05),见表3、图4。
3 讨论
近年来,世界范围内心肌梗死的发病率显著增加,严重威胁人类健康。患者的心肌梗死面积与其长期临床预后密切相关,早期经皮冠状动脉介入再灌注是现有减少心梗后梗死面积和改善临床预后的最有效策略[8]。然而,心肌梗死仍然是心力衰竭的常见诱因,且此类患者的死亡率很高。因此,针对减轻心肌缺血损伤作用的心脏保护策略显得至关重要。尽管目前已经报道了一些潜在的心脏保护疗法,但仍缺乏针对再灌注损伤的治疗方法和药物。因此,笔者通过建立心肌缺血小鼠模型,探讨罗沙司他预处理对小鼠心肌缺血再灌注损伤的作用,以及其潜在的机制。
罗沙司他是全球首个口服强效可逆低氧诱导因子脯氨酸羟化酶抑制剂,是阿斯利康中国在国内研发的Ⅰ类新药,主要用于治疗慢性肾病透析患者贫血。为了维持更持久的药效,罗沙司他临床上治疗慢性肾脏病患者贫血通常采用间歇性给药策略。罗沙司他的半衰期约为10 h,每周给药三次,可使低氧诱导因子(HIF-1)转录活性在两次给药之间恢复到基线水平,并诱导HIF-1及其靶基因介导的红细胞生成[9]。在本研究中,笔者首次将罗沙司他预处理应用在心肌缺血实验小鼠上,发现给予罗沙司他预处理的小鼠,其心肌缺血再灌注后心肌梗死面积显著减少,心肌酶水平降低,心肌凋亡程度减轻,心肌组织中HIF-1α、Ddit4和Ndufa4l2的表达均显著升高。
HIF-1α是在心血管系统生理和病理中发挥关键作用的转录因子。西門子等在1991年首次发现HIF-1α作为促红细胞生成素的转录因子[10];另有学者研究揭示了HIF-1α在常氧下被VHL降解、以及缺氧下HIF-1α激活的机制[11]。在缺氧情况下,HIF-1α由抑制脯氨酸羟化酶结构域蛋白诱导产生,在缺血预处理扮演着重要的角色。在复氧条件下,脯氨酸羟化酶低氧诱导因子-1α被希佩尔林道(VHL)连接,募集泛素连接酶,进一步降解和泛素化蛋白酶体。与此相反,在缺氧条件下,HIF-1α的羟基化以及接下来的泛素化和降解均中止[12-13]。因此,HIF-1α在细胞中可作为转录和非转录因子聚集。在本研究中,笔者发现罗沙司他可以显著减少小鼠心肌梗死面积,显著升高小鼠心肌中HIF-1α的表达,从而减轻实验小鼠的心肌缺血再灌注损伤。
Ddit4是一种高度保守的细胞应激性蛋白,在缺氧、DNA损伤、内质网应激、能量匮乏、营养消耗等细胞应激情况下显著高表达,已被报道参与调节细胞压力应激、DNA损伤修复、凋亡和自噬等细胞进程[14]。作为缺氧诱导型应激反应基因,Ddit4基因是HIF-1α的直接转录靶点。Ndufa4l2蛋白是线粒体呼吸链复合体Ⅰ亚基家族的一员。研究表明,Ndufa4l2蛋白是唯一在低氧环境下高表达的线粒体呼吸链复合体Ⅰ亚基蛋白,且其基因是HIF-1α的直接靶基因。在低氧环境下,嗜铬细胞瘤细胞以及脑细胞等的Ndufa4l2蛋白水平均高表达,Ndufa4l2参与介导细胞低氧适应性以及损伤保护等生理病理机制[15]。研究证实,在缺氧/复氧心肌细胞模型中,Ndufa4l2可通过调节线粒体呼吸链复合体Ⅰ亚基蛋白减轻心肌细胞凋亡、改善线粒体功能障碍,进一步预防心肌缺血再灌注损伤[16]。此外,丁苯酞可通过HIF-1α/Ndufa4l2调节线粒体呼吸链复合体Ⅰ亚基蛋白表达,进一步保护线粒体、减轻氧化应激,发挥对PC12细胞的保护作用,可能参与脑缺血损伤的修复[17]。本研究结果表明,罗沙司他组小鼠心肌中HIF-1α的表达显著上调,且Ddit4和Ndufa4l2的mRNA表达水平均显著升高,提示罗沙司他可上调HIF-1α以及低氧反应基因Ddit4和Ndufa4l2的表达,进而减轻实验小鼠的心肌缺血再灌注损伤。
然而,本研究尚存在一定不足。例如,本研究虽揭示了罗沙司他可通过调节心肌中HIF-1α表达进而减轻小鼠的心肌缺血再灌注损伤,但关于罗沙司他是如何作用在小鼠心肌HIF-1α上的,是通过通路调节还是与之直接相结合,是否存在其他靶点,尚不清楚,有待进一步深入探究。
综上所述,本研究发现罗沙司他可通过上调HIF-1α和低氧反应基因Ddit4和Ndufa4l2的表达,减轻实验小鼠的心肌缺血再灌注损伤,提示罗沙司他药理学预处理可能成为对抗心肌缺血再灌注损伤的新策略。
参考文献
[1]王雅枫,周璐,雷少青,等.缺血再灌注对大鼠心肌损伤及氧化应激的影响[J].中华实用诊断与治疗杂志,2018,32(12):1157-1159.
[2] HAUSENLOY D J.Cardioprotection techniques: preconditioning, postconditioning and remote conditioning (basic science)[J].Curr Pharm Des,2013,19(25):4544-4563.
[3]丁然然,哈艳平,王振良,等.低氧诱导因子-1与缺血性心肌损伤保护的研究进展[J].中国细胞生物学学报,2015,37(10):1447-1457.
[4] BISHOP T,RATCLIFFE P J.HIF Hydroxylase Pathways in Cardiovascular Physiology and Medicine[J].Circ Res,2015,117(1):65-79.
[5] ZHENG J,ZHANG M,WENG H.Induction of the mitochondrial NDUFA4L2 protein by HIF-1a regulates heart regeneration by promoting the survival of cardiac stem cell[J].Biochem Biophys Res Commun,2018,503(4):2226-2233.
[6] PROVENZANO R,BESARAB A,WRIGHT S,et al.Roxadustat (FG-4592) versus epoetin alfa for anemia in patients receiving maintenance hemodialysis: A phase 2, randomized, 6- to 19-week, open-label, active-comparator, dose-ranging, safety and exploratory efficacy study[J].Am J Kidney Dis 2016,67(6):912-924.
[7]陳楠.罗沙司他在慢性肾脏病患者肾性贫血治疗中的应用[J].中华内科杂志,2019,58(12):919-920.
[8]何奔,韩雅玲.中国ST段抬高型心肌梗死救治现状及应有对策[J].中华心血管病杂志,2019,47(2):82-84.
[9] CHEN N,HAO C,LIU B C,et al.Roxadustat Treatment for Anemia in Patients Undergoing Long-Term Dialysis[J].N Engl J Med,2019,381(11):1011-1022.
[10] SEMENZA G L,NEJFELT M K,CHI S M,et al.Hypoxia-inducible nuclear factors bind to an enhancer element located 3’ to the human erythropoietin gene[J].Proc Natl Acad Sci USA,1991,88:5680-5684.
[11] CHAKRABORTY C,MITRA S,ROYCHOWDHURY A,et al.Deregulation of LIMD1-VHL-HIF-1α-VEGF pathway is associated with different stages of cervical cancer[J].Biochem J,2018,475(10):1793-1806.
[12] VILLA J C,CHIU D,BRANDES A H,et al.Nontranscriptional role of Hif-1α in activation of γ-secretase and notch signaling in breast cancer[J].Cell Rep,2014,8(4):1077-1092.
[13] SEMENZA G L.Hypoxia-inducible factors in physiology and medicine[J].Cell,2012,148(3):399-408.
[14]张怡,高维娟.DDIT4对脑缺血再灌注损伤中自噬的调控作用[J].中国病理生理杂志,2018,34(5):956-960.
[15] TELLO D,BALSA E,ACOSTA-IBORRA B,et al.Induction of the mitochondrial NDUFA4L2 protein by HIF-1α decreases oxygen consumption by inhibiting Complex Ⅰ activity[J].Cell Metabolism,2011,14(6):768-779.
[16] LI J,BAI C,GUO J,et al.NDUFA4L2 protects against ischaemia/reperfusion-induced cardiomyocyte apoptosis and mitochondrial dysfunction by inhibiting complex Ⅰ[J].Clin Exp Pharmacol Physiol,2017,44(7):779-786.
[17]肖本杰,高丽,耿冠男.丁苯酞诱导缺氧条件下NDUFA4L2蛋白的高表达并参与脑保护的机制[J].实用老年医学,2019,33(10):954-957.
(收稿日期:2021-07-30) (本文编辑:姬思雨)

