四黄栓制备工艺和质量标准研究*
吴安超,林咏梅,施娅妮,张 静,陈军亮
(云南省中医医院,云南 昆明 650100)
四黄软膏由大黄、黄芩、黄连、黄柏、冰片5味中药材组方,主要用于湿热下注所致痔疮、肛裂、肛漏、肛周肿痛或瘙痒、大便带血,肛管炎见上述证候者。方中,大黄、黄连、黄柏、黄芩清热解毒,散肿,化瘀止痛;冰片辛香走窜,散热结,消肿痛,燥湿热,具有去恶生新功效[1]。原方为云南中医药大学第一附属医院肛肠科钟传珍教授的经验方,临床应用疗效明显。但原制备工艺过于简单,有效成分未经提取纯化,载药量低,稳定性较差,质量难以控制。软膏剂不易准确定量,使用过程中易造成二次交叉污染,且换药过程中极易造成伤口疼痛,药物残渣滞留于肛门,不利于痔疮康复[2-3]。为此,本研究中将四黄软膏的剂型改成栓剂,通过正交试验优化了处方药材的醇提工艺,并建立了控制栓剂的质量标准。现报道如下。
1 仪器与试药
1.1 仪器
BSA224S 型电子分析天平(德国Sartorius 公司,精度为0.1 mg);R-300HL 型旋转蒸发仪(瑞士步琦有限公司);DLSB- /510型低温冷却液循环泵(巩义市予华仪器有限责任公司);DHG-9140A 型电热鼓风干燥箱(广东泰宏君科学仪器股份有限公司);SHB-Ⅲ型循环水式多用真空泵(郑州长城科工贸有限公司);RBY-A型融变时限试验仪(上海黄海药检仪器有限公司);岛津LC-20AD型高效液相色谱仪(日本岛津公司),配有LCsolution工作站,可变波长扫描紫外检测器;硅胶H薄层板、硅胶G板、聚酰胺薄膜(青岛海洋化工厂)。
1.2 试药
盐酸小檗碱对照品(批号为110713-201814,纯度为86.8%),大黄对照药材(批号为120984-201202),黄连对照药材(批号为121752 - 201801),黄芩对照药材(批号为120955 - 201810),黄柏对照药材(批号为121510 - 201807),均购于中国食品药品检定研究院;大黄酸对照品(批号为DST20081909,纯度为86.8%),黄芩苷对照品(批号为DST200601,纯度不低于98%),均购于成都德思特生物技术有限公司;甲醇、乙腈为色谱纯,其余试剂均为分析纯。
2 方法与结果
2.1 提取浸膏中盐酸小檗碱含量测定
2.1.1 色谱条件[1]
色谱柱:Phenomenex C18柱(250 mm × 4.6 mm,5 μm);流动相:0.05 mol/L磷酸二氢钠溶液(每100 mL中加十二烷基硫酸钠0.4 g,加磷酸调pH至4.0)-乙腈(50∶50,V/V);流速:0.8 mL/ min;检测波长:345 nm;柱温:25 ℃;进样量:10 μL。
2.1.2 浸膏粉制备
以75%乙醇为提取溶剂,于75 ℃水浴加热,回流提取,滤液置旋转蒸发仪,回收乙醇,蒸至流浸膏状,转移至蒸发皿中,置105 ℃恒温箱中烤干,得浸膏粉。
2.1.3 溶液制备
取盐酸小檗碱对照品适量,精密称定,加甲醇-盐酸溶液(100∶1,V/V),超声处理(功率为120 W,频率为65 kHz)20 min至完全溶解,得质量浓度为0.19 mg/mL的对照品溶液。取浸膏粉,研成细粉,混匀,取0.1 g,精密称定,加甲醇 - 盐酸溶液(100∶1,V/V)100 mL,密塞,称定质量,摇匀,60 ℃水浴加热15 min 使溶解,超声处理(功率为120 W,频率为65 kHz)30 min,放至室温,擦干锥形瓶外壁的水,称定质量,用甲醇- 盐酸溶液(100∶1,V/V)补足减失的质量,摇匀,滤过,取滤液,加甲醇 - 盐酸溶液(100∶1,V/V)稀释5倍,摇匀,以0.45 μm微孔滤膜滤过[1],即得供试品溶液。
2.1.4 含量测定
分别取2.1.3 项下供试品溶液和对照品溶液,按2.1.1 项下色谱条件进样测定,用外标法计算样品中盐酸小檗碱的含量。
2.2 制备工艺研究
2.2.1 提取工艺优化
正交试验:采用SPSS 19.0 统计学软件设计正交试验,以提取时间(因素A)、加溶剂量(因素B)、提取次数(因素C)为考察因素,每个因素设计3 个水平,因素与水平设计见表1。按处方量称取大黄、黄连、黄柏和黄芩4味药材9份,正交试验测定出膏率和浸膏中盐酸小檗碱的含量,以二者为综合指标优选最佳提取工艺。出膏率和浸膏中盐酸小檗碱含量所占权重分别为0.4 和0.6,综合评分=出膏率得分+盐酸小檗碱含量得分[4]。正交试验设计与结果见表2。方差分析结果见表3。
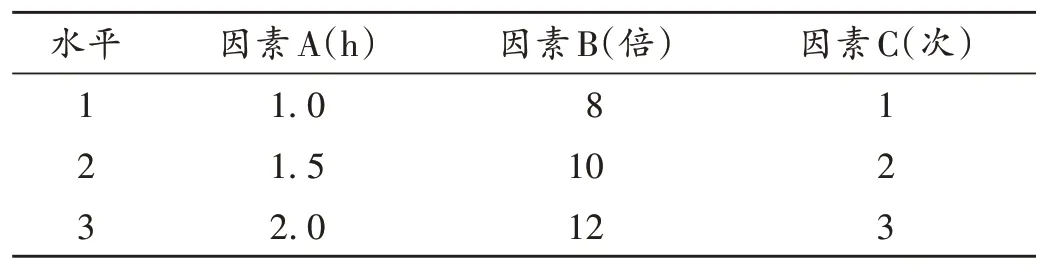
表1 因素与水平Tab.1 Factors and levels of L9(33) orthogonal test

表2 L9(33)正交试验设计与结果(n=9)Tab.2 Design and results of L9(33)orthogonal test(n=9)

表3 正交试验方差分析结果Tab.3 ANOVA results of orthogonal test
结果分析:由表2 可知,各因素对指标影响程度由大至小依次为C > A > B,各因素对提取工艺的影响次序为A1>A2>A3,B1>B3>B2,C3>C2>C1。由方差分析结果可知,提取次数对提取结果有显著影响,提取时间在F0.1水平对提取结果有显著影响,加溶剂量对提取结果无显著影响。最终确定处方药材最佳提取工艺为A1B1C3,即加8倍量处方药材溶剂,回流提取3次,每次1 h。
最佳提取工艺验证:按10 倍处方量称取药材2 份,按最佳提取工艺进行平行验证试验,计算得平均出膏率为23.38%,提取浸膏中盐酸小檗碱含量为89.49 mg/g,说明优选的提取工艺合理、稳定、可行。
2.2.2 成型工艺研究
基质选择:根据处方药物的性质、常用基质的特点,本研究中选择评价以含药栓外观形状、硬度、融变时限为评价指标,以36型、38型、36型 +38型(1∶1,m/m)混合脂肪酸甘油酯为栓剂基质进行考察,根据所得栓剂的外观形状是否光滑圆整、硬度是否适中、融变时限是否符合规定,选择合适的基质。由表4可知,36型+38型混合脂肪酸甘油酯按1∶1(m/m)混合时所得的栓剂外观均匀,软硬适中,融变时限符合2020 年版《中国药典(四部)》规定。故选择基质为36型+38型混合脂肪酸甘油酯(1∶1,m/m)。

表4 基质筛选Tab.4 Screening of the matrix
置换价测定:取36 型、38 型混合脂肪酸甘油酯各10 g,70 ℃加热熔融后制成不含药粉的空白栓10 粒,称定质量。取36型、38型混合脂肪酸甘油酯各7 g,加热熔融,根据处方量称取浸膏粉4.25 g,少量多次加入,不断搅匀,于40 ℃注模,-5 ℃冷却20 min,脱模取出,制成含药粉栓剂10粒,称定质量。按公式计算本处方的置换价(DV),DV=W/[G-(M-W)]。其中,G为空白栓的平均质量;M为含药栓的平均质量;W为每枚栓剂的平均含药质量。按G为 1.696 3 g,M为 1.814 9 g,W为0.425 0 g,计算得DV为1.39。按公式X=(G-W/DV)×n(n为预制栓剂枚数)计算制备含药栓所需基质的质量。若制备100 枚四黄栓剂,需加入理论基质质量为140 g,即36型、38型混合脂肪酸甘油酯各70 g。实际操作中可能会有损失,故基质使用量暂定为150 g,即36型、38型混合脂肪酸甘油酯各加入75 g。
2.2.3 四黄栓制备[5]
取浸膏粉、冰片,研细,过100 目筛,按处方量称取浸膏粉42.5 g,冰片12.5 g,备用。取36 型、38 型混合脂肪酸甘油酯各75 g,置烧杯中,于70 ℃水浴加热融化,少量多次加入浸膏粉,不断搅匀,待温度降至45 ℃时加入冰片,搅匀,于40 ℃条件下注模,-5 ℃冷却20 min,取出,刮去溢出模口部分,脱模,即得四黄栓(批号分别为2021022101,2021022102,2021022103)。
2.3 四黄栓质量标准研究
2.3.1 薄层色谱鉴别
大黄:取同一批(批号为2021022103)样品10枚,将样品切成小块,混匀,取1.8 g(相当于1 枚栓剂的量),置锥形瓶中,加入甲醇100 mL,超声处理(功率为80 W,频率为50 kHz)45 min,滤过,吸取5 mL 滤液,水浴加热蒸干,残渣加10 mL 纯化水,搅拌溶解,加入1 mL 盐酸,水浴加热回流45 min,取出,冷却至室温,转移至分液漏斗,加20 mL 乙醚,振摇萃取,重复2 次,合并乙醚液,水浴蒸干,加入1 mL 三氯甲烷使溶解,滤过,即得供试品溶液[6]。取大黄对照药材2 g,按供试品溶液制备方法制备对照药材溶液。取大黄酸对照品适量,加甲醇溶解,制成质量浓度为10 mg/mL 的对照品溶液[1]。按处方制备缺大黄的阴性对照药材,按供试品溶液制备方法制备阴性对照品溶液。按2020 年版《中国药典(四部)》通则0502 薄层色谱法进行试验,将上述4 种溶液分别点于同一硅胶H 板(黏合剂为羧甲基纤维素钠)上,点样量为5 μL,展开剂为石油醚(37 ℃)-乙酸乙酯-甲酸(15∶5∶1,V/V/V)的上层液,展开,烘干,用3%三氯化铝显色,置紫外光灯(365 nm)下检视[1]。供试品溶液、对照品溶液、对照药材溶液色谱在相应位置显相同的粉红色荧光斑点,且缺大黄的阴性对照品溶液色谱无此斑点。详见图1 A。
黄连、黄柏[1]:取同一批(批号为2021022103)样品10枚,切成小块,混匀,取1.8 g(相当于1枚栓剂的量),置锥形瓶中,加100 mL 75%乙醇溶液,超声处理(功率为120 W,频率为65 kHz)45 min,放入 - 5 ℃冰箱冷冻4 h,摇匀,滤过,取续滤液2 mL,加甲醇 - 盐酸溶液(100∶1,V/V)稀释,定容于10 mL 容量瓶中,制得供试品溶液。取黄连、黄柏对照药材粉末(过20目筛)各0.5 g,精密称定,置三角瓶中,加100 mL 75%乙醇溶液,超声处理(功率为120 W,频率为65 kHz)45 min,静置,滤过,取滤液20 mL,水浴蒸干,加2 mL 甲醇- 盐酸溶液(100∶1,V/V)使溶解,即得对照药材溶液。取盐酸小檗碱对照品,精密称定,加甲醇 -盐酸溶液(100∶1,V/V),摇匀,完全溶解,即得质量浓度为0.19 mg/mL 的盐酸小檗碱对照品溶液。按处方制备缺黄连、黄柏的阴性对照药材,按供试品溶液制备方法制备缺黄连、黄柏的阴性对照品溶液。照2020 年版《中国药典(四部)》通则0502 薄层色谱法进行试验,吸取上述5 种溶液各适量,点于同一硅胶G 板上,点样量为5 μL,先用浓氨试液预饱和10 min,展开剂为氨水-甲苯-乙酸乙酯-甲醇-异丙醇(12.5∶6∶3∶2∶1.5,V/V/V/V/V),展开,取出,烘干,置紫外光灯(365 nm)下检视[1]。供试品溶液与盐酸小檗碱对照品溶液、黄连对照药材溶液、黄柏对照药材溶液、缺黄连阴性对照品溶液和缺黄柏阴性对照品溶液色谱在对应位置显相同的荧光绿色斑点;黄连对照药材和缺黄柏阴性对照品溶液色谱中还有2 个亮黄色的斑点,黄柏对照药材和缺黄连的阴性对照品溶液色谱中无亮黄色斑点,阴性对照无干扰。详见图1 B。

图1 薄层色谱图(365 nm)1.Reference solution 2.Test solution 3.Negative reference solution 4,4′.Phellodendri Chinensis Cortex and Coptidis Rhizoma reference medicinal materials solution 5,5′.Negative reference solution lacking Phellodendri Chinensis Cortex and Coptidis RhizomaA.Rhei Radix et Rhizoma B.Coptidis Rhizoma and Phellodendri Chinensis Cortex C.Scutellariae RadixFig.1 TLC chromatograms(365 nm)
黄芩:取同一批(批号为2021022103)样品10枚,计算平均装量,将样品切成小块,混匀,取1.8 g(相当于1 枚栓剂的量),置锥形瓶中,加75%乙醇100 mL,超声处理(功率为120 W,频率为65 kHz)45 min,溶解,滤过,滤液水浴蒸干,残渣加甲醇5 mL使溶解,滤过,即得供试品溶液[1]。称取黄芩对照药材1 g,参照供试品溶液制备方法制备对照药材溶液。取黄芩苷对照品适量,精密称定,加甲醇溶液,摇匀,使完全溶解,制成质量浓度为1 mg/mL 的黄芩苷对照品溶液。按处方制备不含黄芩的对照阴性药材,按供试品溶液制备方法制备阴性对照品溶液[1,7]。参照2020年版《中国药典(四部)》通则0502薄层色谱法进行试验,将上述4种溶液分别点于同一硅胶H板(65 ℃烤箱烘烤30 min)上,点样量为3 μL,先预饱和15 min,以正丁醇 - 冰醋酸 - 水(7∶1∶2,V/V/V)为展开剂,展开,烘干,喷显色剂三氯化铁,显色,置紫外光灯(365 nm)下检视[8]。供试品溶液与对照药材溶液、对照品溶液色谱对应位置上显相同的橘黄色斑点,且阴性对照无干扰。详见图1 C。
2.3.2 盐酸小檗碱含量测定
1)色谱条件[1]
色谱柱:Phenomenex C18柱(250 mm × 4.6 mm,5 μm);流动相:0.05 mol/L磷酸二氢钠溶液(每100 mL中加0.4 g 十二烷基硫酸钠,加磷酸调pH 至4.0)- 乙腈(50∶50,V/V);流速:1.0 mL/min;柱温:30 ℃;检测波长:345 nm;进样量:10 μL。
2)溶液制备
取盐酸小檗碱对照品适量,精密称定,加甲醇-盐酸溶液(100∶1,V/V)超声(功率为120 W,频率为65 kHz)20 min 至完全溶解,配制成质量浓度为200.97 μg/mL的对照品溶液。取样品10 枚,切碎混匀,取0.5 g,精密称定,置具塞锥形瓶中,加甲醇 -盐酸溶液(100∶1,V/V)100 mL,密塞,称定质量,超声处理(功率为120 W,频率为65 kHz)45 min,放至室温,加甲醇 - 盐酸溶液(100∶1,V/V)补足减失的质量,放入-5 ℃冰箱内冷冻4 h,待基质全部析出,取出,摇匀,迅速滤过,滤液放至室温,用甲醇 - 盐酸溶液(100∶1,V/V)稀释5 倍,即得供试品溶液[9]。按处方工艺称取缺黄连、黄柏的其余药材,按四黄栓制备方法制备空白栓剂,按供试品溶液制备方法制备缺黄连、黄柏的阴性对照品溶液。
3)方法学考察
专属性试验:分别取对照品溶液和供试品溶液各适量,按2.3.2项下色谱条件进样测定,记录色谱图。结果盐酸小檗碱峰的理论板数不低于3 000,阴性对照品溶液中无干扰峰出现,对照品溶液与供试品溶液中,盐酸小檗碱峰的保留时间一致,盐酸小檗碱峰周围无干扰峰,分离度好,方法专属性良好。色谱图见图2。
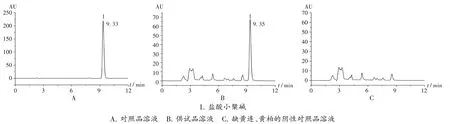
图2 高效液相色谱图1.Berberine hydrochlorideA.Reference solution B.Test solution C.Negative reference solution lacking Coptidis Rhizoma and Phellodendri Chinensis CortexFig.2 HPLC chromatograms
线性关系考察:取溶液制备项下对照品溶液,加甲醇 - 盐酸溶液(100∶1,V/V)分别稀释至质量浓度为10.049,20.097,40.194,60.291,80.388,100.485 μg/mL的系列溶液,按2.3.2 项下色谱条件分别进样测定。以峰面积(Y)为纵坐标、盐酸小檗碱质量浓度(X,μg/mL)为横坐标进行线性回归,得回归方程Y=43 307X+17 865(R2=1.000 0,n=6)。结果表明,盐酸小檗碱质量浓度在10.049~100.485 μg/mL范围内与峰面积线性关系良好。
日内、日间精密度试验:分别取线性关系考察项下盐酸小檗碱对照品溶液(质量浓度为60.291,10.049 μg/mL),按拟订色谱条件1 d 内连续重复进样6 次;连续3 d,每天进样测定2次。结果盐酸小檗碱峰面积的平均值分别为 2 637 859 和 444 360,RSD分别为 0.06% 和 0.16%(n=6),表明仪器日内、日间精密度良好。
重复性试验:取同一批(批号为2021022103)样品10 枚,切碎,取6 份,每份 0.5 g,精密称定,依法制备供试品溶液,按2.3.2 项下色谱条件进样测定。结果盐酸小檗碱含量的平均值为18.78 mg/ g,RSD为0.41%(n=6),表明方法重复性良好。
稳定性试验:取重复性试验项下供试品溶液,按2.3.2 项下色谱条件分别于4,8,12,16,20,24 h 时进样测定。结果峰面积的平均值为834 180,RSD为0.19%(n=6),表明供试品溶液在室温下24 h内稳定性良好。
加样回收试验:取盐酸小檗碱含量为18.82 mg/g的样品(批号为20210212103)6份,精密称定,根据栓剂样品中盐酸小檗碱含量,按1∶1(m/m)加入对照品溶液,依法制得供试品溶液,按2.3.2 项下色谱条件进样测定。结果见表5。
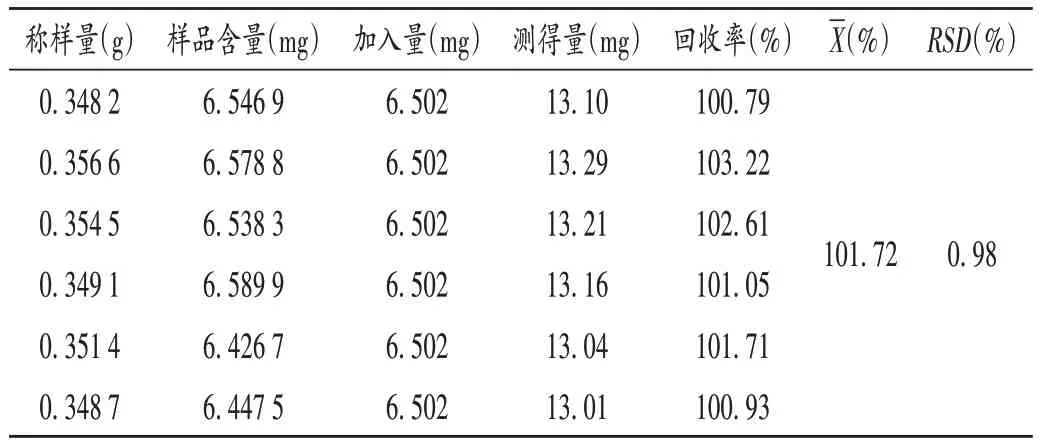
表5 盐酸小檗碱加样回收试验结果(n=6)Tab.5 Results of recovery test of berberine hydrochloride(n=6)
4)样品含量测定
取3 批样品,各10 枚,切碎,依法制备供试品溶液,拟订色谱条件进样测定,并计算含量。结果见表6。以本品中含黄连、黄柏以盐酸小檗碱计,暂订本品质量标准确定的含量限度,不得少于18.58 mg/g。
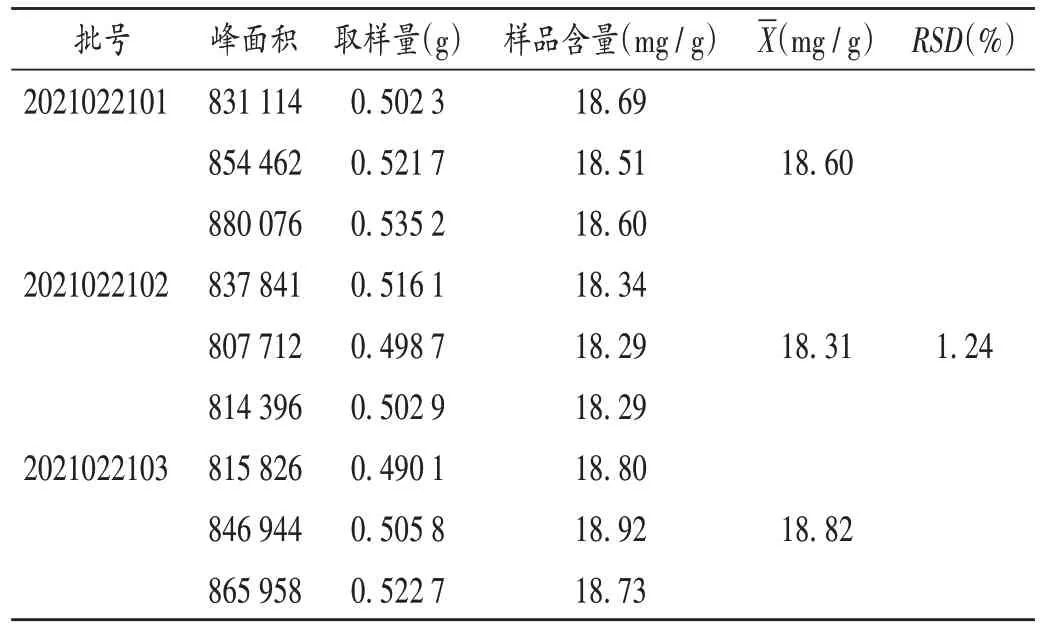
表6 样品含量测定结果Tab.6 Results of content determination of samples
3 讨论
3.1 含量测定指标性成分选择
中药复方制剂成分复杂,通常只对主要有效成分进行定性、定量鉴别[10]。四黄栓由大黄、黄芩、黄连、黄柏等中药组方,具有清热利湿、活血化瘀、消肿止痛功效,用于治疗痔疮及肛门各种炎症。黄连、黄柏中主要抑菌成分为小檗碱,选取小檗碱为主要代表成分进行含量测定以保证药栓的药效,同时参照2020年版《中国药典(一部)》黄连羊肝丸、黄连上清片、清胃黄连丸(水丸)等复方中成药的含量测定方法[7]。故选择盐酸小檗碱作为含量测定的指标性成分。
3.2 正交试验考察指标选择
药材的提取出膏率是衡量中药材提取是否完全和有效成分是否完全转移的重要指标,也是提取工艺优化的重要考察指标。中药复方制剂成分较复杂,单一指标往往不能衡量工艺的好坏,有效成分含量常作为提取浸膏考察指标。故选择出膏率和主要活性成分盐酸小檗碱的含量作为提取工艺正交试验的综合评价指标。
3.3 供试品溶液配制溶剂选择
从基质中提取分离有效成分是供试品溶液处理的关健,同时还要最大程度地降低基质对仪器测定的干扰[11-12]。本研究中四黄栓使用的基质为36型+38型混合脂肪酸甘油酯(1∶1,m/m),溶于甲醇、乙醇,不溶于水。因此,在制备供试品溶液时,先测定目标成分的极性和酸碱性等。提取碱性成分时,先用酸性试剂提取,再用酸水使其游离,最后用适当极性的有机溶剂反复萃取,达到除杂的目的。本研究中采用甲醇、75%乙醇提取栓剂中有效成分,薄层鉴定结果良好[13-14]。供试品溶液配制过程中,加甲醇-盐酸溶液(100∶1,V/V)超声(功率为300 W,频率为54 kHz,20 ℃)处理1 h,基质和盐酸小檗碱完全溶解,加盐酸有助于游离盐酸小檗碱,放入- 0.5 ℃冰箱内冷冻4 h,基质全部析出,可达到去除基质的目的。
3.4 定性鉴别条件选择
黄连、黄柏的薄层鉴别时,盐酸小檗碱荧光绿色斑点下方存在黄色斑点,曾用不同展开剂分离斑点,但分离效果不理想。最终以氨水-甲苯-乙酸乙酯-甲醇-异丙醇(12.5∶6∶3∶2∶1.5,V/V/V/V/V)为展开剂,因盐酸小檗碱呈碱性,在展开槽另一边放置等体积的浓氨试液饱和10 min 后再展开,可明显改善斑点的形状,但饱和时间不能过长,否则其斑点会呈扁圆形,甚至变为一条短线[15]。黄芩薄层鉴别时,因黄芩苷具有一定酸性,故展开剂中需要添加酸性成分,以减少拖尾现象[16]。参照2020 年版《中国药典(一部)》黄芩薄层鉴别项下方法,以甲苯-乙酸乙酯-甲醇-甲酸(10∶3∶1∶2,V/V/V/V)为展开剂,斑点基本分离,但可能由于展开剂极性太小,黄芩苷的比移值过小,斑点基本处于基线,达不到分离要求。通过调整展开剂的酸度、极性等,分离效果、拖尾现象明显改善,结合文献[8],以正丁醇-冰醋酸 - 水(7∶1∶2,V/V/V)为展开剂,喷以三氯化铁显色,进行黄芩薄层色谱鉴别。结果黄芩苷对照品溶液色谱斑点与供试品溶液色谱中黄芩苷的斑点在一条直线上,显色结果明了、直观,容易判断。
3.5 含量测定方法选择
2020 年版《中国药典(一部)》中黄连、黄柏含量测定项下测定盐酸小檗碱含量的色谱条件中,流动相均采用0.05 mol/L 磷酸二氢钾溶液(每100 mL 中加十二烷基硫酸钠0.4 g,加磷酸调节pH至4.0)-乙腈(50∶50,V/V),黄连和黄柏中小檗碱的检测波长分别为345 nm和265 nm[1]。查阅文献[17-20],以保留时间和分离度为指标,反复调整流动相系统。十二烷基硫酸钠(每100 mL含0.4 g)在0.05 mol/ L 磷酸二氢钾溶液中不易溶解,需加热才能溶解,但冷却后又析出形成浑浊液。将磷酸二氢钾换成磷酸二氢钠,调整流动相比例[0.05 mol/L磷酸二氢钠 - 乙腈(50∶50,60∶40,55∶45,V/V)]和流速(0.6,0.7,0.8,0.9,1.0 mL/ min),盐酸小檗碱峰与杂质峰分离较好。最终采用本研究中确定的色谱条件。

