基于指纹图谱和多成分含量测定的关黄柏及川黄柏差异性研究
冯 媛,郭 龙, 2,常雅晴,郑玉光,张清清, 4*
基于指纹图谱和多成分含量测定的关黄柏及川黄柏差异性研究
冯 媛1,郭 龙1, 2,常雅晴1,郑玉光2, 3*,张清清1, 4*
1. 河北中医学院药学院,河北 石家庄 050200 2. 河北省中药炮制技术创新中心,河北 石家庄 050200 3. 河北省中药资源利用与质量评价国际联合研究中心,河北 石家庄 050200 4. 河北省高校中药组方制剂应用技术研发中心,河北 石家庄 050091
采用HPLC法建立关黄柏及川黄柏药材指纹图谱,并同时测定5种有效成分的含量,评价关黄柏及川黄柏药材的质量差异。运用HPLC法分别建立10批关黄柏药材和10批川黄柏药材指纹图谱,通过对照品比对,对共有峰进行指认,并测定5种有效成分的含量;对关黄柏及川黄柏药材指纹图谱进行相似度评价,并利用主成分分析(principal component analysis,PCA)和正交偏最小二乘法-判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)方法对关黄柏及川黄柏中差异性成分进行分析。关黄柏和川黄柏药材指纹图谱有6个共有峰,指认出其中5个峰,分别是木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱。通过PCA和OPLS-DA分析筛得关黄柏与川黄柏的3个差异性标志物,分别为木兰花碱、巴马汀和小檗碱,其中巴马汀的含量差异最显著。该方法能有效分析关黄柏及川黄柏质量的差异性,为关黄柏及川黄柏的质量评价与控制提供参考。
关黄柏;川黄柏;高效液相色谱法;指纹图谱;多元统计分析;木兰花碱;巴马汀;小檗碱;小檗红碱;盐酸药根碱
关黄柏为芸香科植物黄檗Rupr.的干燥树皮,川黄柏为芸香科植物黄皮树Schneid.的干燥树皮。两者均具清热燥湿、泻火除蒸、解毒疗疮的功效[1],主要治疗黄疸泻痢、肠痔、口疮、热淋涩痛、遗精、目热赤痛等病症[2-3]。目前,关黄柏中已知的化学成分包括生物碱、内酯、酚酸、苯丙素等类成分[4-5],川黄柏的主要化学成分为酚酸、黄酮、三萜、苯丙素和生物碱等类成分[6],其中生物碱类是关黄柏和川黄柏的的主要活性成分。《中国药典》2020年版川黄柏与关黄柏有相同的功效和性味,但随着现代分析技术的进步,发现二者在成分组成尤其是含量上存在较大差异,进而在药理、生物活性上有不同的侧重,但在临床使用中,二者仍存在混用的现象[6]。关黄柏中巴马汀含量远高于川黄柏,而川黄柏的小檗碱含量是关黄柏的5~6倍[7],《中国药典》2020年版规定关黄柏的指标性成分为盐酸小檗碱和盐酸巴马汀;川黄柏的指标性成分为盐酸小檗碱与盐酸黄柏碱。仅以少数成分作为关黄柏和川黄柏的含量测定指标,较难客观全面地评价关黄柏及川黄柏的质量,本实验通过建立HPLC指纹图谱方法并同时测定木兰花碱、盐酸药根碱、小檗红碱、巴马汀和小檗碱的含量,研究其二者质量的差异性,为关黄柏及川黄柏的质量控制及临床合理用药提供参考。
1 仪器与材料
1.1 仪器
Agilent 1260型高效液相色谱仪;Diamonsil C18色谱柱(250 mm×4.6 mm,5 μm);Sartorius型电子分析天平(德国赛多利斯);Eppendorf Centrifuge 5418离心机(德国Eppendorf AG公司);Milli-Q型超纯水仪(美国Milipore公司)。
1.2 材料
关黄柏药材收集自全国3个产地共10批样品,川黄柏药材共10批样品,经河北中医学院郑玉光教授鉴定为芸香科植物黄檗Rupr.及芸香科植物黄皮树Schneid.的干燥树皮,样品及产地信息见表1。对照品木兰花碱(批号19082004,质量分数99.84%)、盐酸药根碱(批号19072609,质量分数98.62%)、小檗红碱(批号19050701,质量分数98.71%)、小檗碱(批号17110105,质量分数98.95%)、巴马汀(批号18022604,质量分数99.01%)均购自成都曼思特生物科技有限公司;乙腈、甲醇(色谱纯,美国飞世尔试剂公司);甲醇(分析纯,天津市永大化学试剂有限公司);超纯水由Milli-Q纯水器制备。
表1 不同产地关黄柏及川黄柏样品信息
Table 1 Sample information of P. amurense and P. chinense from different producing areas
样品编号名称批号产地样品编号名称批号产地 S1关黄柏1804001C吉林S11川黄柏1901001四川 S2关黄柏190601辽宁S12川黄柏190303CP287四川 S3关黄柏190901吉林S13川黄柏180301四川 S4关黄柏1908797131吉林S14川黄柏19072301四川 S5关黄柏1904001吉林S15川黄柏202002001四川 S6关黄柏20191201河北S16川黄柏191002831四川 S7关黄柏202008001河北S17川黄柏1905001四川 S8关黄柏190602151吉林S18川黄柏190804491四川 S9关黄柏190307辽宁S19川黄柏18061501四川 S10关黄柏20200719河北S20川黄柏17081601四川
2 方法与结果
2.1 关黄柏及川黄柏HPLC指纹图谱的建立
2.1.1 色谱条件 色谱柱:Diamonsil C18色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~5 min,10%~13% A;5~20 min,13%~15% A;20~28 min,15%~20% A;28~40 min,20%~40% A;40~55 min,40%~50% A;55~65 min,50%~75% A;65~67 min,75% A;67~69 min,75%~10% A);检测波长265 nm;体积流量1 mL/min;柱温30 ℃;进样量10 μL。
2.1.2 混合对照品的制备 精密称取木兰花碱、盐酸药根碱、小檗红碱、小檗碱、巴马汀对照品适量,分别置于10 mL量瓶中,加入70%甲醇定容,配制成单标母液。准确吸取各母液适量至5 mL量瓶中,加70%甲醇定容,摇匀,配制成质量浓度分别为木兰花碱4.9 μg/mL、盐酸药根碱0.6 μg/mL、小檗红碱0.2 μg/mL、巴马汀6.2 μg/mL、小檗碱18.7 μg/mL的混合对照品溶液,备用。
2.1.3 供试品溶液的制备 分别精密称取关黄柏、川黄柏粉末各0.5 g,置于100 mL具塞锥形瓶中,浸泡30 min后加入30 mL 68%甲醇。超声40 min(恒温25 ℃)后用68%甲醇补足减失质量,混匀,取续滤液4 mL,13 000 r/min离心5 min,取上清液于5 mL EP管中,再精密吸取上清液1 mL于10 mL量瓶中,用色谱甲醇定容至刻度,用0.22 μm微孔滤膜滤过,得关黄柏及川黄柏供试品溶液。
2.1.4 精密度试验 精密吸取关黄柏、川黄柏供试品溶液,连续进样6次,关黄柏中木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱相对保留时间的RSD值分别为0.12%、0.34%、0.76%、0.28%、0.66%;相对峰面积的RSD值依次为0.24%、0.31%、0.36%、0.25%、0.19%;川黄柏中以上5个成分相对保留时间的RSD值分别为0.69%、0.83%、0.92%、0.51%、0.36%;相对峰面积的RSD值依次为0.56%、0.62%、0.48%、1.25%、0.81%,结果表明仪器的精密度较好。
2.1.5 重复性试验 精密称取同一批关黄柏、川黄柏药材粉末,按照“2.1.3”项下方法制备6份供试品溶液,按“2.1.1”项下色谱条件进行分析测定,关黄柏中木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱这5个成分含量的RSD值分别为0.69%、1.94%、1.36%、1.44%、1.68%;川黄柏中以上5个成分含量的RSD值分别为0.47%、0.96%、1.28%、0.52%、1.49%,结果表明该方法的重复性较好。
2.1.6 稳定性试验 精密吸取同一批关黄柏及川黄柏供试品溶液,按“2.1.1”项下色谱条件,分别在0、3、5、8、13、20、24 h进样,关黄柏木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱在不同时间峰面积的RSD值分别为1.69%、1.98%、1.64%、1.83%、1.54%,川黄柏中以上5个成分在不同时间峰面积的RSD值分别为1.29%、1.59%、0.81%、1.29%、2.67%。
2.1.7 指纹图谱的建立及共有峰的指认 采用国家药典委员会《中药色谱指纹图谱相似度评价系统》(2004版本)分别对10批关黄柏与10批川黄柏的HPLC指纹图谱进行共有峰匹配,设置时间窗宽度为0.1,以S1关黄柏样品(批号1804001C)及S8川黄柏样品(批号1901001)的指纹图谱为参照图谱,以小檗碱为Mark峰进行保留时间校正,同时采用中位数法进行全峰匹配,关黄柏及川黄柏生成的共有峰模式图见图1。关黄柏标定出6个共有指纹峰,共有指纹峰的相对峰面积RSD值在22.74%~35.91%;川黄柏标定出6个共有指纹峰,共有指纹峰的相对峰面积RSD值在11.67%~19.82%。关黄柏指纹图谱的相似度在0.912~1.000;川黄柏指纹图谱的相似度在0.998~1.000,相似度均大于0.9,说明相似度良好[8-9]。
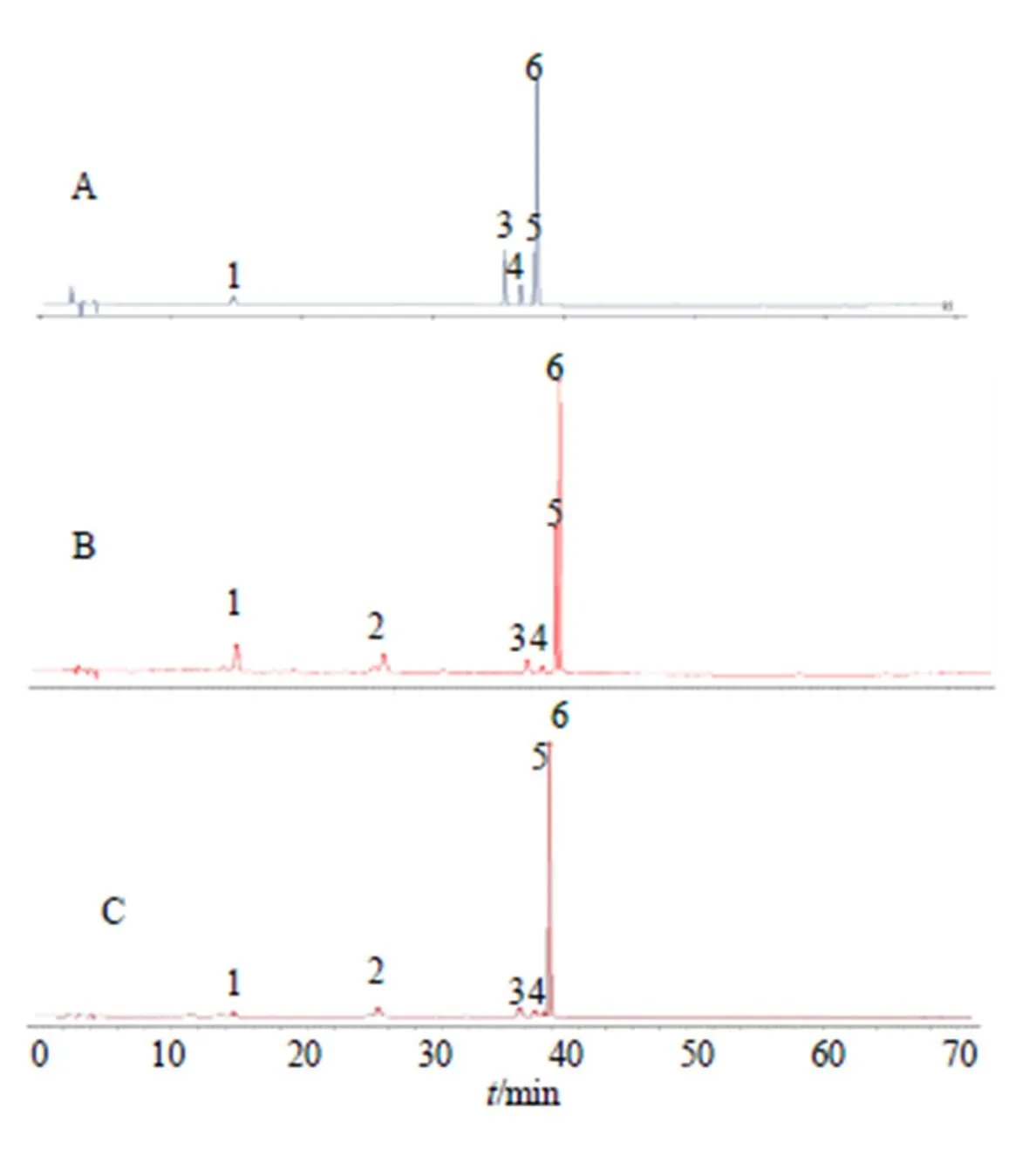
1-木兰花碱 3-盐酸药根碱 4-小檗红碱 5-巴马汀 6-小檗碱
2.2 关黄柏及川黄柏指纹图谱的差异性分析
2.2.1 主成分分析(principal component analysis,PCA) 采用SIMCA14.0软件,对关黄柏及川黄柏进行PCA分析,关黄柏及川黄柏的Scores图和Loading图如图2、3所示,由Scores图可知,关黄柏和川黄柏药材分别聚集在2个不同的区域,说明关黄柏和川黄柏化学成分存在较大差异,二者得到较好地区分。Loading图距离原点越远表明该成分对样品的差异贡献率越大[10-11],通过Loading图可知,对主成分1的影响顺序由大到小依次为峰6、5、1;对主成分2的影响顺序由大到小依次为峰3、4、6。
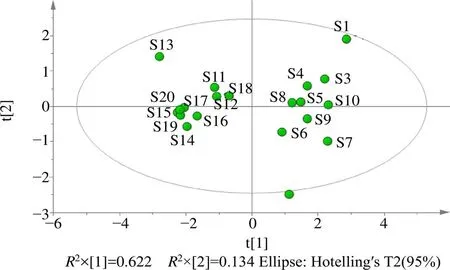
图2 关黄柏及川黄柏药材Scores图
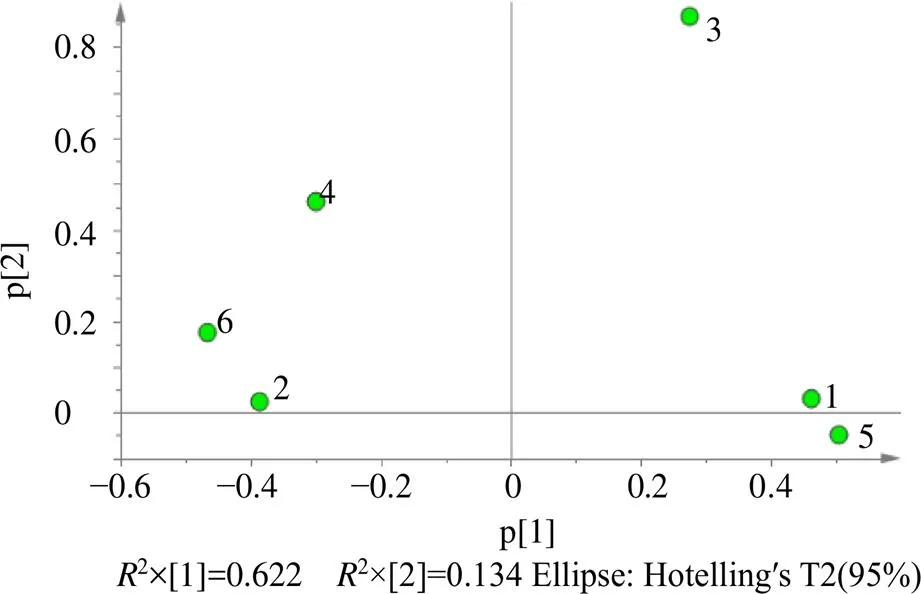
图3 关黄柏及川黄柏药材Loading图
2.2.2 正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA) 为了进一步分析川黄柏及关黄柏的差异性,将关黄柏及川黄柏分为2组,以关黄柏及川黄柏指纹图谱的原始数据为变量,利用SIMCA14.0软件建立关黄柏与川黄柏指纹图谱的OPLS-DA模型。在OPLS-DA得分图中,10批关黄柏及10批川黄柏可很好地区分为2类,如图4所示。模型2(cum)为0.730,2(cum)为0.951,2(cum)为0.924,说明建立的模型有良好的拟合能力[12]。生成的VIP图如图5所示。以VIP>1.0为标准,共有3个差异性标志物,为峰5、6、1,分别为巴马汀、小檗碱和木兰花碱,其中巴马汀的VIP值最大,说明关黄柏和川黄柏中巴马汀的含量差异最显著。
2.3 特征性成分含量测定
2.3.1 线性关系考察 分别精密吸取“2.1.2”项下混合对照品溶液1、3、5、10、15、20 μL,按“2.1.1”项下的色谱条件进样,测定各峰保留时间及峰面积,以各对照品的质量浓度为横坐标(),峰面积为纵坐标()绘制标准曲线,得到各待测组分的回归方程,结果见表2。
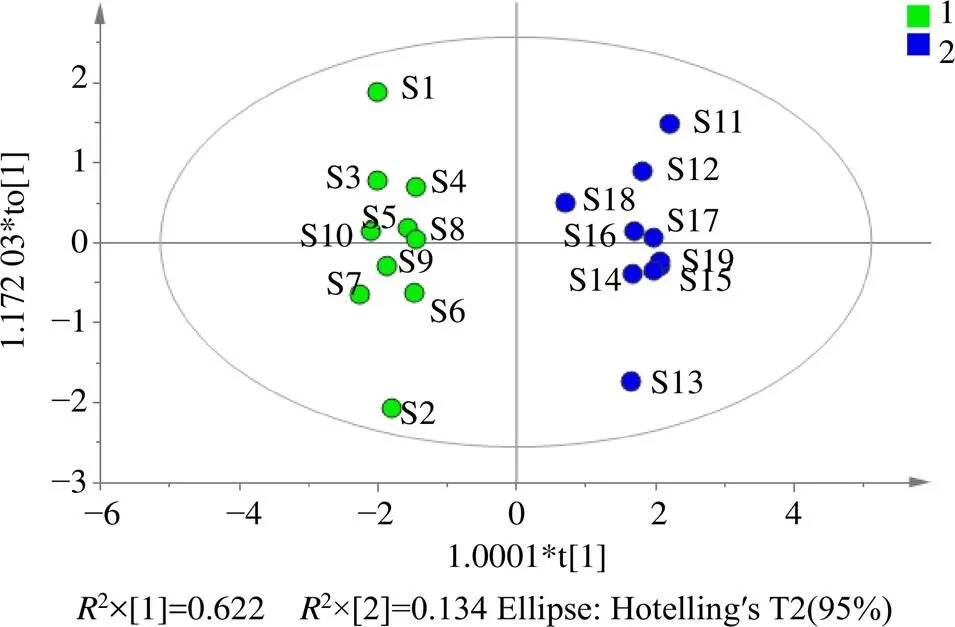
图4 关黄柏及川黄柏OPLS-DA图
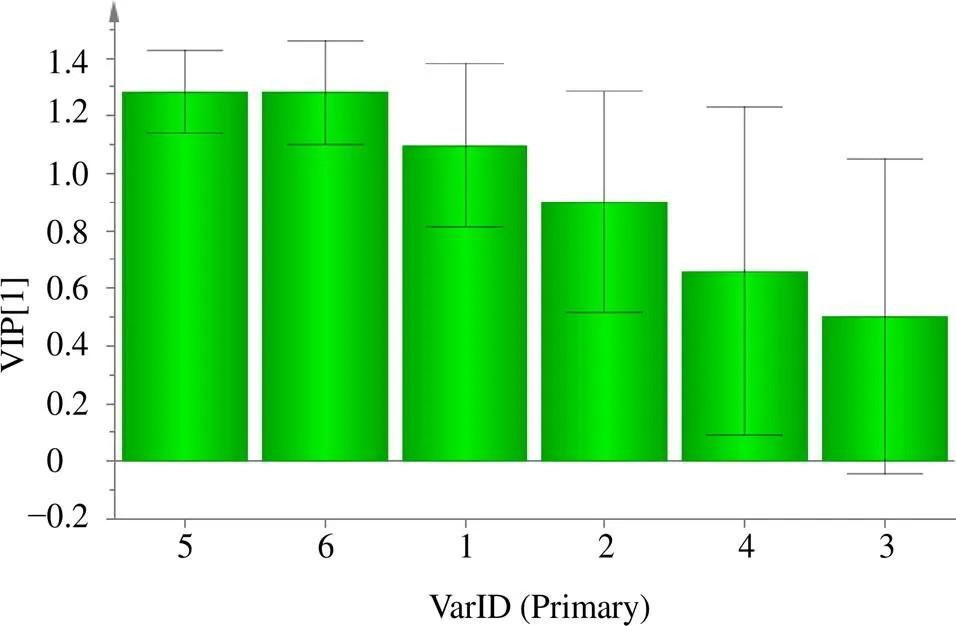
图5 关黄柏及川黄柏共有峰VIP图
表2 回归方程
Table 2 Regression equation
成分回归方程r线性范围/(μg·mL−1) 木兰花碱Y=29 267 X-1.776 30.999 7 0.60~12.00 盐酸药根碱Y=30 422 X-3.073 20.999 4 0.04~0.80 小檗红碱Y=75 554 X-0.662 40.999 70.003~0.06 巴马汀Y=20 404 X-20.0320.999 2 1.31~26.20 小檗碱Y=55 452 X-59.7850.999 6 3.39~67.8
2.3.2 精密度试验
(1)日内精密度:精密吸取关黄柏及川黄柏供试品溶液,连续进样6次,关黄柏样品中木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱这5个成分峰面积的RSD值依次为1.23%、1.41%、0.84%、0.73%、0.49%,川黄柏样品中以上5个成分峰面积的RSD值依次为1.63%、0.92%、1.21%、1.38%、0.87%,结果表明仪器的日内精密度较好。
(2)日间精密度:精密吸取关黄柏及川黄柏供试品溶液,连续进样3 d,关黄柏中木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱这5个成分峰面积的RSD值依次为1.69%、0.93%、0.62%、1.47%、1.03%,川黄柏中以上5个成分峰面积RSD值依次为1.85%、0.49%、1.16%、1.93%、1.82%,结果表明仪器的日间精密度较好。
2.3.3 重复性试验 精密称取同一批关黄柏及川黄柏药材粉末,按照“2.1.3”项下方法制备6份供试品溶液,按“2.1.1”项下色谱条件进行分析测定,关黄柏木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱这5个成分含量的RSD值分别为1.32%、1.92%、1.54%、1.10%、1.39%,川黄柏中以上5个成分含量的RSD值分别为1.59%、1.01%、1.83%、1.14%、1.05%,结果表明该方法的重复性较好。
2.3.4 稳定性试验 精密吸取同一关黄柏及川黄柏供试品溶液,按“2.1.1”项下色谱条件,分别在0、3、5、8、13、20、24 h进样,关黄柏木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱这5个成分在不同时间峰面积的RSD值分别为1.05%、1.41%、0.93%、1.16%、0.98%,川黄柏中以上5个成分含量的RSD值分别为1.72%、1.94%、1.82%、1.09%、1.48%,结果表明供试品溶液在24 h内稳定性较好。
2.3.5 加样回收率试验 精密称取已测定的关黄柏药材粉末0.25 g共6份,置于100 mL具塞锥形瓶中,分别加入与样品中各成分等量的对照品,按照“2.1.3”项下制备供试品溶液,按“2.1.1”项色谱条件进行分析测定,木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱这5个成分的加样回收率分别为102.16%、99.85%、100.38%、101.73%、101.91%,RSD分别为1.54%、1.15%、1.44%、0.92%、1.39%。表明该方法的回收率符合要求。
2.3.6 关黄柏及川黄柏样品含量测定 取10批关黄柏及10批川黄柏粉末,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件进样测定,记录色谱图,通过标准曲线计算各批次样品木兰花碱、盐酸药根碱、小檗红碱、巴马汀及小檗碱的含量,结果见表3。
表3 样品含量测定结果
Table 3 Determination content results of samples
批号质量分数/% 木兰花碱盐酸药根碱小檗红碱巴马汀小檗碱 S10.640.100.0031.56 2.64 S20.780.080.0011.21 2.00 S30.660.080.0021.32 2.01 S40.570.070.0011.11 1.39 S50.890.060.0011.03 2.08 S60.730.050.0010.80 1.69 S70.720.040.0011.44 1.83 S80.910.060.0021.03 2.20 S90.660.060.0011.24 1.97 S100.620.060.0021.40 2.03 S110.160.050.0050.07 8.72 S120.190.050.0070.0915.63 S130.140.040.0020.0714.48 S140.150.040.0040.0712.32 S150.190.040.0070.0412.38 S160.160.050.0030.0812.34 S170.160.050.0040.0812.37 S180.140.060.0030.2211.13 S190.170.040.0060.0513.46 S200.180.040.0080.0712.37
根据《中国药典》2020年版的规定,在关黄柏药材中,含盐酸小檗碱不得少于0.60%,盐酸巴马汀不得少于0.30%;川黄柏药材中含盐酸黄柏碱不得少于0.34%,盐酸小檗碱不得少于3.0%[13]。10批关黄柏样品及10批川黄柏样品均符合药典的规定,并且关黄柏中巴马汀含量是药典规定的3~5倍;小檗碱的含量是药典规定的2~4倍。川黄柏药材中小檗碱的含量是药典规定的3~5倍。此外,从含量测定的结果可以看出,关黄柏中木兰花碱和巴马汀的含量整体高于川黄柏,而川黄柏中小檗碱的含量整体高于关黄柏。盐酸药根碱、小檗红碱的含量在关黄柏和川黄柏中无明显差异。
3 讨论
实验前期对流动相进行了筛选,由于关黄柏和川黄柏中小檗碱和巴马汀为原小檗碱型生物碱,结构极为相似,因此选用乙腈-0.1%甲酸溶液作为流动相时,小檗碱和巴马汀的分离度较差,改为乙腈- 0.1%磷酸溶液作为流动相后,关黄柏和川黄柏中小檗碱和巴马汀成分均得到良好分离,因此选用乙腈- 0.1%磷酸溶液作为后续试验的流动相。本实验前期也对关黄柏的最优提取工艺进行了考察,最终确定关黄柏的最佳提取工艺为:甲醇体积分数为70%、液料比为60 mL/g、提取时间为40 min。
关黄柏及川黄柏中主要含有生物碱类、内酯类、酚酸类、苯丙素类等多种成分,生物碱类成分主要有木兰花碱、盐酸黄柏碱、盐酸药根碱、小檗红碱、巴马汀和小檗碱等。《中国药典》2020年版中关黄柏含量测定成分为小檗碱和巴马汀,川黄柏含量测定成分为盐酸黄柏碱及小檗碱,指标较少,不能全面反反映关黄柏和川黄柏的质量。另外,虽然盐酸黄柏碱是药典规定的川黄柏指标性成分,但本次指纹图谱实验中,没有检测到该成分,推测是由于提取工艺和提取溶剂的原因,使关黄柏及川黄柏中的生物碱成分没有提取完全。故本研究选择木兰花碱、盐酸药根碱、小檗红碱、巴马汀及小檗碱5种生物碱类成分作为含量测定的指标成分,以期较全面反应关黄柏及川黄柏的质量。
在关黄柏和川黄柏的差异性研究中,小檗碱的含量差异最为显著[14],其次为巴马汀。此外,在含量测定的实验中,发现关黄柏中的木兰花碱含量整体高于川黄柏,因此木兰花碱也可作为区分二者的指标性成分。另外,在对照品HPLC色谱图中,4号峰小檗红碱在关黄柏和川黄柏样品中均含量较低,5号峰巴马汀在川黄柏样品中含量较低,因此在《中药色谱指纹图谱相似度评价系统》(2004版本)中,无法在指纹图谱中对这2个峰进行共有峰的指认。2号峰的结构信息也有待于进一步确认。后期可结合液质联用技术对关黄柏和川黄柏的化学成分进行更为全面的鉴定和区分,为关黄柏及川黄柏质量标志物的筛选及质量标准的制定提供进一步参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 李先宽, 冯杉, 郑艳超, 等. 黄柏与关黄柏的化学成分及生物活性研究进展 [J]. 药物评价研究, 2019, 42(5): 1033-1037.
[2] 李嘉诚, 吴岚, 蔡同凯, 等. 黄柏化学成分及其药理作用研究进展 [J]. 药学实践杂志, 2018, 36(5): 389-391.
[3] 徐珊, 张凡, 刘蓬蓬, 等. 黄柏及其不同炮制品的HPLC指纹图谱分析 [J]. 中国实验方剂学杂志, 2015, 21(3): 10-13.
[4] 魏颖, 李雪瑶, 陈维佳, 等. 中国关黄柏资源及其开发利用研究进展 [J]. 人参研究, 2019, 31(2): 44-51.
[5] 贾艾玲, 王仁广, 董雪莲, 等. 不同生长年限黄檗树枝与关黄柏中生物碱类成分相关性研究 [J]. 中国兽药杂志, 2019, 53(4): 45-51.
[6] 高妍, 周海芳, 刘朵, 等. 黄柏化学成分分析及其药理作用研究进展 [J]. 亚太传统医药, 2019, 15(4): 207-209.
[7] 王荣. 川黄柏的化学成分及药理活性研究进展 [J]. 临床合理用药杂志, 2020, 13(1): 173-174.
[8] 陶晓赛, 龚海燕, 谢彩侠, 等. 基于UPLC指纹图谱结合化学计量学评价不同产地盾叶薯蓣药材质量 [J]. 中草药, 2021, 52(1): 227-233.
[9] Chen Y, Zhang Z, Zhang Y,. A new method for simultaneous determination of phenolic acids, alkaloids and limonoids incortex [J]., 2019, 24(4): E709.
[10] 李振雨, 何嘉莹, 童培珍, 等. 基于UPLC指纹图谱和多成分定量的辛夷药材产地差异性研究 [J]. 中草药, 2021, 52(1): 234-240.
[11] Wang L H, Yan G L, Zhang A H,. Fingerprinting and simultaneous determination of alkaloids and limonins incortex from different locations by high-performance liquid chromatography with diode array detection [J]., 2015, 53(1): 161-166.
[12] 崔誉文, 何昊, 张丽, 等. HPLC指纹图谱结合多指标含量测定的八角莲质量评价研究 [J]. 天然产物研究与开发, 2020, 32(12): 2051-2060.
[13] 中国药典 [S]. 一部. 2020: 153.
[14] Chen Y, Zhang Z, Zhang Y,A new method for simultaneous determination of phenolic acids, alkaloids and limonoids incortex [J]., 2019, 24(4): 709-723.
Research on difference ofandbased on fingerprint and multicomponent content determination
FENG Yuan1, GUO Long1, 2, CHANG Ya-qing1, ZHENG Yu-guang2, 3, ZHANG Qing-qing1, 4
1. College of Pharmacy, Hebei University of Chinese Medicine, Shijiazhuang 050200, China 2. Hebei Traditional Chinese Medicine Processing Technology Innovation Center, Shijiazhuang 050200, China 3. International Joint Research Center on Resource Utilization and Quality Evaluation of Traditional Chinese Medicine of Hebei Province, Shijiazhuang 050200, China 4. Hebei Higher Education Institute Applied Technology Research Center on TCM Formula Preparation, Shijiazhuang 050091, China
To evaluate the difference ofandby establishing HPLC fingerprint and determining contents of five effective components.The HPLC fingerprints of 10 batches ofand 10 batches ofwere established by HPLC method, and the common peaks were identificated by reference substances. The contents of five effective components were determined. Similarity evaluation of the fingerprints were carried out, principal component analysis (PCA) and orthogonal partial least squares discriminant analysis (OPLS-DA) were used to find the differential components ofand.There were six common peaks in the fingerprints ofand. By comparing with the reference substances, five common peaks were identified, they were magnoflorine, jatrorrhizine, berberrubine, palmatine and berberine, respectively. Three biomarkers were determined by PCA and OPLS-DA method in the fingerprints ofand, they were magnoflorine, palmatine and berberine respectively. The content difference of palmatine was the most significant.This method can effectively analyze the quality differences ofandand provide reference for its quality evaluation and control.
Rupr.;Schneid.; HPLC; fingerprint; multivariate statistical analysis; magnoflorine; palmatine; berberine; berberrubine; jatrorrhizine
R286.2
A
0253 - 2670(2022)16 - 5179 - 06
10.7501/j.issn.0253-2670.2022.16.027
2021-12-06
河北省基础研究计划自然科学基金资助项目(H2019423103);河北中医学院优秀青年教师基础研究计划项目(YQ2018008);河北省二期现代农业产业技术体系创新团队项目(HBCT2018060205)
冯 媛,女,硕士,研究方向为中药质量评价与控制。Tel: 18232189233 E-mail: 670794139@qq.com
郑玉光,男,博士,教授,从事中药鉴定及中药资源研究。Tel: 13931856959 E-mail: zyg314@163.com
张清清,女,博士,副教授,从事中药药效物质和质量评价研究。Tel: (0311)89926414 E-mail: janezh1987@sina.com
[责任编辑 时圣明]

