石杉碱甲改善Aβ诱导的PC12细胞线粒体毒性
侯添志 陈庆状 欧阳勇 肖晓丹,3
1 广州市花都区第二人民医院 广东广州 510850; 2 广州市中西医结合医院 广东广州 510800; 3 广东医科大学 广东湛江 524023
阿尔茨海默病(AD)是痴呆症最常见的病因,患者临床表现为逐渐丧失记忆和认知功能[1-3]。β-淀粉样蛋白(amyloid-β,Aβ)作为AD的主要神经毒性物质,其刺激小胶质细胞产生的炎症诱导神经元线粒体功能障碍越来越被认为是AD发病的最具代表性的病理生理特征[4-5]。石杉碱甲(huperzine A,HupA)是一种石松类生物碱,除具有典型的抑制胆碱酯酶活性的特性之外,研究显示其尚可减轻脑外伤炎症,并对Aβ直接诱导的神经元线粒体毒性发挥保护作用[6]。另外,我们前期研究显示石杉碱甲对APP/PS1小鼠神经细胞线粒体具有保护作用[7],但对其能否在Aβ间接诱导的神经元线粒体毒性过程中发挥保护作用仍需进一步探讨。因此,本研究将利用Transwell构建小胶质细胞和神经元细胞共培养体系,向小胶质细胞层加入Aβ1-42可模拟AD患者脑内的炎症环境,向神经元细胞层加入石杉碱甲,观察其对Aβ间接诱导的神经元线粒体毒性的保护作用。
1 主要材料
新生SD大鼠(出生后1~2 d)由南方医科大学实验动物中心提供。0.4 μm Transwell培养板(Corning)、ATP试剂盒、ROS试剂盒、总SOD活性检测试剂盒、MDA试剂盒、MTT试剂盒(碧云天)。
2 方法
2.1 细胞培养
2.1.1 小胶质细胞培养 取出生1~2 d的SD大鼠,75%酒精消毒,断头,取海马组织,巴氏管吹散,胰酶消化,过滤,离心,得到离散细胞,重悬于含有10% FBS、100 U/mL青霉素、100 μg/mL链霉素的DMEM/F12培养液。接种于预包被多聚赖氨酸的75 cm2培养瓶中,2 d后全量换液,培养7~10 d,手摇法分离小胶质细胞。
2.1.2 PC12细胞培养 PC12细胞接种于含有10% FBS的DMEM/F12培养液的25 cm2细胞培养瓶中,置于5% CO2、37 ℃的孵育箱中培养,待细胞占瓶底70%~80%时进行传代。
2.2 共培养系统构建
小胶质细胞与PC12细胞以1 ∶1的比例依次接种于Transwell培养板下室(6孔板,1×105细胞/毫升)和上室(1×105细胞/毫升)。
2.3 实验分组
实验共分为3组。①对照组:小胶质细胞和PC12细胞分别接种于Transwell培养板下室和上室;②Aβ1-42组:操作同①,小胶质细胞层加入Aβ1-42(终浓度10 μmol/L)。③HupA组:操作同②,PC12细胞层加入HupA(终浓度1 μmol/L)预处理4 h。
2.4 活性氧(ROS)检测
收集处理好的PC12细胞。根据ROS检测试剂盒说明书提示,用DCFH-DA(10 μL,10 μM)在37 ℃下染色20 min,用流式细胞仪检测。
2.5 总SOD活性和MDA水平检测
收集处理好的PC12细胞,然后用WST-8总超氧化物歧化酶(T-SOD)试剂盒测定T-SOD活性,并根据脂质氧化MDA(丙二醛)试剂盒说明书的指示测定PC12细胞MDA水平。
2.6 ATP检测
收集处理好的PC12细胞,根据ATP检测试剂盒说明书提示,加入100 μL ATP释放剂,加入荧光素底物和荧光素酶避光孵育10 min,Perkin Elmer酶标仪检测生物发光强度。
2.7 MTT检测
收集各组PC12细胞,接种于96孔板(3×104细胞/孔),加入MTT(20 μL,0.5 mg/mL),在37 ℃孵育4 h。去除上清液,加入150 μL DMSO。用酶标仪在波长为492 nm处检测吸光度。
2.8 统计学分析
用SPSS 25.0软件分析数据,数据用均数±标准误表示。多组间比较分析用单因素方差分析(ANOVA),组间两两比较采用最小显著性差异法(LSD法)。p<0.05被认为具有统计学意义。
3 结果
3.1 石杉碱甲减轻Aβ1-42间接诱导的PC12细胞线粒体损伤
图1A结果显示,Aβ1-42组的PC12细胞ROS水平相对对照组有显著性上升,增加约70%~80%(P<0.001),HupA处理后的PC12细胞则有显著性的下降(P<0.001)。图1B显示,与对照组相比,Aβ1-42组PC12细胞MDA水平上升约50%(P<0.001),而PC12细胞经HupA预处理后的MDA水平较Aβ1-42组显著性下降约20%~30%(P<0.001)。从图1C中可以看到,Aβ1-42组PC12细胞的T-SOD水平显著性下降(P<0.001),而HupA可以有效地逆转这种下降的趋势(P<0.001)。另外,从图1D中可以看到,与对照组对比,Aβ1-42组PC12细胞线粒体的ATP呈现显著性下降,下降幅度约为50%(P<0.001),而HupA预处理后的PC12细胞线粒体的ATP水平有明显的上升(P<0.001)。
3.2 石杉碱甲改善Aβ1-42间接诱导的PC12细胞毒性
图2结果显示,与对照组对比,Aβ1-42组的PC12细胞活性降至只有60%左右(P<0.001)。而HupA预处理后的PC12细胞活性则显著性上升至约为对照组的80%左右(P<0.001)。
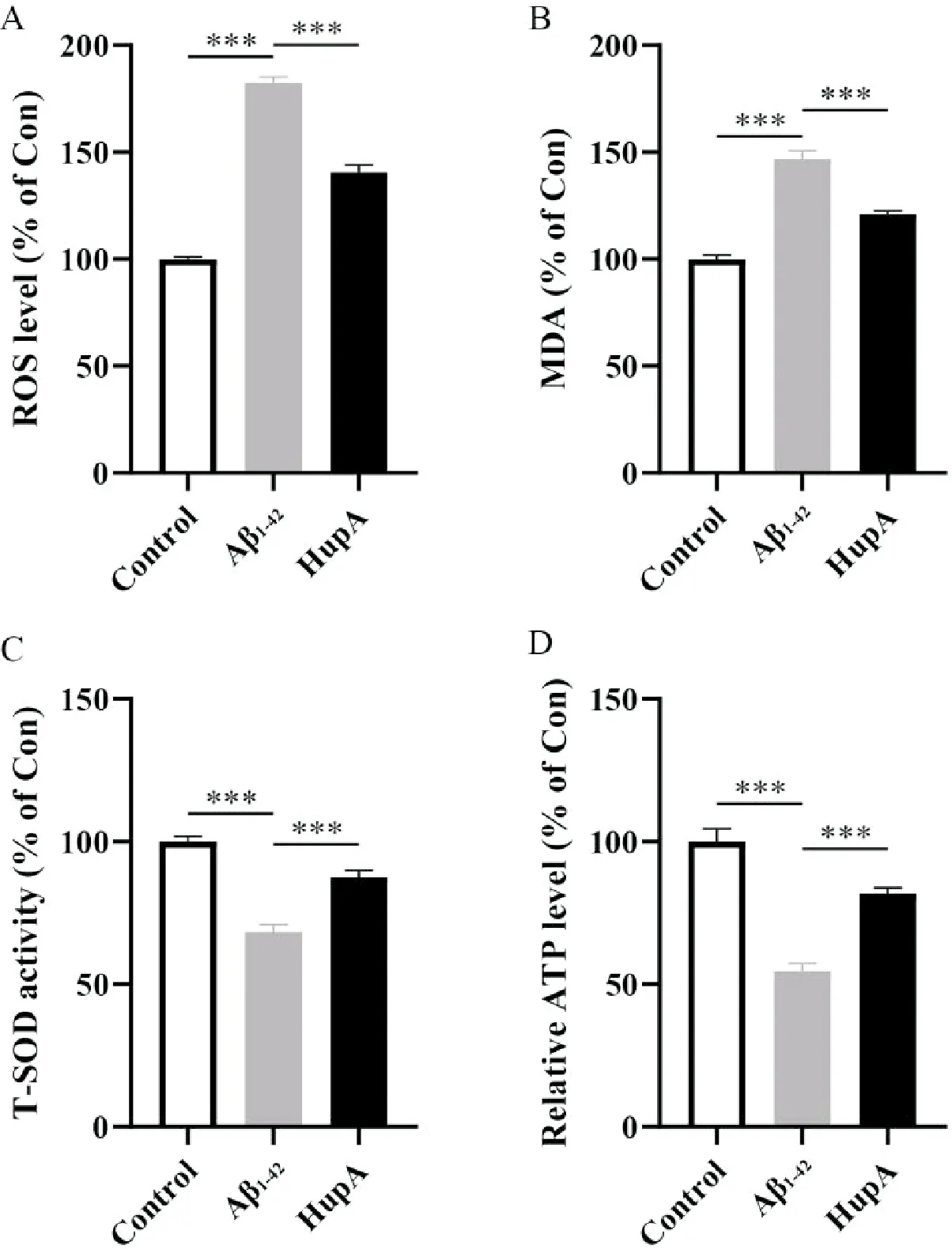
注:A为活性氧(ROS)水平检测(n=6);B为脂质氧化(MDA)水平检测(n=6);C为总超氧化物歧化酶(T-SOD)水平检测(n=6);D为线粒体ATP水平检测(n=6), Mean±SEM, ***P<0.001
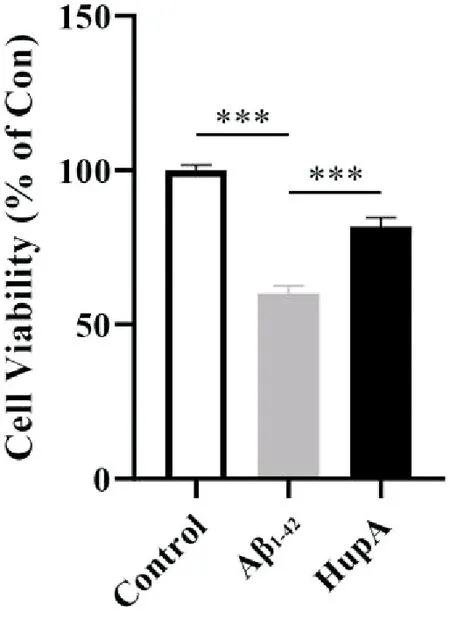
注:采用MTT试剂盒检测PC12细胞活性, n=8,Mean±SEM, ***P<0.001
4 讨论
石杉碱甲是中国食品药品监督管理局批准的AD治疗药物,在中国临床上广泛使用,目前正在美国进行临床前试验[8]。在本研究中,我们探讨了HupA在Aβ1-42刺激小胶质细胞介导的PC12细胞线粒体毒性过程中的作用。
ROS主要来源于线粒体,是一类具有较高氧化活性的分子或离子。ROS的过量产生可损害蛋白质、核酸和脂质等生物大分子的活性,导致线粒体损伤和细胞凋亡[9-10]。为了检测石杉碱甲是否能减轻Aβ1-42刺激小胶质细胞介导的PC12细胞线粒体氧化应激反应,本实验采用ROS敏感的DCFH-DA染料测定细胞内的ROS水平。Aβ1-42介导的PC12细胞的ROS水平显著升高,而石杉碱甲可以有效逆转ROS升高的趋势。众所周知,ROS引起细胞损伤的一个重要方面的体现是导致蛋白质和脂质的氧化[11-12]。MDA是脂质过氧化的副产品,也可以反映细胞的氧化应激反应水平[13]。通过采用MDA试剂盒检测PC12细胞的MDA水平,我们发现Aβ1-42刺激小胶质细胞介导的PC12细胞MDA水平增加到约为对照组的1.5倍,石杉碱甲干预后可将PC12细胞MDA水平降低至约为对照组的1.2倍。结合上述结果,提示石杉碱甲可以显著减轻Aβ1-42刺激小胶质细胞诱导的PC12细胞线粒体氧化应激反应的程度。
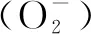
ATP作为线粒体电子传递中最重要的产物,是维持细胞正常功能所必需的能量物质[15]。ROS的增加,将导致线粒体氧化磷酸化失常,从而影响ATP的生成。因为ATP水平与线粒体活性密切相关,所以我们进一步检测ATP水平来评估PC12细胞线粒体功能。结果表明Aβ1-42刺激小胶质细胞对共培养的PC12细胞线粒体ATP水平有显著的下降,而石杉碱甲可以有效地逆转PC12细胞线粒体ATP水平。总之,石杉碱甲可以有效抵抗Aβ1-42刺激小胶质细胞对PC12细胞线粒体的损伤。
过量的ROS加剧线粒体功能障碍,增加线粒体通透性转换孔(mitochondrial permeability transition pore, mPTP),加速细胞色素c(cytoc)向细胞质的释放,进而诱导caspase相关的凋亡级联反应,触发caspase依赖的凋亡级联[16]。因此我们利用MTT试剂盒检测PC12细胞活性,进一步探讨石杉碱甲是否发挥神经细胞活性保护作用。结果显示经石杉碱甲预处理的PC12细胞活性对比Aβ1-42组显著增加,提示石杉碱甲在Aβ1-42诱导的PC12细胞毒性过程中具有保护作用。
综上所述,石杉碱甲通过改善Aβ1-42刺激小胶质细胞介导的PC12细胞线粒体毒性发挥对神经细胞活性的保护作用。

