两种方法检测血清梅毒螺旋体特异性抗体的符合率比较
杨绪岩
摘 要:目的 比较高敏化学发光法(HISCL)和临床常用的梅毒螺旋体明胶凝集试验(TPPA)检测血清梅毒螺旋体特异性抗体的符合率。方法 选择2018年11月~2019年12月山东省新泰市皮肤病防治所采集的1 123份临床检测的血清样本为研究对象,对血清样本分别采取HISCL、TPPA与重组抗原免疫印迹法(RIBA)3种方法进行梅毒螺旋体检测,以RIBA为金标准,对2种检测方法的结果进行符合性分析。结果 在1 123份临床检测的血清样本中,HISCL与TPPA检测结果均为阳性的样本为116份,均为阴性的样本数为1 001份,该检测结果与重组抗原免疫印迹法检测结果一致,检测结果不一致的样本数为6份,该6份样本中TPPA检测法均为阳性,HISCL检测法均为阴性,但在RIBA检测结果中仅1份为阳性,5份为阴性;HISCL 检测结果与RIBA检测结果一致有1 122份,符合性为99.91%,TPPA 检测结果与RIBA检测结果1 118例,符合性为99.55%,差异无统计学意义(P>0.05)。结论 HISCL与TPPA 2种检测方法的检测结果与重组抗原免疫印迹法均具有较高的符合性,但在实际操作过程中HISCL方法具有可以更好地实现自动化、样本分析时间短、操作简单便捷、结果可靠的特点,在大批量样品检测中具有一定的优势。
关键词:高敏化学发光;梅毒螺旋体明胶凝集试验;梅毒特异性抗体;结果符合性
中图分类号:R446文献标识码:A文章编号:1009-8011(2022)-11-0-03
梅毒螺旋体是引起梅毒的主要病原体,具有传染性,患者发生皮肤损害时的破损处、血液、乳汁、精液以及唾液中均有梅毒螺旋体存在,与梅毒患者的溃疡处或皮肤破损处密切接触,都有可能发生传染,性传播与血液传播是主要的传播途径,而且梅毒螺旋体可以通过胎盘屏障引起母婴传播[1-3]。梅毒作为我国乙类传染病中的一种,为保证医护人员以及医院医疗环境的安全,在手术、输液等医学操作前均需要进行梅毒筛查。在医学检验过程中,检测结果的可靠性与可操作性是临床检验学科中对检测方法的可应用性评价的主要因素,目前临床上常用的检测方法为梅毒螺旋体明胶凝集试验(treponema pallidum particle assay,TPPA),该方法具有较高的灵敏度与特异性,但是其检测过程中步骤相对复杂、检测时间长,对大批量样本检测时存在困难。在保证准确率的前提下,寻找新的检测方法以提高检测效率与可操作性是检验人员首要考虑的。在本研究中,通过对1 123份血清样本同时进行TPPA与高敏化学发光法(high sensitivity chemical iuminescence method,HISCL)进行梅毒螺旋体检测,并与金标准重组抗原免疫印迹法(rebinant immunoblot assay,RIBA)进行比较,探讨2种方法的符合性与准确度,为HISCL的临床应用提供参考。
1 资料与方法
1.1 一般资料
选择2018年11月~2019年12月山东省新泰市皮肤病防治所采集的1 123份临床检测的血清样本为研究对象,其中男517例,女606例;年龄7~68岁,平均年龄(39.8±3.32)岁。本研究经山东省新泰市皮肤病防治所伦理委员会批准后开展。所选的样本对象对此次研究开展均知情同意。
1.2 纳入与排除标准
纳入标准:①患者年龄≤70岁;②患者需要进行梅毒生化筛查;③临床资料完整。
排除标准:①伴血液疾病者;②伴免疫性系统病症者。
1.3 仪器与试剂
HISCL:①HISCL-5 000全自动化学发光免疫分析仪[生产企业:希森美康株式会社,产地:日本,注册证编号:国械注进20192221950,结构及组成:该产品是由加样模块、反应模块、检测模块、数据处理模块、温控模块、清洗模块、气动装置、软件(发布版本号:Ver.00-13)组成];②梅毒螺旋体抗体检测试剂包(HISCL)(生产企业:奥森多临床诊断(英国)有限责任公司Ortho Clinical Diagnostics,产地:日本,注册证编号:国械注进20173401367,规格:100测试/包装),③梅毒螺旋体抗体校准品HISCL Anti-TP Calibrator[生产企业:Japan Lyophilization Laboratory,产地:日本;注册证编号:国械注进20183402426,结构及组成:梅毒螺旋体阴性校准品(HISCL TP NC)、梅毒螺旋体阳性校准品(HISCL TP PC)]。
TPPA:梅毒螺旋体抗体检测试剂盒,方法为凝集法(生产企业:富士瑞必欧株式会社FUJIREBIO INC,注册证编号:国械注进20173406813,结构及组成:由溶解液、血清稀释液、致敏粒子、未致敏粒子、阳性对照血清组成,盒内还包含滴管)。
RIBA:梅毒螺旋体IgG抗体检测试剂盒(间接免疫熒光法)[生产企业:欧蒙医学实验诊断股份公司EUROIMMUN Medizinische Labordiagnostika AG,注册证编号:国械注进20163402984,结构及组成:生物载片、异硫氰酸荧光素(FITC)标记的二抗、阳性对照、阴性对照、磷酸盐(PBS)、吐温 20、FTA吸附剂、RF吸附剂,试剂盒中还包含封片介质和盖玻片]。
梅毒螺旋体抗体质控品[生产企业:奥森多临床诊断(英国)有限责任公司Ortho Clinical Diagnostics,注册证号:国械注进20173401360,结构及组成:VITROS梅毒TPA质控品1和2(含有抗菌剂的人体血浆)]。749A67E7-4AF0-4AD6-94CB-60315305E7B6
1.4 方法
血清样本的制备:采患者空腹时静脉血,自然凝固20 min后,以4 ℃、3 000 转/min条件下离心20 min,取上清,待测。对全部血清样本分别采取HISCL、TPPA与RIBA 3种方法进行梅毒螺旋体检测,以RIBA为金标准,对2种检测方法的结果进行符合性分析。以上样品检测均由2名熟悉检测过程的检验人员(具有1年及以上同方法检测经验)进行。
HISCL:以HISCL-5 000全自动免疫分析仪操作规程以及试剂包的使用说明书按照检测程序进行操作,在检测前对全自动免疫分析仪的仪器性能进行检测,梅毒螺旋体抗体质控品检测后且其结果符合质控要求后,方可进行样本检测,在检测的同时,同时对梅毒螺旋体阴性校准品(HISCL TP NC);梅毒螺旋体阳性校准品(HISCL TP PC)进行同步检测,测定血清样本的发光强度。结果判断:以临界值指数(cut-off Index,COI)为最终结果进行判定,阴性:COI<1.0,阳性:COI>1.0。
TPPA:按照梅毒螺旋体抗体检测试剂盒(凝集法)说明书与TPPA法检验操作规程要求进行操作:在微量反应板第1孔中加入血清稀释液,采取微量滴管或移液枪每次吸取25 μL,共4次;在第2、3、4孔中加入25 μL;随后采取微量滴管或移液枪加入样品,第1孔加入25 μL,第2、3、4孔以2n的方式进行加入。并将25 μL致敏粒子加入第3孔中。将微量反应板放在平板混合器上振荡30 s(力度:内容物不得溅出),盖上盖子后于15~30 ℃条件下水平静置。2 h后,将反应液用观察镜观察或利用免疫稀释判定装置,记录现象并进行结果判定。结果判定:第1种:粒子的聚集状态为纽扣状,外周边缘均匀、平滑的图形则为阴性(-);第2种:粒子的聚集形状外周边缘均匀且平滑的圆形,其状态为小环状,则为不确定性(±);第3种:粒子外周边缘也不均匀且杂乱地凝集在周围,环明显变大,则为阳性(+);第4种:产生均一的凝集,呈膜状延展则为强阳性(++)。
当在该方法中出现阳性结果,则将样品按照下述方法继续进行试验:在微量反应板第1孔中加入血清稀释液,采取微量滴管或移液枪每次吸取25 μL,共4次;在第2、3、4孔中加入25 μL;随后采取微量滴管或移液枪加入样品,第1孔加入25 μL,第2、3、4孔以2n的方式进行加入。并将25 μL未致敏粒子加入第3孔中,并将25 μL致敏粒子加入第4孔至最后一孔。将微量反应板放在平板混合器上振荡30s(力度:内容物不得溅出),盖上盖子后于15~30℃条件下水平静置。2 h后,将反应液用观察镜观察或利用免疫稀释判定装置,记录现象并进行结果判定。在试验过程中需要进行对照试验。结果判定:阳性:最终稀释倍数为1∶40的未致敏粒子的反应图像判定为(-),最终稀释倍数1∶80以上致敏粒子的反应图像判定为(+)时,最终判定为阳性,并将最终显示出反应图像为(+)时的最终稀释倍数作为抗体效价;阴性:无论未致敏粒子呈现何种反应图像,只要最终稀释倍数1∶80致敏粒子的反应图像显示为(-)时,最终判定即为阴性。
RIBA:按照试剂盒说明书进行操作,结果与参比卡进行比较,印迹膜条上出现2条及以上相对分子质量为 4.7×104、1.7×104和1.4×104 的特异性色带时,结果判为阳性;结果为一条特异度条带时,结果判为可疑;反之则为阴性;可疑结果需要进行后续临床观察与复测。
1.5 评价标准
2种检测结果符合性分析:统计HISCL与TPPA两种检测方法中阴性结果与阳性结果,并将检验结果与RIBA法检测的结果进行分析,分析两种方法与RIBA法检测结果的符合性。计算公式:符合性=A/B×100%(A:各方法与RIBA检测结果相同的样本量;B:总样本量)
1.6 统计学分析
采用统计学软件SPSS 25.0进行统计分析。计数资料采用[n(%)]描述,数据组间差异比较采用χ2检验。P<0.05表示差异有统计学意义。
2 结果
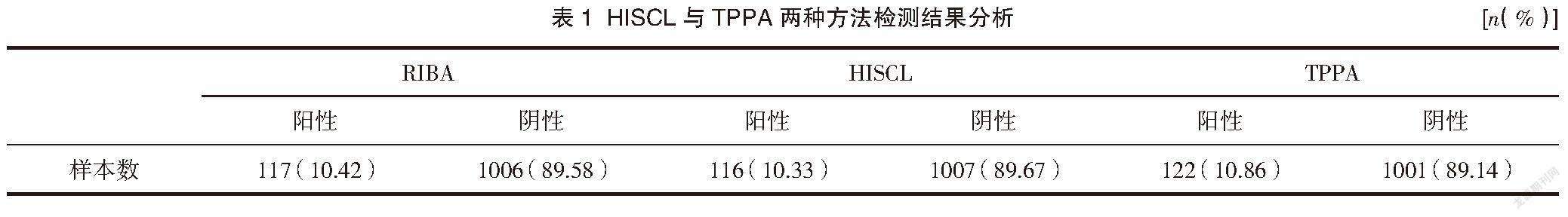
2.1 HISCL与TPPA检测结果分析
在1 123份临床检测的血清样本中,RIBA检测结果中,1 006份为阴性,117份为阳性;HISCL与TPPA 2种方法检测结果均为阳性的样本为116份,均为阴性的样本数为1 001份,检测结果不一致的样本数为6份,该6份样本中TPPA检测法均为阳性,HISCL检测法均为阴性。HISCL 检测结果与RIBA检测结果一致有1 122份,符合性为99.91%(1 122/1 123),TPPA 检测结果与RIBA检测结果1 118份,符合性为99.55%(1 118/1 123),差异无统计学意义(P>0.05)。见表1。
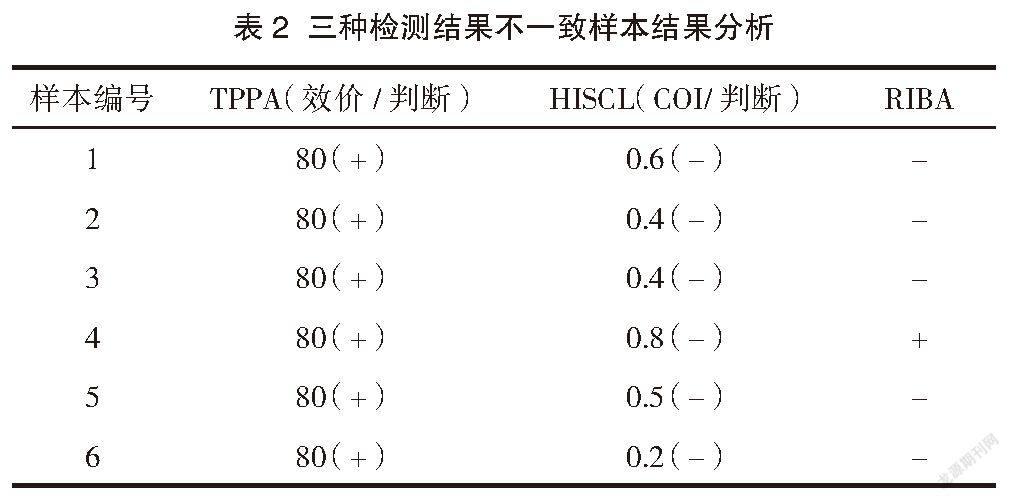
2.2 3种检测结果不一致样本结果分析
将6例结果不一致的样本的检测结果进行分析。见表2。
3 讨论
研究统计发现,近年来,梅毒的发生率不断呈递增趋势增加。根据全国性控制中心统计发现,梅毒的病例数于1994年开始增长幅度显著。梅毒不仅危害着患者的身体健康,同时作为传染病,可以通过血液等途径进行传播,如若未加控制,会引起公共卫生问题,因此在进行手术、侵入性检查、输液等医学手段实施前需要对患者进行梅毒筛查。随着检测技术的不断发展,目前应用在临床上针对梅毒检测的方法有免疫印迹法、胶体金法、酶联免疫吸附法、明胶凝集试验、化学发光分析法等。本研究将RIBA作为金标准,分析对比HISCL与TPPA的检测效果。将RIBA作为金标准其原因是,RIBA是以重组基因抗原转印到载体上,检测相应抗体的酶免疫试验方法,该方法与免疫印迹法具有相同之处,通过SDS-PAGE进行不同分子量的蛋白片段进行分离,不同之处是在于特异性抗原不通过电泳分离转运,而是直接分条通过电转移加在固相膜上,对其进行酶免疫定位,SDS-PAGE的高分辨力和ELISA法的高特异性和敏感性,避免了其他蛋白对反应的干扰,RIBA的反应原理主要是采取硝酸纤维素膜对各种不同的抗原成分进行吸附,在膜上以线条的形式显现,将不同的抗原进行收集并与标本(一抗)和酶标二抗混合,在适宜的条件下进行温育和洗涤,并与底物反应,当样本中存在具有针对吸附抗原的特异性抗体时,出现显色反应,通过对条带的位置以及分子量大小判断结果。明胶凝集试验的实施,由于该方法容易出现假阴性、检测过程复杂、实验人员主观参与度較高、耗时长、占用检验资源多等缺点,已逐渐被其他检测方法替代[4-5]。分子发光光谱分析法已经得到了广泛的应用,其中高敏化学发光法是其中的一种[6],在临床上用于定性或者定量检测人血清或血浆中的特定物质,包括蛋白质和多肽、感染症、激素、肿瘤标记物、凝血分子等项目,具有广泛的应用。该产品基于化学发光酶免疫测定原理,与配套检测试剂共同使用,待测物浓度与化学发光强度在一定检测范围内呈线性关系[7],仪器通过光学检测对体系产生的光强度进行检测并进行换算,从而得到待测物质具体的含量或浓度,该方法具有高灵敏度、高特异性与宽线性范围[8]。该方法使用的样本量极少,所有项目仅需要10~30 μL,检测时间短,仅需要15~17 min,一次性检测样本数量为100份,结果直观,避免了人为判断的误差。使检验分析过程流程化、机械化,节省了医疗资源,提高了检验效率与检验结果的可靠性。749A67E7-4AF0-4AD6-94CB-60315305E7B6
在本研究中,在1 123份临床检测的血清样本中,HISCL与TPPA 2种方法检测结果均为阳性的样本为116份,均为阴性的样本数为1 001份,该检测结果与重组抗原免疫印迹法检测结果一致,检测结果不一致的样本数为6份,该6份样本中TPPA检测法均为阳性,HISCL检测法均为阴性,但在RIBA检测结果中仅1分为阳性,5份为阴性;HISCL 检测结果与RIBA检测结果一致有1 122份,符合性为99.91%,TPPA 检测结果与RIBA检测结果1 118份,符合性为99.55%,差异无具有统计学意义(P>0.05)。
综上所述,HISCL与TPPA 2种检测方法的检测结果与均具有较高的符合性,但在实际操作过程中HISCL方法具有可以更好地实现自动化、样本分析时间短、操作简单便捷、结果可靠的特点,在大批量样品检测中具有一定的优势。
参考文献
[1]景文博,姚秀.梅毒螺旋体明胶凝集试验定量检测在神经梅毒诊疗中的临床意义研究[J].贵州医药,2021,45(5):802-803.
[2]蓝蔚蔚,陈颖,蓝海鹰,等.不同检测法对血清梅毒螺旋体抗体的检测价值[J].现代实用医学,2020,32(5):479-481.
[3]高洪元.三种不同血清学方法对梅毒螺旋体抗体的检测效果比较[J].检验检疫学刊,2020,30(3):76-78.
[4]符颖,陈菊香,何瑞英,等.3种不同梅毒血清学实验方法在临床中的应用价值及效能比较[J].中国性科学,2018,27(10):121-123.
[5]杨卫华,王文惠,杨乐园,等.高敏化学发光法检测血清梅毒特异性抗体临床应用价值[J].国际检验医学杂志,2019,40(16):1973-1975,1979.
[6]杨雅琼,官士珍,方琳,等.高敏化学发光法在输血患者梅毒筛查中的应用评价[J].中国输血杂志,2019,32(4):381-383.
[7]郭靖,姜小建,王鑫,等.化學发光法在梅毒螺旋体特异性抗体检测中的应用[J].山西医药杂志,2020,49(24):3477-3479.
[8]钟敏,赖章辉.化学发光免疫分析法检测梅毒抗体在早期梅毒诊断中的应用价值分析[J].首都食品与医药,2021,28(14):110-111.749A67E7-4AF0-4AD6-94CB-60315305E7B6

