超高效液相色谱-四极杆/静电场轨道阱高分辨质谱法非靶向筛查苹果中苯脲类农药
岳 宁,李晓慧,李敏洁,王 琦,邵 华,郑鹭飞,王 静,金 芬
(中国农业科学院农业质量标准与检测技术研究所,北京 100081)
我国是苯脲类农药的生产和使用大国,苯脲类农药主要用作除草剂和杀虫剂,其中苯脲类除草剂(Phenylurea herbicides,PUHs)作为光合系统电子传递抑制剂,在世界范围内广泛使用,主要用于防治果园及大田作物中的禾本科杂草和阔叶杂草[1];而苯甲酰脲类杀虫剂(Benzoylurea insecticides,BPUs)主要是在PUHs 的结构骨架上引入苯甲酰基和卤素取代基[2],可干扰目标害虫的几丁质合成[3],是防治农产品抗性害虫的主要农药品种之一。然而,苯脲类农药的水溶性高,多具有内吸性,在土壤中残留的半衰期长,对农产品和地下水可能造成污染[4-8]。美国环境保护总局(EPA)将敌草隆和杀铃脲等苯脲类农药定为Ⅲ类毒性或Ⅳ类毒性[9],欧盟也将其列入优先控制污染物清单[10-11]。近年来,苯甲酰脲类杀虫剂作为第三代杀虫剂,以独特的作用机制和高效的杀虫活性,成为新型农药创制活跃领域之一[12]。为应对新型化合物的发现和预警需求,有必要建立农产品中苯脲类农药的非靶向快速筛查方法。
现有关于农产品以及水体中苯脲类农药的残留分析方法均为靶向分析技术[13-14],无法实现对新型苯脲类农药的快速非靶向筛查。近年来,超高效液相色谱-四极杆/静电场轨道阱高分辨质谱(UPLCQ/Orbitrap HRMS)由于具有分析时间短、选择性高及分辨率高等特点[15],在新型危害物和天然产物质谱裂解规律研究中的应用日益增多。目前,该技术已成功用于农产品中有机磷类等农药残留、苏丹红等食品添加剂及大环内酯类等兽药残留的快速非靶向筛查[16-18]。然而,目前尚无基于质谱特征碎裂规律的苯脲类农药残留高分辨质谱快速筛查方法的报道。
本研究采用UPLC-Q/Orbitrap HRMS 技术解析了13 种PUHs 和9 种BPUs 共22 种苯脲类农药的特征离子碎片和特征中性丢失。将22 种苯脲类农药按取代基的不同分为4 类,并分析了其主要裂解途径、特征碎片离子和规律,并将基于该特征裂解规律的筛查方法应用于北京市售苹果中苯脲类农药的非靶向筛查,为苯脲类农药残留的快速筛查提供参考。
1 实验部分
1.1 仪器与试剂
超高效液相色谱仪(Vanquish Flex UHPLC Systems,美国Thermo Fisher 公司);四极杆/静电场轨道阱高分辨质谱仪(Q Exactive HF-HRMS 质谱仪,美国Thermo Fisher 公司);Milli-Q 超纯水器(美国Millipore公司)。
乙腈、甲醇、甲酸均为色谱纯,购自美国Fisher 公司。N-丙基乙二胺(PSA,50 μm)、十八烷基键合硅胶(C18,50 μm)分散固相萃取吸附剂,购自美国Sigma-Aldrich 公司;13 种苯脲类除草剂标准品,纯度>98.7%,购自德国Dr.Ehrenstorfer 公司;9 种苯甲酰脲类杀虫剂标准品,质量浓度均为100 μg/mL,购自农业部环境保护科研监测所。12 批红富士苹果样品分别于2021 年10 月购自北京地区的3 个超市。
1.2 标准溶液配制
分别称取13 种苯脲类除草剂标准品,用甲醇溶解并定容配成100 μg/mL 的标准储备液;准确量取13种苯脲类除草剂和9种苯甲酰脲类杀虫剂的储备液(100 μg/mL),用甲醇稀释定容配制成200 μg/L 的混合标准溶液,待分析。
1.3 仪器条件
色谱条件:色谱柱:Acquity BEH C18色谱柱(100 mm×2.1 mm,1.7 μm,美国Waters公司)。柱温:40 ℃;流动相:A 相为0.1%的甲酸水溶液,B 相为甲醇;流速0.4 mL/min;进样量5 μL。流动相梯度洗脱程序:0~1.0 min,90%A;1.0~2.0 min,90%~70%A;2.0~4.0 min,70%~40%A;4.0~5.0 min,40%~0%A;5.0~9.0 min,0%A;9.0~9.1 min,0%~90%A;10.0 min,90%A。
质谱条件:离子源:热电喷雾离子源(HESI);离子模式:正离子;归一化碰撞能(NCE):20%、40%、60%;鞘气流速:40 Arb;辅助气流速:10 Arb;喷雾电压:3.50 kV;毛细管温度:320 ℃;辅助气加热温度:300 ℃;脱溶剂气和锥孔气:氮气。标准品扫描模式:平行反应监测模式(PRM):通过Xcalibur Instrument Setup 软件界面Global lists 中Iclusion List 输入22 种苯脲类化合物的分子式;分辨率:90 000;S-lens电压:55 V;隔离窗口:2.0 u;样品扫描模式:数据采集使用一级母离子全扫描和数据依赖的二级子离子扫描模式(Full MS/dd-MS2),质量扫描范围m/z100 ~1 500。一级分辨率:70 000,二级分辨率:17 500。自动增益控制进入轨道阱中的离子数(AGC target)为1e6,最大注入时间为100 ms。
1.4 样品前处理
参照国家标准GB 20769-2008[19]进行样品前处理。准确称取10.00 g(精确至0.01 g)样品匀浆于50 mL塑料离心管中,加入10 mL乙腈混合,涡旋(转速为2 000 r/min)提取5 min,放冷,在室温条件下以6 000 r/min离心5 min。取1 mL上清液加入装有30 mg PSA和25 mg C18净化剂混合物的2 mL塑料离心管中,涡旋5 min 后,在室温条件下以6 000 r/min 离心5 min,取上清液经0.22 μm 微孔滤膜过滤,供进样分析。
2 结果与讨论
2.1 正离子模式下苯脲类农药的质谱分析
根据基本结构骨架,苯脲类农药可分为苯脲类除草剂(PUHs)和苯甲酰脲类杀虫剂(BPUs)两大类。其中PUHs 的基本结构骨架由脲基和苯环两部分构成(图1A);而BPUs 是在PUHs 的结构骨架基础上引入苯甲酰基活性亚结构和卤素取代基,其基本结构骨架包括苯甲酰基、脲桥和苯胺三部分。不同的BPUs结构差异主要体现在酰胺、苯甲酰基和苯胺上取代基的不同。因此根据苯甲酰基上卤素取代基的不同,可将BPUs 分为氟原子取代的BPUs(图1B)和氯原子取代的BPUs(图1C)。典型PUHs 和BPUs 中不同取代基的具体信息见表1。

图1 苯脲类农药的一般结构通式Fig.1 General structural formulas of phenylurea pesticides

表1 苯脲类农药结构通式中R取代基的详细信息Table 1 The substituents of general structural formula of phenylurea pesticides

(续表1)
本研究22 种苯脲类农药的分子离子精确质量数和主要特征离子碎片的信息见表2。在正离子模式下,13 种PUHs 和9 种BPUs 均可产生特征明显的准分子离子峰[M+H]+,其准分子离子峰的精确质量数与理论值的偏差小于5×10-6(表2),可作为定性依据。4 类典型PUHs 和BPUs 的二级全扫描质谱图见图2。

图2 典型PUHs(A、B)和BPUs(C、D)的二级全扫描图Fig.2 Secondary full scan spectra of typical PUHs(A,B)and BPUs(C,D)

表2 13种苯脲类除草剂和9类苯甲酰脲类杀虫剂的高分辨质谱数据Table 2 High resolution mass spectrometric data of 13 PUHs and 9 BPUs
2.2 质谱裂解途径
2.2.1 PUHs 的主要裂解途径根据取代基R3(甲基或甲氧基)的不同,PUHs可分为2种亚型。其中,绿麦隆等9 种PUHs 的取代基R3均为甲基,其准分子离子[M+H]+发生断裂,产生特征碎片离子N,N-二甲基酰胺结构[(CH3)2NCO]+(m/z72.044 59);[M+H]+也可丢失中性分子二甲胺(m/z45.058 03)得到特征离子碎片[C6H3NHCOR1R2]+,或氢原子重排后发生脲基中碳氮键断裂得到特征离子碎片[C6H3NH3R1R2]+。绿麦隆的特征离子碎片的主要裂解途径见图3。

图3 绿麦隆的主要裂解途径Fig.3 Proposed fragmentation pathways of chlorotoluron
而绿谷隆、溴谷隆、利谷隆和氯溴隆等4 种PUHs 的取代基R3均为甲氧基。该亚类PUHs 的准分子[M+H]+的裂解与取代基为甲基的PUHs亚型相似,均发生N-甲氧基-N-甲基甲酰胺中氢原子重排,产生特征性离子碎片[C6H3NH3R1R2]+;与之不同的是,取代基R3均为甲氧基的4 种PUHs 的[M+H]+也可发生脲基中氮氧键断裂,分别丢失中性分子甲醇[CH3OH]和卤化氢[HR1],产生特征离子碎片[R1R2C7H6N2OCH3]+和[R2C7H6N2OCH3]+。以绿谷隆为例,特征离子碎片可能的裂解途径见图4。

图4 绿谷隆的主要裂解途径Fig.4 Proposed fragmentation pathways of monolinuron
2.2.2 BPUs 的主要裂解途径根据卤素取代基的不同,BPUs 可分为含氟和含氯原子2 种亚型。其中,除虫脲、氟苯脲、氟虫脲、氟铃脲、氟酰脲、虱螨脲和氟啶脲7种BPUs结构中苯甲酰基上的卤素取代基均为氟原子。与PUHs 相比,含氟BPUs 的准分子离子[M+H]+也可发生脲桥中脲基碳氮键断裂,产生特征离子碎片[C7H3F2ONH3]+(m/z158.040 47),该离子可进一步提示中性分子氨产生特征离子碎片[C7H3F2O]+(m/z141.015 00)。此外,[M+H]+也可丢失中性分子2,6-氟苯甲酰胺结构[C8H3F2O2NH2](m/z183.013 21),产生特征离子碎片[C7H2NOR1R2R3R4]+。以除虫脲为例,特征离子碎片可能的裂解途径见图5。

图5 除虫脲的主要裂解途径Fig.5 Proposed fragmentation pathways of diflubenzuron
杀铃脲和灭幼脲为含氯的BPUs,其准分子离子[M+H]+的裂解途径与含氟的BPUs类似,但由于结构中苯甲酰基上的卤素取代基与除虫脲等不同,[M+H]+裂解产生的部分特征碎片离子的质荷比有所不同,分别为[C7H3ClONH3]+(m/z156.020 22)和[C7H3ClO]+(m/z138.993 82)。与上述苯脲类农药不同的是,杀铃脲和灭幼脲还存在特征碎片离子[C6H5Cl]+(m/z113.015 28),这可能是苯甲酰基结构中酰基与苯环相连的碳碳键断裂后形成共轭结构所致。以杀铃脲为例,特征离子碎片可能的裂解途径见图6。
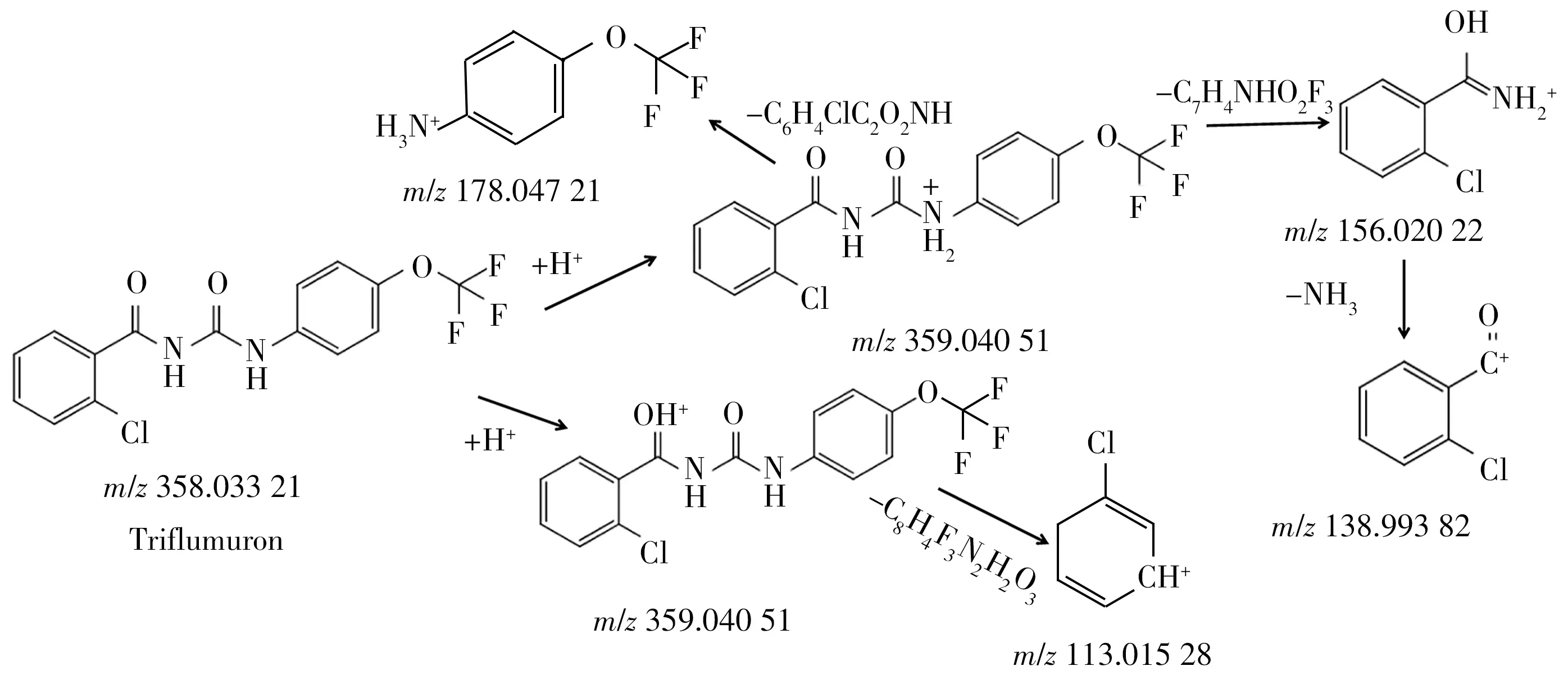
图6 杀铃脲的主要裂解途径Fig.6 Proposed fragmentation pathways of triflumuron
2.3 实际样品测定
应用上述裂解规律,对北京市售12 批苹果样品进行Full MS/dd-MS2模式下的二级离子碎片全扫描,在1 份苹果样品中检测到离子碎片m/z72.044 59 和m/z168.020 85,准分子离子为m/z213.078 96的可疑化合物。根据标识性离子碎片m/z72.044 59推测,该化合物可能是一种苯脲类除草剂,推测碎片m/z168.026 85由准分子离子m/z213.078 96中性丢失(CH3)2NH(m/z45.058 03)产生,因此样品中可能含有绿麦隆。进一步采用标准品进行验证,绿麦隆标准品的保留时间为4.96 min,母离子为m/z213.078 90,子离子为m/z72.044 59、168.020 89、140.999 82。而在实际样品中,该物质的保留时间为4.97 min,母离子为m/z213.078 96,子离子为m/z72.044 59、168.020 85,与标准品的保留时间以及二级质谱信息一致,由此确定样品中含有绿麦隆,验证了本文总结的苯脲类农药的质谱裂解规律。
3 结 论
本文采用UPLC-Q/Orbitrap HRMS 技术在正离子模式下对22 种苯脲类农药的裂解规律进行研究,根据取代基的不同,将22 种待测农药分为4 类,以绿麦隆为代表的9 种含甲基的苯脲类除草剂的主要特征离子碎片为m/z72.044 59,特征丢失中性分子二甲胺(m/z45.058 03);以绿谷隆为代表的4种含甲氧基的苯脲类除草剂发生特征丢失中性分子甲醇或卤化氢产生离子碎片;除虫脲等7 种氟原子取代的苯甲酰脲类杀虫剂的特征离子碎片为m/z158.040 47、m/z141.015 00,特征丢失中性分子2,6-氟苯甲酰胺结构(m/z183.013 21);杀铃脲等2 种氯原子取代的苯甲酰脲类杀虫剂的主要特征离子碎片为m/z156.020 25、m/z138.993 76 和m/z113.015 28。基于上述裂解规律,实现了苹果中苯脲类农药的非靶向筛查。

