响应曲面法优化多电极介质阻挡放电等离子体处理印染废水
蒋香玉,王红涛,樊子文
(太原理工大学 环境科学与工程学院,山西 太原 030024)
近年来,随着染料和纺织行业的快速发展,产生了大量的印染废水,其具有成分复杂、有机物含量高、毒性大、难生物降解的特点[1-3]。低温等离子体水处理技术作为一种高级氧化技术[4-6],因氧化过程无选择性、 氧化性强等特点受到广泛关注[7-8]。
本文利用自制多电极介质阻挡放电反应器对甲基橙溶液进行脱色处理,考察甲基橙溶液的初始浓度、放电时间、通气速率及电源输出电压等参数对降解效果的影响,通过回归模型的建立及显著性检验[9],得到多电极介质阻挡放电中试反应器处理甲基橙溶液的最佳参数。
1 实验部分
1.1 材料与仪器
甲基橙,分析纯。
CTP-2000K等离子电源;AL-104分析天平;2000型可见分光光度计;LZB-10玻璃转子流量计;PC-07数字调制器。
1.2 实验方法
本实验采用多电极介质阻挡放电等离子体处理装置见图1、图2。反应装置容积为15 L,总高60 cm,长宽均为25 cm;三根直径φ14 mm螺丝不锈钢棒作为高压电极,置于石英璃管(外径2.5 cm,内径2.0 cm,管壁厚0.25 cm)内,反应装置内液体作为低压电极,气体通过装置顶部的进气管进入石英玻璃管进行电离后,携带电离过程产生的臭氧等活性粒子通过底部曝气装置分散于有机溶液内部,活性粒子与有机污染分子接触反应,更有利于有机物的降解[10]。

图1 低温等离子体发生器示意图及实物图片Fig.1 Schematic and physical picture of low temperature plasma generator
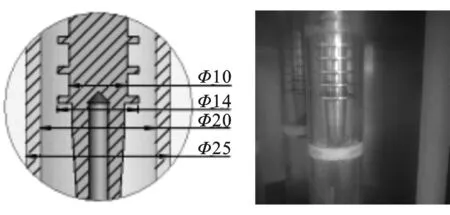
图2 电极部分示意图及实物图Fig.2 Electrode section diagram and physical diagram
1.3 甲基橙溶液浓度测定
甲基橙的最大吸收波长为465 nm[1]。配制一定浓度的甲基橙溶液,制作甲基橙溶度的标准曲线,见图3。

图3 甲基橙溶液标准曲线图Fig.3 Standard curve of methyl orange solution
由图3可知,浓度在0~20 mg/L 的范围内甲基橙的浓度和吸光度满足朗伯比尔定律。故当测量甲基橙的浓度时,需要将其稀释到 20 mg/L以下,以便测量的甲基溶液的吸光度与浓度成线性关系。
甲基橙降解率η=[(A0-A)/A0]×100%
式中,A0为溶液初始吸光度;A为处理后溶液吸光度。
2 结果与讨论
2.1 响应面实验结果
以甲基橙初始浓度、反应时间、通气速率和电源输出电压为主要考察因素,采用Box-Behnken实验原理设计了4因素3水平的响应面实验,因素水平及实验结果分别见表1、表2。
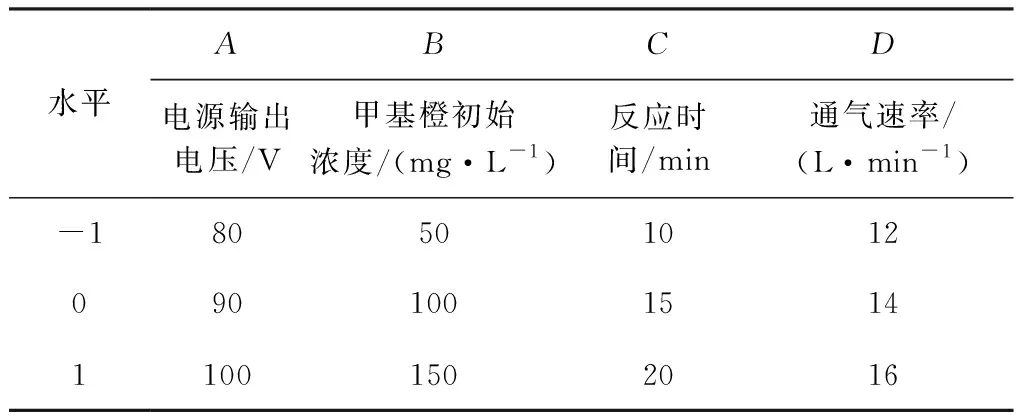
表1 响应面因素水平表Table 1 Response surface factor level table
对表2响应曲面实验结果利用Design Expert软件,进行多元回归拟合,得到甲基橙溶液降解率的二次多项回归方程:Y=55.08+3.83A-19.04B+14.14C+1.15D+2.20AB-0.30AC+0.15AD-4.35BC+0.18BD-0.025CD-5.04A2-4.05B2+0.30C2-4.46D2,回归方程系数显著性检验及方差分析见表3。

表2 响应曲面实验结果Table 2 Experimental results of response surface
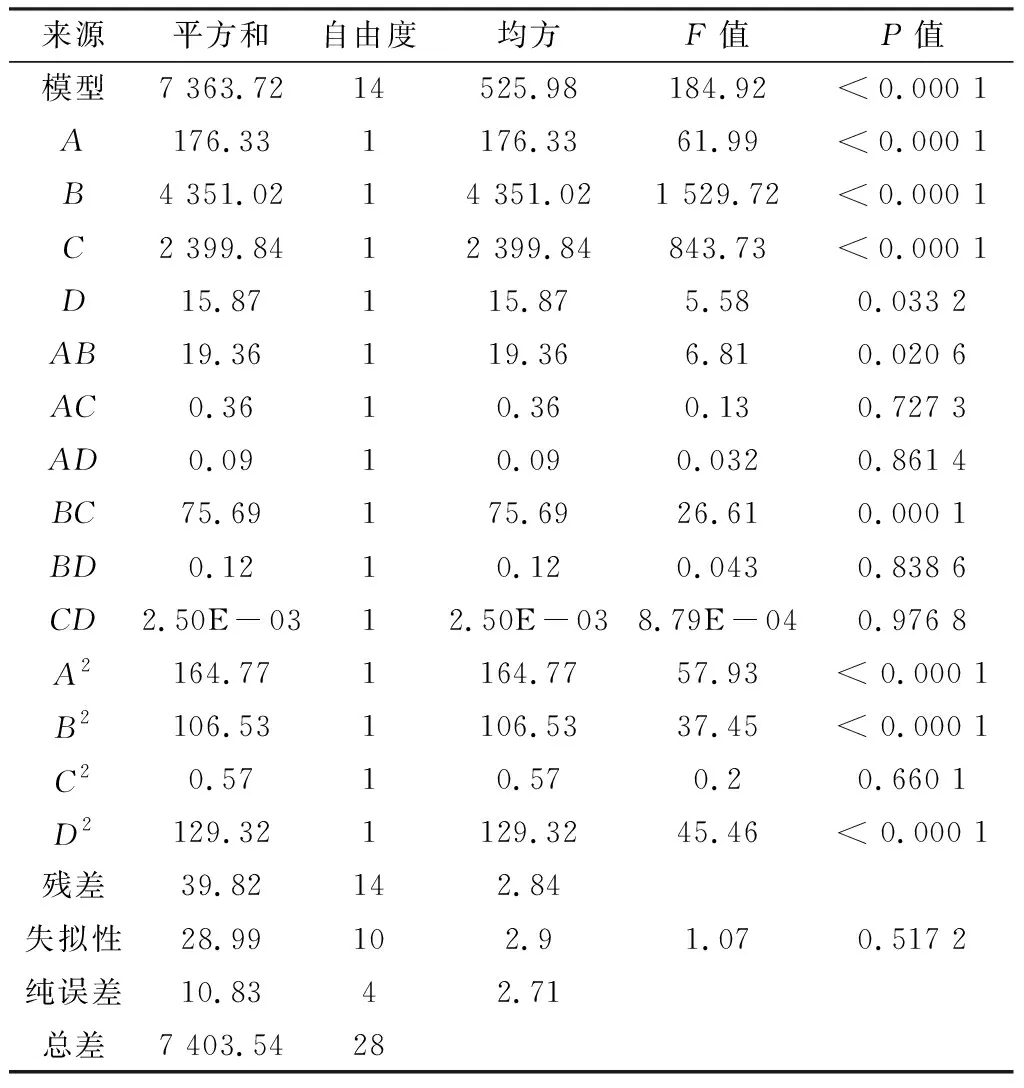
表3 回归方程系数显著性检验及方差分析Table 3 Significance test and variance analysis of regression equation coefficients
2.2 响应曲面分析
取其中任意两个因素及其交互作用,固定其他因素保持不变,得到响应曲面图见图4。
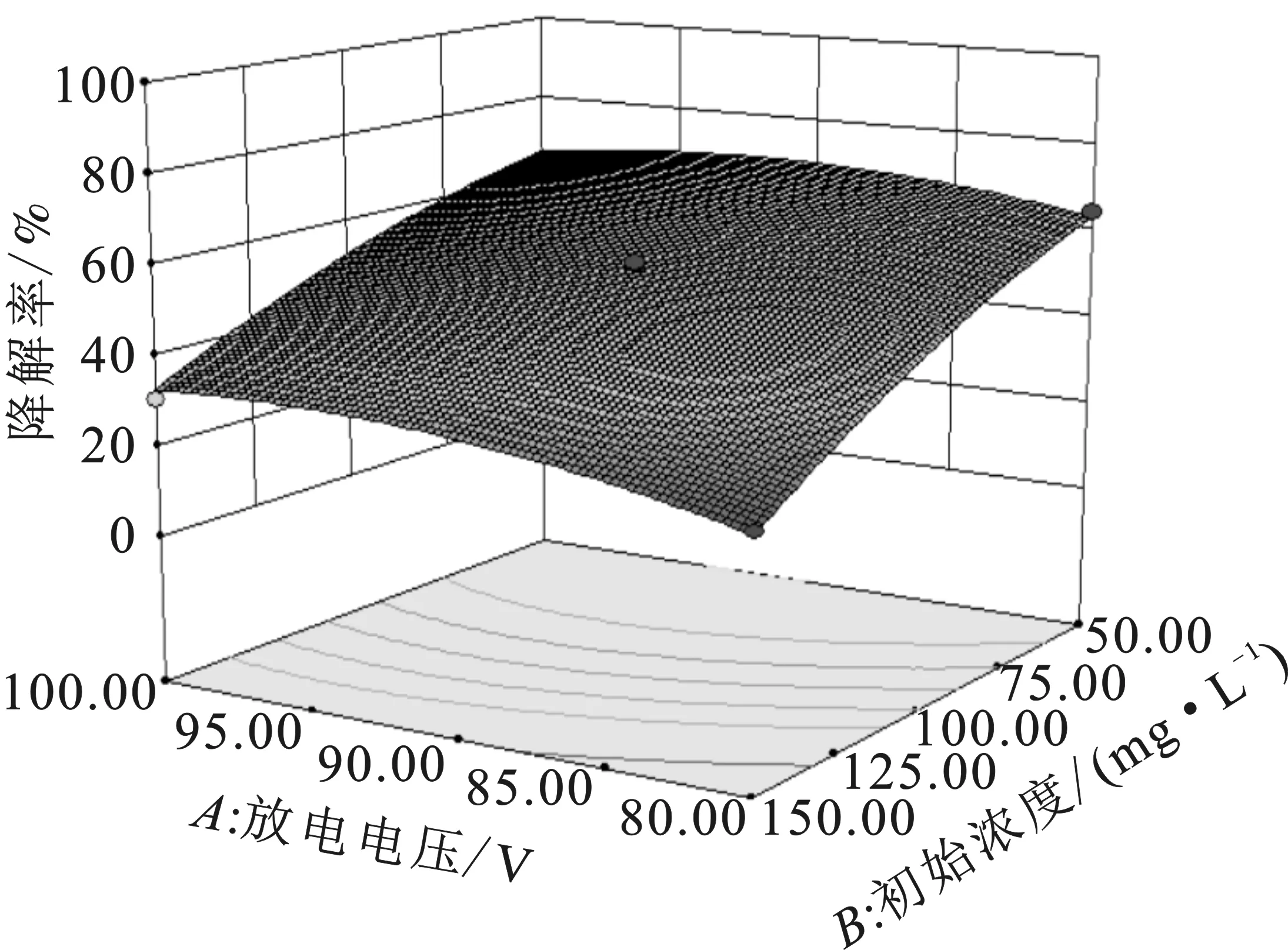
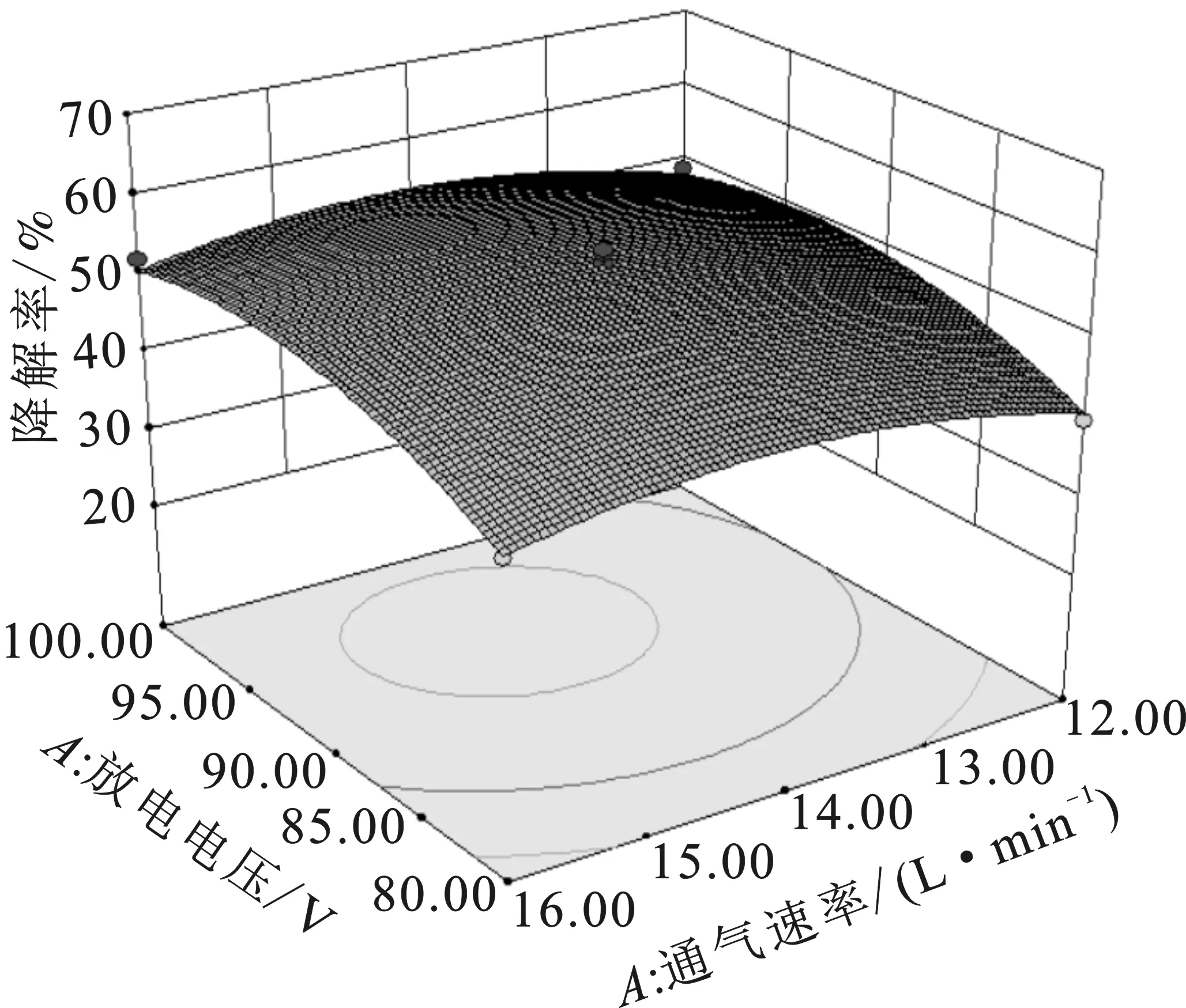

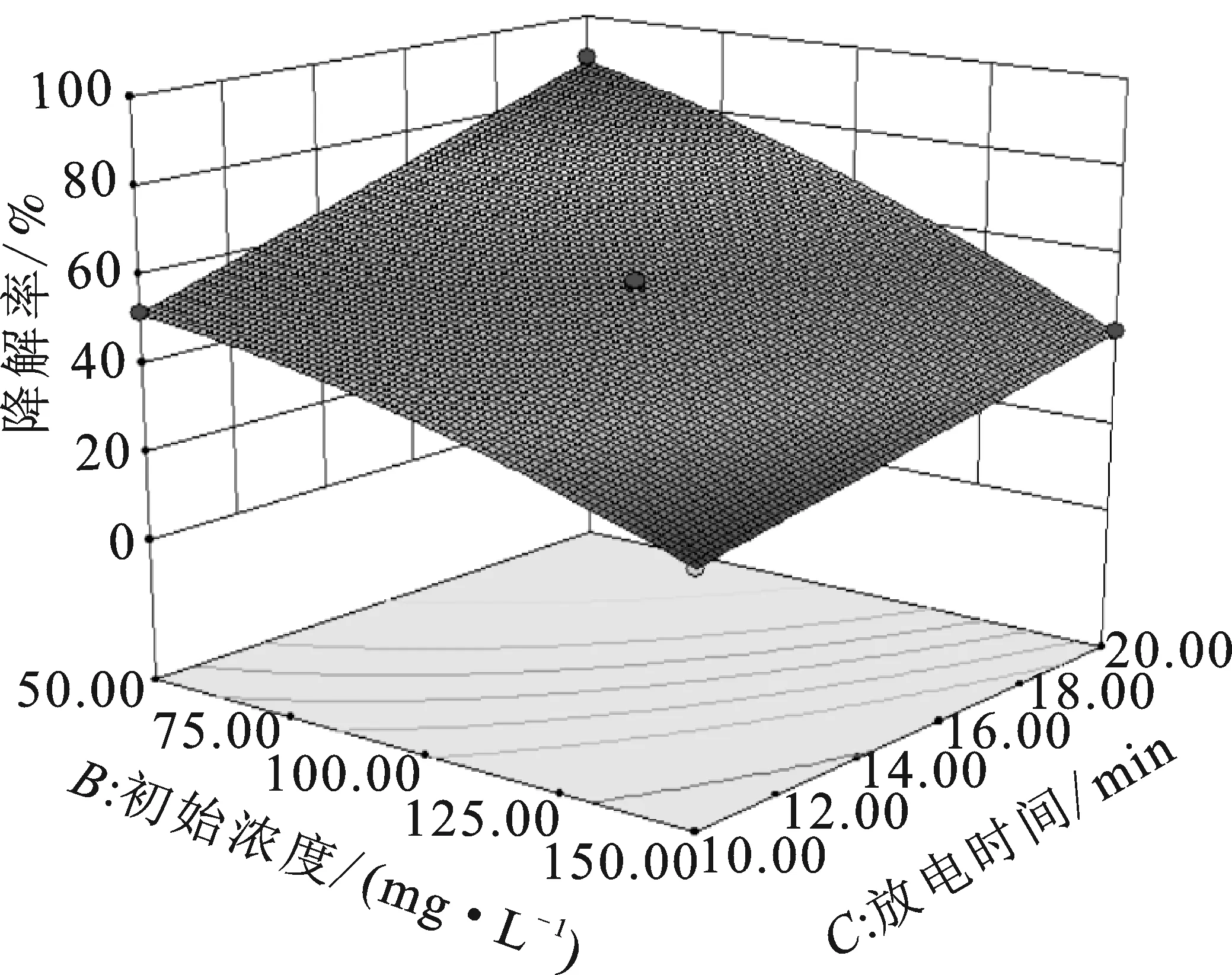
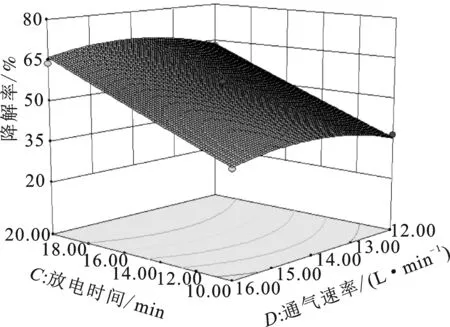
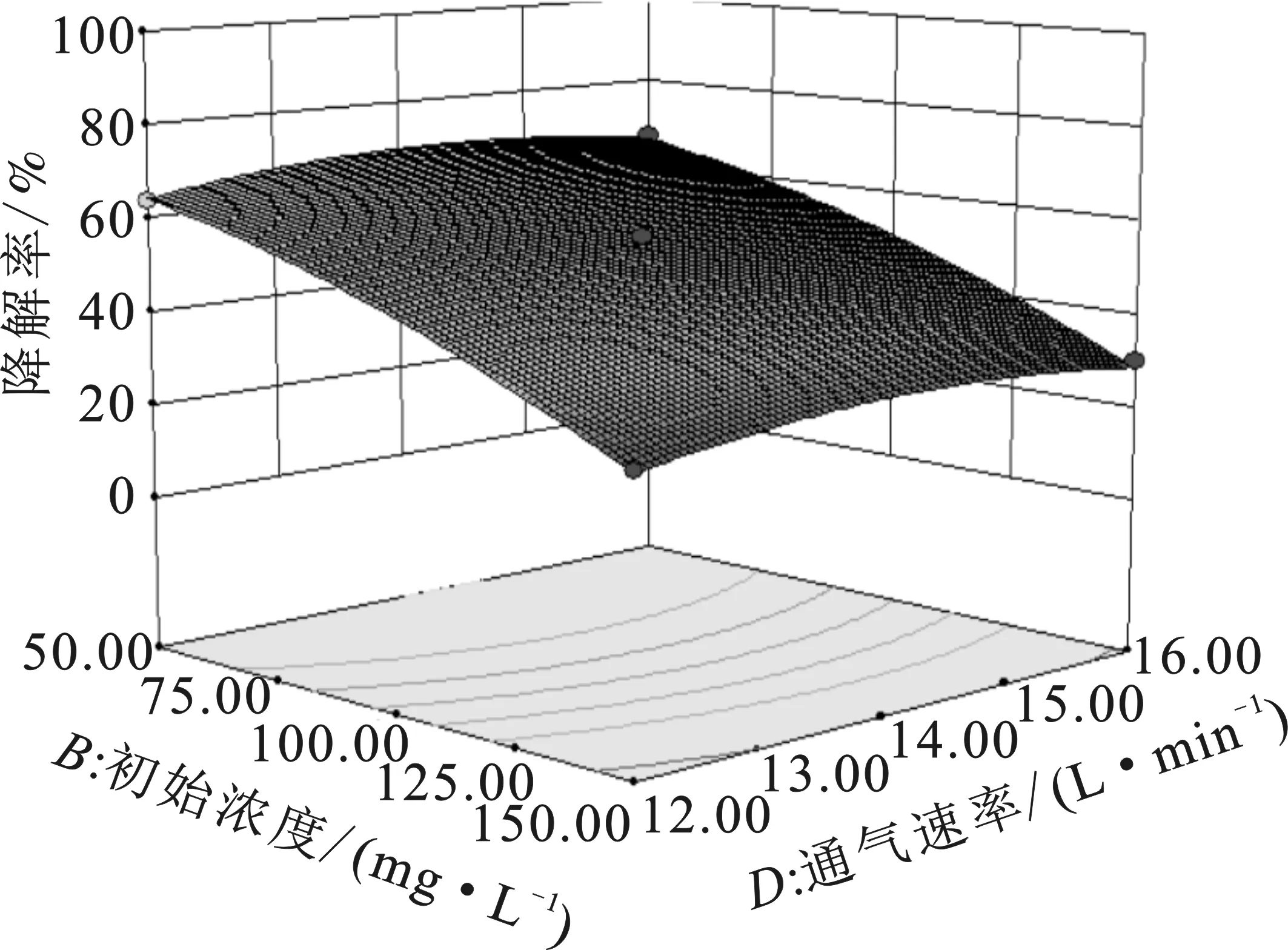
图4 甲基橙初始浓度、放电电压、放电时间、 通气速率交互影响甲基橙降解率模拟曲面图Fig.4 Methyl orange initial concentration,discharge voltage,discharge time,and aeration rate interactively affect the degradation rate of methyl orange
由图4可知,甲基橙溶液初始浓度、放电电压、通气速率和放电时间都在该反应体系中对等离子体降解甲基橙有一定影响。3D响应面图中,响应面越陡,表明因素影响越大[11]。由图4可知,初始浓度和放电时间对甲基橙降解率的影响最大。随着放电时间的增加和初始浓度的减少,甲基橙溶液降解率均有显著提高。介质阻挡放电反应器放电参数确定后,单位时间内产生的活性物质的量是相对稳定的,随着反应时间的延长,参与反应的活性物质变多,甲基橙的降解率也随之提高。单位时间内溶液中的有机物与活性物质的反应量是一定的,所以当溶液初始浓度增加时,故呈现出降解率变低的现象,但随着时间的推移,最终都能达到较高的脱色效果。
放电电压及通气速率的增加对甲基橙的降解效率则呈现出先增加后减少的规律。介质阻挡放电的强度由于电压的升高而增加,产生活性物质效率也增加,甲基橙的降解效率随电压升高而增大;随着电压的继续升高,介质阻挡放电的热效应也越来越明显,溶液温度升高,导致放电产生的活性物质中起主要脱色作用的臭氧溶解度降低及臭氧分解,从而导致甲基橙降解率的降低[12-14]。甲基橙的降解效果随通气量的增加先增大后减少,原因是通气速率较小时,放电空间中的O2较少,导致产生少量O3,同时较低的通气速率,对溶液搅拌效果差,导致O3利用率低。当通气速率过快时,导致介质阻挡放电产生的O3不能充分和有机分子接触而逸出,O3等活性物质的效率也会变低。
基于交互效应分析可知,同时增加反应时间、降低甲基橙初始浓度,降解率提升效果最显著,而放电电压及通气速率有最佳的中间值。
2.3 参数优化与对比实验
通过响应曲面优化,得到最优参数为放电电压91.37 V,初始浓度为50 mg/L,放电时间为20 min,通气速率为14.20 L/min,预测甲基橙降解率最大值为88.99%。为验证预测结果,在最优实验条件下进行3组测定,甲基橙降解率,见表4。

表4 最优参数下实验值与预测值的比较Table 4 Comparison of experimental and predicted values under optimal parameters
由表4可知,利用模拟得到的甲基橙溶液降解率的预测值与实际值十分接近,误差仅为 0.51%。
3 结论
(1)多电极介质阻挡放电反应器对甲基橙的最佳降解条件如下:放电电压91.37 V,初始浓度为50 mg/L,放电时间为20 min,通气速率为14.20 L/min。 在此条件下,甲基橙的降解率为89.5%,与预测值高度吻合,实验值和预测值仅相差 0.51%,因此,可以使用该模型来分析及预测多电极介质阻挡放电中试反应器在此条件下对甲基橙的降解率。
(2)因素的显著关系为初始浓度>反应时间>放电电压>通气速率。

