甲烷催化双重整过程模拟
庄炜杰, 仇 鹏, 曾泽李, 代正华, 王辅臣
( 华东理工大学资源与环境工程学院,上海市煤气化工程技术研究中心, 上海 200237)
天然气作为一种优质、清洁的能源,对于我国优化能源结构、保护生态环境、提高人民生活质量、促进国民经济和社会可持续发展具有重要意义。在2019年,我国天然气消费量在一次能源消费总量中的占比达8.1%,同比增长9.1%[1]。
目前,有多种可有效利用天然气等气态烃制取合成气的重整工艺[2],其中,甲烷水蒸气重整工艺在1926年已经实现工业化应用[3],是庞大的合成氨和甲醇等工业的基础。工业中通常采用高水碳比(n(H2O)∶n(CH4),2.5~3.0)以减少积碳的生成,所得合成气的n(H2)/n(CO)远大于理论值3[4]。富氢的合成气可用于制氢和合成氨[5],但需要补充额外的CO才能得到合适的n(H2)∶n(CO),以用于费托合成及甲醇合成等其他重要的化工生产。甲烷二氧化碳重整反应能够充分利用甲烷和二氧化碳这两种温室气体来生产合成气,该合成气通常具有较低的n(H2)∶n(CO),可直接用于羰基合成、二甲醚合成、费托合成等反应[6],但由于反应温度较高,催化剂容易发生积碳、烧结现象而降低寿命[7-8]。
甲烷水蒸气二氧化碳双重整过程将上述两种工艺耦合[9],既可以提高催化剂的稳定性[10],减少积碳的生成,又能灵活调节合成气中的n(H2)∶n(CO)以适应多种工艺和工况需求,具有重要的研究意义和工程价值。在工艺方面,Oezkara[11]和Jang等[12]采用Gibbs自由能最小法对甲烷水蒸气二氧化碳双重整过程进行了热力学平衡分析,认为在氧化剂量(n(CO2)+n(H2O))保持不变的情况下,改变水碳比不会影响甲烷的消耗速率;但随着压力增大,二氧化碳的转化率与n(H2)∶n(CO)都逐渐降低;当(n(CO2)+n(H2O))∶n(CH4)大于1.2时可以抑制高温区域积碳的生成。Wu等[13]在甲烷水蒸气二氧化碳双重整工艺中加入氧气形成甲烷三重整过程,通过提高n(H2O)∶n(CH4)、降低n(O2)∶n(CH4)与n(CO2)∶n(CH4)以提高n(H2)∶n(CO)。当n(CH4)∶n(O2)∶n(H2O)∶n(CO2)=1.0∶0.5∶1.0∶1.0,进料温度达到500 ℃以上时,该甲烷三重整反应可自发进行。Minette等[14]提出了一种使用薄涂层结构的Zoneflow反应器用于甲烷双重整工艺,可在低压条件下提高产能,改善热传递并降低压降,与传统的颗粒填充床相比通量提高达25%。
在催化剂制备方面,Itkulova等[15]研制了一种新型Co-Pt/Al2O3催化剂,可在相对较低的温度(700~750 ℃)下对甲烷进行双重整以生产合成气,其中Pt是形成稳定性强、分散度高的还原性双金属纳米粒子的主要因素。任盼盼等[16]研制了一种新型的Ni/ZrO2双重整催化剂,Ni晶粒尺寸小、分散度高并能加强金属-载体的相互作用,提高了催化剂的抗烧结和抗积碳能力。Shakouri等[17]制备了一种新型Ni-Co催化剂,在进料组成为CH433% (摩尔分数,余同)、CO221.5%、H2O 12%、H23.5%以及N230%的沼气中,二氧化碳转化率达到70%,n(H2)/n(CO)为1.8 ~ 2.0。
尽管前人已较为详尽地研究了工艺条件对甲烷双重整过程的影响,但大多基于热力学分析。本文通过Aspen Plus软件建立了甲烷双重整过程的动力学模型,并探究了温度、压力和进料物质的量之比对反应产物以及n(H2)/n(CO)的影响。
1 模型建立
1.1 结构描述
甲烷双重整反应示意图如图1所示。混合原料气经过对流段预热后导入上集气管中,通过上集气管分配至各个转化管。转化管内填充催化剂,原料气自上而下流动,经过反应管内的催化剂床层发生重整反应。反应所需热量由管外燃料气与空气燃烧产生的高温烟气供给,主要传热方式为辐射传热。反应完毕后的高温出口气在下端出口流出,在集气管汇合后进入后续工段[18]。

图1 甲烷双重整反应器示意图Fig. 1 Schematic diagram of methane bi-reforming reactor
1.2 数学模型
利用化学计量反应器模拟非甲烷的烷烃与水蒸气的反应过程和燃料气的燃烧过程,利用平推流反应器模拟甲烷水蒸气二氧化碳的双重整反应,如图2所示。利用Fortran语言编写反应动力学模型、压降模型与传热模型。

图2 甲烷双重整反应过程模拟图Fig. 2 Simulation diagram of methane bi-reforming reaction process
1.2.1 双重整反应的动力学方程 甲烷水蒸气二氧化碳双重整过程的催化转化主要为两个甲烷水蒸气重整反应与水气变换反应,分别如式(1)~式(3)所示。

其动力学模型[19]分别为:

其中:r表示反应速率;Keq和k分别是化学平衡常数和反应速率常数;Kj是组分j的吸附常数,具体数值分别如表1~表3所示,下标1、2、3分别对应式(1)~式(3)。pj是组分j的分压,单位为Pa。已有研究表明不必考虑特定的二氧化碳重整反应动力学[20]。该动力学模型主要用于甲烷水蒸气重整反应,但文献[21]表明该动力学模型在甲烷双重整反应中也有较好的应用。

表1 化学平衡常数[12]Table 1 Chemical equilibrium constants[12]

表2 反应速率常数[12]Table 2 Reaction rate constants[12]

表3 组分吸附常数[12]Table 3 Adsorption constants of the components[12]
甲烷、水蒸气与二氧化碳的转化率(X)、n(H2)/n(CO)分别根据式(8)~式(11)进行计算。

其中:FCH4,in、FH2O,in、FCO2,in为反应器进口气体的摩尔流量,FCH4,out、FH2O,out、FCO2,out、FH2,out、FCO,out为反应器出口气体的摩尔流量,单位为kmol/h。
1.2.2 压降微分方程 平推流反应器的压降表达式为:

其中:Z为反应器长度,单位为m;pfact为压降影响因子,取值为0.8。计算结果表明,床层压降计算值与实际工厂数据较为吻合。
1.2.3 传热模型 转化炉内的主反应为吸热反应,传热速率主要由管内外传热系数、烟气温度以及管内气体温度决定。高温烟气与反应管内的主要传热方式为辐射传热。为便于计算,本文定义了内、外部传热系数。

其中:Q为管内区域的热通量,W/m2;hin和hout分别为内部传热系数及外部传热系数,W/(m2·K);Tf和Tw分别为高温烟气温度和管壁温度,单位为K,其中Tf取值为1473 K。内、外部传热系数都随着气体温度T的改变而改变。
管内传热系数由流体性质决定[22]:
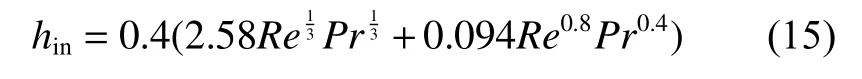
其中:Re为雷诺数;Pr为普朗特常数。
反应管热通量受辐射传热机制的影响:

其中:Din和Dout分别为反应管的内径与外径;c为Stefan-Boltzman常数与有效发射率的乘积。
2 结果与讨论
2.1 模型验证
2.1.1 甲烷水蒸气重整模拟验证 反应器长度11 m,直径0.17 m,管数88根,进口天然气压力3.25 MPa,水碳比2.7,过量空气系数为1.2,催化剂床层密度2337.9 kg/m3,床层空隙率0.528。进料气基本条件见表4。

表4 进料气的基本条件Table 4 Basic conditions of feed gas
甲烷水蒸气重整模拟验证结果如表5所示,出口干气中甲烷体积分数的误差为6.12%,模拟结果与工厂数据[23]相差较小,说明模型具有较好的准确性。

表5 甲烷水蒸气重整模拟结果与工厂数据对比Table 5 Comparion of simulation results and plant data of methane steam reforming
2.1.2 甲烷双重整模拟验证 甲烷双重整的工业数据鲜见报道,因此将模拟结果与文献报道实验数据[24]进行了比较,反应条件为T=800 ℃、p=0.1 MPa、n(CH4)∶n(H2O)∶n(CO2)=1∶0.8∶0.4,对比结果如表6所示。模拟结果与文献数据非常接近,二氧化碳转化率误差为5.15%,模型较为准确,可用于进一步讨论甲烷双重整反应过程的影响因素。

表6 甲烷双重整模拟结果与实验数据对比[24]Table 6 Comparion of simulation results and experimental data of methane bi-reforming
2.2 温度对反应产物的影响
在p=3.2 MPa、n(CH4)∶n(H2O)∶n(CO2)=1∶0.8∶0.4下考察了反应温度在550~900 ℃时甲烷双重整反应中气体组分的分布情况与甲烷、水蒸气和二氧化碳的转化率,结果如图3所示。由图3可以看出,甲烷双重整反应需要较高的温度才有利于甲烷与二氧化碳发生反应。反应温度越高,甲烷、水蒸气和二氧化碳的转化率越高。当反应温度为550~650 ℃时,甲烷水蒸气重整反应为主要反应,二氧化碳在该温度下不发生反应;当反应温度为650~750 ℃时,甲烷与水蒸气的转化程度有所提高,二氧化碳开始进行转化,这是因为水气变换反应为放热反应,升高温度有利于促进二氧化碳的转化,但二氧化碳的转化率仍低于水蒸气的转化率,甲烷水蒸气重整反应仍为主要反应。当反应温度为750~900℃时,甲烷、水蒸气和二氧化碳的转化率都大幅度提高,且在810℃时,二氧化碳的转化率超过了水蒸气的转化率,表明在较高的反应温度与压力下,温度对甲烷二氧化碳重整反应速率的影响更大。

图3 温度对甲烷双重整反应产物的影响Fig. 3 Effect of temperature on the products of methane bi-reforming reaction
2.3 压力对反应产物的影响
为提高经济效益,大多数甲烷双重整过程都是在高压下进行的,因此有必要研究压力对甲烷双重整反应的影响。在T=800 ℃、n(CH4)∶n(H2O)∶n(CO2)=1∶0.8∶0.4下考察了压力在0.1~3.5 MPa范围内反应产物的转化率及n(H2)/n(CO),结果如图4所示。从图4可以看出,随着压力的增大,甲烷、水蒸气和二氧化碳的转化率都快速下降。这是因为压力增大使甲烷水蒸气重整反应向逆反应方向进行,导致甲烷与水蒸气的转化率降低,生成的氢气也相对减少,因而水气变换反应中逆反应的反应程度也下降,使得二氧化碳的转化率降低。当压力达到3.5 MPa时,甲烷、水蒸气和二氧化碳的转化率分别为35.5%、30.3%、28.4%。压力对n(H2)/n(CO)的影响不显著,压力增大,n(H2)/n(CO)缓慢增加。

图4 压力对甲烷双重整反应产物的影响Fig. 4 Effect of pressure on the products of methane bi-reforming reaction
2.4 进料组成对反应产物的影响
通过调节进料组成,可使产物分布更加灵活。在T=800 ℃、p=3.2 MPa条件下考察了不同进料组成对甲烷双重整反应物甲烷、水蒸气和二氧化碳转化率的影响。
2.4.1n(CO2)∶n(CH4)对反应产物的影响 图5所示为n(CH4)∶n(H2O)=1∶1时不同n(CO2)∶n(CH4)对甲烷、水蒸气和二氧化碳转化率及n(H2)∶n(CO)的影响。随着n(CO2)∶n(CH4)从0升高到2.5,甲烷转化率由35.35%升高到68.95%。二氧化碳转化率在n(CO2)∶n(CH4)从0~1.0时快速增加,之后基本不变,说明在高压下,当n(CO2)∶n(CH4)>1.0时继续提高n(CO2)∶n(CH4)对二氧化碳转化率的影响较小。水蒸气转化率随着n(CO2)∶n(CH4)的提高显著下降,这是因为在高压下,二氧化碳含量相对增多抑制了甲烷水蒸气重整反应过程。在n(CO2)∶n(CH4)=2.5时,水蒸气转化率仅为2.36%。在n(CO2)∶n(CH4)=0时,700 ℃下n(H2)∶n(CO)远大于反应式(1)的化学计量比3∶1,说明水气变换反应起着显著的作用。随着温度升高,n(H2)∶n(CO)逐渐减小,说明温度升高促进了逆水气变换反应的进行,消耗了H2并生成了一氧化碳。当n(CO2)∶n(CH4)为1.0或2.0时,温度对n(H2)∶n(CO)的影响较小。

图5 不同n(CO2)∶n(CH4)对甲烷双重整反应产物的影响(n(CH4)∶n(H2O)=1∶1)Fig. 5 Effect of different n(CO2)∶n(CH4) on the products of methane bi-reforming reaction (n(CH4)∶n(H2O)=1∶1)
2.4.2n(H2O)∶n(CH4)对反应产物的影响 图6所示为n(CH4)∶n(CO2)=1∶1时不同n(H2O)∶n(CH4)对甲烷、水蒸气和二氧化碳转化率及n(H2)∶n(CO)的影响。由图6(a)可知,随着n(H2O)∶n(CH4)的升高,甲烷和水蒸气的转化率均增大,主要原因是n(H2O)∶n(CH4)的增大促进了反应(1)、(2)的进行,当n(H2O)∶n(CH4)大于2.0时,能有效提高反应(2)的反应程度,从而提高甲烷和水蒸气的转化率。二氧化碳的转化率随着n(H2O)∶n(CH4)的增大而减小,主要原因是水蒸气含量的相对增多强化了水气变换反应。增加水蒸气的量有利于提高生成物中n(H2)∶n(CO)。当n(H2O)∶n(CH4)=0时,n(H2)∶n(CO)随着反应温度的升高而增大。当n(H2O)∶n(CH4)=1.0时,温度对n(H2)∶n(CO)的影响较小,在800 ℃时,n(H2)∶n(CO)为1.35。当n(H2O)∶n(CH4)=2.0时,n(H2)∶n(CO)随着温度升高而降低,这是因为升高温度促进了甲烷二氧化碳重整反应的进行,因而n(H2)∶n(CO)下降趋势较为明显。

图6 不同n(H2O)∶n(CH4)对甲烷双重整反应产物的影响(n(CH4)∶n(CO2)=1∶1)Fig. 6 Effect of different n(H2O)∶n(CH4) on the products of methane bi-reforming reaction (n(CH4)∶n(CO2)=1∶1)
3 结 论
(1) 甲烷、水蒸气和二氧化碳的转化率均随温度的升高而增大。与甲烷水蒸气重整反应相比,提高甲烷与二氧化碳的转化率所需的反应温度更高,二氧化碳于650 ℃开始转化。
(2) 随着反应压力的增大,甲烷、水蒸气和二氧化碳的转化率均快速下降。当压力达到3.5 MPa时,甲烷、水蒸气和二氧化碳的转化率均小于40%。但压力对n(H2)∶n(CO)的影响不明显。
(3) 在p=3.2 MPa时,随着n(CO2)∶n(CH4)的增大,甲烷的转化率呈线性增加,水蒸气的转化率显著降低,二氧化碳的转化率呈现先快速增加后稳定的趋势。可以通过调节温度和进料中水蒸气和二氧化碳物质的量之比来调整n(H2)∶n(CO),以进行后续的工业生产。

