甲醇和乙腈二元体系中奥美拉唑热力学模型分析
戴明明,潘英敏,陶 宁,朱凤梅,陈顺平,吴海建,吴 刚,吴 伟
南京正大天晴制药有限公司,江苏 南京 210038
奥美拉唑是一种白色粉末或类白色粉末状固体,分子式为C17H19N3O3S(图1),其CAS 号为73590-58-6,由1 个亚砜基因连接苯并咪唑与取代吡啶环组成。作为胃质子泵H+/K+-ATP 酶的可逆抑制剂,奥美拉唑及其制剂常被广泛使用于胃溃疡、十二指肠溃疡、反流性食管炎和卓-艾综合征的治疗[1-3]。奥美拉唑是目前国际上使用最广泛的处方药之一,同时在一些国家也作为非处方药进行销售。奥美拉唑及其衍生物具有较高的医药价值和工业生产前景。

图1 奥美拉唑的化学结构式
众所周知,药物的纯化处理、含量测定是药品生产过程的重要组成部分。药物的溶解度特性,特别是药物的固-液相平衡、液-液相平衡常数对研究药物的作用机制具有重要作用。本文旨在对奥美拉唑的固-液相平衡数据进行收集、拟合、分析,为奥美拉唑的药学应用、分析纯化研究提供基础数据。此外,基于基础数据还可以进一步探讨奥美拉唑的萃取结晶、含量测定等工艺问题及其改进。
采用质量法测定常压下奥美拉唑于5~60 ℃(278.15~333.15 K)下在甲醇和乙腈二元溶剂体系中的溶解度,并将溶解度数据采用修正的Apelblat 模型、近理想二元溶剂/Redich-Kister(CNIBS/R-K)模型和Jouyban-Acree 模型进行拟合,同时利用范德霍夫分析和吉布斯方程可以计算热力学参数(包括焓、熵和吉布斯自由能)。根据实验数据,从混合溶剂中找出奥美拉唑相平衡规律。此外,热力学性质分析也有助于得出不同温度、不同组分下溶解度的变化趋势[4],以充实奥美拉唑基础理论研究,为奥美拉唑的生产、应用、分析工艺提供一定指导,以期对奥美拉唑的使用、药物制剂开发、色谱分析测定等方面提供参照。
1 实验
1.1 材料与仪器
所用材料的详细信息见表1。分析天平(BS124S 型,量程0~120 g,精度值±0.1 mg),赛多利斯科学仪器(北京)有限公司;循环恒温水浴系统(WDC-0540 型,量程-5~100 ℃,精度值±0.1 ℃),南京舜玛仪器设备有限公司。

表1 化学试剂属性及来源
1.2 实验方法
通过质量法进行溶解度测定[5-6]。将过量的奥美拉唑与不少于8 mL 的甲醇和乙腈的二元有机溶剂加入带塞子的10 mL 玻璃试管中(以避免实验过程中溶剂蒸发),将所有玻璃试管置于循环恒温水浴系统并开启磁力搅拌器连续搅拌24 h 以上(以确保玻璃试管中的液体达到平衡),然后关闭搅拌,并保持温度至少6 h(以确保未溶解固体在玻璃试管底部沉淀)。用移液枪吸取1 mL 透明澄清的饱和溶液,迅速转移至5 mL 已称质量的烧杯中,立即称量含有溶液的烧杯总质量,然后将烧杯置于室温下的干燥器中,定期(如每星期一次)对烧杯称质量,直至质量没有变化。为了检查溶解度测定的重复性,每个实验至少重复3 次。用同样的方法,在不同的温度下测量了3 个样品的溶解度,并用平均值计算了溶解度的摩尔分数。以摩尔分数表示溶质奥美拉唑的溶解度(x),数据计算见式(1)~(2)。
式中:xA为二元溶剂体系中甲醇的摩尔分数;i可为1、2、3,分别代表奥美拉唑、乙腈和甲醇;m1、m2、m3分别代表奥美拉唑、乙腈和甲醇的质量;M1、M2、M3分别代表奥美拉唑、乙腈和甲醇的摩尔质量。
2 结果与讨论
2.1 数据与模型
测定在278.15~333.15 K 时奥美拉唑在甲醇和乙腈二元溶剂混合物中的溶解度(x),详见表2,不同甲醇含量中溶解度与温度的关系曲线见图2。

图2 二元溶剂体系中奥美拉唑的摩尔分数溶解度(x)与温度(T)关系

表2 奥美拉唑在甲醇和乙腈二元溶剂中的溶解度

续表

续表
由表2和图2可知:奥美拉唑在甲醇和乙腈二元溶剂体系中的溶解度随温度升高而增加;相同温度时奥美拉唑的溶解度随二元溶剂中甲醇含量的增加而增加。
2.2 修正的Apelblat模型
奥美拉唑的溶解度随温度的变化关系可利用修正的Apelblat模型进行拟合[7-9]。

式中:T代表绝对温度(K),A、B、C代表模型参数,x代表奥美拉唑在二元溶剂中的溶解度。参数A和B代表溶液活度系数的变化,表示溶质溶解度的非理想溶液效应,参数C表示温度对熔融焓的影响,即热容(△Cp)[10-11]的修正。修正后的Apelblat模型回归曲线参数见表3。

表3 奥美拉唑在二元溶剂体系中修正的Apelblat模型的参数
2.3 CNIBS/R-K 模型
近理想二元溶剂/Redich-Kister(CNIBS/RK)模型也是计算二元溶剂体系中溶质溶解度的理论模型之一[12-16]。在等温条件下溶解度随混合溶剂中甲醇摩尔分数的变化趋势常用CNIBS/R-K 模型进行拟合,CNIBS/R-K 模型可用式(4)表示。
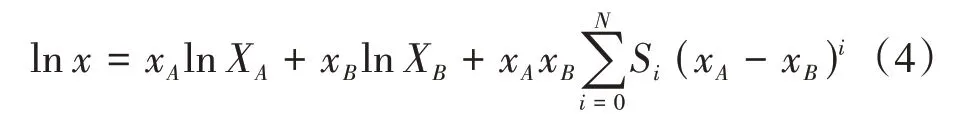
式中:x代表奥美拉唑的溶解度,xA和xB代表未添加溶质时二元溶剂乙腈和甲醇的初始组成(以摩尔分数表示),XA和XB分别代表奥美拉唑在纯乙腈和纯甲醇中的溶解度。Si是模型常数,N可以等于0、1、2 和3。当N=2 时,可用(1-xA)代替xB,则式(4)可重排为
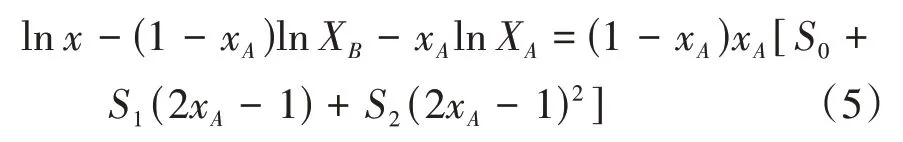
这是CNIBS/R-K 模型的一种变形,参数Si可以通过拟合[lnx-(1-xA)lnXB-xAlnXA]与{(1-xA)xA[S0+S1(2xA-1)+S2(2xA-1)2]}得到。
拟合得到的参数值见表4。然而,CNIBS/R-K模型只能用来描述溶解度数据和预测不同浓度混合溶剂在固定温度下的溶解度数据。为了描述溶剂组成和温度对奥美拉唑溶解度的影响,可采用Jouyban-Acree 模型。

表4 奥美拉唑二元溶剂体系用CNIBS/R-K 模型拟合的参数
2.4 Jouyban-Acree 模型
Jouyban-Acree 模型是一种描述溶质溶解度随温度和二元溶剂初始组分的变化而变化的常见模型[17],具体计算见式(6)。

式中:Ji是模型常数。当N=2 时,可用(1-xA)代替xB,由式(6)可得到

可以进一步简化为
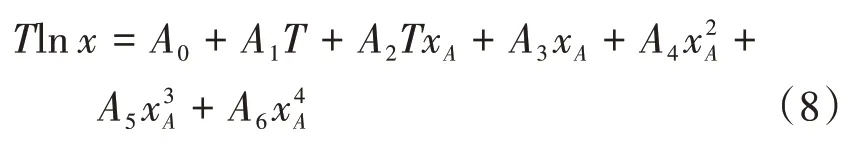
式中:A0、A1、A2、A3、A4、A5和A6是该模型的参数,可以通过最小二乘法将Tlnx与T、TxA、xA、x2A、x3A、x4A进行非线性回归获得,结果如表5所示。
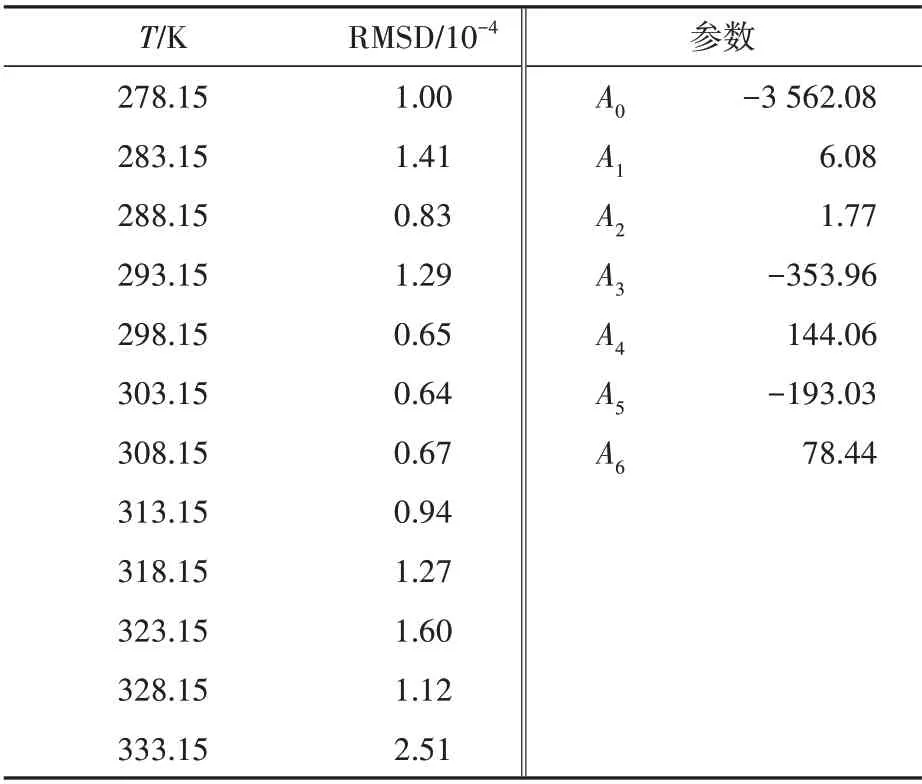
表5 奥美拉唑二元溶剂体系的Jouyban-Acree模型参数
2.5 标准偏差
通过模型拟合,可得到拟合计算数据xcal,通过实验数据x和计算数据xcal之间相对偏差比较,可数据化表现出各模型拟合情况,相对偏差数据详见表3~5。由表3~5 可知,修正的Apelblat 模型和Jouyban-Acree 模型在温度较低情况下,其相对偏差值相对较大,随着温度的升高,相对偏差值逐渐变小。这可能是因为溶解度数值相对较小时,其相对偏差值可能相对较大。
相对标准偏差亦称均方根误差[18],可用来描述预测值与真实值的偏差情况,也常用于衡量实验数据与计算数据的偏差。本研究中用其评估比较各模型与实验数据的拟合适用情况。

式中:N表示实验点的个数,x和xcal分别表示实验数据和计算数据。表3~5 列出了相应模型的RMSD值。
由表3~5 可知,修正的Apelblat 模型、CNIBS/R-K 模型和Jouyban-Acree 模型的RMSD 值之和分别为4.66×10-4、1.47×10-4和1.393×10-3。由此可见,CNIBS/R-K 模型拟合效果最好。修正的Apelblat模型更关注于温度对溶解度的影响,Jouyban-Acree 模型更多从整体阐述二元溶剂体系中的溶剂间比例对溶解度的影响,可以通过上述2 种模型实现对CNIBS/R-K模型的补充完善。
2.6 热力学参数
范德霍夫分析是热力学领域中常用的方法。标准摩尔溶解焓(ΔsolH0m)的表达式为

式中:R为通用气体常数(8.314 J/(mol·K))。平均温度时,标准摩尔溶解焓亦可用式(10)表达[19-20]。由此可以得到式(11)。

式中:Tmean表示实验温度范围的平均温度,即305.65 K。图3即为奥美拉唑溶解度lnx与(1T-1Tmean)对应的曲线[21]。摩尔吉布斯能量方程(ΔsolG0m)可以表示为

根据吉布斯方程,可以得到溶液的标准摩尔熵(ΔsolS0m)。同时可以得出吉布斯能对应的焓和熵的贡献度(分别以ξH和ξS表示)[22],为判断溶解过程的状态与自发性提供基础。

平均温度下奥美拉唑在二元溶剂体系溶解过程的热力学函数ΔsolH0m、ΔsolS0m、ΔsolG0m、ξH和ξS的值见图3和表6。由图3和表6可知,热力学参数ΔsolH0m和ΔsolG0m均为正值,这说明奥美拉唑在所研究的二元溶剂体系中的溶解过程是吸热和非自发的。此外,所有的ξH均高于61.45%,表明在溶解过程中焓是标准吉布斯能的主要贡献者。同时,可以发现,伴随着甲醇摩尔分数的梯度上升,标准摩尔熵梯度随之增加,而标准吉布斯能呈现一定比例的等额下降,这说明在所研究的二元溶剂体系中,甲醇所占比例的上升在一定程度上增加了溶液体系混乱度,从而促进奥美拉唑的溶解过程。
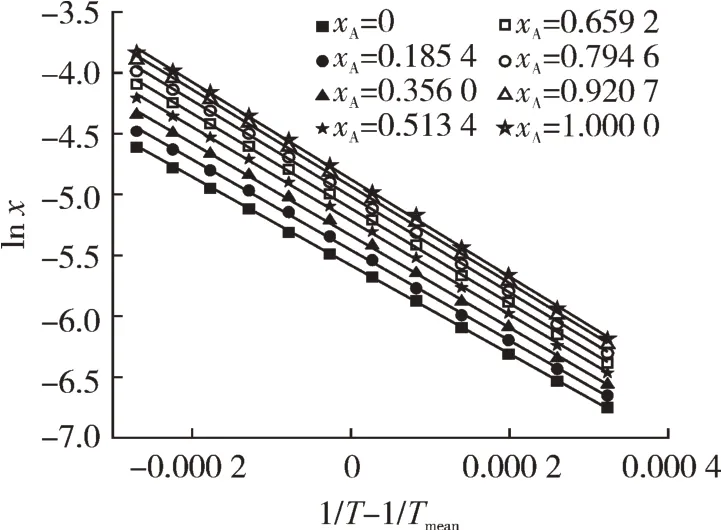
图3 二元溶剂体系中奥美拉唑的摩尔分度溶解度(ln x)对应(1/T-1/Tmean)的范德霍夫分析
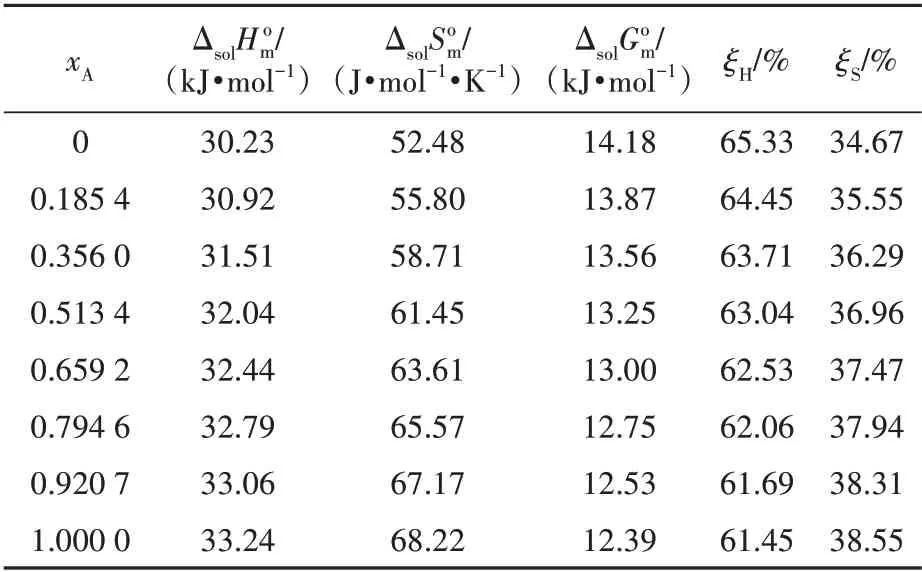
表6 平均温度下奥美拉唑在二元溶剂体系溶解过程的热力学函数
3 结论
1)奥美拉唑在甲醇和乙腈二元溶剂中的溶解度随温度升高而增加,随甲醇比例增加而增加。
2)采用修正的Apelblat 模型、CNIBS/R-K 模型和Jouyban-Acree 模型均可成功拟合溶解度数据,其中CNIBS/R-K 模型因RMSD 值最小而拟合情况更好,并可以通过其他2 个模型实现对CNIBS/R-K模型的补充完善。
3)由范德霍夫分析的热力学参数和吉布斯方程可知,奥美拉唑在甲醇和乙腈二元溶剂体系中的溶解过程是吸热的、非自发的。
由此可见,本研究的实验数据和参数能在奥美拉唑的纯化分析工艺上提供一定指导,同时在实际工业生产中,在奥美拉唑的色谱分析、化合物纯化等方面具有一定的参考意义。诸如利用热力学数据,在色谱分析、化合物测定特别是检验方法学开发时,作为流动相的甲醇比例上升时,可一定程度上促进奥美拉唑的溶解,实现对奥美拉唑分离、测定的作用。

