列线图在老年COPD患者发生肺动脉高压风险预测中的应用
朱建丰 徐英
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种常见的呼吸系统疾病,简称慢阻肺[1]。COPD多表现出气流受限等特征并持续存在和发展,属于不完全可逆的气道病症[2],导致患者肺功能减退,出现呼吸困难等症状并逐渐丧失劳动能力。据WHO统计数据显示,COPD已成为世界第三大高致死率疾病[3],仅次于缺血性心脏病、中风。临床中COPD会导致慢性呼吸衰竭、慢性肺源性心脏病、肺动脉高压(pulmonary hypertension,PH)等一系列并发症,其中PH最为常见[4]。PH是指肺动脉内压力过高而出现血流动力学及病理学改变,最终发展成心力衰竭等严重心脏疾病,严重影响患者的预后及生存时间[5],多认为是由低血压症致使肺血管发生痉挛等病变,另外肺部炎症的存在也是COPD并发PH的因素之一[6]。由于PH病症并不具有临床特异性,心导管、彩超及超声心动图等检查手段存在时效性滞后的缺点,导致部分患者治疗不及时而影响预后[7]。因此,探寻预测老年COPD患者发生PH的独立风险因素对于患者的治疗及预后有重要意义。列线图模型是一种可同时将多个危险因素指标纳入一个带有刻度的图形内的平面模型,通过各因素对应刻度分值总和预测疾病发生的概率,具有较高应用价值[8]。该研究通过回顾性分析并建立预测老年COPD患者发生PH的危险因素列线图预测模型,为降低PH发生率提供临床依据。
1 资料与方法
1.1 临床资料 选取2015年1月至2019年1月湖州市第三人民医院收治的COPD老年患者420例,根据患者是否发生PH分为发生PH组(80例)和未发生PH组(340例)。(1)纳入标准:年龄≥60岁;明确诊断为COPD。(2)排除标准:合并支气管炎、支气管扩张、肺结核等呼吸系统疾病;严重心脑血管疾病及肝肾功能不全患者;恶性肿瘤患者;临床病理资料及回访记录不全者。(3)PH的诊断标准:彩超检查可见肺动脉压力>35 mmHg或经肺部CT检查肺主动脉径>29 mm。
1.2 研究方法 收集患者的性别、年龄、身体质量指数(BMI)、居住环境、病程、吸烟史、高血脂、糖尿病(DM)、尿酸(UA)、左心房内径、C-反应蛋白(CRP)、白介素-6(IL-6)、Toll样受体(TLR4)、平均血小板体积(MPV)、白细胞(WBC)计数、中性粒细胞比率(NE%)、脑钠肽(BNP)、第1秒用力呼气容积比率(FEV1%)、PaO2值、PaCO2值及红细胞沉降率(ESR)。其中,TLR4采用ELISA检测试剂盒进行检测。
1.3 统计学方法 采用SPSS 20.0统计软件。计数资料以[n(%)] 表示,采用卡方检验;计量资料符合正态分布以(±s)表示,采用t检验;以P<0.05为差异有统计学意义。采用Logistic回归对独立风险因素进行筛选,采用R(R3.6.0)软件对筛选出的独立危险因素建立列线图模型,并应用rms程序包和Bootstrap法构建验证集模型对列线图预测模型进行验证,计算一致性指数(C-index)、制作ROC曲线。
2 结果
2.1 两组临床资料比较 两组患者的年龄、BMI、居住环境、病程、吸烟史、UA、左心房内径、CRP、IL-6、TLR4、MPV、WBC、BNP、FEV1%、PaO2值、PaCO2值及ESR比较,差异有统计学意义(P<0.05)。见表1。
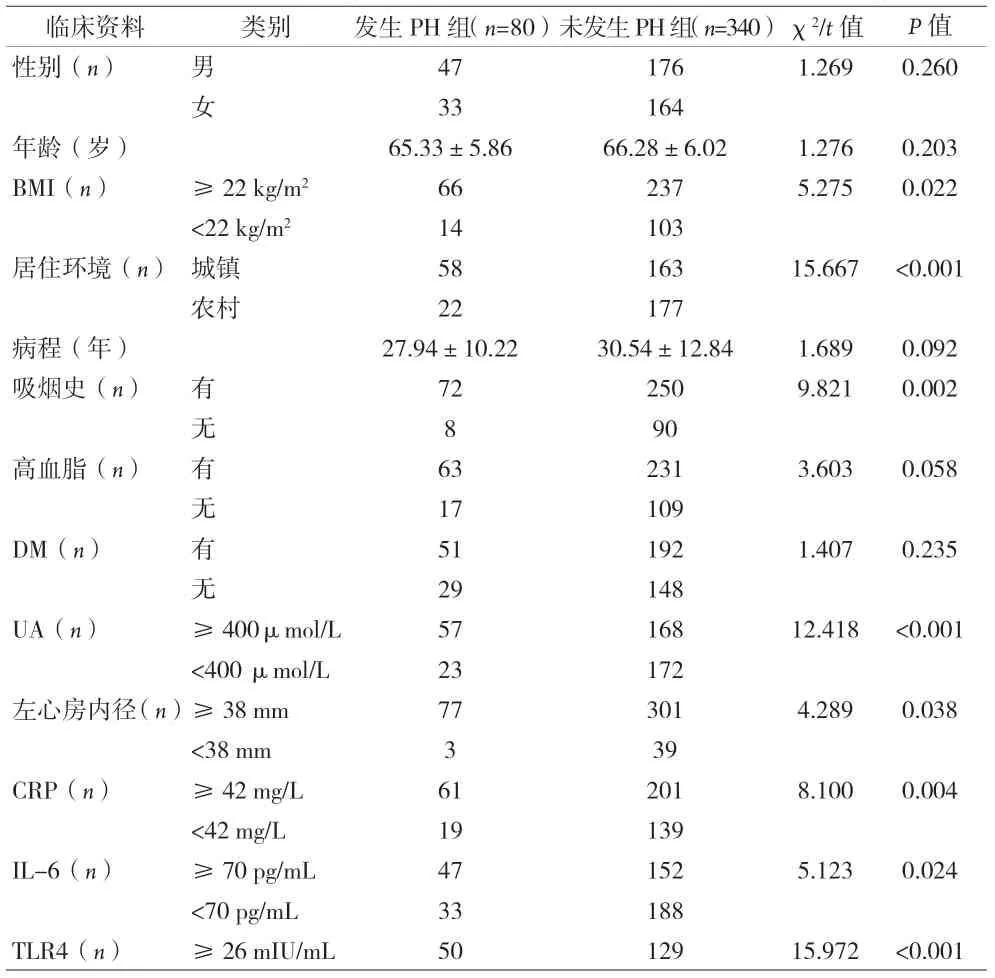
表1 两组的临床资料比较
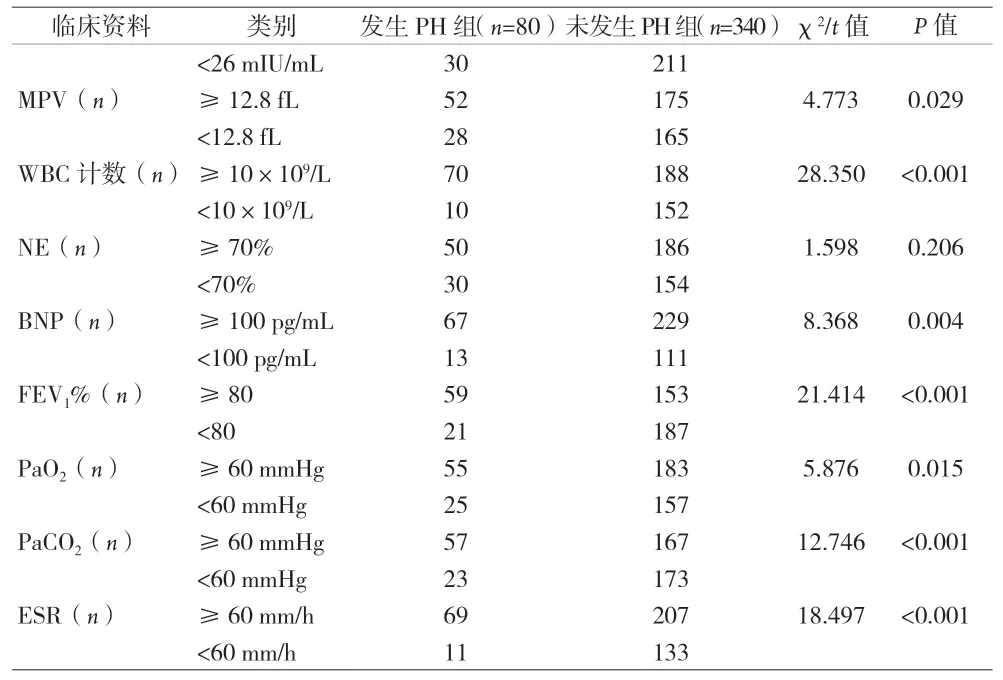
表1 (续)
2.2 多因素Logistic回归分析 结果显示,发生PH组和未发生PH组患者的年龄、BMI、病程、UA、左心房内径、IL-6、TLR4、MPV、BNP、PaO2值及ESR比较,差异均无统计学意义(P均>0.05);筛选出居住环境(OR=2.861,95%CI:1.575~5.198)、. 烟 史(OR=3.034,95%CI:1.318~6.984)、CRP(OR=3.028,95%CI:1.599~5.733)、WBC计数(OR=6.156,95%CI:2.915~12.997)、FEV1%(OR=3.443,95%CI:1.891~6.270)、PaCO2(OR=2.746,95%CI:1.513~4.984)为老年COPD患者发生PH的独立危险因素,差异有统计学意义(P<0.05)。
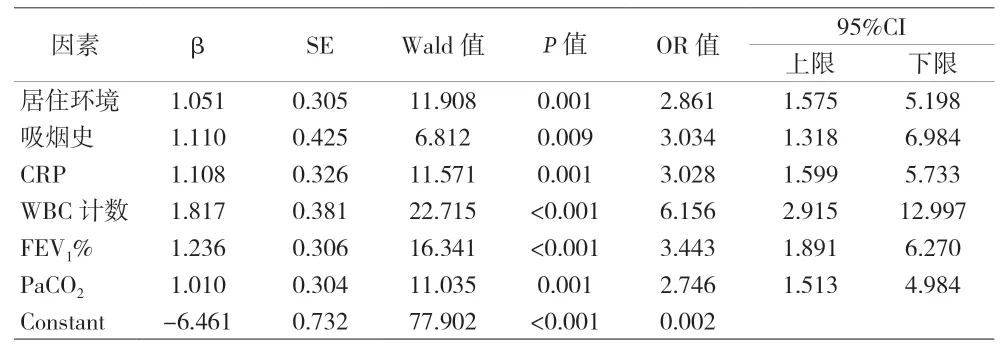
表3 多因素Logistic回归分析结果
2.3 个体化预测老年COPD患者发生PH的风险模型建立与验证 预测老年COPD发生PH的列线图模型,见图1。将建模集原始数据重复抽样600次后(Bootstrap 法)对模型进行内部验证,比较建模集与验证集差异,结果显示建模集和验证集的C-index指数分别为0.829(95%CI:0.733~0.925)、0.830(95%CI:0.734~0.924),两组的校正曲线均与标准曲线拟合较好,见图2;两组ROC曲线下面积(AUC)分别为0.829和0.830,见图3;证明该模型具有良好的预测精准度。
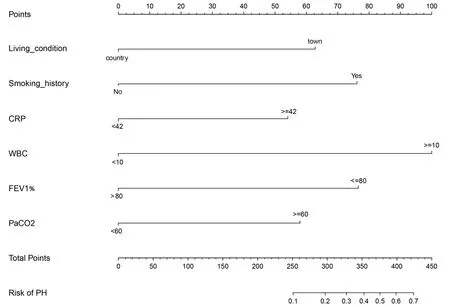
图1 预测老年COPD患者发生PH的风险模型
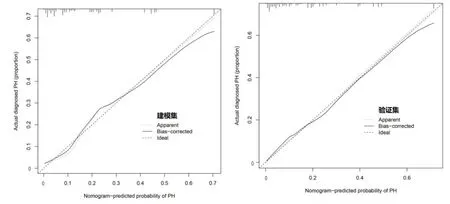
图2 列线图模型的校正曲线验证
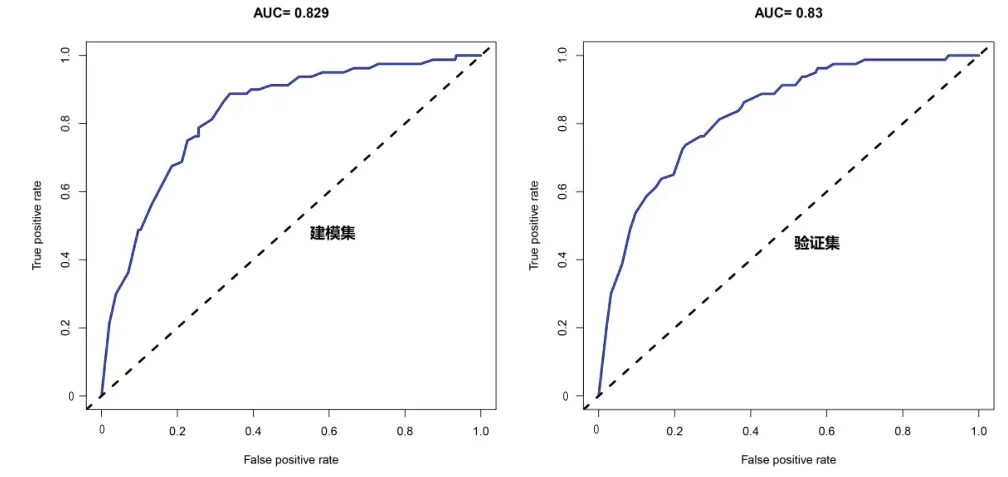
图3 列线图模型的ROC曲线验证
3 讨论
随着COPD的发病率在全球范围内的不断上升及死亡人数的增加[9],其并发症预测及预防逐渐得到重视。PH是COPD最常见同时也是最危险的并发症之一,此类PH患者的5年生存率仅为48%[10],早期均无明显症状表现,随着病情的发展开始表现出呼吸困难、耐受力差等症状[11]。COPD患者的症状特征同样表现为气流阻塞、呼吸不畅及运动不耐受等,与PH的症状高度相似,因此临床上很难诊断出COPD是否并发PH[12]。同时,随着患者的年龄增长,老年患者身体状况变差,PH发生率大大升高[13]。研究表明,PH作为老年COPD的一大独立危险因素,严重影响了老年COPD患者的预后[14-15]。因此,分析老年COPD患者发生PH的特点,找出其风险因素并进行预测或预防,对治疗COPD并发PH有着重要临床意义。
该研究采用单因素和多因素Logistic回归分析法筛选出城镇居住环境、存在吸烟史、CRP≥42 mg/L、WBC≥10×109/L、FEV1%≥80、PaCO2≥60 mmHg是老年COPD患者发生PH的独立危险因素(P<0.05)。有研究证实,空气中尘霾/烟雾等污染、职业暴露及各种化学染料挥发是PH发病的重要原因之一,其中的有害物质被吸入后可加重患者肺部的炎症反应,进而增加PH的发生率[16]。该研究城镇中老年COPD患者发生PH的概率是农村患者的1.051倍,可能是因为农村居住环境较城镇优良,空气中的污染有害物质较少。而患者长期吸烟会增加PH发病率,可能与吸烟会损害肺血管、加剧肺部炎症及氧化应激有关[17]。周雪萍等[18]研究显示,吸烟在一定程度上会减弱血红细胞的携氧能力,致使肺部多处腺体分泌物增加阻塞小微气道从而引发缺氧应激反应,导致肺血管的收缩甚至重塑而并发PH。另有研究提示,吸烟会造成血管内皮功能发生改变,导致COPD患者全身炎症的发生,继而发生PH[19]。CRP及WBC水平上升表明机体炎性反应的增加,炎性反应的发生是COPD并发PH的重要病理基础之一[20],其机制在于阻塞肺血管,引发肺血管阻力的加剧。该研究中其他炎性因子的水平差异无统计学意义(P>0.05),可能是统计量较少的原因,但CRP、WBC指标水平更具有特异性,对预测风险的建立有着重要作用。FEV1%越小,则提示患者的呼吸困难越严重[21]。本研究中FEV1%<80的老年COPD患者发生PH的情况是FEV1%>80患者的1.236倍,证实了上述研究观点。PaO2值与PaCO2值的异常将导致低氧性的肺血管收缩[22],同样增加了并发PH的风险,但PaO2值的异常可能与患者治疗时存在吸氧进而产生干扰致使结果存在偏差,因此不列入独立风险因素中。
基于以上筛选出的独立危险因素,建立了预测老年COPD患者发生PH的列线图模型,同时为验证预测模型的准确性,采用内部验证的方式建立验证集,对模型进行进一步的预测效能检验,结果显示建模集和验证集的C-index指数分别为0.829(95%CI:0.733~0.925)和0.830(95%CI:0.734~0.924),两组ROC曲线下面积(AUC)分别为0.829、0.830,校正曲线均与标准曲线拟合较好。因为研究中构建的列线图模型可清晰反映老年COPD患者发生PH危险因素的影响程度,具有使用方便、直观连续的优势。然后,可根据列线图中各项危险因素进行转换,获取各危险因素的相应赋分值并计算总分值,个体化预测老年COPD患者发生PH的概率,进而指导临床。
综上所述,基于多项老年COPD患者发生PH的危险因素建立的列线图模型具有较高的预测价值,临床上可根据患者的居住环境、吸烟史、CRP、WBC、FEV1%、PaCO2等危险因素在早期进行有效防范与干预,进而减少PH的发生,改善患者预后,提高患者存活时间。

