HPLC测定豆制品中丙酸钙结果的不确定度评价*
刘强欣,林 婷,闻佳钰,王志超,钟寒辉,董叶箐
(绿城农科检测技术有限公司,浙江 杭州 310522)
豆制品营养丰富,豆能够降低人体血液中的胆固醇,有预防消化系统癌症及其他疾病的功效。因此被广大消费者誉为21世纪最喜爱的食品之一[1]。然而豆制品保存却相对较难容易变质腐败,为了延长豆制品的保质期,人们会添加一些食品防腐剂。丙酸(propanoic acid)及其盐类是世界卫生组织(WHO)和联合国粮农组织(FAO) 批准使用的安全可靠的食品防霉剂[2],具有抑制微生物增殖和杀灭微生物的作用,是天然防腐剂的重要组成部分,能参加人体正常新陈代谢,对于人体无害[3],常以丙酸钙或丙酸钠的形式存在,用于食品防腐和防霉[4]。有关研究表明人体长期过量摄入含丙酸及其盐类的食品会导致呕吐、腹痛和肺水肿等[5-6],食品安全国家标准GB 2760-2014《食品安全国家标准 食品添加剂使用标准》[7]规定豆类制品限量为2.5 g/kg(以丙酸计)。
测量不确定度是对测量结果质量的定量表征,很大程度上决定了测量结果的可靠性[8-10],为了保证豆制品中丙酸钙含量检测结果科学性,依据测定不确定度准则[11-13]参照标准GB 5009.120-2016 《食品安全国家标准 食品中丙酸钠、丙酸钙的测定》[14],建立数学模型,对结果进行不确定度评估,为结果的可靠性、准确性提供了科学依据。
1 材料与方法
1.1 材料与试剂
实验采用的试剂为:甲醇(色谱纯),Fisher;磷酸氢二胺(分析纯),浙江长青化工;磷酸(分析纯),浙江长青化工;丙酸钙(纯度98.0%),Dr.Ehrenstorfer;其余试剂均为市售分析或以上规格,浙江长青化工;超纯水仪制备;混合微孔滤膜(0.22 μm);豆制品,超市购买。
1.2 仪器与设备
实验采用的仪器为:岛津LC-2030C高效液相色谱仪器(配有二极管阵列检测器),日本岛津公司;BSA224S型电子天平,德国赛多利斯;Kjeltec 8400凯式定氮仪,foss;pHS-3C酸度计,雷磁;色谱柱(Agela Innoval ODS-2 ;250 mm× 4.6 mm,5.0 μm);超纯水系统,美国Millipore超纯水仪制备。
1.3 液相色谱参考条件
(1)色谱柱:Agela Innoval ODS-2(250 mm×4.6 mm, 5.0 μm);
(2)流动相:甲醇+1.54 g/L磷酸氢二胺=5+95;
(3)检测波长:214 nm;
(4)柱温:40 ℃;
(5)流速:1.0 mL/min;
(60进样体积:20 μL。
1.4 试样处理
准确称取25 g置于250 mL烧杯中,转移置于500 mL蒸馏瓶中加入100 mL水,再用50 mL水冲分多次冲洗烧杯,洗涤液合并至蒸馏瓶中,加入20 mL磷酸溶液(1 mol/L),通过水蒸气蒸馏,将250 mL容量瓶作为吸收液装置,待蒸馏至约 240 mL时取出,在室温下放置30 min,用1 mol/L磷酸溶液调pH为3左右,加水定容至刻度,摇匀,经0.45 μm 微孔滤膜过滤后,进液相色谱测定。
2 模型建立
根据样品测试方法的过程,建立豆制品中丙酸钙(以丙酸计)残留量不确定度评估数学模型为:
注:X为试样中丙酸含量,g/kg;ρ为由标准曲线得出的试样液中待测物的质量浓度,mg/L;V为样液最终定容的体积,mL;m为试样的称样量,g;1000为由mg/kg转换为g/kg的换算因子。
3 结果与分析
3.1 不确定度的引入:标准溶液
标准储备液的配制过程:精确称取0.234201 g丙酸钙标准物质(纯度为98.0%),加水溶解并定容至25 mL,折算为丙酸后标样浓度为7304.2 mg/L。
标准工作液的配制过程:分别吸取丙酸标准储备液0.171 mL、0.342 mL、0.856 mL、1.711 mL、3.423 mL 于500 mL蒸馏瓶,按照试样处理进行蒸馏,最终用水定容置250 mL容量瓶,配制成浓度为0.005 g/L、0.01 g/L、0.025 g/L、0.05 g/L、 0.1 g/L的标准工作溶液。
3.1.1 不确定度u(p)的引入:标准物质纯度
丙酸钙标准物质证书上的相对不确定度urel(p)=2.0%
3.1.2 不确定度u(m)的引入:标准物质称量
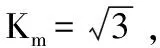
丙酸钙标准物质的称取量为0.234201 g,通过配恒体方法两次的测量值相减得出,则由称量产生的相对标准不确定度应为:
3.1.3 不确定度u(V)的引入:标准物质配制
(1)不确定度的引入:配制标准储备液所有容器
将称取的丙酸标准物质溶解并定容至25 mL的容量瓶中,根据JJG 196-2006[15]《中华人民共和国国家计量检定规程》,在(25±1)℃时25 mL单标线容量瓶(A级)容量允许为 ±0.03 mL,其不确定度为矩形分布(B类评定),则容量瓶的不确定度为:
(2)不确定度的引入:配制标准工作液所有容器
①引入的不确定度来源:移液管
移液管准确移取标准储备液置于500 mL 蒸馏瓶中,经蒸馏配制成相应浓度的工作液,根据JJG 196-2006[15], 移液管(A级)对于的允许误差如表1所示。
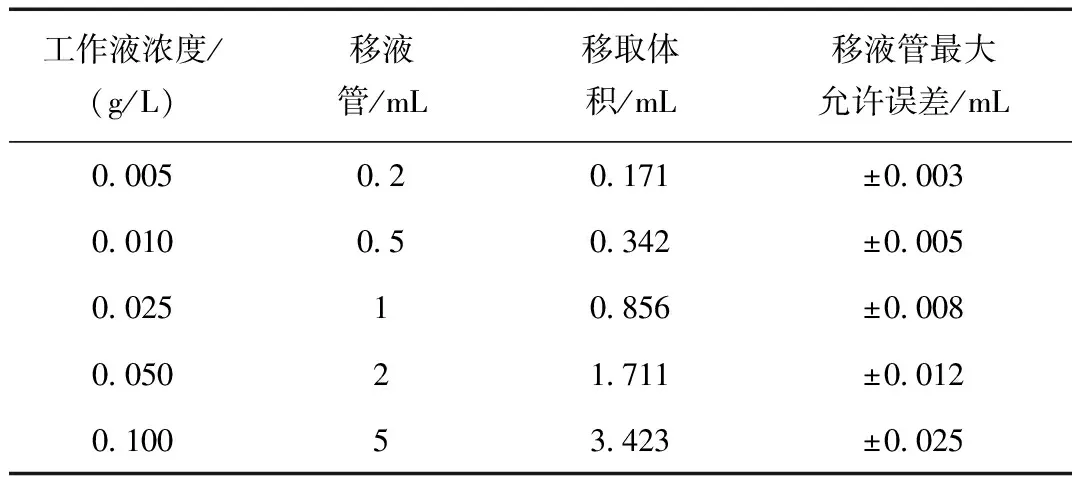
表1 工作液浓度、移取体积及对于移液管最大允许误差
则移液管的不确定度为:
②不确定度的引入:容量瓶
丙酸标准工作液最终定容至250 mL 容量瓶,依据JJG 196-2006[15],(25±1)℃时250 mL 单标线容量瓶(A级)允许容量为±0.15 mL,则不确定度为矩形分布(B类评定),容量瓶的不确定度是:
因此容器引入的相对不确定度为:

=1.54%
3.1.4 不确定度u(g)的引入:标准曲线拟合
上机测定丙酸标准曲线上5个不同工作液浓度,对应的峰面积与浓度如表2所示。

表2 标准工作液浓度与对应峰面积
采用最小二乘法,以丙酸的浓度X与其对应的平均峰面积Y进行线性拟合,得丙酸的标曲线:Y=339743X-35.992,线性相关系数为0.999。
对测试样进行6次测量,得峰面积A,由标准曲线方程求得提取液中丙酸的浓度分别为0.258 g/kg、0.252 g/kg、0.249 g/kg、0.255 g/kg、0.249 g/kg、0.261 g/kg,平均值为0.254 g/kg,最小二乘法拟合标准工作曲线求得样品中丙酸含量过程所引入的相对不确定度为:
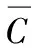
其中:
则最小二乘法拟合过程产生的相对标准不确定度为:
3.2 液相色谱仪测定引入的不确定度
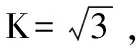
3.3 样品引入的不确定度
3.3.1 样品称量引入的不确定度u(M)
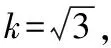
3.3.2 样品定容引入的不确定度u(a)
试样最终定容至250 mL 的容量瓶,依据JJG 196-2006[15],(25±1) ℃时250 mL 单标线容量瓶(A级)允许容量为 ±0.15 mL,则不确定度为矩形分布(B类评定),容量瓶的不确定度是:
3.4 不确定度的引入:样品测量重复性
对待测样品进行六次重复性测定,所得结果见表3所示。
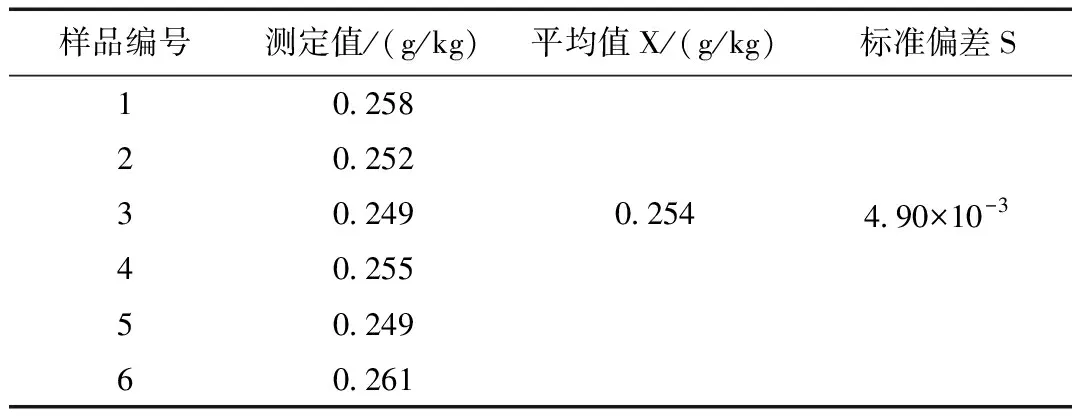
表3 样品六次平行所测结果
得出测量重复性引入的相对不确定为:
3.5 标准不确定度分量
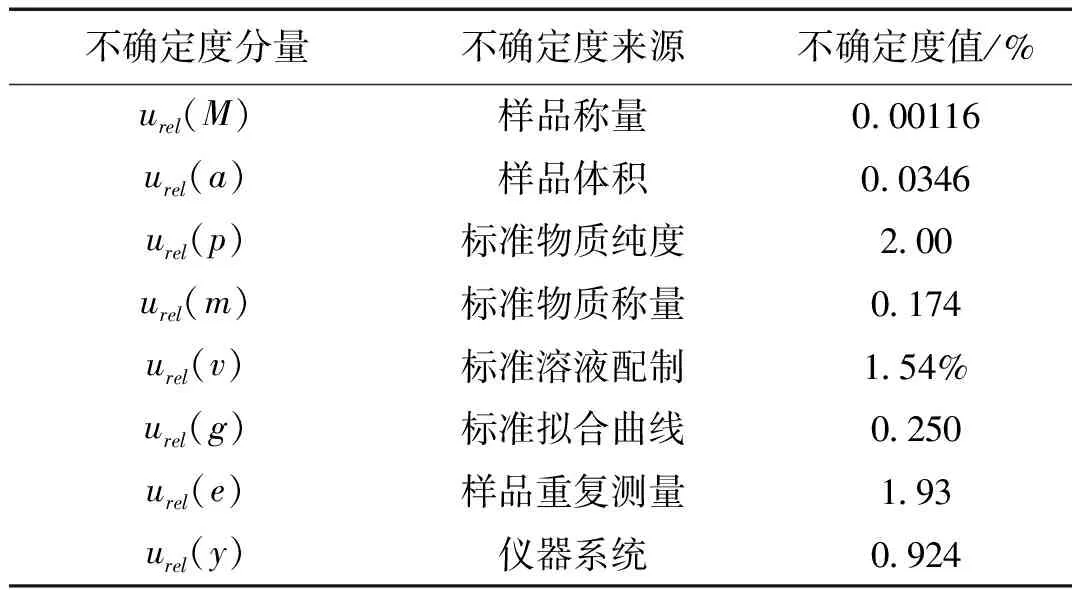
不确定度分量不确定度来源不确定度值/%u rel(M)样品称量0.00116u rel(a)样品体积0.0346u rel (p)标准物质纯度2.00u rel(m)标准物质称量0.174u rel(v)标准溶液配制1.54%u rel(g)标准拟合曲线0.250u rel(e)样品重复测量1.93u rel(y)仪器系统0.924
3.6 合成标准不确定度的计算
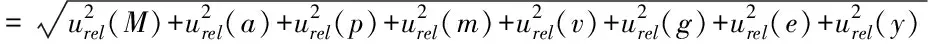
=3.32%
3.7 扩展不确定度
在95%的置信区间下,取包含因子k=2,其相对扩展不确定度为:
Urel(X)=k×urel(X)=2×3.32%=6.64%
豆类制品中丙酸钙(以丙酸计)的含量为0.254 g/kg,得扩展不确定度为
U=0.254 g/kg×6.64%=0.0169 g/kg
综上可得豆类制品中丙酸钙(以丙酸计)含量的不确定度报告为:(0.254±0.0169)g/kg(k=2)。
4 结 论
通过对豆制品中丙酸钙含量的不确定度评定,得出样品中丙酸钙(以丙酸计)的含量为 (0.254±0.0169) g /kg,k=2,置信概率 P=95%。本文全面地分析了HPLC法测定丙酸含量实验过程不确定度的来源,并计算了各不确定度分量。结果表明,标准物质纯度和样品重复性测定是合成不确定度的主要来源。因此日常检测中所使用的仪器、配制溶液的步骤,环境、试剂等客观影响因子都必须达到标准要求,不断提高操作人员的熟练程度以提升检测结果的准确性。

