消化道恶性肿瘤Ⅳ期患者营养相关调查及分析
张续乾 宫一凡 廖原 翟爱军
近年来消化道恶性肿瘤严重威胁人类健康和生命。根据全球癌症统计[1],2020年全球新增癌症病例1 930万例,癌症死亡1 000万例,其中超过1/3的癌症患者患有消化道肿瘤,超过60%的消化道肿瘤死亡病例发生在亚洲。我国国家癌症中心2019年数据显示,消化道恶性肿瘤逐年增加,胃癌(GC)发病率为10.79%,死亡率为12.45%,结直肠癌(CRC)发病率为9.74%,死亡率为8.0%[2]。研究表明,50%~90%的恶性肿瘤患者存在体重减轻、营养不良[3]。营养不良即营养不足,由于摄入不足或利用障碍引起的能力或营养素缺乏的状态并导致机体生理和精神功能下降,可引发不良临床结局,是恶性消化道肿瘤患者常见的并发症,其与治疗效果较差、生活质量降低及生存率相关[4,5]。据报道,中国有40.0%~70.5%的胃癌患者有营养不良的风险[6]。早期定期营养筛查并进行及时的营养干预,对消化道恶性肿瘤患者预后至关重要。我们应用营养风险筛查2002(NRS-2002)对我科消化道肿瘤Ⅳ期患者进行回顾性分析,评估患者的营养状态,并进行相应人体测量和相关实验室检查,分析其之间的关系。
1 材料与方法
1.1 一般资料 选取2019年1月~2020年1月我院消化科住院消化道恶性肿瘤Ⅳ期选择姑息性治疗的患者,均签署知情同意书。
纳入标准:①年龄18~90岁,有意识,无沟通障碍,可以配合相关检查;②符合消化道恶性肿瘤Ⅳ期姑息性治疗;③有完整的病史记录和随访数据:④患者及其家属自愿参加本研究,并已知情同意。
排除标准:①艾滋病或器官移植患者:②病情危急、难以评估的患者:③拒绝或者不配合调查者。
1.2 调查内容 患者入院24小时内由专门培训的调查人员调查完成以下内容:患者体重及体重变化、身高、非利手握力值、营养指标[白蛋白(ALB)、前白蛋白(PA)]、NRS-2002评分。住院期间调查完成以下内容:患者饮食医嘱、营养支持途经、营养支持时间等。采用NRS-2002进行风险筛查,总评分≥3分说明存在营养风险,<3分为无营养风险。ESPEN 2015营养不良判定标准[7]:经筛查确定有营养不良风险的个体中,营养不良的诊断标准应基于低BMI(<18.5kg/m2),体重下降且至少负荷低BMI(年龄特异性)或低FFMI(性别特异性)二者之一。
1.3 统计学方法 采用SPSS 22.0软件,正态分布的计量资料以±s表示,非正态分布计数资料以中位数表示,组间比较采用t检验;计数资料以百分比表示,采用卡方检验;采用Pearson相关分析。P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 共纳入患者105例,男60例,女45例,平均年龄(77.39±10.26)岁,其中食管癌48例(45.7%),胃癌26例(24.8%),大肠癌14例(13.3%),胰腺癌17例(16.2%),平均BMI(21.69±4.50)kg/m2,平均非利手握力值(11.38±6.95)kg。
2.2 营养评估 经过NRS-2002筛查后,存在营养风险患者为67例(63.8%),营养不良患者为43例(40.9%)。男女患者营养风险发生率比较差异无统计学意义(P>0.05);女性患者营养不良发生率高于男性患者,差异有统计学意义(P<0.05);≥70岁患者营养风险发生率及营养不良发生率均明显高于<70岁患者,差异有统计学意义(P<0.05);不同疾病患者营养风险发生率比较差异无统计学意义(P>0.05);胰腺癌营养不良发生率明显高于其他疾病(P<0.05)。见表1。

表1 不同性别、年龄、不同疾病患者营养风险及营养不良发生率比较[n(%)]
2.3 营养支持 67例有营养风险患者中,接受营养支持者61例,营养支持率为91.0%,肠外营养60例,肠内营养5例(其中4例接受肠内营养联合肠外营养支持);38例无营养风险患者中,接受营养支持者34例,营养支持率为89.5%,均为肠外营养。有营养风险患者ALB与PA均低于无营养风险患者,差异均有统计学意义(P<0.05)。见表2。
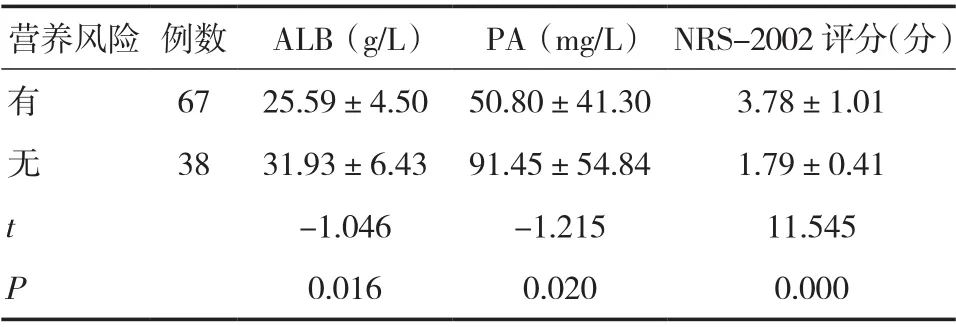
表2 有无营养风险患者营养指标及营养不良比较
2.4 NRS-2002评分与ALB、PA相关性分析 将所有患者NRS-2002评分与ALB、PA进行相关性分析,结果显示NRS-2002评分与ALB呈负相关(r=-0.96,P<0.05),与PA呈负相关(r=-0.38,P<0.05)。
3 讨论
晚期癌症患者被定义为远期转移、晚期疾病和/或预后为6~24个月的患者,肿瘤负担、营养不良或疾病严重程度均会导致预后不佳。营养障碍在晚期癌症患者中越来越普遍,营养不良成为恶性肿瘤治疗中严重副作用的独立危险因素之一[8]。据报道,至2020年中国消化道肿瘤占癌症死亡总数的45%[9],8%~87%的恶性肿瘤患者会出现营养不良[10,11]。恶病质和厌食症被称为癌症的隐形杀手,约20%~30%癌症患者死亡归因于营养不良,而非癌症本身[12,13]。营养不良的发生率因不同类型的恶性肿瘤而异,而晚期消化道肿瘤的患者近一半存在严重营养不良[14,15],本研究发现消化道肿瘤晚期患者中,营养不良发生率高达40.9%,其中胰腺癌营养不良发生率最高(14.3%)。有研究发现,营养不良与患者的性别和年龄有关,女性患者更可能出现严重的营养不良[16]。而本研究发现消化道恶性肿瘤Ⅳ期患者营养风险发生率与性别无关,但女性患者营养不良发生率高于男性患者,≥70岁的患者更容易发生营养不良。
一个便捷的营养风险评估工具,具有良好的风险预测价值,更有利于临床医疗决策。NRS-2002侧重于患者的营养状况和疾病严重程度,以评估营养干预对临床结果的影响,中国临床肿瘤学会(CSCO)推荐NRS-2002作为医院营养风险筛查的首选工具[17,18]。体重是营养评估中最简单、最直观的指标,连续测量体重是筛查营养充分性和营养状况改变最简单的方法,低BMI值(<18.5kg/m2或<20kg/m2)作为营养缺乏的标志,其准确度有限。血清ALB是营养不良和炎症的常见标志物,是监测癌症患者蛋白质能量代谢及营养不良的适当生物标志物。本研究发现消化道恶性肿瘤Ⅳ期患者NRS-2002评分分别与ALB、PA呈负相关,提示NRS-2002评分越高,血清ALB、PA越低,患者营养不良发生率越高。
营养风险筛查是必要的,营养支持对于癌症患者的治疗至关重要。本研究发现消化道恶性肿瘤Ⅳ期患者无论有无营养风险,营养支持率均较高,以肠外营养支持为主,可能与晚期癌症经口摄入障碍、厌食、精神抑郁等有关。代谢紊乱可导致蛋白质能量代谢负平衡,营养支持疗法可以满足癌症患者营养需求,提高姑息性抗癌治疗的耐受性[19],营养不足会削弱免疫系统,早期肠道营养支持可以保护胃肠道粘膜的完整性,增强患者免疫功能,促进术后恢复,降低肺部感染等并发症的发生率[20,21]。有效的营养评估,并进行针对性的营养干预,可改善癌症患者的生存、功能状态和体重。消化道恶性肿瘤晚期患者在姑息治疗阶段,及时有效的营养管理仍然是临床医生面临的一大挑战。对于口服摄入量减少的患者需要营养治疗,以保持营养状况并满足能量和蛋白质需求,但肠道营养过程中喂养不耐受率高达68%[22,23],如腹痛、腹胀、恶心和呕吐等。制定个性化膳食建议、选择最佳的营养途径均作为营养支持的一部分,应与每个患者的营养需求和主要症状相符[24]。
癌症患者姑息治疗阶段的营养支持可能更有助于改善其生存质量。开展规范的营养风险筛查,促进营养支持的个性化、规范化使用,有助于改善消化道晚期癌症患者的生存质量并延长生存期。

