乙基溴化镁与二异丙基酮反应的计算化学研究
黄职钱,杨一莹,马玉臣,张冬菊
山东大学化学与化工学院,济南 250100
格氏试剂(Grignard reagent)是一类有机镁卤化物的统称,通常表示为R-MgX,由法国化学家维克多·格林尼亚(Victor Grignard)在1900年发现[1]。格氏试剂的出现,在有机合成领域具有里程碑的意义[2],它将烷基由亲电基团转变为亲核基团,成为构建碳-碳键的重要手段,是有机合成化学中应用最多的有机化学试剂之一,意义重大、影响深远,被列入基础有机化学教科书,其发明人格林尼亚因此获得了1912年诺贝尔化学奖。
格氏试剂中Mg-C键是强极性共价键,富电子的碳具有很强的碱性和亲核性,化学性质极为活泼。格氏试剂最典型的反应是与羰基化合物的亲核加成反应,形成醇镁盐,经水解后得到相应的醇。该反应可以在羰基碳原子上引入一个烃基,使醛酮碳链延长,成为合成各种复杂的伯、仲、叔醇的重要策略。格氏试剂与羰基化合物除了发生亲核加成反应((1)式)之外,还涉及一些竞争的副反应,主要包括羰基化合物的还原反应((2)式)和烯醇化反应((3)式)等,这些副反应的存在是导致主产物产率不够理想的关键因素[3]。
尽管格氏试剂的使用已有100多年的历史,但由于其结构的复杂性致使人们对其反应机理的认识仍不够清晰,缺乏共识[3]。教科书[4]中对这些反应的介绍,仅是简单地进行定性描述,如图1所示,用格氏试剂的化学式R-MgX描述其与醛酮的反应机理,缺乏详细的定量信息。

图1 EtMgBr和CO(iPr)2的亲核加成反应、还原反应和烯醇化反应
最近,Eisenstein和Cascella课题组通过量子化学计算和从头算分子动力学模拟研究了甲基氯化镁格氏试剂(CH3MgCl)与乙醛和芴酮的加成反应[5],获得了一些关于反应机理的新结果,在学术界引起了较大反响,“phys.org”网站以“The 120-year old cold case for the Grignard reaction is finally solved”为题,对该工作进行了专题报道[6];“高分子科学前沿”(入选“2020学术公众号100强”)媒体号也以“诺奖‘格氏试剂’之谜终获解!或将更新教科书?”为题,对该工作进行了详细介绍[7]。Eisenstein和Cascella等研究者的主要发现是,格氏试剂在四氢呋喃溶剂中由于Schlenk平衡[8]((4)式)的存在,可通过多种形式同时与醛酮发生亲核加成反应,四氢呋喃溶剂对反应有明显的促进作用。

Eisenstein和Cascella课题组的最新研究成果,改进了人们对格氏试剂与羰基化合物亲核加成反应的理解。文献调研表明,对于格氏试剂与羰基化合物的还原反应和烯醇化反应,尚未有公开报道的理论研究。本文以(1)-(3)式所示的反应为例,通过量子化学计算系统研究乙基溴化镁和二异丙基酮的反应,以期澄清反应的分子机理,定量描述反应的动力学和热力学性质,加深对格氏试剂与羰基化合物反应性能的理解。
1 模型和计算方法
如(1)-(3)式所示,研究对象为乙基溴化镁(EtMgBr)与二异丙基酮(CO(iPr)2)的反应,溶剂为乙醚[9]。根据(4)式所示的Schlenk平衡,EtMgBr和MgEt2在乙醚溶剂中平衡共存,因此,计算考虑了EtMgBr和MgEt2两种组分的有机镁与CO(iPr)2的反应。为便于描述,将CO(iPr)2中羰基C原子和参与反应的三级C原子分别标记为C1和C2,EtMgBr中亚甲基C原子和甲基C原子分别标计为Cα和Cβ,如图1所示。
本研究基于密度泛函理论,使用M062X泛函[10]和6-311G(d,p)标准基组[11]对全部稳定点进行了结构优化和频率计算,确保局域最小点没有虚频,过渡态(一级鞍点)有且仅有一个虚频,并通过内禀反应坐标(IRC)[12]分析,确认了每个过渡态连接的反应物和产物。应用PCM连续介质模型[13]评估了溶剂化效应,在乙醚溶剂中对稳定点进行了全构型优化。全部计算使用Gaussian 16程序[14]完成。
2 结果与讨论
2.1 乙基溴化镁和二异丙基酮的反应
非显含溶剂情况下,计算的反应机理及势能面上各稳定点的相对能量示于图2a。反应从EtMgBr与CO(iPr)2的配位开始,形成络合物1a,放热43.1 kJ·mol−1,将该络合物的相对能量设置为参考点。图中黑色路径表示格氏试剂与羰基化合物的亲核加成反应,EtMgBr的Cα亲核进攻CO(iPr)2的C1,同时羰基O进攻Mg,形成四元环状过渡态TS1a,其相对能量为96.1 kJ·mol−1,得到醇镁盐产物2a,放热21.3 kJ·mol−1。蓝色路径表示羰基化合物的还原反应,EtMgBr上的Cβ-H迁移到CO(iPr)2的C1上,同时羰基O进攻Mg,形成六元环过渡态TS2a,克服98.2 kJ·mol−1的能垒,形成还原产物3a和乙烯,吸热20.9 kJ·mol−1。红色路径表示烯醇化过程,CO(iPr)2中的C2-H迁移到EtMgBr的Cα上,同时羰基O进攻Mg,形成六元环状过渡态TS3a,该过程需克服118.3 kJ·mol−1的能垒,得到烯醇化产物4a和乙烷,放热2.9 kJ·mol−1。这些结果表明,烯醇化反应显然是不利的,似乎可以解释实验观察到的极少量烯醇化产物,但亲核加成和还原过程的能垒仅相差2.1 kJ·mol−1,是相互竞争的反应,这与实验结果不符,实验报道的亲核加成产物与还原产物之比为77 : 21[9],即反应明显有利于亲核加成反应。

图2 EtMgBr与CO(iPr)2发生亲核加成(黑色)、还原反应(蓝色)和烯醇化反应(红色)的势能剖面图
根据Eisenstein和Cascella的研究[5],溶剂对反应有重要影响,因此进一步考虑了显含溶剂的情况。计算发现,EtMgBr与乙醚(Et2O)分子的配位是一个放热过程,其中两分子Et2O配位形成四面体配合物是热力学最有利的过程,放热88.9 kJ·mol−1,如(5)式所示。
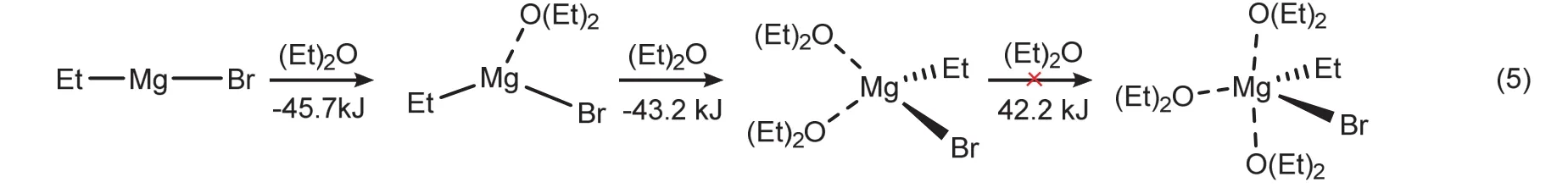
显含溶剂的计算结果示于图2b,将两分子Et2O配位的格氏试剂1b设置为能量参考点。反应从配体交换开始,CO(iPr)2取代一个Et2O分子,形成中间体2b,吸热13.0 kJ·mol−1。2b分别经过TS1b、TS2b、TS3b发生亲核加成、还原反应和烯醇化反应,从计算的过渡态结构参数,可以看出,Et2O分子在反应中是形式上的“旁观者”,相应的能垒分别为91.5、93.6和113.3 kJ·mol−1,这些结果与图1中未考虑溶剂参与反应的情况相比,能垒降低约5 kJ·mol−1,但三个反应的相对能垒定性没有变化,例如,TS1b与TS2b的能垒依然仅相差2.1 kJ·mol−1。
2.2 二乙基镁和二异丙基酮的反应
如(4)式所示,格氏试剂在溶剂中存在Schlenk平衡,乙基溴化镁EtMgBr与二烷基镁MgEt2共存。MgEt2中的烷基类似于格氏试剂中的烷基,具有强亲核性。因此,我们以MgEt2和CO(iPr)2为反应底物,重新对上述三个反应进行了计算,结果示于图3,其中图3a和3b分别描述非显含溶剂和显含溶剂的情况。
非显含溶剂时,将MgEt2与CO(iPr)2的配位物1c设置为能量参考点。亲核加成、还原反应和烯醇化反应分别经过TS1c、TS2c和TS3c得到相应的产物,对应的能垒分别为81.9、85.7和99.9 kJ·mol−1。与EtMgBr的反应(图2a)相比,能垒降低约12-18 kJ·mol−1。
显含溶剂时,三个反应的能垒分别进一步降低到69.0、76.9和97.0 kJ·mol−1,与EtMgBr对应的三个反应(图2b)相比能垒更低,特别是更有利于亲核加成反应,使其能垒比还原反应低7.9 kJ·mol−1。
将图3与图2比较,可以发现,MgEt2比EtMgBr更容易与CO(iPr)2发生反应,反应的能垒更低,放热更多。这些结果区别于教科书中对反应机理的定性描述(图1)。另外,对于本文研究的反应体系,根据阿伦尼乌斯公式,无论用EtMgBr或MgEt2作为反应底物,无论非显含溶剂或显含溶剂的反应,均是亲核加成反应最为有利,其次是还原反应,烯醇化反应的能垒最高,不能与亲核加成和还原反应竞争。这些结果与实验观察基本吻合,实验发现亲核加成产物产率为77%,还原产物产率为21%,而烯醇化产物产率仅为2%[9]。

图3 EtMgBr与CO(iPr)2发生亲核加成(黑色)、还原反应(蓝色)和烯醇化反应(红色)的势能剖面图
2.3 烷基取代基和溶剂对反应性能的影响
如上所述,MgEt2比EtMgBr更容易与CO(iPr)2反应,并且Et2O溶剂在Mg中心的配位使反应的能垒进一步降低。这些结果与取代基及醚配体的电子性质有关,EtMgBr中Br是吸电子取代基,而MgEt2中Et是给电子取代基、Et2O是富电子配体,上述三个反应均涉及Mg-C键的异裂,给电子取代基(Et)和富电子配体(Et2O)配体有利于Mg-C键的极化和异裂,从而使反应更容易进行。为定量理解烷基取代基和溶剂对反应性能的影响,进一步计算了MgEt2和EtMgBr中Mg-C键异裂过程的焓变,比较了Et2O配位数对焓变的影响,结果列于表1。可以看出,当底物相同时,随着Et2O溶剂配位数的增加,Mg-C键异裂的解离能显著降低;当Et2O配位数相同时,EtMgBr中Mg-C键的解离能明显高于MgEt2中Mg-C的键解离能。因此,MgEt2中的Mg-C键较弱,更容易断裂,反应能垒更低,反应更容易进行。
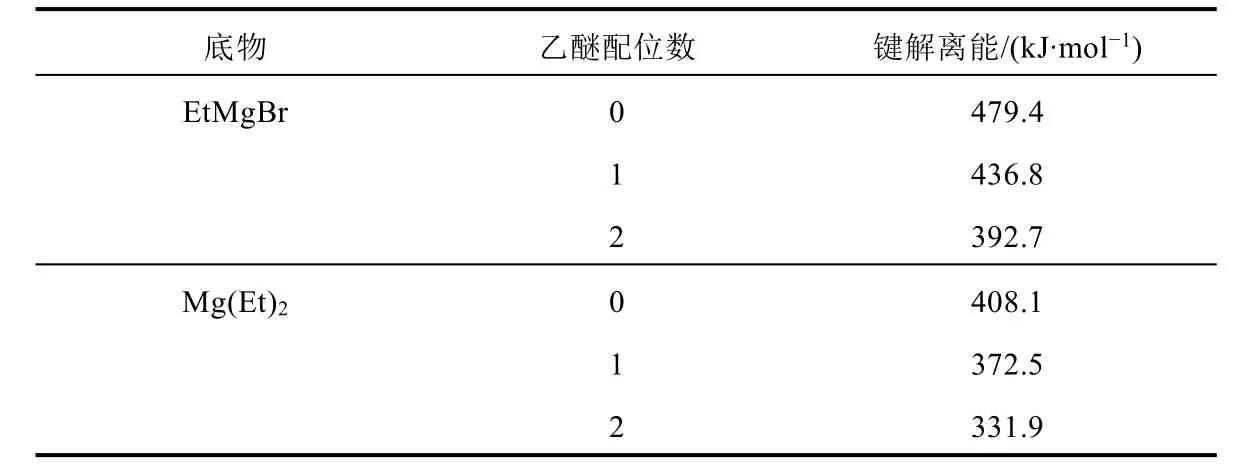
表1 EtMgBr和Mg(Et)2中Mg-C键异裂的键解离能
3 结语
基于密度泛函理论计算,系统研究了乙基溴化镁和二异丙基酮的亲核加成反应、还原反应和烯醇化反应。计算结果表明,相关的反应机理与教科书中描述的反应机理不同,MgEt2比EtMgBr具有更高的反应活性,是反应的主要活性组分;Et2O溶剂对反应性能有重要影响,通过与Mg配位促进Mg-C键极化,使反应更容易发生;亲核加成反应最容易发生,其次为还原反应,烯醇化反应最困难。理论结果为深刻理解格氏试剂与羰基化合物的反应提供了一定的理论依据。

