不同酯化度果胶钙的结构特征与体外消化稳定性
刘 娜,蒋茂婷,王 超,张广文,黄雪松
(暨南大学理工学院 广州 510632)
果胶钙是果胶中半乳糖醛酸(Galacturonic acid,GalA)上自由羧基(非酯化羧基)与Ca2+通过离子键结合形成的产物。酯化度(DE)是果胶分子中含酯化羧基的GalA 占总GalA 的百分比。一般地,DE≥50%的果胶为高酯果胶 (High methoxyl pectin,HMP),DE<50%的果胶为低酯果胶(Low methoxyl pectin,LMP),且LMP 中非甲酯化的GalA 区域能与Ca2+形成“蛋箱”结构[1]。果胶DE 是影响果胶钙结构及性能的重要因素[2]。目前尚未有不同DE 果胶的钙结合能力及所得果胶钙结构特点的相关报道。
果胶钙具有食用安全及生物相容性好的优点[3],常以水凝胶[4-5]、薄膜[6-7]、药物载体[8-9]等形式用于食品、药品、化工等诸多领域,虽应用广泛,但未见有关其消化性及补钙潜力的报道。果胶是易获得且具有益生元作用的多糖,可促进钙吸收,调节肠道菌群,改善宿主健康[10-11];其与Ca2+反应所得果胶钙,除具有果胶的上述作用外,还有补钙功能。本文探究不同DE 的果胶钙在体外模拟胃肠环境中的钙释放情况和消化稳定性,研究其结构特点。
1 材料与方法
1.1 材料与试剂
DE=10%,18%,41%,50%,59%的柑橘果胶粉,由浙江果源康品生物科技有限公司提供;半乳糖醛酸标准品、咔唑,上海麦克林生化科技有限公司;浓硫酸,广州市信洪贸易有限公司;乙二胺四乙酸(EDTA)、碳酸钙、氯化钙、氯化钠、碳酸氢钠、氯化钾、氢氧化钠,天津大茂化学试剂厂。
1.2 仪器与设备
FC204 型电子天平,上海精科天平厂;PL602-S 型电子天平,梅利勒-托利多中国地区;PHS-3C精密1pH 计,上海安亭雷磁仪器厂;UV-9600 紫外-可见分光光度计,北京瑞利分析仪器公司;LC-20AT 高效液相色谱仪,日本岛津公司;2000ES 蒸发光散射检测器,美国奥泰公司;DHG-9070 电热恒温鼓风干燥箱,上海一恒科技有限公司;KDC-1044 低速离心机,科大创新股份有限公司;SCIENTZ-10N 冷冻干燥机,宁波新芝生物科技有限公司。
1.3 方法
1.3.1 果胶钙的制备 将同一系列不同DE 的果胶分别制成1 g/100 mL 的果胶溶液,然后以果胶中半乳糖醛酸及Ca2+物质的量之比n果胶GalA∶nCa2+=1∶2 的比例加入氯化钙溶液,在50 ℃下恒温反应2 h 后,离心收集得到果胶钙粗品,再用蒸馏水反复洗涤沉淀,洗至其上清液中的Ca2+浓度与蒸馏水无异,洗后沉淀经冷冻干燥后得到相应的果胶钙纯品。即以DE=10%,18%,41%,50%,59%的果胶制备的果胶钙分别命名为DE10-CaP、DE18-CaP、DE41-CaP、DE50-CaP、DE59-CaP。
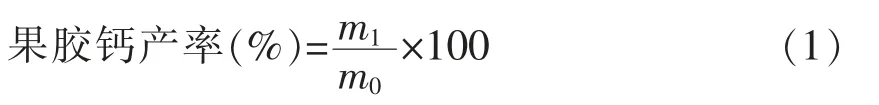
式中,m1——果胶钙冻干后的质量,g;m0——果胶粉原料的质量,g。
1.3.2 高效凝胶色谱法测定相对分子质量[12]采用色谱柱PolySep-GFC-P4000 柱 (7.8 mm×300 mm),进样量15 μL,纯水流动相,流速0.5 mL/min,柱温30 ℃,检测器为2000ES 蒸发光散射检测器的条件进行高效凝胶色谱测定。
分别用葡萄糖和T-400 葡聚糖标定保留时间Vt和V0,将已知相对分子质量的Dextran 系列标准品(T-5、T-20、T-40、T-200、T-500)溶于水中,配制成1 mg/mL 的标准溶液,过0.45 μm 微孔滤膜后进样。由保留时间(Ve)计算得到相应的分配系数(Kav),Kav 和Ve存在如下关系:

以lgMw(分子质量的对数)为横坐标,Kav 为纵坐标绘制标准曲线,得到线性回归方程后,将待测样品配制成1 mg/mL 的溶液,按上述测定条件测定,并将结果代入标准曲线,计算得到其分子质量。
1.3.3 X-射线衍射 采用波长为0.1542 nm 的单色Cu-Kα 射线,测试条件为:管压36 kV,管流20 mA,扫描速度2°/min,扫描区域10°~30°,采样步宽0.05[13]。
1.3.4 傅里叶红外光谱的测定 果胶的红外扫描图谱采用KBr 压片法,以1∶100 的质量比将样品KBr 混合并研磨均匀,用压片机进行压片(压力为10 MPa)30 s,取下后得到薄片,用傅里叶变换红外光谱仪进行红外光谱的扫描,扫描范围500~4 000 cm-1。
1.3.5 扫描电子显微镜 采用扫描电子显微镜观察该果胶钙的微观结构。将干燥后的果胶钙粘到铜台的导电胶上,在样品表面喷金后上机观察。试验条件:加速电压为20 kV,电子束的穿透能力0.6 nm。
1.3.6 测定不同DE 果胶钙在体外模拟肠胃体系[14]中的稳定性 果胶钙的消化过程需经过胃肠道再被肠道微生物降解利用,人体胃肠道中并未含有可分解果胶或果胶钙的酶,且对果胶钙消化影响最大的是胃肠酸碱环境,故本试验用胃肠电解质液模拟其在人体胃肠中的消化情况。
胃电解质液的配制:准确称取3.1 g NaCl、1.1 g KCl、0.6 g NaHCO3,用蒸馏水定容1 L 后,用0.5 mol/L 的HCl 溶液将pH 值调至2;肠电解质液的配制:准确称取5.4 g NaCl 与0.65 g KCl,用蒸馏水定容至1 L 后用0.5 mol/L 的NaOH 溶液将pH值调至8。
量取5 mL 胃电解质液放入试管中,加入50 mg 果胶钙样品后放入恒温振荡器(37 ℃)中消化2 h 后向试管加入5 mL 肠电解质液并用NaOH 溶液将pH 值调至7.5,在将其放入恒温振荡器(37℃)中消化2 h。

1.3.7 钙含量测定方法 果胶酸钙中钙含量的测定用GB 5009.92-2016《食品安全国家标准 食品中钙的测定》 中的第一法——火焰原子吸收光谱法进行测定。
胃肠液中钙含量的测定方法用GB 5009.92-2016《食品安全国家标准 食品中钙的测定》中的第二法——EDTA 法进行测定。
1.3.8 数据处理 用SPSS 软件分析,用Origin 软件作图。
2 结果与分析
2.1 果胶DE 对果胶钙产率的影响
从图1a 中可以看出:随DE 的增大,果胶钙产率先增加后减少。DE=41%的果胶与氯化钙反应所得果胶钙(DE41-CaP)产率最高(87%),DE10-CaP 产率最低(50%)。从理论分析可知,Ca2+是与果胶分子中的自由羧基结合,即DE 越低(其自由羧基越多),其结合钙的能力越强,果胶钙产率越高[15];然而,由图1a 可知,果胶钙产率变化趋势并不符合上述规律,这是因为果胶钙产率除与果胶DE 有关外,还应与其分子质量大小有关,即果胶DE 相同时,分子质量越大,单位果胶分子结合Ca2+的能力越强[16](因实际上难以得到同一分子质量且DE 不同的果胶,故本试验购买的不同DE 果胶,其分子质量有所差异,如图1a),故图1a 中果胶钙产率并未完全随果胶DE 的减小而增加,可能与果胶分子质量不同有关。
如果引入果胶钙中Ca2+与果胶物质的量之比A(A=n果胶∶nCa2+,可反映单个果胶分子结合钙的能力),则从图1b 可以看出,对于低酯果胶钙(Ca-LMP)来说,其A 值与果胶原料的分子质量大小成正比;而对于高酯果胶钙(Ca-HMP)来说,其A 值则与果胶原料中自由羧基量成正比。这说明分子质量对LMP 分子结合钙的能力(即A 值)影响较大,而DE 对HMP 分子结合钙的能力影响较大。此外,Ca-HMP 的A 值范围为716~859,Ca-LMP的A 值范围为1 372~1 548,远大于Ca-HMP 的A值,从总体来说,果胶DE 对单个果胶分子钙结合能力的影响比分子质量更大。
由图1a 可知,Ca-LMP 的钙含量较高,适合做补钙剂,且未经洗涤的果胶钙中钙含量更高。周建烈等[17]的报道称正常成人钙摄入推荐量为800 mg/d,而我国居民每日从饮食中摄入的钙约为400 mg,故额外摄入4~5 g DE10-CaP 可满足正常成人每日钙需求。果胶钙进入肠道后,经肠道菌群逐步发酵分解,可改善肠道健康、缓解便秘,且不会产生反射性抑制钙吸收作用,是良好的钙制剂原料[18]。

图1 不同DE 果胶所得果胶钙的产率及Ca2+与果胶物质的量之比Fig.1 The yield of pectin calcium obtained from pectin with different DE and its ratio of amount of substance of Ca2+ to pectin
2.2 果胶DE 对果胶钙含钙率和果胶钙结构的影响
由图2可知,DE10-CaP 的钙含量最高(88 mg/g),DE59-CaP 的钙含量最低(43.6 mg/g),随果胶DE 的增大,果胶钙的钙含量逐渐减小,且Ca-HMP 的钙含量远低于Ca-LMP,是因为果胶DE越小,自由羧基的比例越高,单位物质的量(或质量) 果胶结合的Ca2+数量越多。分析图2中不同DE 果胶与钙反应时的Ca2+物质的量数与自由羧基物质的量数之比(I=nCa2+:n-COOH)可知:5 种果胶钙的I 值均在0.51~0.72 范围,I 值可在一定程度上反应自由羧基与Ca2+的结合方式,而钙离子与自由羧基的结合方式有3 类[19](如图3):(a)桥式配位型,(b)Ⅱ双齿配位型(螯合);(c)Ⅲ单齿配位型。其中,Ⅰ型结合可分为2 种:①一个自由羧基结合两个Ca2+,I=2,其电荷不平衡,难以形成稳定的果胶钙结构;②两个自由羧基与两个Ca2+结合,I=1,可达到电荷平衡;Ⅱ型属于稳定的四元环结构,其I=1,可达到电荷平衡;Ⅲ型结构也可分为2种:①一个自由羧基结合一个Ca2+,I=1,其电荷不平衡;②两个自由羧基结合一个Ca2+,I=0.5,可达到电荷平衡。
由图2可知,果胶钙的I 值更接近0.5,故果胶钙中自由羧基与Ca2+最可能的结合方式是Ⅲ型中第②种,即一个Ca2+结合两个自由羧基的单齿配位结构,由此进一步了解并完善果胶钙的结合示意图(如图4)。部分果胶钙的I>0.5,可能是因为大分子果胶具有包埋力,致使少量Ca2+虽未与自由羧基结合但仍残存在果胶钙内。

图2 不同DE 果胶钙的钙含量及Ca2+与自由羧基物质的量之比Fig.2 The calcium content and the ratio of amount of substance of Ca2+ to the free carboxyl groups of pectin calcium with different degrees of esterification

图3 羧酸根与Ca2+的配位方式Fig.3 Coordination mode of carboxylate and Ca2+

图4 果胶钙中羧酸根与Ca2+的结合形式示意图Fig.4 The binding form of carboxylate and Ca2+ in pectin calcium
从图4可以看出,羧酸根与Ca2+的结合区域可分为以下2 种类型:1)A 型,连续结合型,即为Grant 等[1]提出的“蛋箱”结构,A 型结合区域的比例会随着自由羧基含量的增加而增加,即低DE、高GalA 含量的果胶钙分子中,A 型结合区域占比更高;其应主要存在于Ca-LMP 中。这种多个离子键的紧密结合会形成较强的结构特性,提高干性果胶钙凝胶的刚性、结晶度等,但该结构的包埋力可能较差。2)B 型,不同果胶链间通过单个或两个Ca2+交联,且交联位置、方向、角度随机;其应主要存在于Ca-HMP 中,该型结合区域对于果胶钙的包埋性质可能有重要影响。3)C 型,同一条果胶分子链上的不同羧基与Ca2+结合,该结合区域存在的概率虽可能较小,但在Ca-HMP 和Ca-LMP 中都应存在;其亦应影响果胶钙的包埋性质。
由此可见,不同DE、分子质量、GalA 含量的果胶所形成的果胶钙,其钙含量、结构特征、物理性能等有很大的差异。需要注意的是,不同DE 果胶钙中羧酸根与Ca2+的结合情况复杂且不均匀,图4为羧酸根与Ca2+结合类型的模式图,不代表所有果胶钙中的实际情况。
2.3 果胶钙中羧酸根与钙结合的红外光谱特征
由图5可知,果胶DE 越大,所得果胶钙中甲基酯羧基的特征峰PK1(1 741~1 744 cm-1)越强。此外,PK2 为羧酸钙COO 的非对称伸缩振动峰(1 612~1 615 cm-1);PK3 为COO 的非对称伸缩振动峰(1 331~1 334 cm-1);PK4 为CH3不对称变角振动与CH2变角振动的重叠峰(1 424~1 436 cm-1)。

图5 不同DE 果胶钙的红外光谱图Fig.5 Infrared spectrum of pectin calcium with different DE
据羧酸盐类化合物基团的振动频率理论[19],Ca2+与自由羧基可能有3 种结合方式(见图3),其中Ca2+与羧酸根以单齿配位结构存在时,其差值应在200 cm-1以上。由表1可知:所得5 种果胶钙的差值都大于200 cm-1,符合Ⅲ型单齿配位结构存在的规律,进一步证实了2.2 节中根据I=0.5 所得的分析与结论。

表1 不同DE 果胶钙中羧酸根(COO)非对称和对称伸缩振动波数差值Table 1 Difference between asymmetric and symmetric stretching vibration frequencies of carboxylate (COO)in pectin calcium with different DE
2.4 不同DE 果胶钙的XRD 衍射图分析
果胶钙的XRD 图只有宽衍射峰(如图6),表明其晶体有缺陷且结晶程度低,其中DE10-CaP、DE18-CaP、DE41-CaP 3 种Ca-LMP 的峰形与峰位置与郭秀君[20]的研究结果接近,即分别在2θ=13°~15°及2θ=21.5°处出现了宽而矮的“馒头峰”,根据布拉格方程,其对应的晶面d 间距约为0.63 nm 和0.41 nm,故2θ=13°~15°衍射峰提供分子链间的横向堆积形式的信息;2θ=21.5°衍射峰则提供沿分子链方向的层间距信息[21-22]。
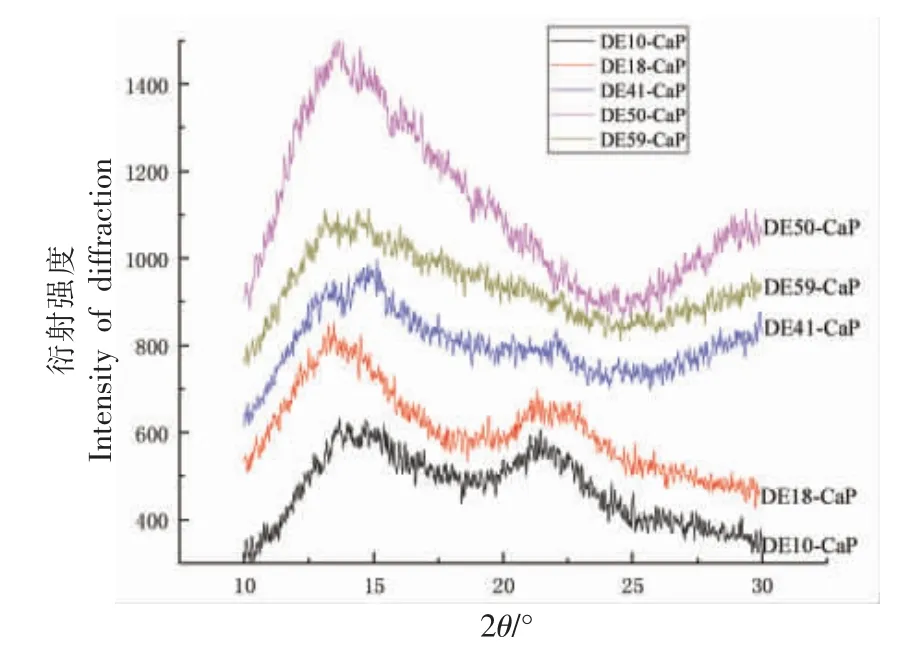
图6 不同DE 果胶钙的XRD 衍射图Fig.6 XRD patterns of pectin calcium with different DE
比较各果胶钙的XRD 衍射图可知,随DE 的增加,果胶钙在2θ=21.5°处的衍射峰逐渐宽化、弥散且衍射强度变小直至消失,表明其对应的晶面数减少或晶面完整度减小。由此推断,Ca-HMP 的特征峰为2θ=13°~15°,而Ca-LMP 的特征峰为2θ=13°~15°及2θ=21.5°。此外,考虑到前述的A 型区域(即“蛋箱”结构)应主要存在于Ca-LMP 中,因此推断2θ=21.5°处的衍射峰应是果胶钙中 “蛋箱”结构的特征峰。
2.5 不同DE 果胶钙消化前、后的表观结构分析
图7a 为以DE10-CaP 为代表的Ca-LMP 的SEM 图,图7c 为以DE59-CaP 为代表的Ca-HMP的SEM 图,DE10-CaP 的空间形貌以厚块状为主,而DE59-CaP 则呈轻薄、光滑、平整的大薄片状。一般地,Ca-LMP 表观结构更致密且呈块状,可能是因为其有更高比例、更完整的A 型结合域,这种结构上的差异会影响消化稳定性。
经模拟消化后,Ca-LMP、Ca-HMP 的表观结构均有不同程度的破坏。消化后的DE10-CaP(7b)表面有许多被分解的残片及絮状物,其中图7b1 是消化后的DE10-CaP 表面残片在2 000×倍下的电镜图,可清晰地看到果胶钙被解离留下的孔洞;而消化后的DE59-CaP(7d)则出现了明显的碎片化,其分解程度较DE10-CaP 更高,这说明Ca-HMP 结构稳定性更差。
2.6 不同DE 果胶钙在模拟胃肠环境中的消化稳定性
由图8可知,随果胶钙DE 增大,其经胃肠消化后Ca2+的释放量及释放率皆呈增加趋势,DE10-CaP 的钙释放率最低 (20.64%),DE59-CaP 最高(57.34%),其消化率及解离程度亦最高,与SEM的表征结果相符。Ca-LMP 的钙释放量、钙释放率比Ca-HMP 低,是因为Ca-LMP 中有更多、更完整的A 型结合区域,Ca2+结合得更稳固;而Ca-HMP则易被破坏。这说明Ca-LMP 的稳定性更强。
由图9可知,随果胶钙DE 的增加,其在胃肠液中的GalA 释放量大体上呈逐渐增大的趋势。对比图8可知,GalA 释放量与钙释放量的趋势存在一定程度的一致性,是因为果胶钙中Ca2+的释放会引起GalA 的释放,其释放量越大,结构破坏则越严重,故图7中消化后的DE59-CaP 表观结构破坏程度比DE10-CaP 严重。

图7 DE10-CaP、DE59-CaP 消化前、后的SEM 图Fig.7 SEM images of DE10-CaP and DE59-CaP before and after digestion

图8 不同DE 果胶钙的钙释放量及释放百分率Fig.8 Calcium release amount and percentage of pectin calcium with different degrees of esterification

图9 不同DE 果胶钙的GalA 释放量Fig.9 The amount of galacturonic acid releasing of pectin calcium with different degrees of esterification
3 结论
本研究用DE=10%,18%,41%,50%,59% 5种果胶制备了5 种果胶钙,所得果胶钙的产率范围为50%~87%;果胶的DE 越小、分子质量越大,所得果胶钙的产率越高;果胶钙的钙含量范围为43.6~88 mg/g,以DE=10%的果胶与Ca2+反应形成的果胶钙(DE10-CaP)的钙含量最高(88 mg/g),DE59-CaP 的钙含量最低(43.6 mg/g);根据果胶钙中的Ca2+与自由羧基的物质的量之比与红外光谱分析,得出Ca-LMP、Ca-HMP 中Ca2+与羧酸根均以单齿配位型结合;进一步提出了果胶钙中羧酸根与Ca2+的3 种结合区域类型,既肯定了果胶钙原有的“蛋箱”结构,又完善了其结合模式。XRD表明,Ca-HMP 仅有一个2θ=13°~15°衍射特征峰,而Ca-LMP 还多一个2θ=21.5°衍射特征峰 (“蛋箱”结构特征峰),这两个峰所代表的具体意义还有待进一步分析;SEM 表明Ca-LMP 的表观结构更紧密且呈块状,Ca-HMP 则呈薄片状。两种果胶钙在包埋能力、干性凝胶刚性等方面的差异,还有待进一步对比研究。
在果胶钙体外消化试验中,通过扫描电镜对以DE10-CaP 为代表的Ca-LMP 及以DE59-CaP为代表的Ca-HMP 进行了分析,发现Ca-HMP 的表观破坏程度明显大于Ca-LMP。最后,对比了5种果胶钙在体外胃肠模拟消化中钙及GalA 的释放情况,发现Ca-HMP 的钙释放率、钙释放量及GalA 释放量均高于Ca-LMP,即Ca-LMP 在胃肠环境中的稳定性高于Ca-HMP。
本文研究有助于深入理解果胶钙的微观结构,同时为以果胶钙为原料的补钙产品开发提供了体外模拟胃肠消化的数据,还需其它更多更深入的研究促进果胶钙在保健品领域的应用,例如探究人体肠道菌群对果胶钙的利用情况。

