仑伐替尼联合信迪利单抗二线治疗肝内胆管癌的效果和安全性
丁晓燕, 孙 巍, 申燕军, 滕 颖, 许雅文, 李文东, 陈京龙
北京地坛医院 肿瘤内科, 北京 100015
肝内胆管癌(intrahepatic cholangiocarcinoma, ICC)是一种恶性程度较高的肿瘤,虽然目前相对比较少见,但发病率及病死率在全球范围内均呈逐年上升趋势[1-2]。手术切除是治疗ICC重要的治疗方式,但由于其早期症状不典型,患者在初诊时往往已丧失手术切除机会,即使患者接受根治性切除,其术后复发率高达70%[3]。联合化疗是中晚期ICC标准一线治疗方式,方案主要为吉西他滨或氟尿嘧啶为基础的联合治疗方案[4-5]。但吉西他滨联合顺铂(GP方案)作为标准一线方案中位无进展生存时间(median progress-free survival, mPFS)亦仅仅只有8.0个月,患者不可避免要接受后线治疗。
目前ICC的二线治疗缺乏有效的治疗方案,虽然 ABC-06研究提示mFOLFOX方案相较于最佳支持治疗可以改善一线GP方案失败后胆道癌患者的一年生存率,但总生存时间(overall survival, OS)改善却不明显(6.2个月vs 5.3个月),而且在亚组分析中ICC组结果类似[6]。近年来随着免疫治疗的兴起,免疫检查点抑制剂在ICC中也逐步被探索应用,免疫检查点抑制剂联合仑伐替尼已在肝细胞癌中展现了优秀的应用前景[7-8],其中程序性细胞死亡蛋白-1(programmed death-1, PD-1)抑制剂信迪利单抗已被广泛用于肝癌治疗。这种具有潜力的联合治疗方案在ICC中研究尚不充分,因此本研究旨在探讨信迪利单抗联合仑伐替尼对后线治疗晚期ICC的效果及安全性。
1 资料与方法
1.1 研究对象 回顾性分析2019年10月31日—2021年10月31日本院收入的使用信迪利单抗和仑伐替尼治疗的术后转移性或无法手术的ICC患者的病例资料,进行电话随访及病例资料收集。患者在接受治疗前已被充分告知临床获益及不良反应。纳入标准: (1)病理诊断为ICC;(2)无法手术根治;(3)一线化疗无法耐受或进展的患者;(4)具有实体瘤评价标准(RECISIT)1.1要求的可测量病灶;(5)临床及随访资料完整。分期采用American Joint Committee on Cancer (AJCC) 分期第8版标准[9]。排除标准:(1)心肺或肝肾功能衰竭;(2)伴随严重或致命性并发症;(3)PD-1抑制剂或仑伐替尼使用禁忌。
1.2 方法 系统性治疗:根据患者体质量予以仑伐替尼口服( ≥60 kg,12 mg;<60 kg,8 mg),1 次/d。信迪利单抗注射液 200 mg,每 3 周 1 次。
1.3 观察终点 主要观察终点为疾病进展时间(time to progress,TTP),次要观察终点为OS,疾病客观缓解率(objective response rate,ORR),疾病控制率(disease control rate,DCR)和不良事件发生率。ORR=[完全缓解(complete response,CR)+部分缓解(partial response,PR)]/总病例数;DCR=[CR+PR+疾病稳定(stable disease,SD)]/总病例数。参考不良事件通用术语标准(CTCAE)v4. 03观察治疗的不良反应并评估。
1.4 随访和疗效评估 治疗期间每2~3个月行腹部增强MRI或CT及胸部增强CT检查等,采用 RECIST 1.1疗效评价标准[10]。 患者治疗后每3周进行1次安全性随访,随访内容包括血压、体质量、不良反应(皮疹、疲劳、食欲下降、恶心、 呕吐、腹泻等) 及血尿常规、肝肾功能、甲状腺功能化验结果。出院后采用电话、微信及门诊复查等方式进行。终点为患者死亡或2021年12月31日。
1.5 统计学方法 采用SPSS 25.0统计软件进行数据分析。计量资料用中位数(最小值~最大值)表示。Kaplan-Meier法绘制生存曲线,组间差异采用log-rank检验。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 本研究共入组患者27例,基线资料和治疗情况见表1。肝功能分级均为Child-Pugh A 级。27例患者中术后转移7例,其中单纯远处淋巴结转移4例,骨转移并肺转移1例,肺转移合并淋巴结转移、肝转移2例;初始无法手术的局部晚期、晚期ICC 20例(Ⅱ期3例,ⅢB期1例,Ⅳ期16例);21例有淋巴结转移(包括腹膜后淋巴结、肝门部淋巴结、纵隔淋巴结和锁骨上淋巴结),13例患者有淋巴结以外的远处转移(肺转移9例,骨转移6例,脾脏转移1例,肾脏转移1例,腹膜转移1例)。27例患者中,因肝硬化采用一线替吉奥方案无法耐受4例,1例无法耐受吉西他滨联合奥沙利铂,其余吉西他滨联合注射用紫杉醇(白蛋白结合型)2例、吉西他滨联合顺铂方案4例、单药替吉奥16例一线治疗后进展。13例患者在一线化疗间期联合TACE(肝动脉化疗栓塞术)。
2.2 临床疗效(ORR和DCR) 根据RECIST 1.1疗效评价标准,27例患者中1例(3.7%)疗效达CR,10例(37.0%)肿瘤明显缩小达PR,8例(29.6%)肿瘤稳定SD,8例(29.6%)患者疾病进展(PD)。ORR为40.7%,DCR为70.4%。2例患者在肿瘤治疗达PR后行根治性手术。肿瘤治疗效果瀑布图见图1。
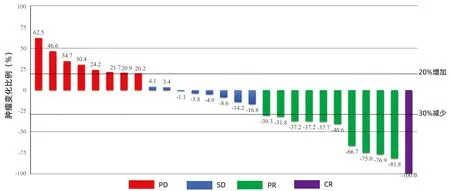
图1 肿瘤治疗效果瀑布图

表1 患者基线特征和治疗情况Table 1 Patients’ baseline characteristics and treatment
2.3 临床疗效(TTP和OS) 截止2021年12月31日,19例(70.4%)患者为PD,中位TTP为5.5个月(95%CI:1.7~9.3)(图2a)。合并淋巴结转移的患者中位TTP[4.5个月(95%CI:1.8~7.2)]与无淋巴结转移患者(18.8个月)比较显著缩短(P=0.035)(图2b)。获得疾病缓解的患者,中位TTP显著延长[11.6个月(95%CI:5.6~17.6) vs 2.8个月(95%CI:1.8~3.8),P<0.001](图2c)。

注:a,全组人群;b,是否合并淋巴结转移的患者;c,不同肿瘤治疗效果的患者。
13例(48.1%)患者因疾病死亡,中位OS为11.2个月(95%CI:5.0~17.4)(图3a)。合并淋巴结转移的患者中位OS有缩短趋势[9.6个月(7.9~11.3) vs 21.9个月(95%CI:0~44.9),P=0.053](图3b),疾病获得缓解的患者中位OS显著延长[16.6个月(95%CI:9.0~24.2)vs 6.9个月(95%CI:3.6~10.2),P=0.011](图3c)。
2.4 不良事件 27例患者中有66.7%(18例)发生了不同程度的不良事件,40.7%(11例)出现了≥3的不良事件。常见不良反应见表2。ALT和AST升高分别为12例(44.4%),1例为Ⅳ度,诊断为免疫相关性肝脏毒性,经激素治疗后缓解无后遗症,导致信迪利单抗永久性停药;高血压10例(37.0%),其中Ⅲ度高血压3例,予以钙通道拮抗剂和血管紧张素转化酶抑制剂联合降压治疗;总胆红素升高和直接胆红素升高8例(29.6%),1例为Ⅳ度,考虑与疾病进展有关;严重不良事件除以上外,还有感染4例,考虑均与TACE治疗相关,6例患者因Ⅳ度转氨酶升高,感染和Ⅲ度血小板下降药物暂停。这些严重不良事件均缓解且无后遗症。
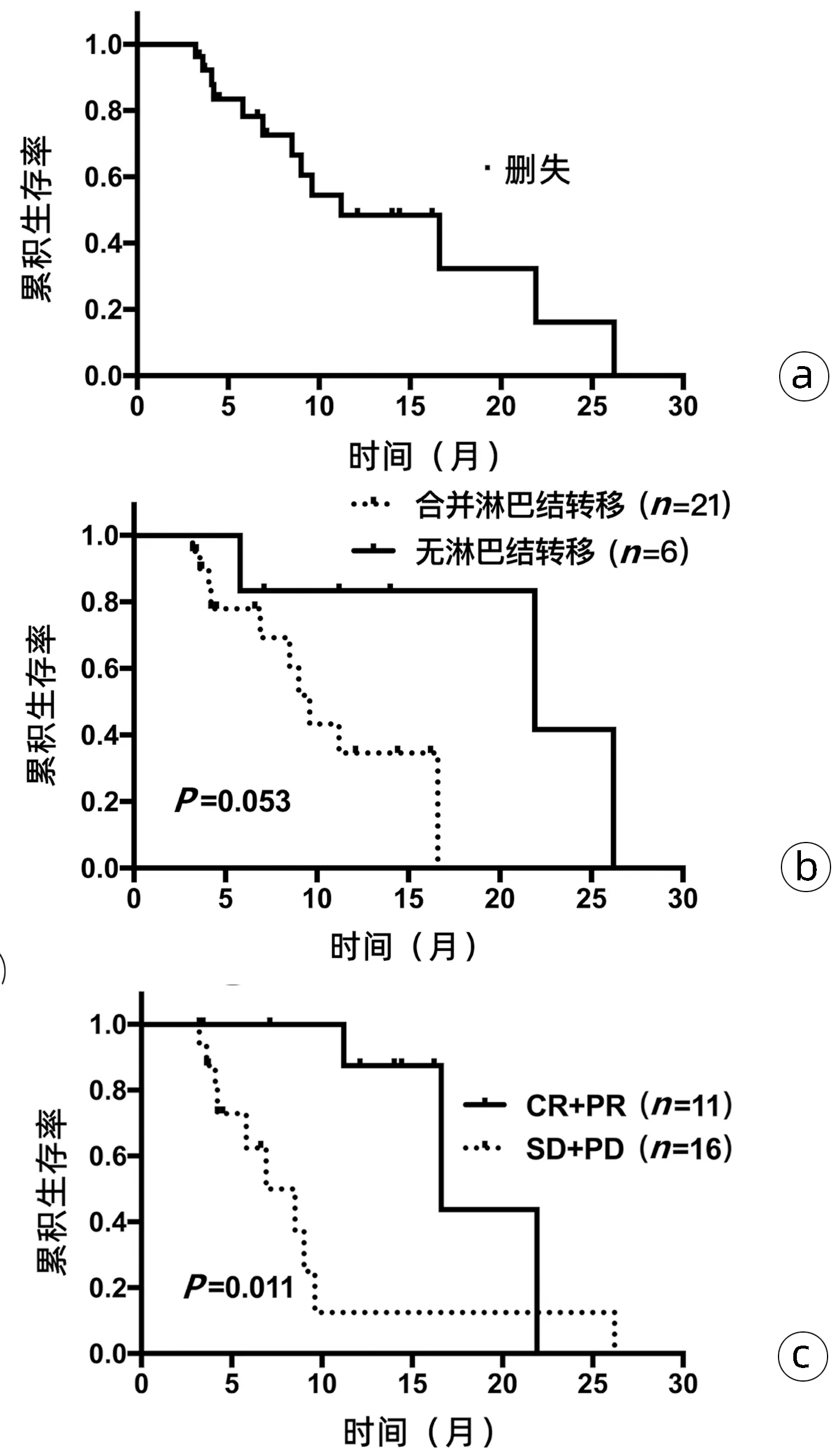
注:a,全组人群;b,是否合并淋巴结转移的患者;c,不同肿瘤治疗效果患者。
3 讨论
迄今为止手术切除依然是根治ICC的最佳方式[3],但多数患者发现时已是中晚期,无手术切除机会[11]。令人遗憾的是一线化疗方案失败的患者目前没有推荐的标准二线治疗方案。血管内皮生长因子(vascular endothelial growth factor, VEGF)、成纤维细胞生长因子受体4和血小板衍生生长因子受体(platelet derived growth factor receptor, PDGFR)在ICC患者中往往高表达,而且与预后不佳有相关性[12-14],仑伐替尼是一种口服多激酶抑制剂(multikinase inhibitor, TKI),靶向作用于VEGF受体、FGFRs、PDGFRα、RET和KIT[15],既往研究[16]显示,仑伐替尼可通过抗血管生成作用增强肿瘤微环境中T淋巴细胞的抗肿瘤活性,从而增强了抗程序性死亡受体1(programmed death-1, PD-1)及其配体(programmed death ligand-1, PD-L1)抗体的抗肿瘤作用。仑伐替尼联合PD-1抑制剂已经在肝细胞癌等瘤种中显示出很好的应用前景[17],但这种治疗方式目前尚未被批准用于ICC。本研究结果表明,仑伐替尼+信迪利单抗注射液二线治疗晚期ICC可能提供强大的抗肿瘤作用,并允许部分患者实现降期和手术治疗。

表2 常见不良反应及发生率Table 2 Common adverse events and frequency
疗效方面,本研究DCR为70.4%,ORR为40.7%,中位TTP为5.5个月,中位OS为11.2月。ABC-06是一项针对一线治疗失败胆道癌的研究[6],对比了单独积极支持治疗和FOLFOX方案联合积极支持治疗;尽管FOLFOX方案组1年OS率较单独支持治疗组有所提高(11.4% vs 25.9%),但无统计学差异,且中位OS并无明显改善;提示二线化疗无法改善晚期胆道癌的预后,亟需探讨其他的治疗方案。一项应用仑伐替尼二线治疗不可切除胆道癌的2期临床研究显示ORR为11.5%(95%CI: 3.2%~27.2%);3例(11.5%)患者PR,19例(73.1%)患者为SD。PFS为3.19个月(95%CI: 2.79~7.23)[18],提示二线单药仑伐替尼针对晚期胆道癌有一定的疗效。此外,KEYNOTE-158研究[19]纳入了104例不可切除或转移性胆道癌,单药帕博利珠单抗治疗的 ORR为5.8%,mPFS为2.0个月,mOS为9.1个月。另一项前瞻性研究[20]应用纳武利尤单抗治疗45例难治性转移性胆道癌,结果显示ORR为22%,mPFS为3.77个月,mOS为10.33个月。两项PD-1抑制剂单药的研究提示晚期胆道癌使用PD-1抑制剂的潜在前景。上述研究结果显示无论是单药TKI还是单药PD-1抑制剂有效率均较低,本研究中ORR高达40.7%,但是鉴于本研究样本量少、肿瘤基线状态和肿瘤类型不一致,对于疗效数据尚需谨慎解读。Lin等[21]一项关于仑伐替尼联合帕博利珠单抗治疗难治性胆道癌的ORR为25%、DCR为78.1%、mPFS及mOS分别为4.9个月(95%CI: 4.7~5.2)、11.0个月(95%CI: 9.6~12.3)。该研究的总体PFS、OS与本研究大体类似,ORR结果略低于本研究,分析原因可能为采用了不同的PD-1抑制剂,且肿瘤类型和肿瘤基线状态不一致。有关仑伐替尼和PD-1抑制剂协同增敏的机制,主要在于仑伐替尼不仅自身具有抗肿瘤活性,还能通过减少肿瘤微环境中的肿瘤相关巨噬细胞,增加CD8+T淋巴细胞的数目、增强CD8+T淋巴细胞分泌IFNγ和颗粒酶B的活性,从而减轻肿瘤免疫抑制的微环境[22]。
当然对于存在微卫星不稳定/错配修缺陷的胆道癌,单药PD-1抑制剂可能具有更好的效果,KEYNOTE-158研究[19]后续分析显示,单药帕博利珠单抗治疗上述人群的ORR可达到40.9%,mPFS为4.2个月。但是二代NGS测序并未纳入医保,费用高,尚需寻找经济、实惠的预测靶免联合治疗ICC疗效的生物标志物。
安全性方面,本研究显示仑伐替尼联合信迪利单抗注射液总体耐受性良好,66.7%的患者存在不良事件,没有治疗相关的死亡;其中40.7%的患者出现3级及以上的不良事件,仅1例诊断为免疫相关性肝毒性,略低于既往靶向免疫联合治疗胆道恶性肿瘤结果,Lin等[21]研究显示100%的患者经历了不良事件, 59.3%的患者经历了≥3级不良事件,略高于本研究,一项应用仑伐替尼联合PD-1抑制剂一线治疗不可切除胆道恶性肿瘤的研究[23]显示不良事件发生率为84.2%、其中≥3级不良事件发生率为34.2%,与本研究类似。本研究最常见不良反应为乏力、高血压、胆红素升高及腹泻等,与既往研究[21,23]结果类似;本研究观察到1例3级及以上免疫相关不良事件,为Ⅳ度免疫性肝炎,经激素治疗后好转,未出现后遗症。总的来说,仑伐替尼+信迪利单抗注射液的联合治疗方案耐受性良好,所有毒性都在可控范围内。
综上所述,仑伐替尼联合信迪利单抗注射液二线治疗ICC具有良好的有效性及安全性,但本研究为回顾性研究且纳入病例数较少,后续仍需大样本、前瞻性随机对照试验来进一步评价ICC的二线联合治疗方式。
伦理学声明:本研究方案经由北京地坛医院伦理委员会审批,批号为京地伦科字(2021)-043号(2021-12-23),所纳入患者均签署知情同意书。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突,特此声明。
作者贡献声明:丁晓燕、陈京龙负责课题设计,资料分析, 撰写论文; 孙巍、申燕军、滕颖、丁晓燕、许雅文、李文东参与收集数据,修改论文; 陈京龙负责拟定写作思路,指导撰写文章并最后定稿。

