非小细胞肺癌铁死亡相关基因筛选及其与患者预后关系生物信息分析
庄文珺
天津市职业病防治院(工人医院)综合内科 300011
新进的癌症统计学数据(2020年)显示,肺癌占所有恶性肿瘤死亡人数的近1/4[1],由于其高发病和高死亡率,NSCLC已成为全球范围内的重大公共卫生问题。尽管随着NSCLC治疗包括靶向治疗、放疗等技术的不断进展,NSCLC的预后仍然不乐观,晚期患者远期生存率仍很低[2]。因此,仍需要对NSCLC有更好的认识,并识别新的生物标志物对患者的预后及相关因素进行分析。铁死亡是一种由铁依赖引起的非限制性脂质过氧化导致的细胞死亡[3]。铁死亡与恶性肿瘤的发生及预后存在明显的相关性。铁诱导的非限制性脂质过氧化在癌细胞中会释放代谢产物,调节免疫反应。已有文献报道,铁死亡相关基因的差异表达在多种肿瘤包括NSCLC中普遍存在,并可能与肿瘤的生物学行为及预后有关[4-5]。因此,筛选肺癌预后相关的铁死亡基因有望为NSCLC的靶向治疗提供新的思路。
1 数据与方法
1.1 数据来源及数据库分析 选取基因表达谱公共数据库GEO,中收录的关于NSCLC基因表达与患者生存期关系的数据集和铁死亡相关基因集合(Luo & Ma 2021,https://www.mdpi.com/2075-4418/11/2/219)为研究对象。选择蛋白—蛋白相互作用数据库STRING(http://string-db.org/cgi/input.pl),进行筛选出的基因蛋白网络构建。采用TCGA数据库对NSCLC患者生存期与筛选出基因表达关系进行分析。
1.2 NSCLC生存差异表达基因筛选 GEO中检索NSCLC基因表达数据集,检索词为“LUNG CANER/NSLCLC”,种属为“humo”。进一步对检索结果进行筛选,选取 GSE37745数据集分析[6]。根据数据集中NSCLC患者3年内是否生存分为生存组和死亡组,采用R软件lima包进行分析,生存组VS死亡组差异基因鉴别。分别对GSE37745数据集和铁死亡基因集中共有的基因进行鉴定,并绘制venn图,进一步筛选出NSCLC预后有关的铁死亡基因。
1.3 功能富集及信号通路分析 在STRING数据库中对鉴定的非小细胞肺癌(NSCLC)预后有关的铁死亡基因进行PPI网络建设,数据来源Textmining,co-expression,gene function和co-occurrence。
1.4 预后分析 TCGA数据库中,将NSCLC预后有关的铁死亡基因根据表达水平分为高表达组和低表达组,比较两组患者生OS和DFS,计算HR。
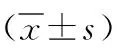
2 结果
2.1 NSCLC与预后有关的铁死亡基因筛选 GSE37745数据集中,下调表达的基因18个,上调表达的基因为92个(图1a),上调或下调表达的铁死亡相关基因为SLC7A11(图1b)。差异表达的110个基因聚类明显(图1c)。

a b

图1 NSCLC与预后有关的铁死亡基因筛选a.GSE37734数据集差异表达基因火山图 b.肺癌预后差异表达基因与铁死亡基因的韦恩图 c.基因聚类图
2.2 SLC7A11基因表达 SLC7A11在不同实体肿瘤中表达存在差异(图2a),SLC7A11在NSCLC癌中表达显著高于癌旁(P<0.05),见图2b。Oncomine数据库中,SLC7A11在肺癌中高表达(图2c)。


b
c图2 SLC7A11在肿瘤的表达情况a.SLC7A11在多种实体肿瘤中的表达水平 b.SLC7A11在肺癌腺癌和鳞癌中的表达比较,*P<0.05 c.Oncomine数据库SLC7A11表达比较
2.3 SLC7A11蛋白相互作用网络(PPI) SLC7A11蛋白网络中有节点数为20个,节点间相互作用72个,平均聚类指数为0.85,SLC7A11蛋白相互作用网络蛋白富集明显(P<0.05),见图3。

图3 SLC7A11蛋白相互作用网络
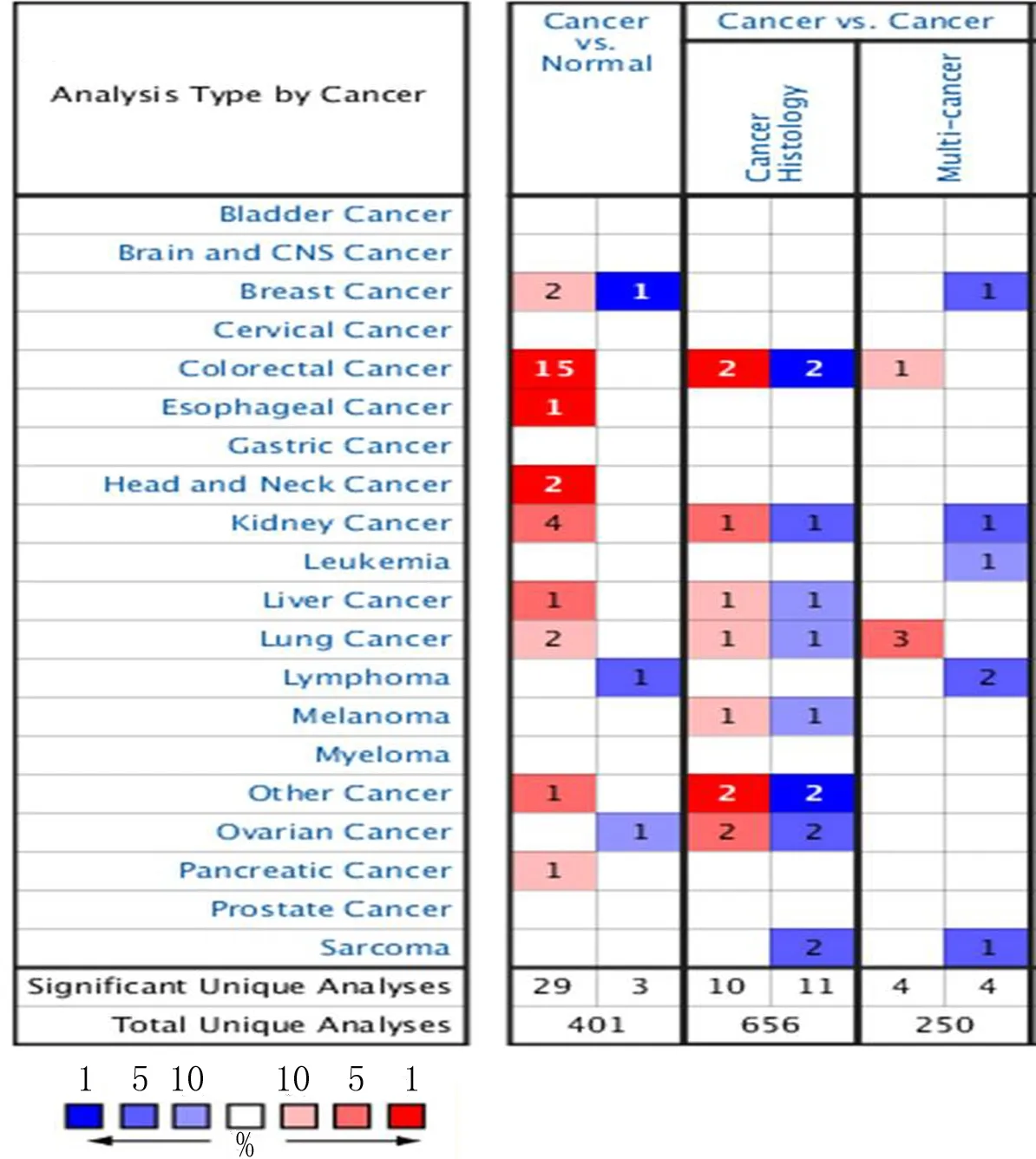
2.4 SLC7A11 KEGG信号通路 SLC7A11信号通路主要富集铁死亡、突触囊泡周期和蛋白质消化吸收等,见表1。
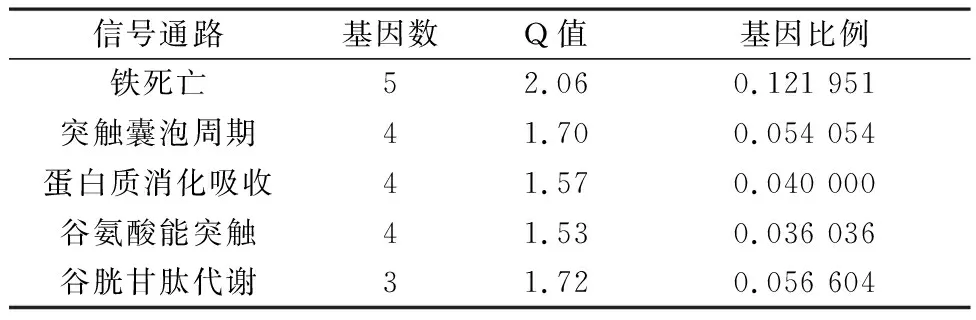
表1 SLC7A11 KEGG信号通路富集
2.5 SLC7A11表达与患者预后 SLC7A11高表达肺腺癌患者总生存(OS)低于低表达肺腺癌患者(HR=1.4,P<0.05),见图4a;而SLC7A11表达水平与肺腺癌无疾病进展生存(DFS)以及肺鳞癌OS和DFS无关(P>0.05),见图4b~d。
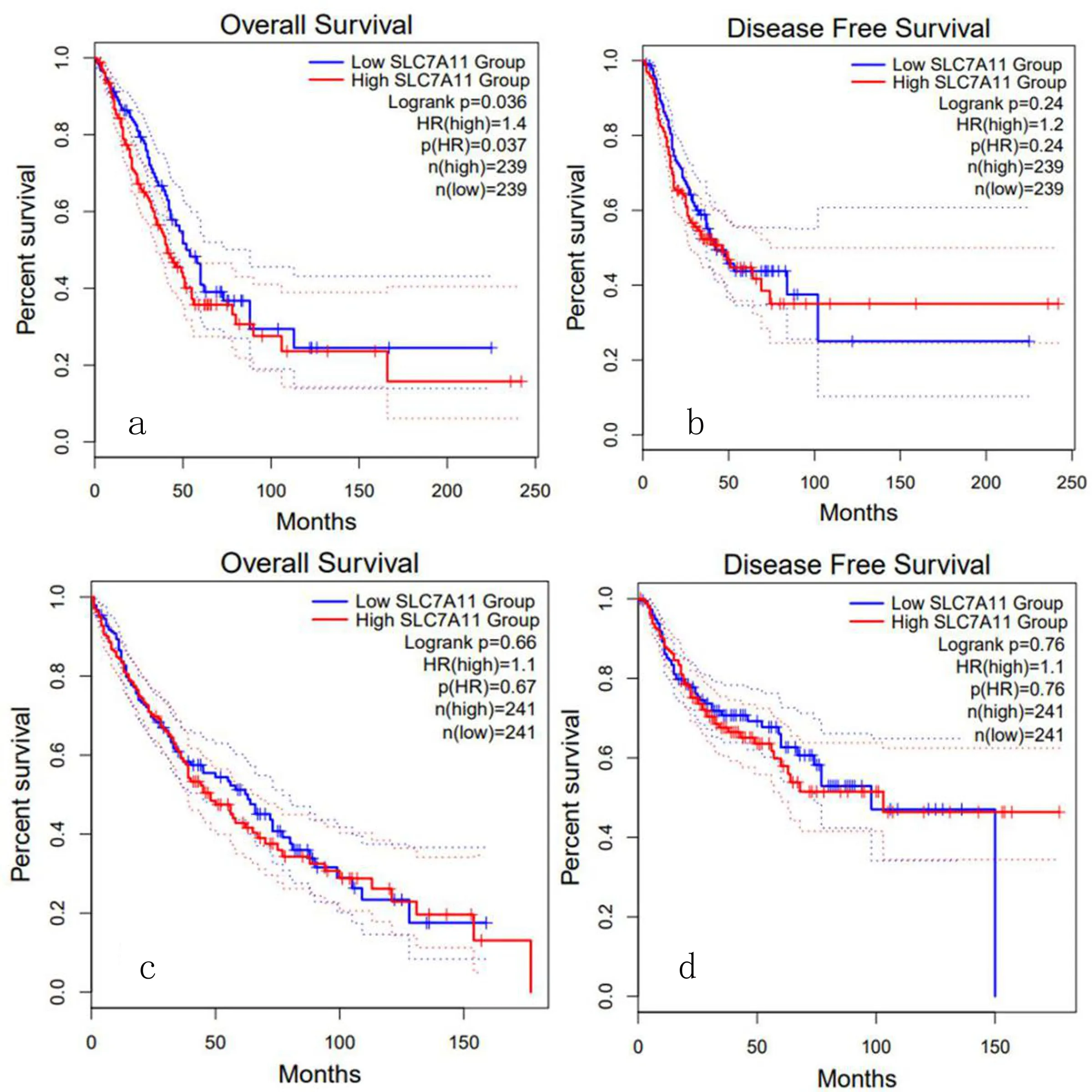
图4 SLC7A11表达与肺腺癌、鳞癌患者预后关系a.肺腺癌OS b.肺腺癌DFS c.肺鳞癌OS d.肺鳞癌DFS
3 讨论
据报道,2020年新诊断的肺癌病例高达210万例,肺癌死亡病例180万,占所有恶性肿瘤死亡病例的近1/5(18.4%)[7]。然而,NSCLC的分子致癌性尚不清楚。近年来,肿瘤新药和癌症数据库的快速发展,使得肺癌的诊断、预后和靶向治疗得到了提高,特别是中晚期肺癌患者,靶向药物的应用显著延长了晚期NSCLC患者的生存期和生活质量[8-9]。
铁死亡被Dixon等[10]首次报道,其特征为铁诱导的脂质过氧化反应。铁死亡可以消除恶性细胞的适应性特征,去除因环境变化而无法获得关键营养因子从而导致细胞破坏而死亡,对肿瘤抑制起关键作用。相关文献报道,铁死亡相关基因众多,Luo等人[11]报道了103个与铁死亡的相关基因,其中对大部分的基因功能及其在肿瘤细胞中的表达、生物学行为及与患者预后关系并不清。因此,筛选与NSCLC预后有关的铁死亡基因并对其可能的分子功能进行分析有望成为NSCLC靶向治疗的靶点。在本研究中,笔者对NSCLC预后相关的芯片数据集GSE37745进行了分析,该芯片数据建立在GLP570平台,共有196例肺癌患者。根据患者预后分为3年内存活组和死亡组,并比较两组直接的差异基因。共筛选出110个预后相关基因,并对110个预后相关基因进行了分析,发现SLC7A11基因为铁死亡相关基因。进一步分析显示,SLC7A11高表达肺腺癌患者OS低于低表达肺腺癌患者(HR=1.4,P<0.05);而SLC7A11表达水平与肺腺癌DFS以及肺鳞癌OS和DFS无关(P>0.05)。
SLC7A11基因编码蛋白为一个异聚的、钠独立的、阴离子氨基酸运输系统的成员,对半胱氨酸和谷氨酸具有高度特异性。该蛋白已被确定为Kaposi肉瘤相关疱疹病毒融合和进入细胞的主要中介物[12]。此外,该基因在原发性胶质瘤中的表达增加(与正常脑组织相比)与谷氨酸通过XCT通道分泌增加有关,从而导致神经细胞死亡。同时,有报道称,SLC7A11在多种癌症中表达上调,可通过抑制铁细胞凋亡激活癌细胞生长[13-14]。
因此,SLC7A11为NSCLC中与患者预后有关的铁死亡基因,在NSCLC中高表达,其高表达与肺腺癌的预后不良有关,并有望成为NSCLC预后标志物和靶向治疗的新靶点。

