吹扫捕集-气相色谱/质谱法测定地表水中的丁基黄原酸
廖爽,雷静,乔茜茜,吕警
(1.新疆昌源水务科学研究院有限公司,新疆乌鲁木齐 830000;2.乌鲁木齐市农产品质量安全检测中心,新疆乌鲁木齐 830000)
丁基黄原酸盐是黄原酸盐的一种,其分子式为C4H9OCSSK(Na)。黄原酸盐在现代工业中常作为有色金属浮选药剂、橡胶硫化促进剂和湿法冶金沉淀剂广泛应用于化工领域。丁基黄原酸盐水溶性较强,废水中极少量的残留都会对水体产生严重的污染,破坏生态环境,危害人体健康。
在《地表水环境质量标准》(GB 3838—2002)中,丁基黄原酸为有严格限值要求的109项中的一项。目前的检测方法主要有铜试剂亚铜分光光度法[1]、紫外分光光度法[2]、气相色谱法/气相色谱质谱法[3]、离子色谱法[4]、液相色谱法[5]和液相质谱法[6]。各方法的优缺点文献中已做详细研究,其中夏勇等[7]对各方法测定难点进行了探讨;张欢燕[8]对测定水中丁基黄原酸不同方法差异性进行了分析,认为对于基质相对干净的地表水,用吹扫捕集-气相色谱/质谱法可以进行准确检测。在实际样品检测中,所接触的地表水基质均较为干净,因此本文根据丁基黄原酸在酸性条件下分解为CS2的原理,采用吹扫捕集-气相色谱/质谱法测定地表水中丁基黄原酸的含量。
1 材料与方法
1.1 仪器与试剂
Trace1310-ISQ气相色谱-质谱联用仪,美国Thermo Fisher Scientific公司;AtomxXYZ吹扫捕集仪器(带自动进样器,吹扫捕集肼填料为1/3Tenax、1/3硅胶及1/3活性炭),美国泰克玛公司;DB-624气相色谱柱(60 m×0.25 mm,1.40 μm),美国Agilent公司。
丁基黄原酸标准溶液(溶剂为水,1 000 μg/mL)、氟苯(溶剂为甲醇,100μg/mL),坛墨质检科技股份有限公司;氢氧化钠(优级纯)、浓磷酸(分析纯),成都市科隆化学品有限公司。
1.2 吹扫捕集-气相色谱/质谱仪器实验条件
1.2.1 吹扫捕集仪器条件
吹扫管体积为5 mL;吹扫管中样品温度为40 ℃;吹扫气为N2,流速维持在40 mL/min;吹扫时间11 min;脱附预热温度为245 ℃,捕集阱脱附温度为250 ℃,脱附时间2 min;吹扫后捕集肼烘烤温度为280 ℃,烘烤时间2 min;吹扫连接气相传输线温度为110 ℃。
1.2.2 气相色谱仪器条件
进样口温度150 ℃;分流比为10∶1;载气为氦气,流速为1 mL/min;柱箱采用程序升温:初始温度40 ℃,保持1 min,然后以5 ℃/min线性升温至120 ℃,保持1 min,总运行时间18 min。
1.2.3 质谱仪器条件
离子源为电子轰击EI源;离子化能量为70 eV;离子源温度235 ℃;气相与质谱间传输线温度280 ℃;四极杆温度180 ℃。为提高质谱检测的灵敏度,扫描模式为选择性离子扫描(SIM),根据本方法采用的实验原理,最终测定成分为CS2,其定量离子m/z为76,辅助离子m/z为32和44;内标物为氟苯,其定量离子m/z为96,辅助离子m/z为70;溶剂延迟时间设置为3 min。
1.3 溶液配制
移液管准确量取5 mL丁基黄原酸标准溶液(1 000 μg/mL),加入20 μL的400 g/L的氢氧化钠溶液,用纯水定容到50 mL,得到浓度为100 μg/mL的丁基黄原酸中间储备溶液。该储备溶液需要在4 ℃的冰箱冷藏保存,保存时间不超过2周。用0.08 g/L的氢氧化钠溶液将丁基黄原酸中间储备液准确稀释到1.0 μg/mL,制得使用液,该使用液临用现配。磷酸溶液(1+6):取10 mL磷酸溶液与60 mL纯水相混合。
1.4 标准曲线绘制
分别取0.01 mL、0.05 mL、0.10 mL、0.50 mL和1.00 mL的丁基黄原酸使用液(1.0 μg/mL),用0.08 g/L的氢氧化钠溶液定容到50.0 mL,得到浓度为0.2 μg/L、1.0 μg/L、2.0 μg/L、10.0 μg/L 和 20.0 μg/L 的系列标准溶液。再将此系列标准溶液倒入40mL与仪器配套的吹扫瓶中,装满密封后,用进样针取出150 μL,然后再用另一只进样针迅速加入100 μL的磷酸溶液(1+6)。用甲醇将氟苯标准溶液浓度稀释到25.0 μg/mL,装入吹扫捕集装置的内标瓶中,由吹扫捕集仪每次自动注入1 μL到5 mL的吹扫管中,使其浓度为5.0 μg/L。将标准曲线系列由低浓度到高浓度按照1.2的实验条件进行测定。
1.5 检出限
丁基黄原酸检出限的测定主要参考《环境监测分析方法标准制订技术导则》(HJ 168—2020)中的相关要求及《水质 丁基黄原酸的测定 吹扫捕集/气相色谱-质谱法》(HJ 896—2017)中的方法检出限。
加入0.05 mL丁基黄原酸使用液(1.0 μg/mL),用0.08 g/L的氢氧化钠溶液定容到500 mL,配制浓度为0.1 μg/L的丁基黄原酸标准溶液。再装入7个吹扫瓶后密封,每个吹扫瓶用进样针取出150 μL,然后再用另一只进样针迅速加入100 μL的磷酸溶液(1+6)。在与标准曲线相同的仪器条件下,平行测定7次。计算得到丁基黄原酸的标准偏差(S),依据HJ 168—2020中检出限(MDL)计算公式如(1)所示:

根据t分布表,当n=7时,t=3.143。
1.6 精密度及准确度
对丁基黄原酸加标量为2.0 μg/L(A)、4.0 μg/L(B)、18.0 μg/L(C)的空白加标样品平行测定6次,计算实验的精密度和准确度。
1.7 加标回收率
根据实际水样中丁基黄原酸的测定浓度,一般加入其浓度0.5~3.0倍的标准溶液计算回收率;若样品未检出,则加入标准曲线上低浓度范围内的点,上机测定,计算回收率。
1.8 水样采集、保存与上机测定
丁基黄原酸理化性质极不稳定,水样的正确合理采集也是地表水监测的重要质量控制环节之一。《水质 丁基黄原酸的测定 吹扫捕集/气相色谱-质谱法》(HJ 896—2017)中要求水样的保存需要在弱碱条件下,因此水样采集时应将40 mL的棕色吹扫瓶直接带至现场进行采集。采样时应将采样瓶装满,每个瓶子中加入1mL氢氧化钠溶液(400 g/L)后,立刻密封保存,及时检测。由于实验中存在假阳性的影响,故每份样品均采集平行双样。实验室在其中一份样品中加入100 μL的磷酸溶液(1+6),另一份加入100 μL纯水,在相同的吹扫和仪器色谱条件下测定,以两者之差计算检测结果。
2 结果与分析
2.1 SIM谱图结果
丁基黄原酸的选择性离子扫描谱图见图1,丁基黄原酸转化后的CS2保留时间为7.82 min,内标物氟苯保留时间为9.16 min,二者分离良好、峰形良好。

图1 丁基黄原酸及内标物SIM谱图
2.2 标准曲线实验结果
以丁基黄原酸的标准曲线浓度为横坐标,以转化后的CS2的峰面积与内标物氟苯的峰面积的比值为纵坐标,绘制曲线。得到标准曲线方程为y=0.046x+0.001,相关系数R=0.999 2,线性关系良好。
2.3 检出限实验结果
检出限实验结果见表1,本方法的检出限与HJ 896—2017中的检出限(0.04 μg/L)一致,满足检测标准要求。
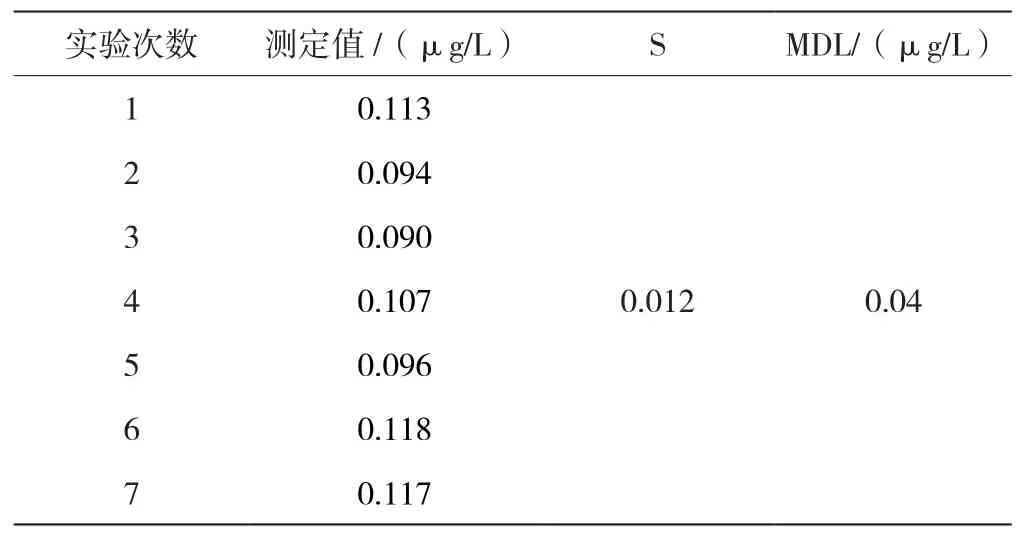
表1 方法检出限(n=7)
2.4 精密度及准确度实验结果
如表2所示,对浓度为2.0 μg/mL、4.0 μg/mL及18.0 μg/mL的丁基黄原酸标准样品平行测定6次,其相对标准偏差均小于3%,相对误差均小于5%,结果满足标准要求。

表2 方法精密度和准确度(n=6)
2.5 地表水实际样品及加标回收率实验结果
选取了新疆某地区地表水10个样品进行加标回收率实验,结果如表3所示。所有地表水中均未检出丁基黄原酸,加标回收率在85.0%~108.0%,满足方法要求。
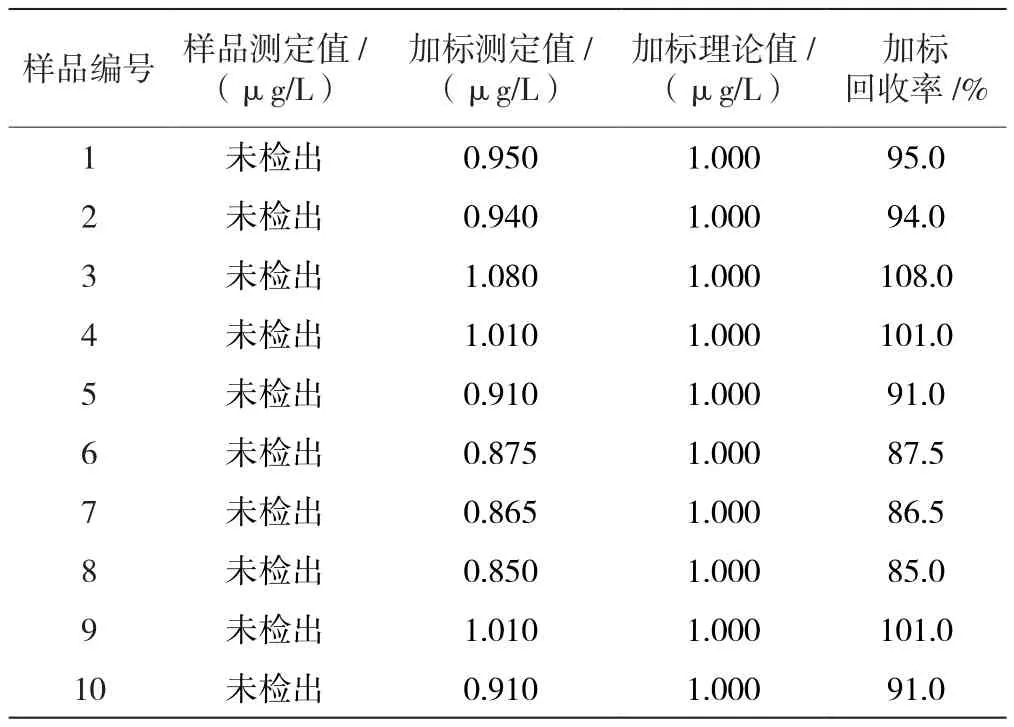
表3 实际样品加标回收率
3 结论
本文针对基质较为干净的地表水建立了具有前处理简单、操作方便快捷、假阳性率低、灵敏度高的吹扫捕集-气相色谱/质谱法测定丁基黄原酸的检测方法。本方法检出限、精密度、准确度及实际加标样品的回收率均满足现有检测标准中的相关要求,可应用于日常的地表水监测工作中。

