干旱区垃圾渗滤液中溶解性有机质与PAEs相互作用的光谱研究*
蔡永会,叶雨萍,魏 斌,王兆炜
(兰州大学资源环境学院/甘肃省环境污染预警与控制重点实验室,甘肃 兰州 730000)
填埋是我国当前城市生活垃圾最常见的处理方法,这种垃圾处理方法的一个主要问题是产生大量渗滤液,其水质主要受垃圾成分、填埋时间、地理区位、气候温度以及填埋场运行方式等的影响,一般具有水质水量变化大、有机物含量高、成分复杂等特点[1]。西北地区是典型的温带大陆性干旱半干旱气候,降雨量小蒸发量大,使得垃圾渗滤液浓度相对较高,且随季节性差异明显[2]。垃圾渗滤液含有氮、磷、钾、氨氮、有机质、重金属、无机盐和新兴污染物等多种有机和无机污染物[3-4]。邻苯二甲酸酯(PAEs)是一类生态环境中普遍存在的环境激素类污染物。PAEs作为增塑剂和软化剂,在数百种工业、医疗、农业和家庭用品中存在,在塑料制品中占10%到60%不等[5-6]。PAEs也可作为非增塑剂用于化妆品、驱虫剂、杀虫剂载体和推进剂等产品的生产[7]。PAEs通常与塑料聚合物通过物理作用并非共价结合[8]。研究表明PAEs具有多种毒性作用,主要包括生殖毒性、内分泌干扰、肝毒性、肾毒性和“三致效应”[9-11]。塑料垃圾通常与生活垃圾一起填埋处理,在微生物和周围环境的作用下迁移转化到渗滤液中,因此渗滤液的排放是PAEs进入环境的重要途径。由于PAEs的水溶性低、辛醇-水分配系数高,在垃圾填埋场厌氧条件下很难被完全生物降解。调研发现国内外垃圾渗滤液中含有含量不同的邻苯二甲酸酯(PAEs)[12-13],渗滤液中PAEs浓度范围为0.7~17200μg·L-1,其中邻苯二甲酸二丁酯(DBP)和邻苯二甲酸二(2-乙基己基)(DEHP)的检出频率和检出浓度值最高[14]。溶解性有机质(DOM)是渗滤液有机组分的主要成分,占总有机碳浓度的80%以上。渗滤液中DOM浓度(以DOC计)在800~20 000 mg·L-1或更高,腐殖质占成熟渗滤液中DOM的72%[15]。腐殖质可以显著影响一些自然环境中污染物的行为,如微量金属的形态和毒性、疏水污染物的溶解和吸附、消毒副产物的形成、水体光化学以及土壤中的氧化还原行为等[16-18]。DOM主要通过氢键作用、疏水作用以及范德华力等与环境中的有机污染物吸附结合,从而影响这些污染物的分布、迁移、转化、降解、毒性、生物利用度和环境归宿等[19-20]。本文利用紫外-可见吸收光谱(UV-vis)、三维荧光光谱(3DEEM)和荧光发射谱等光谱手段,结合平行因子分析(PARAFAC)研究了西北干旱地区垃圾渗滤液中DOM和两种PAEs(DBP、DEHP)的相互作用机制,以期为制定干旱区垃圾渗滤液处理工艺和修复策略提供理论基础。
1 材料和方法
1.1 渗滤液的收集和预处理
渗滤液于2021年5月13日取自兰州新区生活垃圾填埋场调节池。渗滤液(LL)基本理化性质见表1。

表1 渗滤液基本理化性质(mg·L-1)
1.2 实验方法
1.2.1 紫外-可见吸收光谱(UV-Vis)
在室温下,通过UV-Vis分光光度计扫描获得不同浓度PAEs(0、1、2、4、5、6、8、10 mg·L-1)强化的渗滤液溶液的UV-Vis吸收光谱,波长范围设置为190~700 nm。此时渗滤液中DBP浓度分别为0.282、1.282、2.282、4.282、5.282、6.282、8.282、10.282mg·L-1;DEHP浓度分别为0.113、1.113、2.113、4.113、5.113、6.113、8.113、10.113 mg·L-1。由于原始光谱通常特征峰不明显,为了提高光谱分辨率,避免渗滤液溶液中本身存在的PAEs的影响,本研究采用紫外差分吸收光谱进行分析[21]。
1.2.2 三维荧光光谱分析(3DEEM)
采用Cary Eclipse型荧光光谱分析仪 (美国Agilent公司)进行三维荧光光谱扫描。荧光滴定前,用超纯水将渗滤液原液稀释5倍(20%LL),降低渗滤液TOC浓度,确保最大荧光信号低于光谱仪的检测上限,降低内滤效应[22]。荧光测定参数设置为:发射(Em)波长为250~700 nm,激发(Ex)波长为200~450 nm,狭缝宽度(Slit Width)为5 nm,扫描速率为24000 nm·min-1,PMT电压为700 V。将3.0 mL 20%LL溶液放入与开放式水浴循环器连接的单个石英比色皿(1 cm,矩形)中,在磁力搅拌下用微量进样器连续加入PAEs母液(1.0g/L),使比色皿中PAEs的强化浓度分别为0、1、2、4、5、6、8、10 mg·L-1。测试前将设备响应值归零。
1.2.3 平行因子分析(PARAFAC)
本研究PARAFAC分析使用matlab R2017b软件(Math Works,Natick,MA)和DOMFluor工具箱进行,通过分半信度方法识别并验证DOM的组分和数量。用最大荧光强度(Fmax)表示各荧光组分的相对浓度。
1.2.4 荧光发射光谱
荧光测量参数设置如下: 发射和激发狭缝宽度均调节为5 nm,扫描速率=600 nm·min-1,PMT电压=700V。按照PARAFAC分析识别的DOM组分,将组分C1的Ex设置为325 nm,Em设置范围为335~600 nm;组分C2的Ex设置为270 nm,Em设置范围为380~600 nm;组分C3的Ex设置为280 nm,Em设置范围为290~540 nm。将3.0 mL 20%LL溶液放入与开放式水浴循环器连接的单个石英比色皿(1 cm,矩形)中,在磁力搅拌下用微量进样器连续加入PAEs储备液,使比色皿中PAEs的强化浓度分别为0、1、2、4、5、6、8、10、15、20、25、30、35 mg·L-1。将温度探针放入比色皿内以控制温度。比色皿内的溶液温度保持在298±1K。测试前将设备响应值归零。扫描并获得渗滤液DOM-PAEs的荧光发射光谱。热力学研究采用相同的方法扫描渗滤液DOM-PAEs体系分别在288±1K和308±1K下的荧光发射光谱。
1.3 数据分析
本研究分别采用Stern-Volmer和site-binding两个方程拟合了渗滤液DOM与PAEs相互结合的相关参数[23-24]。
Stern-Volmer方程为:

其中F0和F分别是渗滤液DOM和分别加入不同浓度PAEs后DOM的荧光强度值。Ksv为猝灭常数,[PAEs]为PAEs的浓度。
site-binding 方程为:
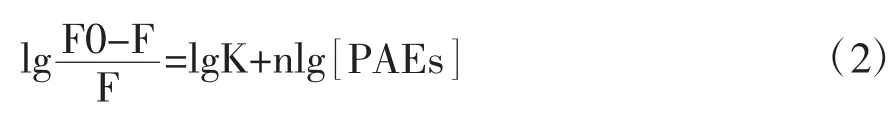
其中K为结合常数,n为结合位点数。
计算渗滤液DOM-PAEs 体系在288K,298K,308K的结合常数以获得热力学参数值,其大小和正负号可用来初步判断促使渗滤液DOM和PAEs结合的主要作用力。热力学公式如下:

式中T是绝对温度;R是理想的气体常数,8.314J/(mol·K);K是结合常数。
计算lnK,利用公式(4)计算得到ΔG0。
以T为横坐标,ΔG0为纵坐标线性拟合,ΔG0=aT+b,则a=-ΔS0,b=ΔH0。
2 结果与讨论
2.1 渗滤液DOM与PAEs相互作用的紫外差分吸收光谱分析
渗滤液DOM与DBP/DEHP体系的紫外差分吸收光谱如图1所示。随着DBP/DEHP浓度的增加,渗滤液DOM-DBP/DEHP体系的紫外吸收强度不断增加。同时,DBP和DEHP加入后渗滤液DOM-PAEs体系在228nm和275nm出现两个吸收峰。这些现象表明,随着PAEs的加入,渗滤液DOM与PAEs之间形成复合物,而渗滤液DOM与DBP/DEHP结合后自生的微结构和环境发生了变化[25]。
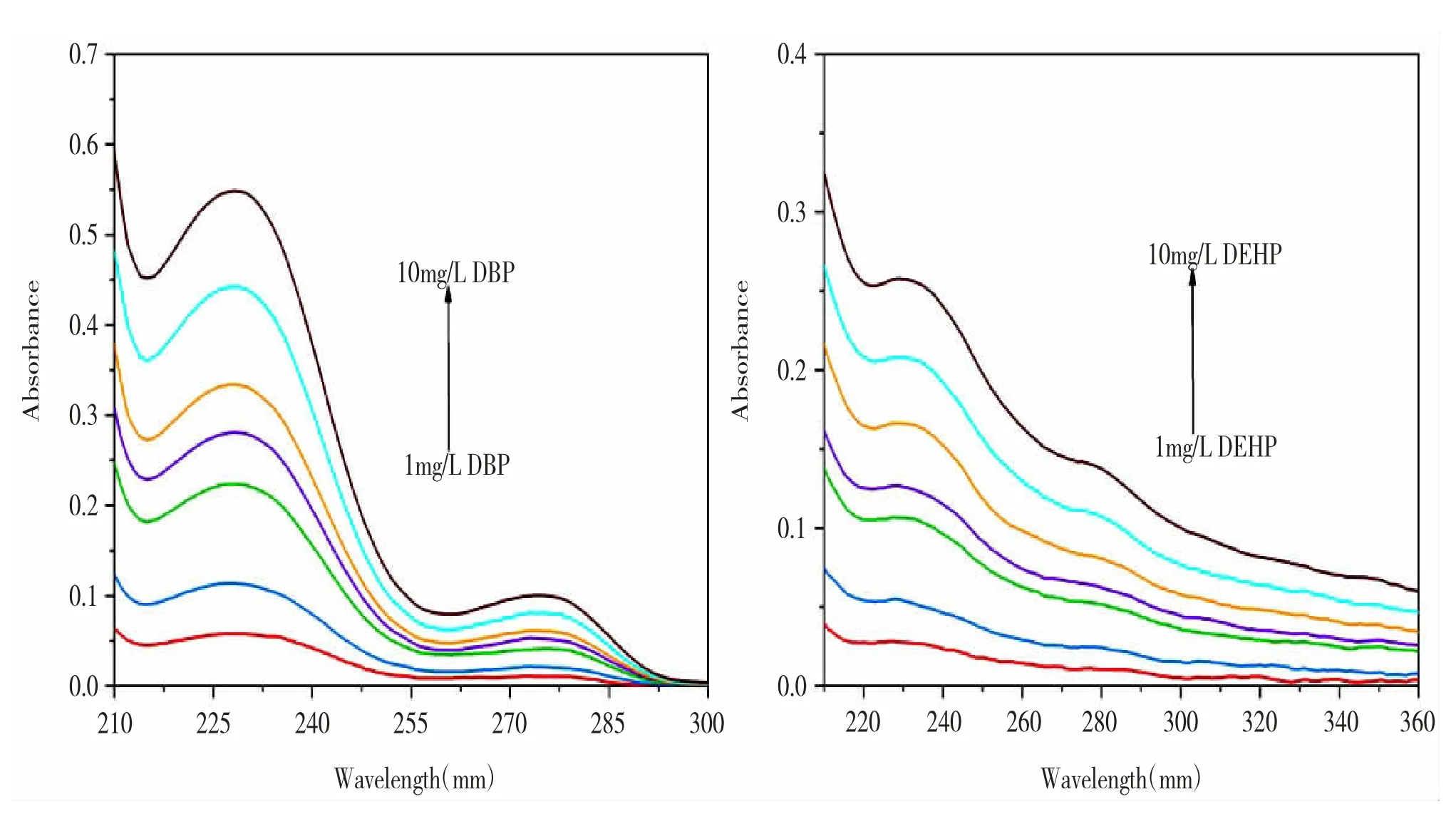
图1 渗滤液DOM-DBP/DEHP体系的紫外差分吸收光谱
2.2 渗滤液DOM与PAEs相互作用的三维荧光光谱分析
渗滤液DOM-PAEs体系的三维荧光光谱如图2所示。一般Em<380 nm的荧光峰含有苯环和给电子基团(羟基和氨基),而Em>380 nm的荧光峰含有多环芳烃结构。因此Em>380 nm的荧光峰属于腐殖质物质,Em<380 nm的峰属于蛋白质物质[26]。结合DOM的EEM谱图区域分布研究结果[27],由图可以看出,20%LL的荧光光谱除去瑞利散射峰(Em=2Ex)和二阶散射峰(Em=Ex)外,主要显示Ex/Em=250/450nm处的高强度峰和Ex/Em=300/400 nm处的次级强峰,分别属于富里酸类物质(FA)和腐殖酸类物质(HA);同时也可以看出,在Ex/Em=225/350nm处存在类蛋白物质的弱峰。在不同浓度DBP/DEHP存在下,渗滤液DOM荧光基团发生了明显的减弱(表2),这表明渗滤液中DOM与PAEs之间的相互作用诱导渗滤液DOM的微结构和环境发生了变化[28]。当DBP浓度达到5mg·L-1时,FA峰的荧光强度下降约为6.55%,HA峰的荧光强度下降约为3.48%,类蛋白物质峰的荧光强度下降约为15.57%;而当加入10 mg·L-1的DBP时,FA峰的荧光强度下降约10.07%,HA峰的荧光强度下降约4.10%,类蛋白物质峰的荧光强度下降约为30.26%。当DEHP浓度达到5 mg·L-1时,FA峰的荧光强度下降约为8.80%,HA峰的荧光强度下降约为3.52%,类蛋白物质峰的荧光强度下降约为26.47%;而当加入10 mg·L-1的DEHP时,FA峰的荧光强度下降约12.84%,HA峰的荧光强度下降约8.47%,类蛋白物质峰的荧光强度下降约为40.75%。由此可以看出,DEHP对渗滤液DOM各组分的结合能力要强于DBP,这可能与DBP和DEHP的结构和性质差异有关,DBP和DEHP的辛醇-水分配系数(logKow)分别为4.27和7.73,DEHP的疏水性强于DBP,DEHP 与DOM之间存在的疏水作用更强[29]。同时实验结果表明类蛋白物质与DBP/DEHP的结合能力强于类腐殖质类物质。
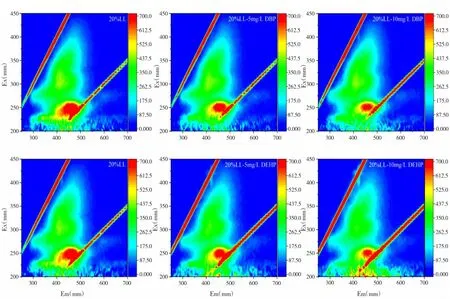
图2 渗滤液DOM-PAEs体系的三维荧光光谱
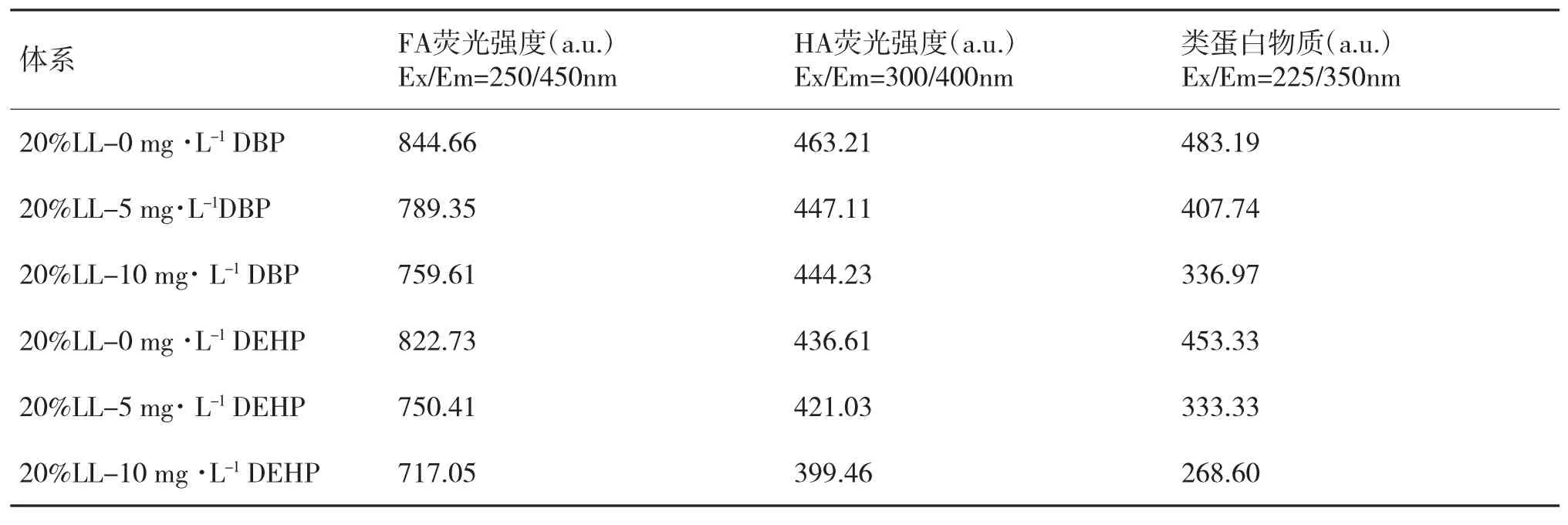
表2 渗滤液DOM-PAEs体系荧光峰强度值的变化
通过对渗滤液DOM-PAEs体系的3DEEM数据的PARAFAC分析,得到渗滤液DOM三种不同组分(图3)。C1和C2位于腐殖质类荧光区域,分别属于腐殖酸类物质和富里酸类物质;C3的Ex/Em范围在200-315/300-450nm之间,涵盖了腐殖质类和色氨酸、酪氨酸等蛋白类的荧光光谱区域。Fmax的变化如图4所示,加入DBP/DEHP后C2和C3均具有明显的猝灭作用,随着DBP/DEHP浓度(0-10mg·L-1)的增加,C2和C3的荧光强度不断降低,而对组分C1的猝灭作用相对较弱。对于DBP,当DBP浓度增加到最大值(10 mg/L)时,C1、C2、C3的可检测分数分别为98.8%、82.9%、81.1%;对于DEHP,当DEHP浓度增加到最大值(10 mg/L)时,C1、C2、C3的可检测分数分别为94.6%、80.4%、71.6%。结合3DEEM分析和之前的研究报道可以得出,PAEs对类蛋白成分的猝灭效果比类腐殖质成分更显著,这也与之前的研究相类似[30]。因此,可以推断出渗滤液DOM的结合特性与其单个成分高度相关,且渗滤液DOM中的类蛋白成分与PAEs的亲和力明显较高。

图3 3个荧光组分及其激发/发射波长荷载值
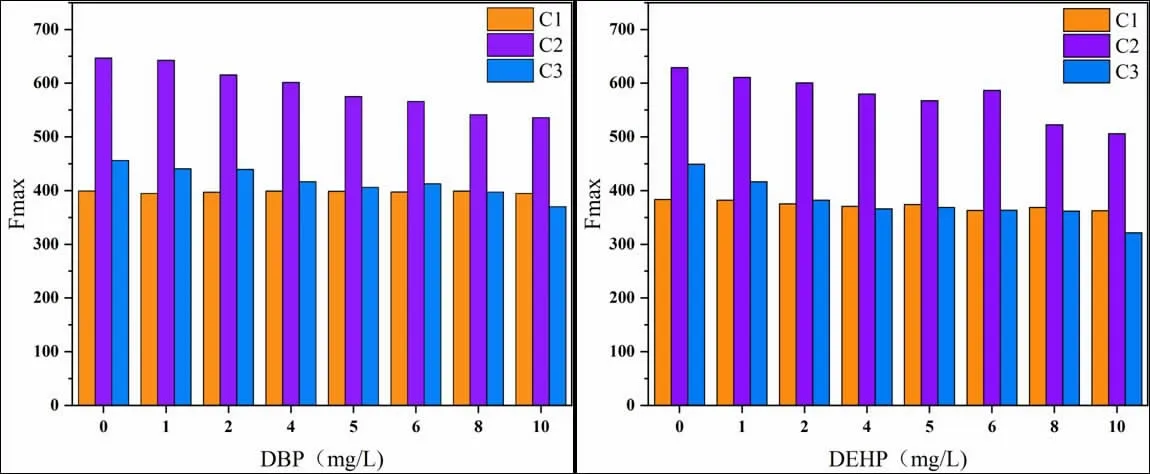
图4 渗滤液DOM三种PARAFAC组分C1-C3在不同DBP/DEHP浓度下的Fmax值
2.3 渗滤液DOM与PAEs相互作用的荧光发射谱分析
渗滤液DOM的三种主要组分C1、C2和C3分别与DBP和DEHP结合的荧光发射谱如图5所示。在298K下,随着DBP/DEHP浓度的增加,渗滤液DOM各组分的荧光发射谱均显著降低,且同时可以看出DEHP对渗滤液DOM的猝灭效果强于DBP,这与三维荧光光谱的分析结果一致。此外,加入DBP/DEHP后,C2和C3组分荧光发射谱的最大发射波长发生了明显的蓝移[31]。这些结果都表明渗滤液DOM荧光团的微结构和环境发生了改变。以上现象与3DEEM和PARAFAC分析结果一致,均表明了渗滤液DOM与PAEs之间存在相互作用,渗滤液DOM与PAEs的结合改变了渗滤液DOM的微结构和环境以及极性[32]。
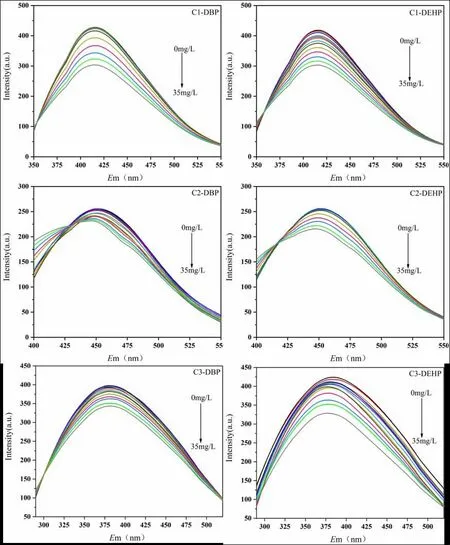
图5 DBP/DEHP-C1、C2、C3体系的荧光发射谱
2.4 渗滤液DOM与PAEs的结合特性
在288、298和308K下分别拟合渗滤液DOM各组分与PAEs结合的相关参数,结果如表3所示。渗滤液DOM各组分与DBP和DEHP相互结合的Ksv和K随着温度的升高而呈现降低的趋势,这表明PAEs对渗滤液DOM各组分荧光猝灭属于静态猝灭过程,低温有利于DBP和DEHP与渗滤液各组分的结合[33]。在三个温度下,结合位点数n约等于1,这表明渗滤液DOM与PAEs之间可能存在单个结合位点。此外,可以看出,DBP-C1/C2/C3作用的Ksv和K小于DEHP-C1/C2/C3之间的Ksv和K。这与上述三维荧光光谱分析和荧光发射谱分析结果相一致。同时可以发现,DBP/DEHP-C2作用的Ksv和K大于DBP/DEHP-C1之间的Ksv和K,这是可能因为FA具有更多的活性官能团所导致的。
2.5 渗滤液DOM与PAEs结合的热力学参数和作用力类型
渗滤液DOM与PAEs结合的热力学参数见表3。组分C1/C2/C3与DBP/DEHP的相互作用过程中ΔH0<0,这表明其作用过程是放热的,在较低温度下更易结合,这与Ksv和K分析过程中低温更有利于DBP和DEHP与渗滤液各组分的结合相一致;渗滤液DOM各组分与DBP/DEHP结合过程中ΔS0<0表明反应均为熵减过程,相互作用后其混乱度降低。ΔG0>0,这表明渗滤液DOM-DBP/DEHP体系相互结合作用并不是自发的热力学过程。有研究表明,ΔS0<0、ΔH0<0可用来解释分子之间存在氢键和范德华力[34]。通常ΔH0<0可用于证明分子之间的静电作用[35]。从表3渗滤液DOM各组分与DBP/DEHP相互作用过程中的ΔS0、ΔH0正负值变化可以得出,渗滤液DOM各组分与DBP/DEHP结合的作用力有范德华力、氢键作用,并存在静电作用。此外,|ΔH|<|TΔS|表明渗滤液DOM各组分-DBP/DEHP络合物的形成主要是由于熵变ΔS0导致的,这是通过静电效应和氢键作用所影响的。

表3 不同温度下渗滤液DOM-PAEs体系的结合常数及热力学参数
3 结论
(1)3DEEM和PARAFAC表明,渗滤液DOM主要成分为富里酸类物质(FA)、腐殖酸类物质(HA)和类蛋白物质。
(2)渗滤液DOM与PAEs之间存在相互作用,渗滤液DOM与PAEs的结合改变了渗滤液DOM的微结构、极性和环境。
(3)DEHP与渗滤液DOM各组分的结合能力要强于DBP,这可能与DBP和DEHP的结构和性质差异有关,DEHP的疏水性强于DBP,使DEHP与DOM之间存在的疏水作用更强;渗滤液DOM的结合特性与其单个成分高度相关,且渗滤液DOM中的类蛋白成分与PAEs的亲和力明显较高;PAEs-FA的结合能力强于PAEs-HA,这是可能因为FA具有更强的亲水性导致的。
(4)PAEs对渗滤液DOM各组分荧光猝灭属于静态猝灭过程。疏水作用、范德华力、氢键和静电作用是渗滤液DOM各组分与PAEs结合的主要作用力。

