离子液体对含卤素VOCs吸收分离计算研究
赵彤彤,刘懿韬,吴天照,史祥睿,李文秀
(沈阳化工大学 化学工程学院,辽宁 沈阳 110142)
挥发性有机污染物(VOCs)是一类对环境和人体健康有危害的空气污染物[1],其种类繁多、组分复杂,尤其是某些含卤素的VOCs 具有诱发癌变、导致畸形等危害[2]。美国国家环保局最新确定的188 种有毒气体名单中含卤素VOCs 有32 种[3],约占总数的17%。绝大部分含卤素VOCs 不溶于水,脂溶性强,人体吸收后会在脂肪中积累而难以降解,对人体造成严重危害[4-6]。氯苯进入人体后会对呼吸道和肺部细胞有刺激作用,容易诱发慢性呼吸道疾病。人体吸入高剂量的氯苯会造成中枢神经麻痹,免疫系统破坏,导致人体免疫力降低并诱发一系列疾病[7]。因此,开发实用高效的含卤素VOCs 控制方法具有重要的现实意义[8-9]。
离子液体作为一种完全由阴阳离子组成的新型溶剂,具有与气体亲和性强、蒸气压低、易解吸再生等独特优势,在气体分离回收工业应用中受到日益广泛的关注,具有巨大的潜力[10-11]。HUDDLESTON[12]等对含苯有机物(如苯、甲苯、苯胺)在水与离子液体相中的分配系数进行了研究,结果表明离子液体是一种很好的液-液萃取溶剂。QUIJANO[13]等通过实验测量了VOCs(甲苯、二甲基二硫醚和甲硫醚)与离子液体([Bmim][Tf2N]、[Bmim][PF6])之间的分配系数,证明了离子液体对VOCs 具有良好的亲和力。BEDIA[14]等通过COSMO-RS模型对272种离子液体与甲苯之间的亨利常数进行筛选,结果表明,阴离子为[Tf2N]-、阳离子取代基为长链烷烃的咪唑类离子液体对甲苯有较好的吸收效果。耿唯唯[15]同样采用COSMO-RS模型分析了459 种离子液体对氯苯的吸收容量,结果表明阴离子对氯苯的吸收量影响相较于阳离子更为明显,并且[Emim][Tf2N]对氯苯的吸收率可达94.05%。目前已有多种角度聚焦此类研究,但对于离子液体中阳离子如何影响含卤素VOCs 吸收量的研究机理不够深入。
本文以阳离子不同的两种离子液体([Bmim][Tf2N]、[Bim][Tf2N])为溶剂,通过量子化学计算来对氯苯-[Bmim][Tf2N]和氯苯-[Bim][Tf2N]之间的相互作用能强弱和相互作用类型进行分析,从分子水平来探究阳离子结构对离子液体对氯苯吸收量的影响,为设计新型离子液体提供理论指导。
1 量子化学计算
本文的量子化学计算是通过Gaussian 09 软件进行的,主要为密度泛函计算。在B3LYP/6-311+G(d)计算水平下对[Bmim][Tf2N]、[Bim][Tf2N]、氯苯-[Bmim][Tf2N]和氯苯-[Bim][Tf2N]之间的初始结构进行了优化,并对优化后的结构进行频率分析,确保其结构稳定无虚频。并在相同的计算水平下对不同离子或分子与NH3分子的结构进行优化,并计算了所有结构的原子电荷和电子能量。计算分子或离子间的相互作用能(ΔEA-B),如公式(1)所示:

式中:EA、EB、EAB—单体A,单体B 和复合物AB 的电子能量。
通过约化密度梯度(RDG)可以研究氯苯-[Bmim][Tf2N]和氯苯-[Bim][Tf2N]分子间的弱相互作用。此理论方法是由杨伟涛[16]等在2010年提出的,目的是为了凸显分子间存在弱相互作用的区域,具体的计算如公式(2)所示:

式中:ρ(r)—电子密度,可通过密度泛函计算获得;
∇—梯度算符。
通过求解Hessian 矩阵得到它的第二特征值λ2符号(sign(λ2))来确定相互作用的类型。卢天[17]等将计算的sign(λ2)与ρ(r)相乘的数值大小用不同的色彩映射到RDG等值面上,使体系的弱相互作用能可视化,如图1所示,能够直观看出不同颜色对应区域的相互作用类型以及强度。

图1 RDG 色彩标度与对应的弱相互作用
图1种左边蓝色区域(sign(λ2)ρ<0)表示强的静电吸引作用,一般对应氢键作用或卤键,颜色越深相互作用越强;中间绿色区域(sign(λ2)ρ≈ 0)为范德华作用;右边红色区域(sign(λ2)ρ>0)为互斥作用,一般是环结构或笼结构的空间位阻效应引起的。
进一步通过COSMOthermX 19.0 软件在TZVP基组下计算了[Tf2N]-、[Bim]+、[Bmim]+和氯苯的极性和电势信息,从而更加深入分析离子液体对氯苯吸收的机理。
2 结果与分析
2.1 相互作用能分析
表1显示了不同组合体之间的相互作用能量(ΔE),结果表明氯苯-[Bim][Tf2N]之间的相互作用强于氯苯-[Bmim][Tf2N]之间的相互作用。图2是氯苯-[Bim][Tf2N]和氯苯-[Bmim][Tf2N]优化后的结构,从图2中可以看出氯苯-[Bim][Tf2N]之间的O∙∙∙H键长要比氯苯-[Bmim][Tf2N]之间的O∙∙∙H键长短,表明氯苯-[Bim][Tf2N]之间结合的更加紧密,[Bim][Tf2N]对氯苯的吸收能力更强。同时从图2可以看出,阴离子与氯苯之间的距离更近,这与前人的研究结果一致,阴离子结构对离子液体吸收VOCs 的影响更大[15]。

表1 各组合体的相互作用能量

图2 氯苯-[Bmim][Tf2N]和氯苯-[Bim][Tf2N]结构优化
2.2 RDG 分析
采用Multiwfn 程序生成了RDG=0.45 的等值面,并通过VMD 程序对等值面进行着色显示,进而分析弱相互作用的类型、强度和位置,结果如图3所示。

图3 Multiwfn 绘制的氯苯-[Bmim][Tf2N]和氯苯-[Bim][Tf2N]之间的等值面图
从图3(a)可以看出,氯苯-[Bmim][Tf2N]之间存在绿色的RDG填色块,表明氯苯[Bmim][Tf2N]之间主要是范德华相互作用。图2(b)显示的氯苯-[Bim][Tf2N]之间存在绿色和蓝色的RDG填色块,表明氯苯和[Bim][Tf2N]之间存在氢键作用和范德华相互作用。图4显示了它们之间的sign(λ2)ρ散点图,对于氯苯-[Bmim][Tf2N]体系(图4(a)),散点图中只有一个带负号的sign(λ2)ρ峰(-0.015),这归因于O∙∙∙H 之间的范德华相互作用。如图4(b)显示,散点图最左边的sign(λ2)ρ峰(-0.040)对应于NH∙∙∙O 之间的氢键作用(图3(b)中的蓝色圆形RDG等值面),在sign(λ2)ρ值为-0.020~0.010 范围之间有多个尖峰被分配给C—H∙∙∙π 和范德华相互作用。由于[Bim][Tf2N]的局部电荷更集中,其空间位阻更小使得[Bim]+与氯苯之间存在较强的π∙∙∙π 堆积作用,从而增强了[Bim][Tf2N]对氯苯的吸收能力。

图4 氯苯-[Bmim][Tf2N]和氯苯-[Bim][Tf2N]构象的散点图
2.3 表面极性和电势分析
为了进一步研究离子液体结构对甲苯吸收的机理,对阴阳离子和甲苯的表面极性和电势进行了分析。图5表示[Tf2N]-、[Bim]+、[Bmim]+和氯苯结构的表面屏蔽电荷分布。
图中红色区域的静电势值为负,表示在这一区域的原子更容易给出电子,相对于其他区域的原子更具有亲核性;而蓝色区域的静电势值为正,表示这一区域的原子更容易获得电子,相对于其他区域的原子更具有亲电性。从图5可以看出,[Tf2N]-的氧原子具有较强的亲核性,更容易失去电子;[Bim]+的质子氢更容易获得电子,具有较强的亲电性;[Bmim]+和氯苯则相对稳定,不容易失去或获得电子。
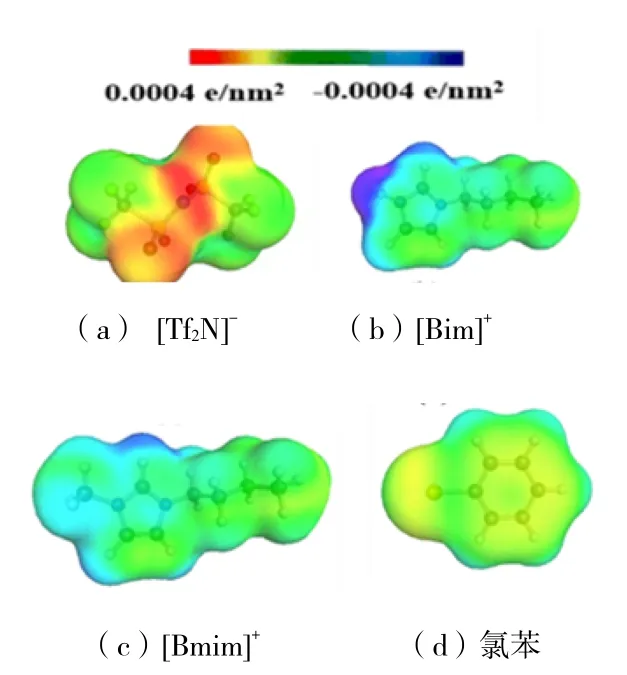
图5 [Tf2N]-、[Bim]+、[Bmim]+和氯苯的表面屏蔽电荷分布信息
图6表示[Tf2N]-、[Bmim]+、[Bim]+和氯苯结构的极性和电势信息,其中的两条虚线是氢键作用类型的分界线。
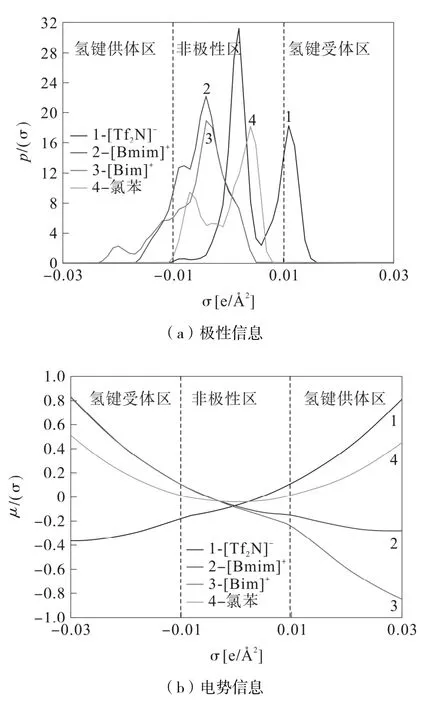
图6 [Tf2N]-、[Bmim]+、[Bim]+和氯苯的极性信息和电势信息
如图6(a)所示,σ-profiles 被分为3 个区域:当σ<-0.010 e·Å-2时表示该区域内的分子或离子具有较强的氢键供体能力,σ>0.010 e·Å-2时表示该区域内的分子或离子具有较强的氢键受体能力,-0.010 e·Å-2<σ<0.010 e·Å-2是非极性区域,在该区域内有峰的物质或离子更倾向于和同样在该区域内的物质或离子形成如范德华作用、静电作用等的非极性互作用[18-19]。如图6(b)所示σ-potentil 也被分为氢键受体区、氢键供体区和非极性区。当分子的横坐标σ<-0.010 e·Å-2、纵坐标以μ<0 时,则代表该分子易与横坐标σ>0.010 e·Å-2、纵坐标以μ<0 的分子形成氢键[20]。
氯苯的峰全部在0.010 e·Å-2<σ<0.010 e·Å-2区域,表明氯苯属于非极性分子。[Tf2N]-阴离子在σ>0.010 e·Å-2区域具有峰值,表明[Tf2N]-阴离子是氢键受体;同时在-0.010 e·Å-2<σ<0.010 e·Å-2区域有强峰,表明其非极性作用很强,可以与氯苯相互作用。对于[Bmim]+和[Bim]+来说,其非极性作用要弱于[Tf2N]-阴离子,并且[Bim]+阳离子的氢键供体作用要强于[Bmim]+阳离子的氢键供体作用。此结果与图5显示的电荷信息一致。基于以上信息可知,[Bim][Tf2N]更容易与氯苯发生相互作用。
3 结 论
通过相互作用能分析、RDG 分析、表面极性和电势分析对阳离子不同的两种离子液体([Bmim][Tf2N]和[Bim][Tf2N])吸收对氯苯吸收的强弱进行了研究。结果表明,[Bim]+阳离子的局部电荷更集中,具有较小的空间位阻和较强的亲核性,使得[Bim][Tf2N]与氯苯的相互作用更强,吸收性能好。
——以高中化学“氢键”的教学为例

