腹腔镜下顺行双保根治性前列腺切除术后患者控尿和勃起功能恢复效果
韦自卫,邹 雲,李配漳,李 龙,王 忠,李文智
(上海交通大学医学院附属第九人民医院 泌尿外科,上海 200011)
前列腺癌是老年男性最常见的肿瘤之一[1],我国多中心资料显示大概1/3患者为局限性肿瘤[2]。随着前列腺特异性抗原(prostate specific antigen,PSA)筛查的广泛开展,越来越多的局限性前列腺癌得以早期诊断[3]。多年来,根治性前列腺切除术(radical prostatectomy,RP)始终是治疗局限性前列腺癌的标准术式[4]。新时期前列腺癌的治疗出现了新的特征:一是手术理念的转变,随着药物控制日趋理想,解剖理解更加清晰,手术理念由切除肿瘤向同时保留功能进步;二是手术需求的改变,新兴技术的不断出现,对临床医生大有助益,手术需求转变为理想的瘤控效果、完美的尿控和良好的勃起功能恢复,追求更少的并发症和早期康复。
腹腔镜下根治性前列腺切除术(laparoscopic radical prostatectomy,LRP)与开放术式在肿瘤控制和术后功能恢复方面效果相似,但具有切口小、住院时间短等优点,因此在临床中被广泛应用[5-7]。而相较于筋膜间LRP,筋膜内LRP能早期恢复控尿功能,且不影响切缘阳性[8-9]。我们在手术经验不断积累的同时,借助3D腹腔镜技术在缝合及精细操作方面的优势[10],结合本院在修复和重建领域的研究成果,总结提出新术式:3D腹腔镜下顺行双保根治性前列腺切除术(laparoscopic antegrade bilateral nerve-sparing radical prostatectomy,LabNSRP),即在保留功能和修复重建的理念下,以3D腹腔镜为手段顺行剜除前列腺。本研究回顾性分析我院于2017年7月-2020年1月采用LabNSRP治疗的50例前列腺癌患者的临床资料,探讨该术式的安全性和“双保”效果。
1 资料与方法
1.1 一般资料本组50例患者年龄(63.0±5.2)岁,术前总前列腺特异抗原(total prostate specific antigen,tPSA)平均(7.3±2.6)ng/mL,前列腺体积(40.2±12.1)cm3。所有患者均于我院行前列腺磁共振检查,并行B超引导下经会阴前列腺穿刺活检确诊为前列腺癌。确诊前列腺癌后手术等待时间平均为(2±1)周。患者均无明显手术禁忌证。本组手术均由同一手术团队完成。纳入标准:首次治疗的低中危前列腺癌患者,PSA≤20 ng/mL,Gleason评分≤7分,术前全身骨扫描均未见转移,均有前列腺癌手术指征,有完整的临床病理及随访资料。排除标准:有盆腔或前列腺手术史者;前列腺根治术前行内分泌治疗者;临床资料不全者。术后控尿标准采用尿垫数量评定:Ⅰ度为24 h使用1个尿垫;Ⅱ度为24 h使用2~3个尿垫;Ⅲ度为日间使用尿垫>3个,夜晚使用尿垫>1个。勃起功能恢复情况依据Rigiscan评估。
1.2 手术方式手术过程(“大家泌尿网”观看手术视频)采取腹膜外入路:①建立通道:气管插管全身麻醉,取仰卧位,头低20°,消毒后置导尿。常规建立气腹、放置4孔Trocar(两大两小),游离腹壁与膀胱前间隙。②离断膀胱颈部:显露出膀胱与前列腺边界,通过锐性和钝性分离形成漏斗形膀胱颈,注意保护逼尿肌围裙结构,使膀胱肌纤维远离前列腺,分离完前面后再环形分离,解剖出前列腺部尿道长1~1.5cm,保留的近端尿道长度0.5~1cm,离断尿道见导尿管非球囊或水囊。显露出导尿管后将导尿管夹起向上提起,显露出尿道侧壁和后壁并切断。尤其注意保留膀胱颈后壁合理厚度和膀胱颈口与尿道对合度。③解剖性精准切除精囊:离断膀胱颈后壁后打开膀胱前列腺肌,游离输精管和精囊,以超声刀切断输精管,将精囊游离并切除。游离前列腺底部、精囊与狄氏筋膜间网格状神经。④分离保留神经血管束(neurovascular bundle,NVB):前列腺血管蒂是NVB的血管组成部分,以两侧前列腺血管为导引做最大程度保留和最小损伤神经。⑤处理前列腺尖部:自前列腺底沿前正中线纵形切开前列腺筋膜至耻骨前列腺韧带处,提起筋膜,沿前列腺包囊向两侧及尖部分离,直至尖部,保留足够长膜部尿道。⑥后壁重建:后方第一层是狄氏筋膜与中央背侧隔缝合重建,第二层是后三角筋膜与中间隔缝合重建,第三层是膀胱颈与尿道横纹肌后层缝合重建。⑦膀胱尿道点对点吻合:采用连续缝合,从3点钟(膀胱截石位)开始,转向后壁(经6点至9点),再逐渐转向前壁,最后缝合前壁,并将膀胱颈部前壁间断缝合以缩小近端吻合口,此时更换F18三腔导尿管。⑧前壁重建:第一层通过缝合膀胱颈肌纤维与 DVC 和尿道之间的尿道周围组织重建最初的解剖,第二层盆内筋膜的脏层和壁层,目的是重建耻骨膀胱韧带的连续性。⑨完成手术:留置负压引流管一根,取出各点Trocar,留取标本送检病理,缝合,术毕。
1.3 随访观察指标①一般指标(表1):术前记录患者年龄、前列腺体积、PSA等,术中记录手术时间、术中出血量,术后记录留置导尿时间、住院时间、切缘阳性率、PSA、术后并发症等。②控尿情况:术后拔出导尿管即刻、1周、1月、3月、6月、1年评估患者控尿情况。③勃起功能:术前及术后3月、12月分别做Rigiscan评估。NPT正常值参考最新的Rigiscan 勃起功能障碍诊治临床应用中国专家共识[11]:正常中国人夜间8 h 睡眠过程中,阴茎发生有效勃起2次以上,每次持续10 min以上,勃起硬度>60%为正常勃起。
2 结 果
本组 50例手术均顺利完成,无中转开放手术,无肠道、血管、膀胱、输尿管、尿道等副损伤并发症,术后无腹股沟斜疝发生。术后病理无切缘阳性结果。术后1周内1例(2%)发生漏尿,经牵拉尿管并延长尿管留置时间后恢复正常。本组50例术后随访(12.4±6.7)个月。术后6周查PSA均达到根治标准;术后12个月1例出现生化复发,给予持续内分泌治疗和严密随访复查,PSA下降至0.003。拔除尿管后即刻控尿率26%(13/50),1周控尿率48%(24/50),1月控尿率62%(31/50)、3月控尿率84%(42/50)、6月控尿率90%(45/50)、1年控尿率为98%(49/50)(图1)。勃起功能恢复率术后3月为56%(28/50),术后12月为80%(40/50)(图2)。
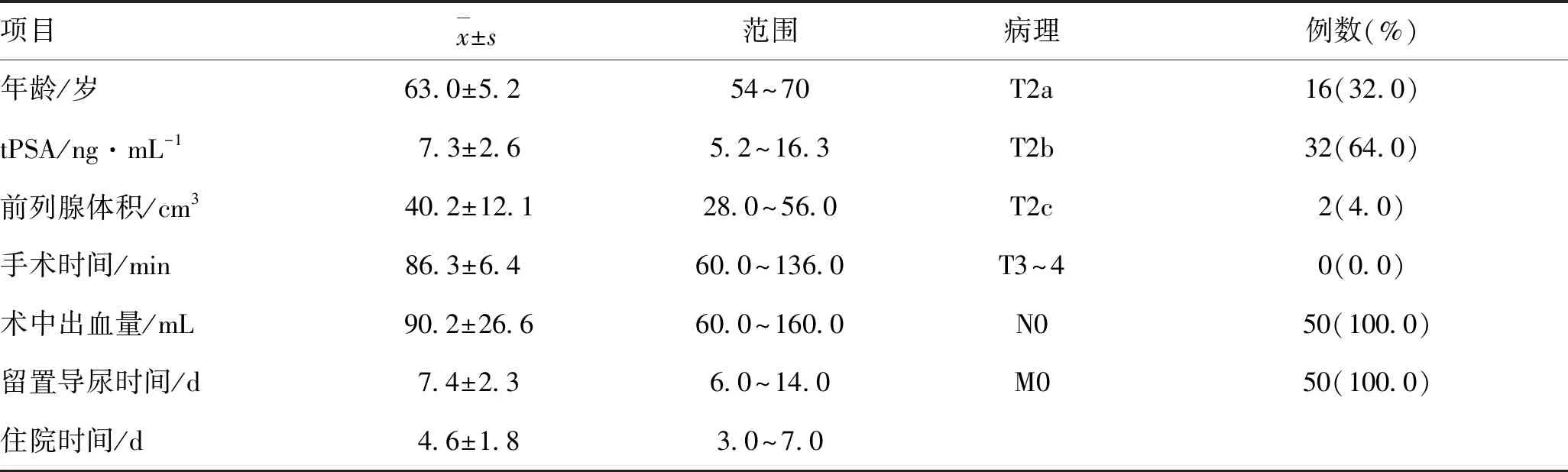
表1 纳入的50例患者的基本信息
3 讨 论
WALSH等[12]首次报道了解剖性经耻骨后根治性前列腺切除术。近年来,随着对前列腺筋膜及其周围NVB解剖结构的进一步认知[13-14],尤其是理清NVB相对于前列腺周围筋膜平面的位置,使得保留NVB的改良术式成功应用,对RP起到了革命性的推动作用[15-17]。在对过往经验总结时,一项Meta分析显示,在低风险局限性前列腺癌患者中,相较于筋膜外术式,筋膜内手术在不影响肿瘤完全控制的情况下,术后并发症少且缩短尿控和勃起功能恢复时间[18]。而相较于标准的二维视图,3D腹腔镜的应用使得解剖更加清晰立体,在肿瘤安全性、术中失血量和术后早期尿控恢复等方面得分更高,相较于2D腹腔镜9%的切缘阳性率,3D腹腔镜的切缘阳性率更低(4%)[19]。虽然达芬奇手术机器人逐渐在临床应用,但由于高昂的价格和培训周期长等因素,在我国广泛开展存在一定限制。本中心通过经验积累及查阅文献,在保留功能和修复重建的理念下,基于前列腺精细膜解剖[20],以3R(retain,reconstruction,replacement)原则为指导,借助3D腹腔镜技术,于经典IN-LRP的基础上对关键手术步骤进行了改良,总结出3D-LabNSRP术式。
RP术式可分为逆行和顺行技术[21]。本组患者采用顺行术式,首先打开膀胱颈,而不打开盆侧筋膜和不缝扎DVC,从而不破坏前列腺外周膜性结构和耻骨尿道韧带,维持稳定的尿控“悬吊系统”。打开膀胱颈过程中注意避免输尿管口的损伤,并且不断辨识膀胱颈厚度,做好膀胱颈的保护,我们认为膀胱颈厚度是保留控尿功能的重要因素。对于初学者而言,精囊输精管的处理可能是一个难点,在掌握精细解剖的基础上,精确游离是关键。
对于NVB的保护,手术过程中应避免热能量的损伤,尽量采用冷刀缓慢分离[23]。注意保护前列腺包膜周围前外侧及腹侧面外周膜结构的神经纤维组织,我们不止对传统的3~5点和7~9点区域进行保护,还尽量涵盖9~10点、2~3点和12~1点区域。将前列腺前外侧筋膜自前列腺包膜处完整分离,从而保留该处神经纤维。手术过程中注意后侧狄氏筋膜、后外侧前列腺筋膜、两者之间的前列腺侧韧带和前列腺动、静脉等4个标识点。在成功分离出NVB后,循序渐进地将其与前列腺分离,最后贴近前列腺包膜离断前列腺侧蒂。期间不间断地在前列腺侧后方检查NVB位置以避免损伤。
前列腺尖部应小心处理。一方面,前列腺外侧和后外侧区域的NVB呈网格状分布,但尖部性神经则呈集束样改变,一旦损伤,可能造成保留勃起神经的失败;另一方面,前列腺尖部功能尿道尽可能地保留足够长,而尖部又是切缘阳性和直肠损伤的高发地带,出血导致的视野模糊会增加切缘阳性率的发生。如果发生出血,我们一般采用3-0线缝扎止血,保证视野清晰。术中发现可疑病理性筋膜或组织,可进行快速冰冻病理切片,如果发现切缘阳性,则扩大切除范围。
尿道及周围组织重建对于术后早期尿控恢复同样具有十分重要的作用[23-24]。如果患者膀胱颈口过大,我们一般采用3-0可吸收线重建樱桃小口,更有利于口口吻合。残余狄氏筋膜、后方尿道组织和膀胱颈后唇的组织重建一方面是对于控尿因素的考虑,还可以缩短膀胱颈口和尿道内口的距离便于下一步的吻合。吻合强调黏膜对黏膜、点对点的吻合。我们一般采用2-0超滑线,后壁4针、前壁3针,一般情况下共7~8针;之后用倒刺线对前壁进行重建和加固,特别是耻骨前列腺韧带和膀胱颈的连续性,尽可能恢复患者术前的组织解剖结构。
改良之后的手术方式,因简化了手术步骤与国外相关报道比较,手术时间更短[25],患者术后2~3 d即可下地活动,留置导尿时间也较短[17],术后康复速度快,这可能与我们始终秉持的加速康复外科的理念运用有关[26]。另外,改良手术强调了手术的标准化和解剖性,手术层次清晰,而3D腹腔镜下视野更清晰,缝合更精细,手术中对周围组织损伤更小;同时,LabNSRP降低了膀胱颈尿道吻合口张力,有利于创面更快愈合。术后并发症方面,未出现脏器副损伤、泌尿道感染、腹股沟斜疝等并发症。
在保证肿瘤控制的前提下,做到控尿功能和勃起功能的稳定性和持久性才是真正做好前列腺癌根治术的关键和重要一环。荟萃分析显示,筋膜内RP在pT2期肿瘤中切缘阳性率为9.7%[9]。MENON等[27]报告的机器人辅助手术系统筋膜内手术46例患者,因严格的入组标准仅有1例切缘阳性。本组患者无切缘阳性发生,这与更加精细的术中解剖相关。国外报道的保留双侧神经LRP术后1月的控尿率为43%~64%[28-29],LabNSRP因做到全过程和全细节(双全)保留控尿技巧,拔除尿管后控尿率效果满意。在勃起功能保护方面,进行精准的筋膜内切除,最大程度保留前列腺筋膜内神经及血管末梢,最小程度损伤神经。当然手术过程中也不可盲目硬保,如出现下列情况,可不保留NVB或仅保留单侧:①术中分离NVB困难;②局部病灶侵犯;③高危前列腺癌;④活检示肿瘤侵犯神经;⑤一侧叶穿刺均阳性。术后阴茎康复结合我们既往经验,从疼痛康复、排尿康复、勃起功能康复三方面着手。我们率先在国内开展Rigiscan用于前列腺癌术后勃起功能的评估,从本组50例患者的监测结果来看,术后3月时患者的勃起功能恢复率为56%,术后12月时恢复率为80%,术后勃起功能恢复效果较为满意。
改良后的LabNSRP手术步骤简化,缩短了手术时间。最大限度保留前列腺外周膜结构,控尿恢复快。可精准筋膜内切除,保留前列腺筋膜内神经及血管末梢,最小程度损伤神经,勃起功能和控尿功能恢复快。但解剖条件复杂的情况下膜间平面无法确认,如慢性炎症、粘连和既往手术史等,筋膜间隙难以辨认和分离。随着机器人辅助LRP的逐步开展[30],3D-LabNSRP与机器人手术的结合能否取得更好效果[19],期待进一步的验证。总之,3D-LabNSRP解剖层次清晰、手术时间短、损伤小,可较大程度保护控尿和勃起功能,远期并发症发生率低。

