液相色谱—串联质谱测定水产品中15种苯二氮卓类镇静剂的药物残留
张秋云 杨洪生,2 谭秀慧 朱晓华,2 陈风蔚 陈慧敏
(1. 江苏省淡水水产研究所,江苏 南京 210017;2. 江苏省水产质量检测中心,江苏 南京 210017;3. 上海爱博才思分析仪器贸易有限公司,上海 200335)
苯二氮卓类镇静剂是1,4-苯并二氮卓类衍生物,为苯二氮卓受体激动剂,可引起中枢神经系统不同部位的抑制[1-3]。长期服用此类药物会产生耐药性及成瘾性,突然停药还会导致戒断症状出现[4-5]。苯二氮卓类镇静剂具有蓄积毒性,在体内吸收快,排泄慢,长期摄入后,会加重肝脏负担,导致肝功能下降,对中枢神经系统造成不良影响,引起头脑昏沉,记忆退化、运动障碍等问题[6-9]。中国于2002年禁止在饲料和动物饮用水中使用硝西泮、奥沙西泮等药物[10]。最新发布的GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》规定,地西泮仅允许治疗使用,但不得检出。
目前,检测镇定剂类药物残留的主要方法有酶联免疫法(ELISA)[11]、液相色谱法(LC)[12-13]、气相色谱—质谱联用法(GC-MS)[14-15]、液相色谱—串联质谱法(LC-MS/MS)[16-18],其中气相色谱—质谱联用法、酶联免疫法和液相色谱法前处理过程复杂,耗时长,稳定性和重复性差,灵敏度低,难以满足日常检测需求,而液相色谱—串联质谱法具有灵敏度高,抗干扰性强,重现性好等特点,是目前检测镇静剂类药物最主要的检测方法。此外,内标法相对于外标法具有简化前处理过程,有效抵消基质效应等优点,是质谱法的最优选择[19]。目前,水产品中检测常用镇静剂类药物定量定性检测主要以外标法为主,如何晓明等[20]建立了水产品中13种镇静剂残留检测的液质联用法,采用外标法定量,其前处理过程采用QuEChERS净化,但操作较繁琐、净化效果较差,也未考虑基质效应可能对结果准确性的影响。有学者采用内标法,但是也仅仅用1~3种内标物,如张璇等[18]建立了液质联用法测定水产品中12种镇静剂及其代谢物残留的内标法,但只用了安眠酮-D7、盐酸氯丙嗪-D6、地西泮-D53种内标,具有一定的局限性。
研究拟建立一种以内标法为基础且能同时检测多种镇静剂类物质及其代谢物的方法,并对样品前处理方法和仪器分析条件进行改进和优化,以期解决基质干扰问题,为水产品中镇静剂残留监测提供方法参考。
1 材料与方法
1.1 材料与试剂
15种镇静剂及14种同位素内标标准储备液(具体名称见表1):质量浓度均为1.0 mg/mL,美国Cerilliant公司;
乙腈、甲醇、氨水、乙酸乙酯和甲酸:色谱纯,德国Merck公司;
Waters Oasis PRIME HLB固相萃取小柱(150 mg/3 mL)、Waters Oasis HLB固相萃取小柱(150 mg/3 mL)、Waters C18柱(200 mg/3 mL)、Waters CORTECS C18液相色谱柱(3.0 mm×100 mm,2.7 μm):美国Waters公司;
Supelclean LC-18 固相萃取仪:德国Merck公司;
草鱼、南美白对虾和中华绒螯蟹等水产品:市售。
1.2 仪器与设备
三重四极杆液质联用仪:SCIEX Triple QuadTM5500型,美国Sciex公司;
高速冷冻离心机:Avanti J-26XP型,美国Beckman Coulter公司;
电子天平:CP225D型,德国Sartorius公司;
全自动浓缩仪:Turbo Vap LV型,瑞典Biotage公司;
纯水仪:Milli-Q型,美国Millipore公司。
1.3 标准溶液配制
(1) 混合标准工作液:分别移取一定体积的15种镇定剂标准储备液用乙腈配制成质量浓度均为100 μg/L的混合标准溶液,-18 ℃保存。
(2) 混合内标标准工作液:分别移取一定体积的同位素内标储备液用乙腈配制成质量浓度均为50 μg/L的混合标准溶液,-18 ℃保存。
1.4 样品前处理
草鱼、南美白对虾和中华绒螯蟹分别取可食部分,充分均质后-20 ℃保存。
于50 mL聚丙烯离心管中准确称取试样2.00 g,添加质量浓度为50 μg/L混合内标标准溶液200 μL,静置5 min,加入提取溶剂乙腈10 mL,涡旋混匀30 s,于常温下超声10 min,然后8 000 r/min离心10 min。准确移取5 mL上清液过Waters Oasis PRIME HLB固相萃取柱,调节流速至小于1滴/s,收集流出液于10 mL刻度离心管中,真空抽干1 min。流出液于50 ℃氮气吹至0.5 mL左右,用乙腈定容至1 mL,过0.22 μm尼龙微孔滤膜,备用待测。
1.5 分析方法
1.5.1 色谱条件 色谱柱:Waters CORTECS C18液相色谱柱(3.0 mm×100 mm,2.7 μm);柱温:35 ℃;进样量1 μL;流速:400 μL/min;流动相A:0.1%甲酸水溶液;B:甲醇。梯度洗脱程序:0~8.00 min,95% A;8.00~12.00 min,95%~10% A;12.00~12.10 min,10%~95% A;12.10~15.00 min,95% A。
1.5.2 质谱条件 离子源:ESI源,正离子模式;监测方式:多反应监测模式(MRM);电喷雾电压:5 500 V;离子源温度:450 ℃;气帘气:0.24 MPa;雾化气:0.38 MPa;辅助雾化气:0.38 MPa。15种镇静剂和14种内标物的监测离子对、去簇电压及碰撞能量等质谱参数见表1(其中普拉西泮对应内标为劳拉西泮-D4)。
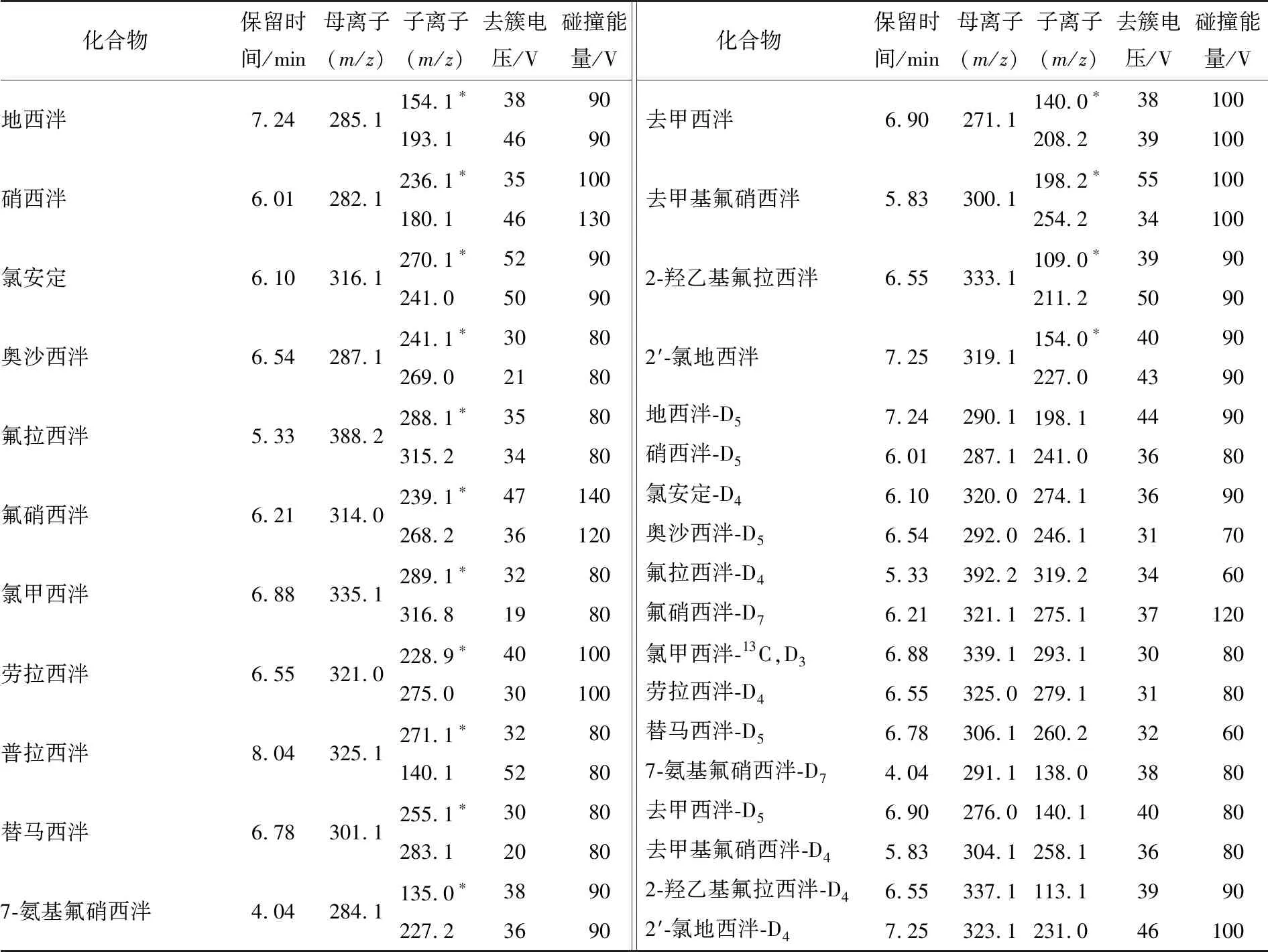
表1 15种镇静剂和14种内标物的监测离子对、去簇电压及碰撞能量†
1.6 数据处理
采用Origin软件对试验数据进行处理,分析检出限、定量限、准确度、精密度及回收率。
2 结果与讨论
2.1 液质条件优化
试验所选的镇静剂均含有仲胺或者叔胺基团,属于苯二氮卓类药物,易与氢离子结合成带正电荷的准分子离子[M+H]+,因此在正离子模式下,采用流动注射的方式分别将质量浓度为1 μg/mL的地西泮等15种镇定剂及14种内标物注入质谱,对目标化合物在m/z为200~450的范围内进行一级质谱全扫描,获得分子离子峰[M+H]+,且强度稳定在1×106以上。以高纯氮气为碰撞气,通过优化碰撞能量和去簇电压等质谱参数,分别选取干扰少、响应值高的2个子离子作为定量离子和定性离子,其中内标化合物只选取1个离子,用于目标化合物的定量。同时,分别考察了0.1%甲酸水溶液—乙腈、0.1%甲酸水溶液—甲醇、5 mmol/L乙酸铵溶液(含0.1%甲酸)—甲醇、5 mmol/L乙酸铵溶液(含0.1%甲酸)—乙腈4种流动相对目标化合物的灵敏度和峰型的影响。经过比较,采用0.1%甲酸水溶液—甲醇为流动相时,目标化合物的质谱响应值高,峰型更尖锐,各物质间的分离效果更好,因此选用0.1%甲酸水溶液—甲醇作为目标化合物检测的流动相,在此条件下15种镇静剂及14种内标化合物的提取离子流色谱图见图1。
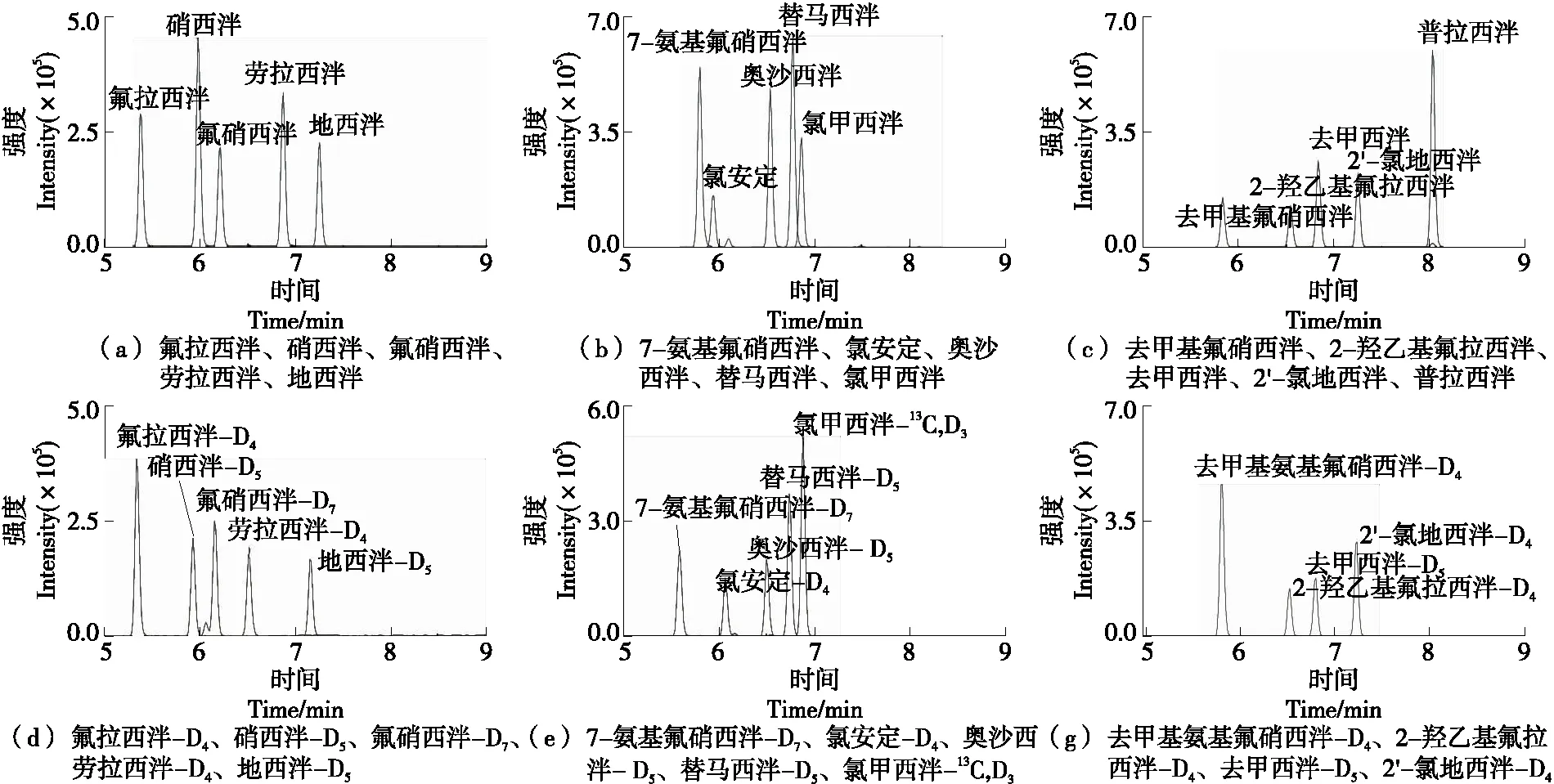
图1 15种镇静剂及14种内标化合物的提取离子流色谱图Figure 1 Extracted ion chromatograms of the 15 kinds of sedatives and 14 kinds of isotope internal standards
2.2 样品提取剂选择
地西泮等15种镇定剂为脂溶性物质,常用的提取剂有乙腈、乙酸乙酯等有机溶剂[21-25]。研究比较了乙腈、1%甲酸—乙腈、1%氨水—乙腈、1%氨水—乙酸乙酯、1%甲酸—乙酸乙酯、乙酸乙酯6种提取剂对目标化合物提取效果的影响。由于1%氨水—乙酸乙酯、1%甲酸—乙酸乙酯为提取溶剂时,提取液较为混浊且出现不同程度的乳化现象,分离效果差,因此在试验前期予以排除。其他4种提取剂的试验结果(如图2)表明,乙酸乙酯相对乙腈系列的提取溶剂来说,其总体回收率偏低,尤其是2′-氯地西泮和2-羟乙基氟拉西泮,其回收率仅为55.8%和60.1%;1%氨水—乙腈、1%甲酸—乙腈和乙腈作为提取溶剂时目标化合物的提取效果相差不大,考虑到地西泮等15种镇静剂的极性较弱,易溶于甲醇、乙腈等试剂,不易溶于水,而乙腈相对操作简便,因此选择乙腈作为目标化合物的提取剂。
2.3 浓缩过程优化
药物残留分析过程中常用的浓缩方法有旋转蒸发、氮吹、真空浓缩、冷冻干燥等,而氮吹由于干燥速度快、处理样品个数多、操作简单等优点而被广泛应用[26-27]。研究以15种镇静剂标准溶液为对象,考察了不同温度下(35,40,50,60 ℃)氮吹对回收率的影响。由图3可知,在不同的温度进行氮吹,目标化合物的响应值有所差异,温度越高耗时越短。35 ℃时氯安定和氯硝西泮的回收率低于70%,60 ℃时温度过高,氯硝西泮和去甲基氯硝西泮回收率低于70%,而且各目标物的回收率比40 ℃ 和50 ℃ 的显著降低,而在40 ℃和50 ℃下氮吹各目标物的回收率均达到70%~120%,由于在40 ℃下氮吹耗时较50 ℃下的长,因此,选择50 ℃为适宜氮吹温度。
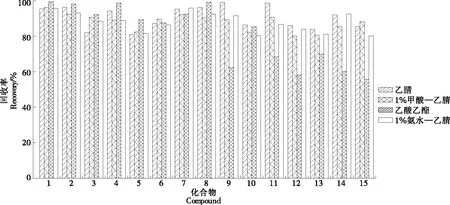
1. 地西泮 2. 硝西泮 3. 氯安定 4. 奥沙西泮 5. 氟拉西泮 6. 氟硝西泮 7. 氯甲西泮 8. 劳拉西泮 9. 普拉西泮 10. 替马西泮 11. 7-氨基氟硝西泮 12. 去甲西泮 13. 去甲基氟硝西泮 14. 2-羟乙基氟拉西泮 15. 2′-氯地西泮 以草鱼为基质,加标水平10 μg/kg
2.4 净化方法选择
研究考察了Waters Oasis PRIME HLB固相萃取柱、Waters Oasis HLB固相萃取柱和Waters C18固相萃取柱对镇定剂的净化效果。结果(图4)表明,Waters C18固相萃取柱净化效果较差,劳拉西泮、奥沙西泮、2′-氯地西泮等目标化合物在Waters C18固相萃取柱净化后回收率低于60%;Waters Oasis HLB固相萃取柱和Waters Oasis PRIME HLB柱对目标化合物的净化效果无显著差异,但Waters Oasis PRIME HLB固相萃取柱与传统的Waters Oasis HLB固相萃取柱相比,省去了活化、平衡步骤,样品提取液直接过柱,简化了前处理过程,同时又能有效去除95%以上的脂肪、磷脂等基质干扰物,样品更加干净,基质效应更小,因此选择Waters Oasis PRIME HLB为净化小柱。
2.5 基质效应
由于同位素内标和待测化学物质的性质相似,因此采用同位素稀释方法,能够有效抵消基质效应。根据式(1)计算不同基质中15种镇静剂的基质效应(ME)[28]。
(1)
式中:
ME——基质效应,%;
K1——基质匹配标准曲线的斜率;
K2——溶剂标准曲线的斜率。
ME值为80%~120%,表示基质效应较弱,即目标化合物在纯溶剂与基质溶液中的信号强度差别不大;ME值<80%,表示有较强的基质抑制效应,使得目标化合物信号显著减弱;ME值>120%,表示有较强的基质增强效应,使得目标化合物信号显著增强。
如图5所示,在草鱼、南美白对虾和中华绒螯蟹3种不同的基质中15种镇静剂均存在不同程度的基质效应。地西泮、硝西泮、氯甲西泮等镇静剂在草鱼、南美白对虾和中华绒螯蟹中基质抑制效应较大,而奥沙西泮镇静剂在中华绒螯蟹基质中有明显基质增强效应。因此,为有效降低基质效应,采用基质标准工作液中添加内标的方法来进行定量分析,以确保结果的准确性。

1. 地西泮 2. 硝西泮 3. 氯安定 4. 奥沙西泮 5. 氟拉西泮 6. 氟硝西泮 7. 氯甲西泮 8. 劳拉西泮 9. 普拉西泮 10. 替马西泮 11. 7-氨基氟硝西泮 12. 去甲西泮 13. 去甲基氟硝西泮 14. 2-羟乙基氟拉西泮 15. 2′-氯地西泮
2.6 方法的线性范围和检出限
在草鱼空白基质液中添加不同浓度的混合标准工作溶液,按1.4和1.5的条件进行测定。以各目标物质量浓度为横坐标(X),目标化合物峰面积和对应内标的峰面积比值为纵坐标(Y),绘制标准曲线。由表2可知,15种镇定剂在质量浓度为1~100 ng/mL的范围内呈良好的线性关系,相关系数(R)均大于0.99。以3倍信噪比(S/N=3)作为方法的检出限(LOD),10倍信噪比(S/N=10)作为方法定量限(LOQ)。
2.7 方法准确度和精密度
在2.00 g空白样品中添加质量浓度为50 μg/mL混合内标标准溶液200 μL,质量浓度为100 μg/L的15种镇定剂的混合标准溶液100,200,500 μL,即添加水平为5,10,25 μg/kg,每个添加水平平行测定6次,其加标回收率为78%~125%,RSD为1.52%~12.02%,见表3。表明该方法具有良好的准确度和精密度。
2.8 实际样品检测
利用上述检测方法对市场上常见的20份不同类型水产品(草鱼、鲫鱼、南美白对虾、中华绒螯蟹等)进行检测,结果显示,在1份草鱼样品中检出地西泮含量为0.85 μg/kg,其余样品中均未检出苯二氮卓类镇静剂。
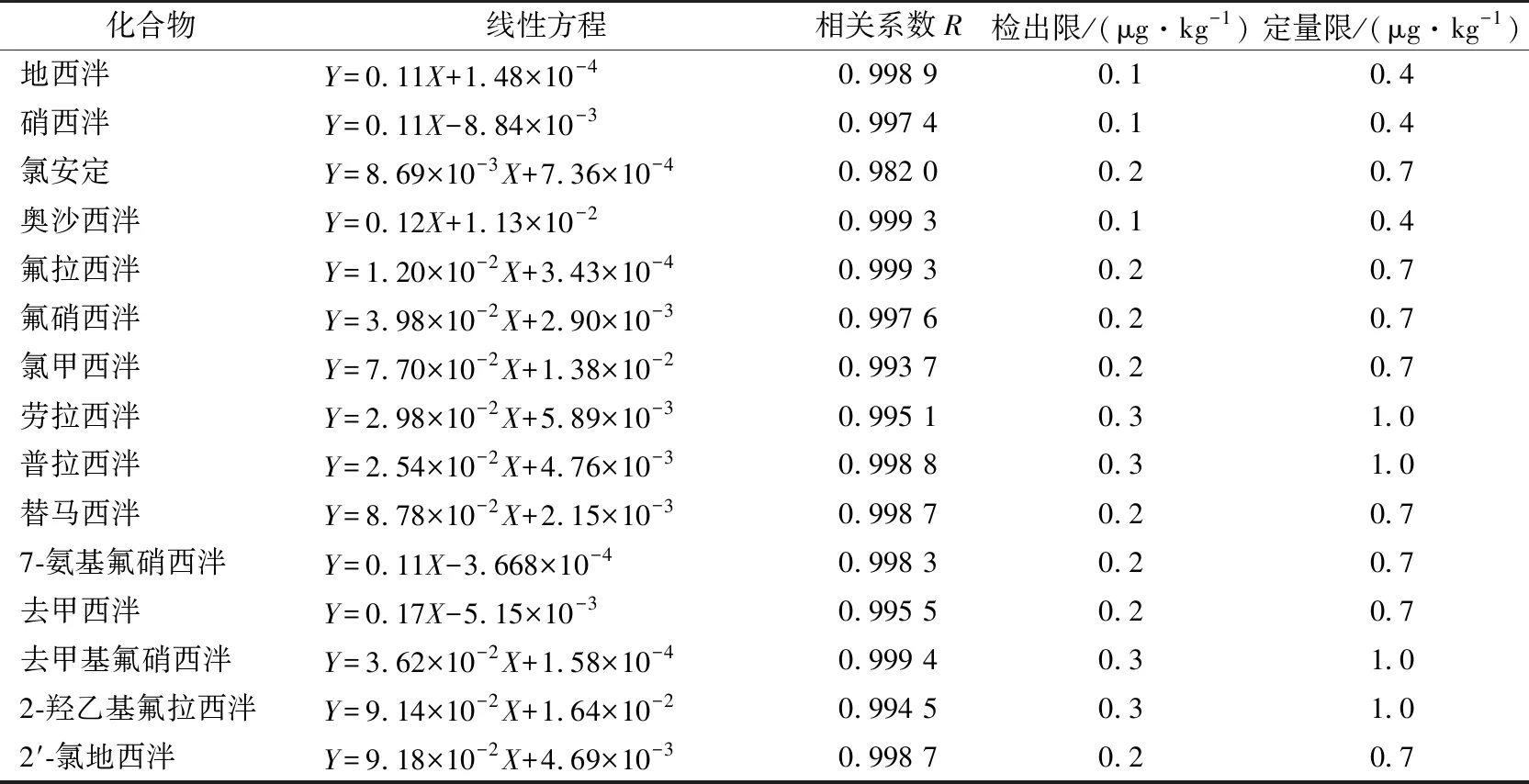
表2 15种镇静剂的线性方程、相关系数、检出限和定量限
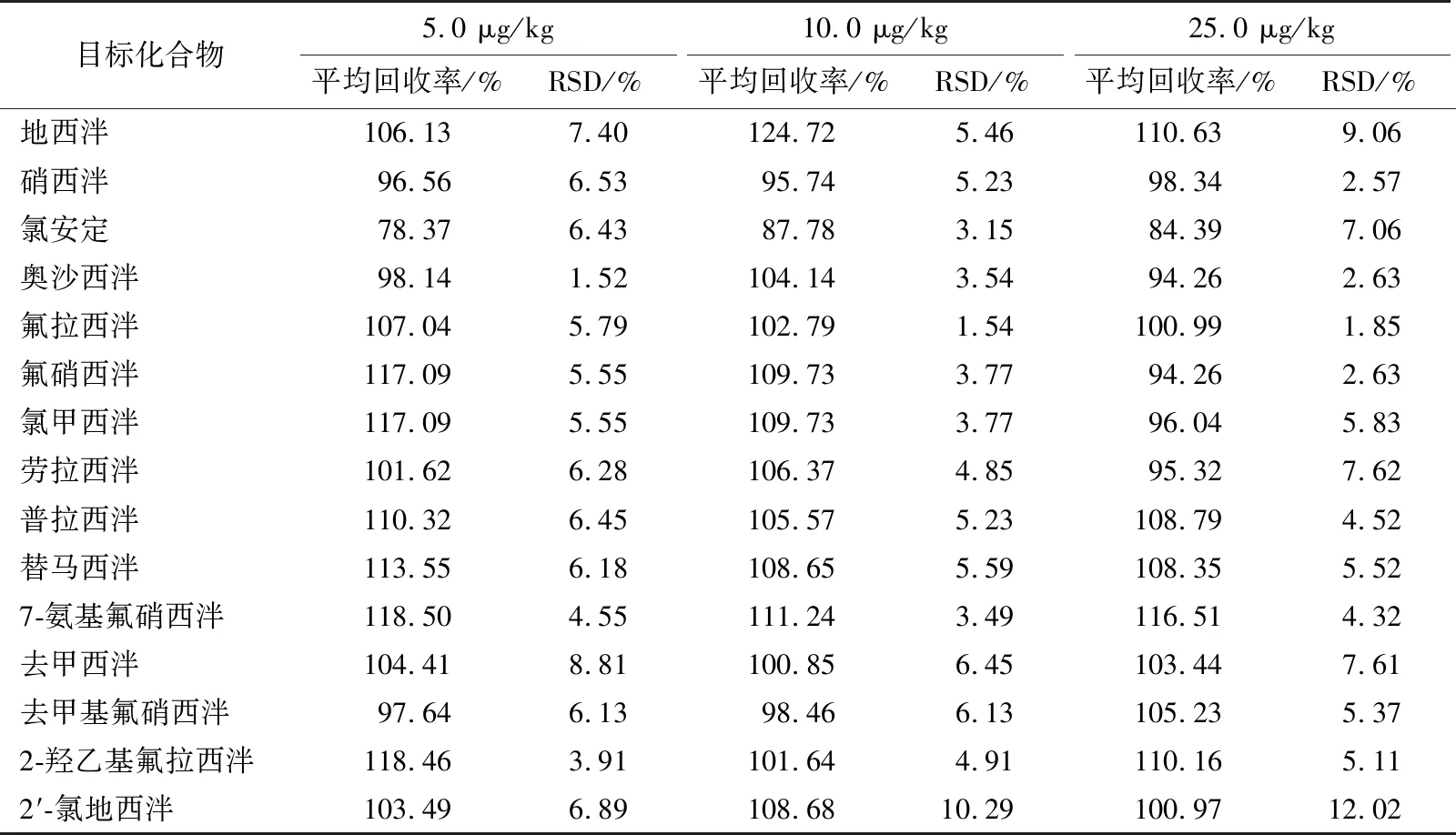
表3 15种镇静剂的准确度和精密度
3 结论
研究建立了液相色谱—串联质谱法测定水产品中15种苯二氮卓类镇定剂的分析方法,对提取溶剂、净化条件、浓缩方式、基质效应等因素进行了优化,采用同位素稀释,有效抑制基质效应干扰,提高了试验准确性。该方法操作简单、经济、高效,方法的准确度、精密度及灵敏度均能满足日常检测要求,适用于实验室大批量水产品样品的快速测定。

