不同澄清剂对中性医药玻璃澄清效果的影响
张晓雨,李常青,赵凤阳,石丽芬,仲召进,高 强
(1.中建材玻璃新材料研究院集团有限公司,浮法玻璃新技术国家重点实验室,蚌埠 233010;2.硅基材料安徽省实验室,蚌埠 233010)
0 引 言
近年来,随着我国制药行业的高速发展,医药玻璃由于具有诸多优良性能[1-2],如透明性、光洁性、阻隔性、化学稳定性、耐温性、遮光性、相容性、再生性等,成为众多医药产品和生物制剂不可替代的包装材料,被广泛应用于疫苗、高端输液剂、抗生素、普粉、冻干、血液、生物制剂等药品包装。医药玻璃按成分可分为钠钙玻璃和硼硅玻璃,其中B2O3含量为8%~12%(质量分数)的中硼硅玻璃是国际上常说的中性医药玻璃,被公认为是安全包装材料[3-4]。
气泡是玻璃熔制过程中比较常见的一种缺陷。气泡的存在会极大影响玻璃的均一性、热稳定性、机械性能及透光性,澄清过程即排出可见气泡的过程。中性医药玻璃气泡熔占比高且气泡个数多,气泡上升速率低,澄清相对困难[5-6]。气泡上升速率(vp)如式(1)所示[7-8]。
(1)
式中:ρ1和ρD分别为液体和空气的密度;g为重力加速度;dp为气泡直径;CD为阻力系数。
从式(1)可以看出,气泡上升速率的平方与气泡直径成正比,与阻力系数成反比。由于液体黏度与阻力成正比,那么气泡上升速率与玻璃液的黏度成反比[7]。因此,要想达到澄清效果,可以通过降低玻璃液黏度和增大气泡直径两种方法来实现。
本文选用添加澄清剂的方式来提高玻璃液澄清效果,根据作用机理可将澄清剂分为:(1)氧化物澄清剂,主要有SnO2、CeO2等;(2)硫酸盐型澄清剂,主要是Na2SO4、BaSO4;(3)卤化物澄清剂,主要有氟化物、NaCl、NH4Cl等;(4)复合澄清剂,主要利用协同效应和叠加效果,充分发挥复合澄清优势,可达到持续澄清的效果,显著增强澄清能力,是单一澄清剂无法比拟的[9-10]。
本文选用了氧化物澄清剂CeO2,卤化物澄清剂NaCl和复合澄清剂NaCl-CeO2、NaCl-CeO2-NaNO3,通过定量分析熔化过程中气泡面积与熔化面积的比例(简称“气泡熔占比”)、气泡个数和气泡平均直径的变化规律,研究不同澄清剂对中性医药玻璃液澄清效果的影响。
1 实 验
1.1 原料及设备
玻璃基础组成如表1所示。在保持玻璃基本组成不变的情况下,添加不同种类、不同含量的澄清剂进行中性医药玻璃澄清效果的研究。添加的玻璃澄清剂为CeO2、NaCl、NaCl-CeO2和NaCl-CeO2-NaNO3,具体见表2,其中A-1~A-6中添加不同含量氧化物澄清剂CeO2,B-1~B-6中添加不同含量卤化物澄清剂NaCl,C-1~C-3中添加不同含量复合澄清剂NaCl-CeO2,C-4~C-6中添加不同含量复合澄清剂NaCl-CeO2-NaNO3。

表1 玻璃样品组成
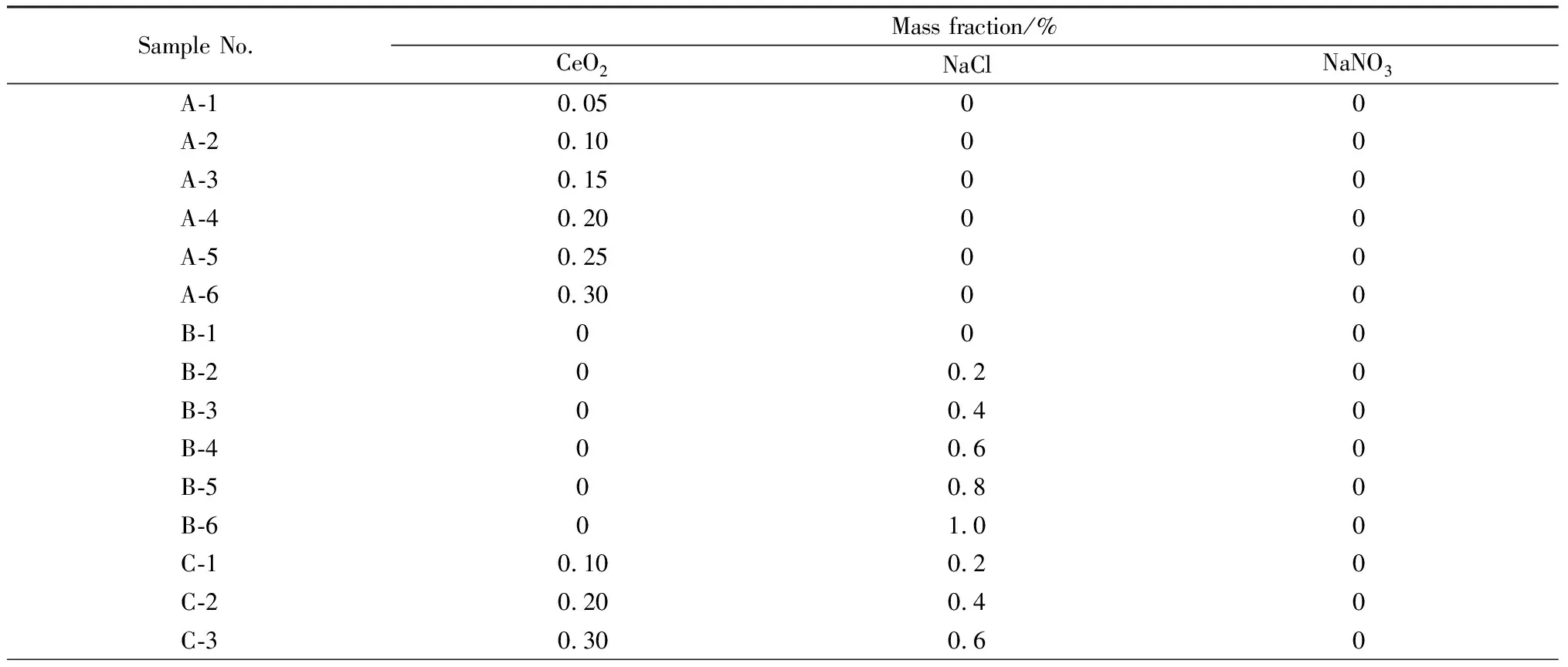
表2 澄清剂组成
1.2 性能测试
使用捷克GLASS SERVICE公司生产的高温熔融观察系统来观察试验过程。利用仪器的高温炉体对玻璃配合料进行加热熔融,最高可加热至1 700 ℃,同时利用仪器的图像采集系统来观察和记录不同温度下玻璃熔融过程的状态,最后通过对记录的数据信息进行处理,可得到玻璃液熔融状态时的气泡熔占比、气泡个数和气泡平均直径。该系统程序设置初始温度为500 ℃,炉体内样品加热至1 600 ℃,持续保温3 h后,再进行降温,随后取出样品。
2 结果与讨论
由于中性医药玻璃组成中SiO2、Al2O3的含量多,熔制温度达1 540~1 600 ℃,图1是加入了复合澄清剂NaCl-CeO2-NaNO3后中性医药玻璃液的高温观察图像。由图1可以看出,该玻璃液中气泡开始明显减少的初始温度主要在1 550 ℃,所以将1 550 ℃作为初始点,观察3 h内玻璃液的气泡熔占比、气泡个数和气泡平均直径,并借此判断其澄清效果。其中,气泡熔占比从0 min开始统计,气泡个数和气泡平均直径均从气泡个数达到最大值的时间点进行统计,由于石英坩埚失透后无法获取数据,因此试验数据的最后一个点为石英坩埚失透点[11-12]。

图1 不同温度下中性医药玻璃液的高温观察图像
2.1 CeO2对澄清效果的影响
CeO2是一种常用的氧化物澄清剂,其澄清机理为:CeO2为变价氧化物,在温度高于1 300 ℃时会分解出O2,随着温度升高,从CeO2的化学结合键中分离出的O2越多,释放出的O2扩散到周围[13],使玻璃液中气泡的气体分压降低,体积增大,气泡加速上升[7-8],达到好的澄清效果,反应式为
(2)
图2是不同CeO2含量样品气泡熔占比的变化。从图2中可以看出,加入澄清剂后,当温度达到1 550 ℃后玻璃液中气泡熔占比开始呈下降趋势。在澄清3 h后,A-1~A-6对应的气泡熔占比分别下降至10.6%、2.4%、4.2%、3.7%、3.5%、4.5%。这是因为高温下CeO2释放出的O2使玻璃液中形成大量的小气泡,在表面能作用下,小气泡富集长大后上升,气泡上升过程中与玻璃液中的大气泡结合,增加气泡体积,加速排出,但玻璃液的黏度较大,仍有少量小气泡残留在玻璃液中[14]。
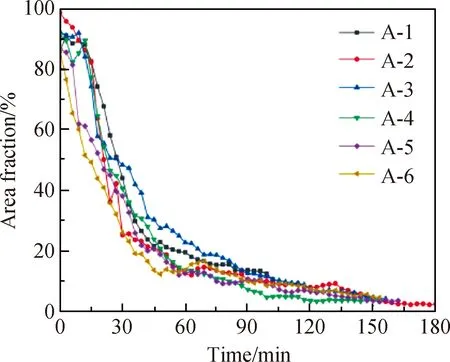
图2 不同CeO2含量样品从1 550 ℃开始3 h内气泡熔占比的变化
图3(a)是不同CeO2含量样品气泡个数的变化。从图3(a)中可以看出,加入澄清剂后,气泡个数随时间延长呈减小趋势。A-1的气泡个数从398个减少至150个,A-2的气泡个数从253个减少至18个,A-3的气泡个数从188个减少至42个,A-4的气泡个数从128个减少至22个,A-5的气泡个数从108个减少至21个,A-6的气泡个数从132个减少至23个。
图3(b)是不同CeO2含量样品从1 550 ℃开始3 h内气泡平均直径的变化。从图3(b)中可以看出,加入澄清剂后,随含量增加,气泡平均直径几乎不断增大。这是由于添加的CeO2较多时,样品在高温时放出的气体更多,更容易形成大气泡。从样品自身来看,气泡平均直径变化不大,大部分在0.4~0.8 mm。当样品在1 550 ℃保温3 h时,A-1~A-6气泡平均直径分别为0.43 mm、0.62 mm、0.47 mm、0.65 mm、0.66 mm、0.71 mm。随着CeO2含量的增加,释放出的O2越多,气泡平均直径越大,越有利于样品的澄清。
从图2和图3综合来看,A-4的气泡熔占比降至3.7%,气泡个数从128个减少至22个,气泡平均直径从0.71 mm减小至0.65 mm,由此认为A-4的澄清效果较佳。
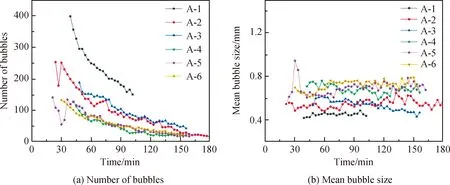
图3 不同CeO2含量样品从1 550 ℃开始3 h内气泡个数和气泡平均直径的变化
2.2 NaCl对澄清效果的影响
NaCl是高温挥发型澄清剂,沸点是1 413 ℃,在高温时会挥发,从玻璃液中扩散到周围气泡里,使气泡体积增大[15-16],气泡上升速率增加。图4是不同NaCl含量样品气泡熔占比的变化。从图4中可以看出,随NaCl含量的增加,在温度上升至1 550 ℃后的3 h内,气泡熔占比不断下降,前30 min下降明显。B-1~B-6的气泡熔占比分别下降至9.6%、8.7%、2.3%、0.3%、0.6%、1.2%。NaCl含量较多时,自身气化效果较好的同时,降低玻璃液黏度的效果更为明显,更容易排出气泡。
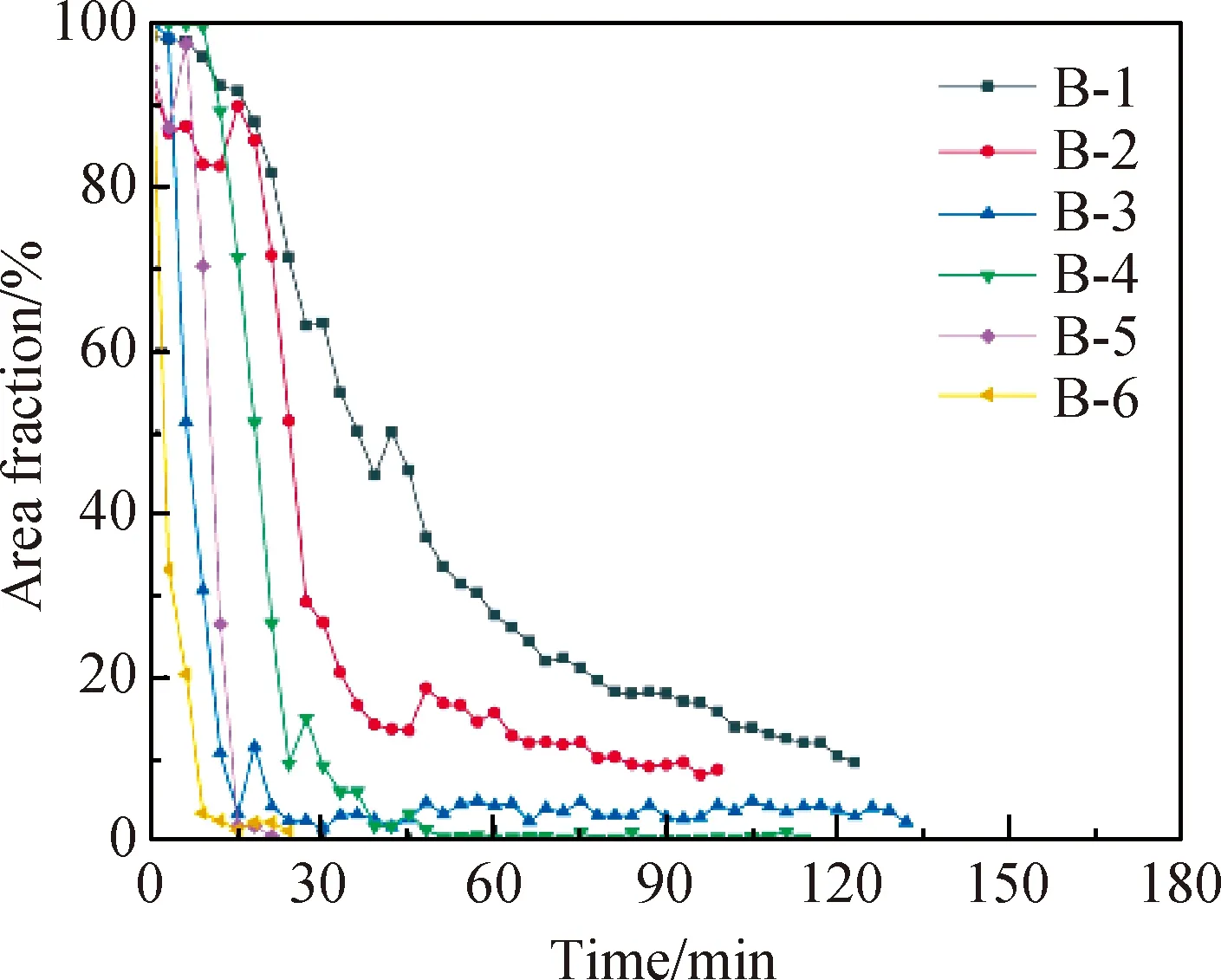
图4 不同NaCl含量样品从1 550 ℃开始3 h内气泡熔占比的变化
图5(a)显示了不同NaCl含量样品从1 550 ℃开始3 h内气泡个数的变化。从图5(a)中可以看出,在1 550 ℃开始后3 h内,气泡个数随澄清时间延长呈减少趋势。B-2和B-3气泡个数分别从156个减少至82个,389个减少至245个。B-4的气泡个数从89个减少至5个,B-5的气泡个数从12个减少到6个,B-6的气泡个数从19个减少到6个,澄清效果显著。
图5(b)是不同NaCl含量样品从1 550 ℃开始保温3 h气泡平均直径的变化。从图5(b)中可以看出,随着NaCl含量的增加,前30 min气泡平均直径呈下降趋势。添加不同含量的NaCl后,B-1气泡平均直径从0.55 mm减小至0.50 mm,B-2气泡平均直径从0.29 mm减小至0.26 mm,B-3气泡平均直径从0.50 mm减小至0.44 mm,B-4气泡平均直径从0.73 mm减小至0.33 mm,B-5气泡平均直径从0.76 mm减小至0.43 mm,B-6气泡平均直径从0.46 mm减小至0.33 mm。因此,从气泡熔占比、气泡个数和气泡平均直径可知,B-5玻璃液中的气泡在较短时间内被完全排出,澄清效果较佳。对比B-4与A-4澄清效果,NaCl作澄清剂时玻璃液中气泡熔占比较小,气泡个数减少较快,气泡平均直径较大,相对于CeO2作澄清剂时澄清效果较佳。
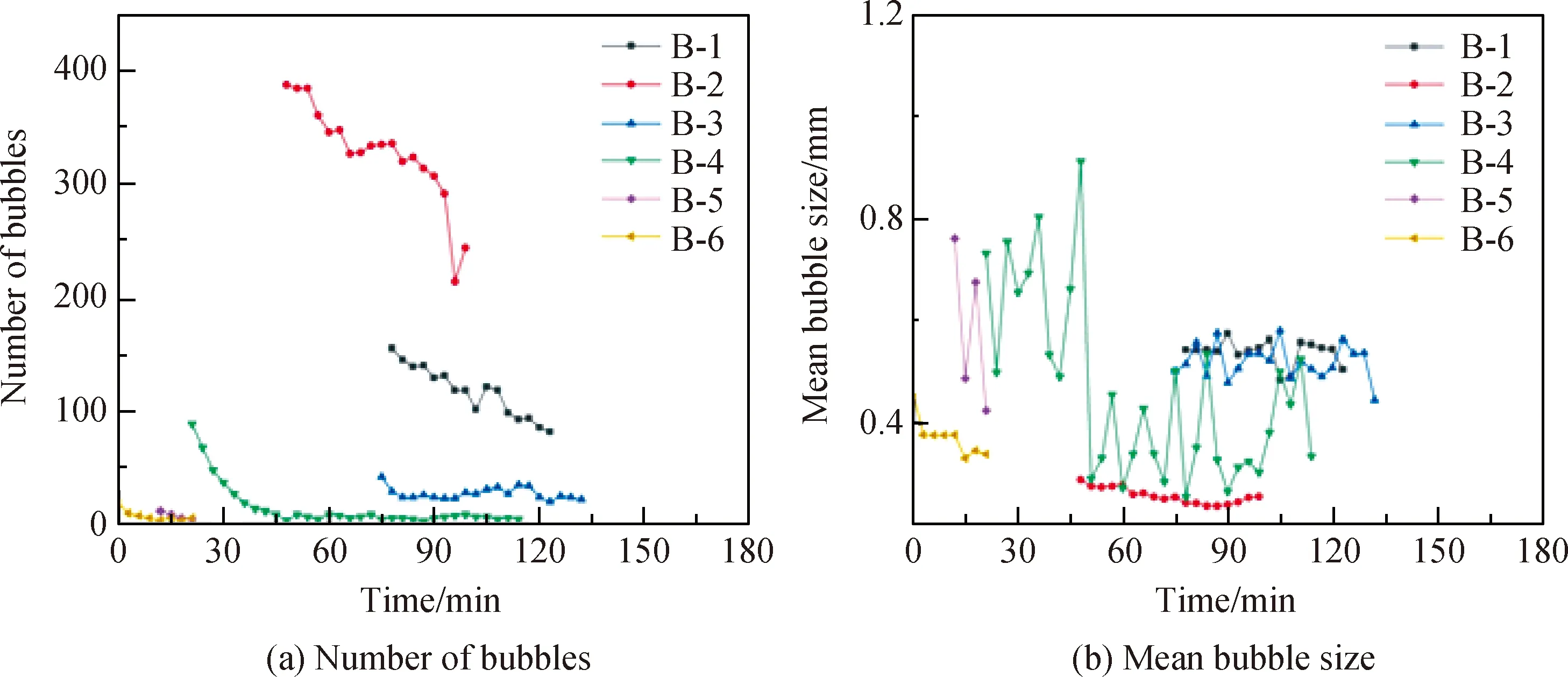
图5 不同NaCl含量样品从1 550 ℃开始3 h内气泡个数和气泡平均直径的变化
2.3 NaCl-CeO2和NaCl-CeO2-NaNO3对澄清效果的影响
单一澄清剂使用量往往都有临界值,达到临界值后再添加用量会影响澄清效果。添加NaCl时澄清效果较佳,但添加量较大时会侵蚀耐火材料,因此考虑以部分CeO2来替代NaCl形成复合澄清剂。为了防止CeO2用量较多时造成玻璃着色,加入NaNO3组合使用,同时NaNO3自身的分解温度为380 ℃,分解后会释放出O2、NO和NO2,使玻璃液中的气泡数量变多,气泡平均直径增大,同时Na+可以进一步降低玻璃黏度,有助于玻璃澄清[17-18]。NaCl-CeO2-NaNO3作为复合澄清剂使用时,CeO2自身排出O2的同时,NaCl也会自身气化,使气泡体积增加更多,气泡上升速率增加,降低玻璃液的黏度,使澄清效果更好。两种澄清过程互不干扰,起作用时甚至可能会使气泡体积更大,气泡排出速度加快[19]。
图6是不同复合澄清剂含量样品从1 550 ℃开始3 h内气泡熔占比的变化。由图6可以看出,保温3 h内C-1~C-6的气泡熔占比分别可降至0.8%、2.8%、1.4%、2.8%、0.6%、1.9%。除C-1外,随时间延长,其余样品的气泡熔占比都呈先下降后平缓的趋势,这是由于一定时间范围内,CeO2和NaCl迅速氧化和气化,同时NaCl减少黏度,使气泡上升速率增加,CeO2和NaCl反应完成后,气泡上升缓慢甚至不再上升。30 min内,C-5的气泡几乎排尽。C-1在保温2 h后,气泡熔占比又开始增大,然后迅速减小。这是由于CeO2和NaCl在短时间内放出较多的气体,使气泡体积增加,气泡上升速率迅速增加,气泡熔占比不断下降,直至趋于平缓;NaCl含量较少,随后剩余的CeO2被消耗放出O2,增加气泡个数和体积,气泡熔占比上升,同时随着气泡个数和体积不断增大,气泡上升速率增加,排出较多,气泡熔占比下降直至平缓。
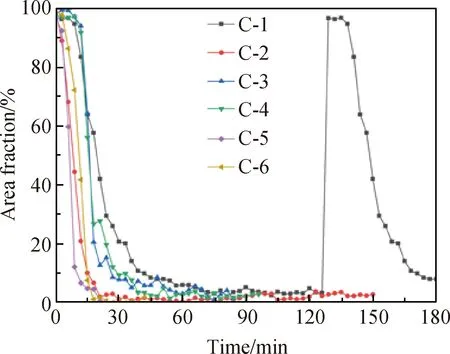
图6 不同复合澄清剂含量样品从1 550 ℃开始3 h内气泡熔占比的变化
图7(a)是不同复合澄清剂含量样品从1 550 ℃开始3 h内气泡个数的变化。从图7(a)中可以看出,C-1~C-6气泡个数分别从88个减少至15个,48个减少至23个,45个减少至15个,70个减少至19个,19个减少至3个,6个减少至4个。C-2气泡个数先减少后略微增加,这是由于NaCl和CeO2含量较多,NaCl消耗完后,剩余的CeO2放出O2,使气泡个数增加。除此之外,其他样品的气泡个数随保温时间的增加而减少。可以看出,C-5和C-6气泡个数较少,保温40 min内,气泡个数几乎为0。
图7(b)显示了不同复合澄清液含量样品从1 550 ℃开始保温3 h气泡平均直径的变化。从图7(b)中可以看出,C-1~C-6的气泡平均直径分别从0.84 mm减小至0.73 mm,0.63 mm减小至0.50 mm,0.92 mm减小至0.47 mm,1.46 mm减小至0.60 mm,0.87 mm减小至0.42 mm。前三组复合澄清剂样品中,C-2的气泡熔占比较小;后三组中C-5的气泡熔占比较小,剩余气泡个数较少,气泡平均直径较大。综合来看,C-5的澄清效果较好。
选取在1 550 ℃下21 min时A-4、B-5和C-5的气泡熔占比、气泡个数和气泡平均直径,见表3。图8是1 550 ℃下保温21 min后A-4、B-5和C-5的高温观测图像。从表3和图8中可看出,C-5的气泡熔占比较小,气泡个数较少,气泡平均直径较大。综合图5和图7来看,与加入NaCl和NaCl-CeO2相比,加入NaCl-CeO2-NaNO3的样品在1 550 ℃时的整体气泡平均直径较大,气泡个数较多。这是因为NaNO3分解温度较低,在NaCl和CeO2高温分解前,NaNO3会提前分解出气体,同时引入更多Na+,可以进一步降低玻璃液黏度,使澄清效果更好。综合来看,C-5的澄清效果最好。

表3 1 550 ℃开始保温21 min时样品的气泡熔占比、气泡个数和气泡平均直径

图8 1 550 ℃开始保温21 min时样品的高温观测图像
3 结 论
(1)CeO2作为氧化物澄清剂,通过放出O2来提高玻璃液的澄清效果。CeO2的质量分数从0.05%添加至0.30%,在升温至1 550 ℃后3 h内,当添加0.20%CeO2时,气泡熔占比降至3.7%,气泡个数减少为22个,气泡平均直径为0.65 mm,澄清效果一般。
(2)NaCl作为卤化物澄清剂,通过高温气化和降低玻璃液黏度来提高澄清效果。NaCl的质量分数从0%增至1.0%,在升温至1 550 ℃后3 h内,添加0.8%NaCl的玻璃液气泡熔占比降至0.6%,气泡个数减少为6个,气泡平均直径为0.43 mm,整体澄清效果较佳,在玻璃实际生产过程中,NaCl会导致耐火材料的腐蚀,影响玻璃制备。
(3)NaCl-CeO2和NaCl-CeO2-NaNO3作为复合澄清剂,通过CeO2、NaCl和NaNO3的协同作用来提高玻璃液的澄清效果。在升温至1 550 ℃后3 h内,添加复合澄清剂NaCl-CeO2和NaCl-CeO2-NaNO3,澄清效果较佳。加入0.4%NaCl-0.20%CeO2-0.005 0%NaNO3后,气泡熔占比降至0.6%,气泡个数减少至3个,气泡平均直径为0.60 mm,与添加CeO2和NaCl相比,整体澄清效果更好。

