星点设计效应面法优化一氧化氮供体型姜黄素胶束的制备工艺
钟荣生, 饶小勇,3,房元英,3,何 雁, 陆浩伟,刘 微,3*,罗晓健,3*
1.江西中医药大学,南昌 330004;2.江西中医药大学附属医院,南昌 330006;3.中药固体制剂制造技术国家工程研究中心,南昌 330006
姜黄素(curcumin, Cur)是从中药姜黄中提取的一种黄色多酚化合物,是一种强天然抗氧化剂,可预防多种疾病,通过抗氧化、抗炎等作用治疗动脉粥样硬化、阿尔茨海默病及脑梗死等疾病[1-3]。但Cur的水溶性较差,生物利用度低,进入体内后很快转化成葡萄糖醛酸结合物而快速排出体外,限制了其应用[4-7]。因此,在治疗脑梗死时,改善Cur溶解度低、透过血脑屏障差等问题,是提高其脑内转移率的重点。
聚合物胶束是由双亲聚合物在选择性溶剂中发生微相分离形成的具有疏水性核与溶剂化壳的一种自组装结构,能增加药物溶解度,借助自身粒径小的优势,协助药物透过血脑屏障,且成本较低,易于产业化生产[8-12],已经成为近年来研究及应用的热点。
在前期实验基础上,确定的关键因素有胶束比例、表面活性剂比例、药物辅料比例、制备温度等。为了满足应用要求,提高胶束对Cur的载药率,本研究用星点设计效应面法对Cur-PLA-NO的制备处方及工艺进行优化,以期利用胶束载药系统的制剂特性提高Cur的溶解度和血脑屏障透过率。
1 仪器与材料
1.1 仪器
Waters 2695型高效液相色谱仪(美国Waters公司);METTLER TOLEDO MS205DU十万分之一天平[梅特勒托利多科技(中国)有限公司];CO2细胞培养箱(美国赛默飞世尔科技公司);Zetasizer Nano ZS90型纳米粒度仪(英国马尔文公司);ZNCL-GS型磁力搅拌器(巩义市予华仪器有限公司);GZLY-1型冷冻干燥机(北京松源华兴科技发展有限公司);Millicell ERS-2、MillicellTranswell Inserts均购自Millipore公司。
1.2 试药
姜黄素原料药(质量分数为98%,南京春秋生物工程有限公司);mPEG-PLA-NO为自制(专利号:CN107998405A);叔丁醇(分析纯,上海麦克林有限公司);吐温80(质量分数为98%,天津市大茂化学试剂厂);L-半胱氨酸(质量分数为98%,日本东京化成工业株式会社);胎牛血清(fatal bovine serum, FBS,美国Gemini公司);DMEM(高),磷酸盐缓冲液(phosphate-buffered saline, PBS)均购自美国Hyclone公司;聚乙二醇-12-羟基硬脂酸酯(polyoxyl 15 hydroxystearate, HS15,北京凤礼精求医药股份有限公司);bEnd.3 细胞完全培养基(武汉普诺赛生命科技有限公司)。
1.3 细胞
bEnd.3细胞来源于美国ATCC细胞库。
2 方法
2.1 Cur-PLA-NO的制备
用溶剂蒸发法制备Cur-PLA-NO[13]。精密称取姜黄素、mPEG-PLA-NO和聚乙二醇-12-羟基硬脂酸酯(polyoxyl 15 hydroxystearate, HS15),加入溶剂叔丁醇,60 ℃磁力搅拌1 h,加入纯化水,搅拌20 min,静置至室温,加入质量浓度1 mg·mL-1甘露醇搅拌至溶解,过0.22 μm滤膜后,-20 ℃预冻7 h,缓慢降温抽真空冻干,即得Cur-PLA-NO。
2.2 姜黄素的含量测定
2.2.1色谱条件 色谱柱为Diamonsil 5 μm C18(250 mm×4.6 mm);流动相为冰醋酸水溶液(40 mL·L-1)-乙腈(52∶48);检测波长为430 nm;柱温为30 ℃;流速为1 mL·min-1;进样量为10 μL。
2.2.2主要溶液的配制 对照品溶液:精密称定姜黄素对照品20.00 mg,置于25 mL棕色量瓶中,用甲醇溶解并稀释至刻度,摇匀,得混合对照品储备液。取上述储备液12.5 mL,置于25 mL量瓶中,用甲醇稀释定容,摇匀即得质量浓度为0.40 mg·mL-1的对照品溶液,备用。
供试品溶液:用纯化水复溶Cur-PLA-NO,得质量浓度为0.702 mg·mL-1的胶束溶液,精密量取胶束溶液0.1 mL,置于1 mL量瓶中,用甲醇超声溶解并稀释至刻度,摇匀,静置,经0.22 μm微孔滤膜滤过,即得Cur-PLA-NO供试品溶液。
2.2.3线性关系与范围 精密量取10 mL对照品溶液,依次用甲醇稀释成质量浓度为0.0125、0.025、0.05、0.1、0.2、0.4、0.8 mg·mL-1的系列溶液,经0.22 μm微孔滤膜滤过,按色谱条件依次进样,记录色谱峰面积。以峰面积(A)为纵坐标,对照品质量浓度(C)为横坐标,绘制标准曲线,并进行线性回归。
2.3 星点设计优化Cur-PLA-NO处方工艺及验证
根据前期单因素实验结果,选择聚合物mPEG-PLA-NO投入量(x1, g)、乳化剂HS15投入量(x2, g)和制备温度(x3, ℃)3个对胶束质量浓度影响较大的因素,设计三因素三水平实验方案,共进行17 次实验。其中聚合物投入量、乳化剂投入量、制备温度的优化范围分别为0.04~0.10 g、0.04~0.08 g、40~70 ℃。通过星点设计效应面法筛选出最佳聚合物胶束的制备工艺,并按照最优处方工艺条件制备Cur-PLA-NO,测定姜黄素质量浓度,将实测值与预测值平行对比,计算两者间的误差。
2.4 包封率与载药率的测定
用高效液相色谱法测定并计算Cur的包封率与载药率。精密吸取胶束溶液400 μL,置于超滤离心管(相对分子质量为3 kDa)中,4 ℃以14 000 r·min-1离心15 min,吸取离心液及未离心胶束,按照2.2.1项下色谱条件进行含量测定,计算Cur-PLA-NO的包封率(encapsulation efficiency, EE)与载药率(drug loading, DL)。
DL=W负载÷(W负载+W胶束)×100%;
EE=W负载÷W总×100%。
W负载表示负载在胶束中姜黄素的质量,W总表示未离心胶束姜黄素的质量,W胶束表示胶束中聚合物的质量。
2.5 平均粒径和Zeta电位的测定
取适量2.2.2项下制备的Cur-PLA-NO溶液,用纯化水稀释至适宜质量浓度,室温下用粒径分析仪测定粒径及Zeta电位,每份样品测定3次。
2.6 姜黄素体外释放行为的研究
用PBS(pH 7.4)复溶Cur-PLA-NO至姜黄素质量浓度为0.75 mg·mL-1,取1 mL置于透析袋(醋酸纤维素酯,相对分子质量为300 kDa)中,以100 mL的1×PBS(室温条件下质量浓度10.5~11 mg·mL-1吐温80和3.5 mmol·L-1的L-半胱氨酸)为溶出介质[14],通过流池法溶出度仪收集溶出液,用高效液相色谱法(high performance liquid chromatography, HPLC)测定姜黄素含量,计算不同时间点Cur-PLA-NO中姜黄素的溶出百分率。
2.7 Cur-PLA-NO体外透过血脑屏障行为的研究
将bEnd.3细胞(2.25×105个·孔-1)接种于24孔Transwell 膜(0.4 μm,透孔聚酯膜)上,建立血脑屏障模型[15-16]。再用bEnd.3专用完全培养基培养7 d后,置于显微镜下观察,待细胞呈铺路石状态后,用Millicell ERS-2伏特欧姆测定跨内皮细胞电阻(TEER),评价血脑屏障体外细胞模型的完整性。TEER大于200 Ω·cm2则认为细胞具有完整性,可用于进一步的渗透性测试[17]。
在Transwell 上室分别加入含有Cur溶液(质量浓度30 μg·mL-1)、Cur-PLA-NO(质量浓度30 μg·mL-1)的培养基,见图1。下室加入新鲜培养基,孵育5 h 后,收集上层、细胞层和过滤层的溶液,用HPLC法测定3层中的含量。以此来判断2种溶液的渗透性。
透过率=过滤层质量浓度÷总质量浓度×100%。总质量浓度为上层溶液、细胞层溶液、过滤层溶液的总质量浓度。

图1 体外血脑屏障模型的构建
3 结果
3.1 线性关系与范围
经回归得姜黄素的线性回归方程为A=8×107C-181 908,R2=0.999 4。结果表明,姜黄素质量浓度在0.012 5~0.8 mg·mL-1范围内时线性关系良好。
3.2 星点设计优化Cur-PLA-NO处方工艺及验证结果
3.2.1星点设计优化Cur-PLA-NO处方 选择中心点为5的Box-Behnken设计,共进行17次实验,具体实验安排及结果见表1。

表1 星点设计效应面响应法实验安排及结果

3.2.3最佳工艺验证 根据前期单因素考察结果,温度设置在40~60 ℃,响应值质量浓度稳定在0.18~0.79 mg·mL-1范围内有利于保持制剂的稳定性。根据星点设计效应面法得到Cur-PLA-NO最优处方工艺:姜黄素、mPEG-PLA-NO及HS15的投入质量比例为1∶20∶15,叔丁醇加入量为20%,以500 r·min-1,55 ℃恒温磁力搅拌1 h,即得。在所选最佳处方工艺下,Cur-PLA-NO的载药量为(0.702±0.08) mg·mL-1;平均粒径为(26.41±0.35) nm,PDI为0.231±0.005,Zeta电位为(-13.25±0.35) mV。见表3和图3。实验结果表明,预测值与实测值的相对偏差为1.00%,表明该工艺准确可靠,重复性良好,经星点设计实验建立的数学模型预测性良好。
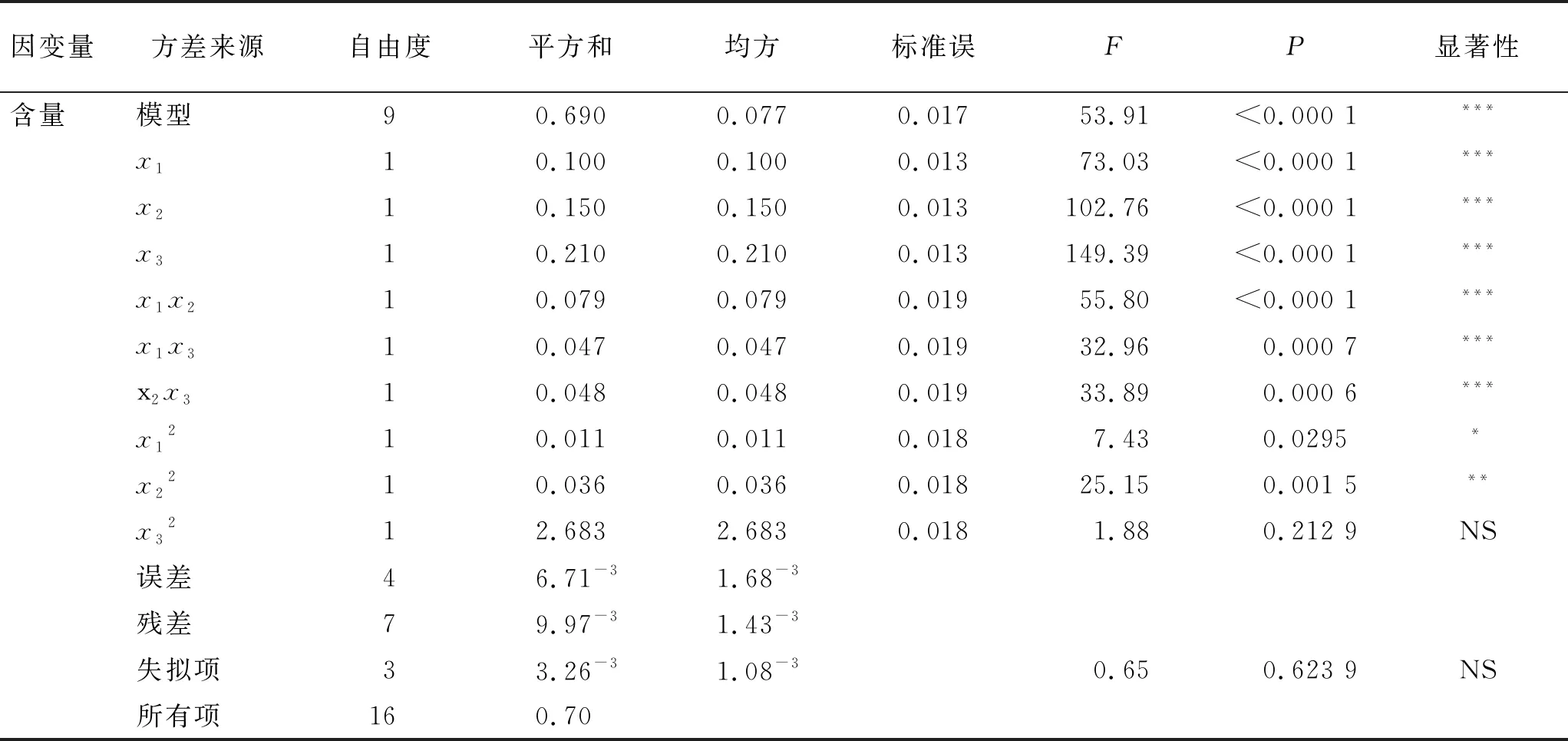
表2 回归模型的方差分析

图2 3个因素对Cur-PLA-NO质量浓度(y)的响应面图

表3 验证及重复性结果
3.3 Cur-PLA-NO体外释放行为的研究结果
实验结果表明,Cur-PLA-NO溶液在60 h内总释放量仅为55.43%±0.006%,见图4,表现出胶束的缓释特性。采用OriginPro 2018C 软件,对姜黄素体外释放曲线进行拟合得方程,见表4。由表4可见,Cur-PLA-NO姜黄素体外释放过程较符合一级动力学方程。
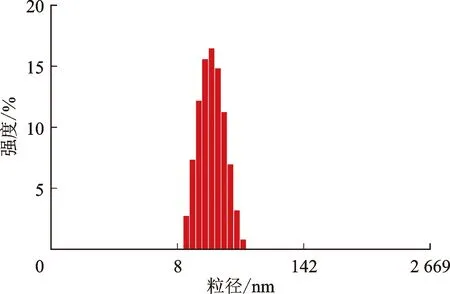
图3 最优处方验证粒径分布

图4 在pH7.4条件下Cur-PLA-NO中姜黄素的释放曲线 (n=3)

表4 姜黄素胶束的不同体外释药模型拟合方程
3.4 Cur-PLA-NO体外透过血脑屏障行为的结果
Cur-PLA-NO体外跨血脑屏障行为的结果见图5。结果表明,Cur-PLA-NO中Cur的血脑屏障透过率较Cur溶液更高,分别为42.2%±0.003%、27.5%±0.003%,表明水溶性差的药物通过两亲性嵌段制备成小分子胶束后,能够协助药物透过血脑屏障。
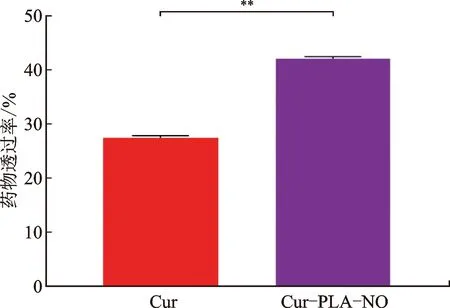
注:与Cur组比较,**P<0.01。
4 讨论
本实验采用星点设计效应面法优化Cur-PLA-NO胶束的处方及工艺,得到回归模型,比较各因素的显著性和各因素之间的交互作用,优选出Cur-PLA-NO胶束制备处方工艺的最佳条件:姜黄素、mPEG-PLA-NO及HS15的投入质量比为1∶20∶15,叔丁醇加入比例为20%,以500 r·min-1、55 ℃恒温磁力搅拌1 h。在所选最佳处方、工艺下,Cur-PLA-NO的粒径均匀、可控,为(26.41±0.35) nm,电位准确、稳定,为(-13.25±0.35) mV,包封率和载药量较高,分别为97.23%±0.17%、3.38%±0.05%,表明所建立的模型及所选工艺参数可靠,具有良好的预测性。
为了尽可能接近体内生理条件,选用pH为7.4的PBS为溶出介质,但Cur在弱碱性条件下易变性,导致溶解度降低[18],在PBS中无法被检测出来。研究表明,采用含吐温80的PBS,能明显改善Cur的溶解性与稳定性[19-21]。Cur-PLA-NO累积释放结果亦表明,Cur在40 h前释放较快,此后释放速率减慢直至60 h后基本保持不变,整个过程中未发生突释现象,可能归因于聚合物胶束的核壳结构。表明Cur-PLA-NO虽然不能保持恒定的释放速率,但符合一级动力学模型的要求,以相关系数为判断依据,具有从快速到缓慢释放的变化[22]。
血脑屏障是主要由脑微血管内皮细胞构建的屏障,可防止大分子进入大脑[23]。2种溶液的血脑屏障透过率结果表明,Cur溶液能够透过体外血脑屏障,这可以解释为Cur本身是脂溶性很强的小分子(油水分配系数lgP4.16[24],lgP越高,血脑屏障渗透率越高)。而将其封装在mPEG-PLA-NO中后,Cur-PLA-NO中Cur的血脑屏障透过率更高,约是Cur溶液的1.5倍,可能是由于分子体积占据主导作用,显著增加了Cur的血脑屏障透过率,且mPEG-PLA嵌段上增加的呋咱环型NO供体化合物,改变了共聚物嵌段的化学组成、长度与亲脂性,表现为与小鼠脑内皮细胞更加活跃的积极作用,同时Cur-PLA-NO表面带有的负电荷与血清蛋白互相排斥,这都有利于Cur-PLA-NO透过血脑屏障进入脑部发挥治疗作用。
综上所述,本实验采用星点设计效应面法对Cur-PLA-NO的制备处方工艺进行了优化,最终确定的最佳制备条件具有耗时短、包封率高及易产业化等优点。同时通过体外血脑屏障模型证明了Cur-PLA-NO的构建能显著提高Cur的血脑屏障透过率,为深入研究Cur-PLA-NO的体内生物性能奠定了基础。

