白花洋紫荆花的化学成分及其胰脂肪酶抑制活性研究
彭 京,何瑞杰,谢桃结,阳丙媛,王亚凤,黄永林*
1广西壮族自治区中国科学院广西植物研究所 广西植物功能物质与资源持续利用重点实验室,桂林 541006;2柳州市园林科学研究所,柳州 545005
豆科(Leguminosae)羊蹄甲属(Bauhinia)植物全世界约600种,遍布于世界热带地区,我国有40种,4亚种,11变种,主产南部和西南部,因树冠雅致花大而艳丽有香气,观赏价值很高,而且容易培植,常栽培于庭园、路边供观赏,是良好的观赏植物[1]。羊蹄甲属植物作为传统中药广泛被用来治疗糖尿病、抗菌消炎、镇痛、止血和利尿等[2]。白花洋紫荆(Bauhiniavariegatavar.candida)是洋紫荆(BauhiniavariegateL.)的变种,属豆科羊蹄甲属落叶乔木,花性味是苦、涩、平,入药可以用来治疗消化不良、风热咳嗽、肝炎,因花开时非常美丽而稠密,且带有香味,民间常用来裹面粉油炸或作为青菜汤吃[3]。但是,目前白花洋紫荆花的化学成分及可食性药理方面的研究还未见有相报道。为了充分掌握白花洋紫荆的物质基础及为其可食性提供科学依据,本研究对白花洋紫荆花乙醇提取物进行了系统的分离纯化,分离鉴定的化合物以黄酮类成分为主,文献报道此类化合物具有较好的胰脂肪酶抑制剂活性,因此又对分离得到的化合物进行了胰脂肪酶抑制剂活性研究,旨在为该植物的开发利用与发现新的用途提供科学依据。
1 材料与方法
1.1 仪器与材料
Bruker Avance 500 MHz超导核磁共振波谱仪(Bruker,德国);LCMS-IT-TOF(日本 Shimadzu 公司);LC52半制备液相色谱仪(赛谱锐思,北京);Sephadex LH-20(25~100 μm;GE Healthcare Bio-Science AB,Uppsala,瑞士);MCI gel CHP 20P(75~150 μm;Mitsubishi Chemical,Tokyo,日本);Toyopearl HW-40F(TOSOH Co,Tokyo,日本);GF254薄层色谱硅胶(Merck,德国);奥利司他(美国MCE);4-甲基伞形酮油酸酯(美国Sigma);猪胰脂肪酶(美国Sigma);磷酸盐缓冲盐水(北京Solarbio);所用试剂甲醇、乙醇等均为分析纯(AR)。
实验所用白花洋紫荆花采自广西柳州市,经柳州市园林科学研究所刘思鉴定为白花洋紫荆(B.variegatavar.candida)的花,凭证样品(2020.03.18)存放于广西植物功能物质研究与资源持续利用重点实验室。
1.2 实验方法
1.2.1 提取与分离
取新鲜白花洋紫荆花25 kg用纯乙醇室温浸提3次,每次7 d,合并提取液并过滤,减压浓缩后得到浸膏1183.5 g,加水溶解后用石油醚、乙酸乙酯分别萃取3次,回收乙酸乙酯溶液得到浸膏192.6 g。乙酸乙酯浸膏190.0 g经MCI gel CHP 20P层析柱(8 cm×18 cm)分离,甲醇-水(0→100%,每10%为1梯度)进行梯度洗脱,得到Fr:1~7共7个组份。Fr2(34.3 g)经Sephadex LH-20层析柱(6 cm×30 cm)分离,甲醇-水(0→100%,每10%为1梯度)进行梯度洗脱,得到Fr:2-1~2-9共9个组分。Fr2-1(3.7 g)过Toyopearl HW-40F层析柱分离得到化合物1(30 mg)。Fr2-7(12.3 g)过硅胶(4 cm×30 cm)柱层析,石油醚:二氯甲烷(4∶1、3∶2、2∶3、1∶4)进行梯度洗脱,得到化合物2(13 mg)、8(26 mg)、12(30 mg)、13(30 mg)。Fr2-8(7.6 g)过Toyopearl HW-40F(4 cm×30 cm)柱层析,甲醇-水(0→100%,每10%为1梯度)梯度洗脱,Fr2-8-4及Fr2-8-6放置后有结晶析出,分别得到化合物16(23 mg)、17(28 mg)。Fr2-8-2再经硅胶柱层析得到化合物11(9 mg)。Fr3(11.0 g)经Sephadex LH-20层析柱(4 cm×30 cm)分离,甲醇-水(0→100%,每10%为1梯度)进行梯度洗脱,得到Fr3-1~3-10共10个组分。Fr3-2(3.0 g)经硅胶柱层析(3 cm×30 cm)分离,经石油醚:二氯甲烷(8∶2、7∶3、5∶5)进行梯度洗脱,得到化合物3(23 mg)、4(4 mg)、5(11 mg)、10(46 mg)。Fr3-5(2.3 g)经硅胶柱层析(3 cm×25 cm)分离,经石油醚:二氯甲烷(8∶2、7∶3、5∶5)进行梯度洗脱,得到化合物6(7 mg)、14(32 mg)、15(26 mg)。Fr.3-8(86 mg)经半制备HPLC(半制备柱:C18,10 mm×250 mm,5 μm,YMC公司;流动相:30%乙腈等梯度洗脱:流速:2 mL/min;柱温:35 ℃)分离得到化合物7(tR=12.5 min,8 mg)、9(tR=14.6 min,15 mg)。
1.2.2 胰脂肪酶抑制活性筛选
采用猪胰脂肪酶抑制剂活性筛选模型对分离得到量较多的化合物10、12、13、14、17进行活性测试,实验方法参照相关文献[4],以奥利司他(orlistat)为阳性对照,以4-甲级伞形酮油酸酯(4-MUO)为底物。将猪胰脂肪酶溶解于PBS缓冲液配置成1 mg/mL的溶液,离心取上清液备用。准确称取1 mmol 4-MUO溶解于10 mL PBS缓冲液配置成0.1 mmol/mL溶液备用。准确称取10 mmol样品溶解于PBS缓冲液并定容至1 mL备用。取25 μL不同浓度的样品与25 μL胰脂肪酶溶液孵育五分钟后再加入50 μL 4-MUO底物,反应20 min后加入100 μL 0.1 mol/mL柠檬酸钠溶液终止反应,在320 nm激发波长和450 nm发射波长下测量吸光度,抑制率的计算公式如下。
胰脂肪酶抑制率=
[1-(A样品-A样品对照)/(A空白-A空白对照)]×100%
式中,A样品为加入样品和活性酶反应后的吸光值;A样品对照为加入样品和失活酶反应后的吸光值;A空白为加入活性酶和PBS反应后的吸光值;A空白对照为加入失活酶和PBS反应后的吸光值,所有反应组中均有4-MUO。
2 结果与分析
2.1 化合物结构鉴定
化合物1无色油状;ESI-MS:m/z195 [M+H]+,分子式为C7H14O6;1H NMR(500 MHz,CD3OD)δ:4.18(1H,d,J=7.8 Hz,H-1),3.87(1H,dd,J=12.0,1.6 Hz,H-6a),3.67(1H,dd,J=12.0,5.4 Hz,H-6b),3.53(3H,s,-OCH3),3.35(1H,t,J=8.9 Hz,H-3),3.31(1H,m,H-5),3.28(1H,m,H-4),3.16(1H,dd,J=8.9,7.8 Hz,H-2);13C NMR(125 MHz,CD3OD)δ:105.3(C-1),75.1(C-2),78.1(C-3),71.5(C-4),77.8(C-5),62.6(C-6),57.3(-OCH3)。以上数据与文献[5]对照基本一致,故鉴定化合物1为β-D-甲基葡萄糖苷。
化合物2白色粉末;ESI-MS:m/z153 [M+H]+,分子式为C8H8O3;1H NMR(500 MHz,CD3OD)δ:7.96(2H,d,J=9.0 Hz,H-2,6),6.97(2H,d,J=9.0 Hz,H-3,5),3.84(3H,s,-OCH3);13C NMR(125 MHz,CD3OD)δ:122.5(C-1),132.1(C-2/6),115.4(C-3/5),160.3(C-4),52.0(-OCH3),167.3(-COO)。以上数据与文献[6]对照基本一致,故鉴定化合物2为对羟基苯甲酸甲酯。
化合物3白色粉末;ESI-MS:m/z153 [M+H]+,分子式为C8H8O3;1H NMR(500 MHz,CD3OD)δ:7.97(2H,d,J=8.6 Hz,H-2,6),6.98(2H,d,J=8.6 Hz,H-3,5),3.86(3H,s,-OCH3);13C NMR(125 MHz,CD3OD)δ:169.8(-COO),165.0(C-4),132.8(C-2/6),124.0(C-1),114.7(C-3/5),56.0(-OCH3)。以上数据与文献[7]对照基本一致,故鉴定化合物3为对甲氧基苯甲酸。
化合物4白色粉末;ESI-MS:m/z165 [M+H]+,分子式C9H8O3;1H NMR(500 MHz,CD3OD)δ:7.60(1H,d,J=15.5 Hz,H-7),7.44(2H,d,J=8.5 Hz,H-3,5),6.81(2H,d,J=8.5 Hz,H-2,6),6.28(1H,d,J=15.5 Hz,H-8);13C NMR(125 MHz,CD3OD)δ:127.2(C-1),131.1(C-2/6),116.8(C-3/5),161.1(C-4),146.8(C-7),115.7(C-8),171.0(-COO)。以上数据与文献[8]对照基本一致,故鉴定化合物4为对香豆酸。
化合物5白色无晶形粉末;ESI-MS:m/z179 [M+H]+,分子式为C10H10O3;1H NMR(500 MHz,CD3OD)δ:7.62(1H,d,J=15.9 Hz,H-7),7.54(2H,d,J=8.7 Hz,H-2,6),6.94(2H,d,J=8.7 Hz,H-3,5),6.32(1H,d,J=15.9 Hz,H-8),3.83(3H,s,OCH3);13C NMR(125 MHz,CD3OD)δ:128.4(C-1),130.1(C-2/6),115.4(C-3/5),163.9(C-4),146.2(C-7),116.6(C-8),170.8(-COO),55.9(-OCH3)。以上数据与文献[9]对照基本一致,故鉴定化合物5为对甲氧基桂皮酸。
化合物6无针形粉末;ESI-MS:m/z271 [M+H]+,分子式为C16H14O4;1H NMR(500 MHz,CD3OD)δ:7.07(1H,t,J=8.1 Hz,H-10),6.93(1H,d,J=11.6 Hz,H-5),6.89(1H,d,J=8.1 Hz,H-9),6.62(1H,d,J=11.6 Hz,H-6),6.58(1H,dd,J=8.2,1.1 Hz,H-8),6.21(1H,s,H-4),3.74(3H,s,-OCH3),2.07(3H,s,-CH3);13C NMR(125 MHz,CD3OD)δ:148.1(C-1),115.0(C-2),156.0(C-3),112.5(C-4),129.5(C-4a),130.6(C-5),129.8(C-6),119.9(C-6a),156.5(C-7),101.8(C-8),125.3(C-9),113.4(C-10),160.7(C-10a),140.3(C-11a),56.1(-OCH3),8.7(-CH3)。以上数据与文献[10]对照基本一致,故鉴定化合物6为pacharin。
化合物7黄色粉末;ESI-MS:m/z273 [M+H]+,分子式为C15H12O5;1H NMR(500 MHz,CD3OD)δ:7.30(2H,d,J=8.5 Hz,H-2′,6′),6.82(2H,d,J=8.5 Hz,H-3′,5′),5.89(1H,d,J=2.0 Hz,H-8),5.88(1H,d,J=2.0 Hz,H-6),5.30(1H,dd,J=13.0,3.0 Hz,H-2),3.10(1H,d,J=17.1,13.0 Hz,H-3a),2.68(1H,d,J=17.1,3.0 Hz,H-3b);13C NMR(125 MHz,CD3OD)δ:80.4(C-2),43.9(C-3),197.8(C-4),165.4(C-5),97.1(C-6),168.3(C-7),96.2(C-8),164.9(C-9),103.3(C-10),131.1(C-1′),129.0(C-2′/6′),116.3(C-3′/5′),158.9(C-4′)。以上数据与文献[11]对照基本一致,故鉴定化合物7为柚皮素。
化合物8黄色粉末;ESI-MS:m/z433 [M+H]+,分子式为C21H20O11;1H NMR(500 MHz,DMSO-d6)δ:8.02(2H,d,J=8.7 Hz,H-2′,6′),6.89(2H,d,J=8.7 Hz,H-3′,5′),6.76(1H,s,H-8),6.27(1H,s,H-3),4.68(1H,d,J=9.2 Hz,H-1″),3.83(1H,t,J=9.2 Hz,H-2″),3.76(1H,d,J=10.8 Hz,H-6a″),3.39~3.24(4H,m,H-3″,4″,5″,6b″);13C NMR(125 MHz,DMSO-d6)δ:163.9(C-2),102.8(C-3),182.3(C-4),156.7(C-5),108.1(C-6),163.8(C-7),94.1(C-8),161.3(C-9),104.0(C-10),121.2(C-1′),128.4(C-2′/6′),116.1(C-3′/5′),160.0(C-4′),78.9(C-1′′),73.6(C-2′′),71.3(C-3′′),70.7(C-4′′),81.2(C-5′′),61.6(C-6′′)。以上数据与文献[12]对照基本一致,故鉴定化合物8为异牡荆苷。
化合物9黄色粉末;ESI-MS:m/z285 [M+H]+,分子式为C15H10O6;1H NMR(500 MHz,CD3OD)δ:8.03(2H,d,J=8.9 Hz,H-2′,6′),6.88(2H,d,J=8.9 Hz,H-3′,5′),6.34(1H,d,J=2.1 Hz,H-8),6.15(1H,d,J=2.1 Hz,H-6);13C NMR(125 MHz,CD3OD)δ:148.0(C-2),137.0(C-3),177.3(C-4),162.4(C-5),99.3(C-6),165.5(C-7),94.5(C-8),158.2(C-9),104.5(C-10),123.7(C-1′),130.6(C-2′/6′),116.3(C-3′/5′),160.5(C-4′)。以上数据与文献[13]对照基本一致,故鉴定化合物9为山柰酚。
化合物10黄色粉末;ESI-MS:m/z465 [M+H]+,分子式为C21H20O12;1H NMR(500 MHz,CD3OD)δ:8.05(2H,d,J=8.9 Hz,H-2′,6′),6.89(2H,d,J=8.9 Hz,H-3′,5′),6.39(1H,s,H-8),5.23(H,d,J=7.4 Hz,H-1″),3.69(1H,dd,J=11.9,2.4 Hz,H-6a),3.53(1H,dd,J=11.9,5.5 Hz,H-6b),3.45(1H,t,J=9.1 Hz,H-3″),3.42(1H,t,J=9.1 Hz,H-4″),3.34(1H,m,H-2″),3.21(1H,m,H-5″);13C NMR(CD3OD,125 MHz)δ:158.5(C-2),135.5(C-3),179.5(C-4),163.0(C-5),100.0(C-6),166.3(C-7),94.8(C-8),159.1(C-9),105.7(C-10),122.8(C-1′),132.3(C-2′/6′),116.1(C-3′/5′),161.5(C-4′),104.2(C-1″),75.7(C-2″),78.4(C-3″),71.4(C-4″),78.1(C-5″),62.7(C-6″)。以上数据与文献[14]对照基本一致,故鉴定化合物10为6-羟基山奈酚3-O-葡萄糖甙。
化合物11黄色粉末;ESI-MS:m/z431 [M-H]-,分子式为C21H20O10;1H NMR(500 MHz,CD3OD)δ:7.74(2H,d,J=8.7 Hz,H-2′,6′),6.91(2H,d,J=8.7 Hz,H-3′,5′),6.32(1H,d,J=2.1 Hz,H-8),6.16(1H,d,J=2.1 Hz,H-6),5.37(1H,d,J=1.7 Hz,H-1″),4.24(1H,dd,J=3.7,1.7 Hz,H-2″),3.73(1H,dd,J=9.0,3.7 Hz,H-3″),3.34(2H,m,H-4″,5″),0.92(3H,d,J=5.6 Hz,H-6″);13C NMR(125 MHz,CD3OD)δ:158.4(C-2),136.1(C-3),179.5(C-4),163.0(C-5),99.8(C-6),165.6(C-7),94.8(C-8),159.2(C-9),105.8(C-10),122.5(C-1′),131.7(C-2′/6′),116.5(C-3′/5′),161.4(C-4′),103.4(C-1″),71.9(C-2″),73.2(C-3″),72.0(C-4″),72.1(C-5″),17.6(C-6″)。以上数据与文献[15]对照基本一致,故鉴定化合物11为山柰酚-3-O-鼠李糖苷。
化合物12黄色粉末;ESI-MS:m/z595 [M+H]+,分子式为C27H30O15;1H NMR(500 MHz,(CD3)2CO)δ:8.09(2H,d,J=8.8 Hz,H-2′,6′),6.94(2H,d,J=8.8 Hz,H-3′,5′),6.48(1H,br s,H-8),6.24(1H,br s,H-6),5.12(1H,d,J=7.8 Hz,H-1″),4.53(1H,br s,H-1′″),3.81~3.32 (10H,m,H-2″、3″、4″、5″、6a″、6b″、2′″、3′″、4′″、5′″),1.08(3H,d,J=6.5 Hz,H-6′″);13C NMR(125 MHz,(CD3)2CO)δ:157.7(C-2),134.9(C-3),178.9(C-4),162.1(C-5),99.4(C-6),165.5(C-7),94.7(C-8),158.8(C-9),104.9(C-10),121.8(C-1′),131.9(C-2′/6′),115.9(C-3′/5′),160.8(C-4′),104.2(C-1″),71.1(C-2″),77.3(C-3″),70.3(C-4″),76.6(C-5″),67.8(C-6″),101.7(C-1′″),74.3(C-2′″),71.7(C-3′″),74.9(C-4′″),68.9(C-5′″),17.8(C-6′″)。以上数据与文献[16]对照基本一致,故鉴定化合物12为百蕊草素。
化合物13黄色粉末;ESI-MS:m/z465 [M+H]+,分子式为C27H30O15;1H NMR(500 MHz,(CD3)2CO)δ:8.10(2H,d,J=8.8 Hz,H-2′,6′),6.93(2H,d,J=8.8 Hz,H-3′,5′),6.48(1H,br s,H-8),6.24(1H,br s,H-6),5.04(1H,d,J=7.8 Hz,H-1″),4.52(1H,br s,H-1′″),3.81~3.32(10H,m,H-2″、3″、4″、5″、6a″、6b″、2′″、3′″、4′″、5′″),1.10(3H,d,J=6.5 Hz,H-6′″);13C NMR(125 MHz,(CD3)2CO)δ:157.7(C-2),135.0(C-3),178.9(C-4),162.1(C-5),99.4(C-6),165.4(C-7),94.7(C-8),158.6(C-9),104.9(C-10),121.8(C-1′),131.9(C-2′/6′),115.8(C-3′/5′),160.9(C-4′),104.7(C-1″),71.2(C-2″),77.4(C-3″),70.3(C-4″),76.8(C-5″),66.4(C-6″),100.9(C-1′″),73.8(C-2′″),72.5(C-3′″),74.3(C-4′″),68.8(C-5′″),17.7(C-6′″)。以上数据与文献[17]对照基本一致,故鉴定化合物13为kaempferol 3-O-α-L-rhamnopyranosyl-(1→6)-β-D-lucopyranoside。
化合物14淡黄色粉末;ESI-MS:m/z303 [M+H]+,分子式为C15H10O7;1H NMR(500 MHz,CD3OD)δ:7.72(1H,d,J=2.2 Hz,H-2′),7.63(1H,dd,J=8.5,2.2 Hz,H-6′),6.88(1H,d,J=8.5 Hz,H-5′),6.39(1H,d,J=2.1 Hz,H-8),6.18(1H,d,J=2.1 Hz,H-6);13C NMR(125 MHz,CD3OD)δ:158.2(C-2),137.2(C-3),177.3(C-4),148.8(C-5),99.3(C-6),165.7(C-7),94.5(C-8),162.4(C-9),104.5(C-10),124.2(C-1′),116.0(C-2′),148.0(C-3′),146.2(C-4′),116.3(C-5′),121.7(C-6′)。以上数据与文献[18]对照基本一致,故鉴定化合物14为槲皮素。
化合物15黄色粉末;ESI-MS:m/z317 [M+H]+,分子式为C16H12O7;1H NMR(500 MHz,CD3OD)δ:7.61(1H,d,J=2.1,H-2′),7.49(1H,dd,J=8.5,2.1 Hz,H-6′),6.88(1H,d,J=8.5 Hz,H-5′),6.30(1H,d,J=2.0 Hz,H-8),6.15(1H,d,J=2.0 Hz,H-6),3.76(3H,s,3-OCH3);13C NMR(125 MHz,CD3OD)δ:158.3(C-2),139.5(C-3),179.9(C-4),157.9(C-5),99.7(C-6),165.8(C-7),94.7(C-8),163.0(C-9),105.8(C-10),122.9(C-1′),116.4(C-2′),146.4(C-3′),149.9(C-4′),116.5(C-5′),122.3(C-6′),60.5(3-OCH3)。以上数据与文献[19]对照基本一致,故鉴定化合物15为3-O-甲基槲皮素。
化合物16黄色粉末;ESI-MS:m/z611 [M+H]+,分子式为C27H30O16;1H NMR(500 MHz,(CD3)2CO)δ:7.89(1H,d,J=2.2 Hz,H-2′),7.57(1H,dd,J=8.7,2.2 Hz,H-6′),6.86(1H,d,J=8.7 Hz,H-5′),6.37(1H,d,J=2.0 Hz,H-8),6.17(1H,d,J=2.0 Hz,H-6),5.07(1H,d,J=7.6 Hz,H-1″),4.54(1H,br s,H-1′″),3.81~3.26(10H,m,H-2″、3″、4″、5″、6a″、6b″、2′″、3′″、4′″、5′″),1.20(3H,d,J=6.5 Hz,H-6′″);13C NMR(125 MHz,(CD3)2CO)δ:158.9(C-2),135.8(C-3),179.4(C-4),162.7(C-5),100.0(C-6),166.0(C-7),94.6(C-8),158.3(C-9),105.6(C-10),123.0(C-1′),117.8(C-2′),149.9(C-3′),145.6(C-4′),116.1(C-5′),122.8(C-6′),105.5(C-1″),72.6(C-2″),78.1(C-3″),70.1(C-4″),75.2(C-5″),68.5(C-6″),101.8(C-1′″),73.8(C-2′″),73.1(C-3′″),75.1(C-4′″),70.2(C-5′″),17.9(C-6′″)。以上数据与文献[20]对照基本一致,故鉴定化合物16为quercetin-3-O-α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranoside。
化合物17黄色粉末;ESI-MS:m/z611 [M+H]+,分子式为C27H30O16;1H NMR(500 MHz,(CD3)2CO)δ:7.67(1H,d,J=2.2 Hz,H-2′),7.61(1H,dd,J=8.7,2.2 Hz,H-6′),6.87(1H,d,J=8.7 Hz,H-5′),6.37(1H,d,J=2.0 Hz,H-8),6.18(1H,d,J=2.0 Hz,H-6),5.10(1H,d,J=7.6 Hz,H-1″),4.53(1H,br s,H-1′″),3.82~3.27(10H,m,H-2″、3″、4″、5″、6a″、6b″、2′″、3′″、4′″、5′″),1.12(3H,d,J=6.5 Hz,H-6′″);13C NMR(125 MHz,(CD3)2CO)δ:159.3(C-2),135.6(C-3),179.3(C-4),162.8(C-5),100.0(C-6),165.9(C-7),94.6(C-8),158.4(C-9),104.6(C-10),123.5(C-1′),117.7(C-2′),149.7(C-3′),145.7(C-4′),116.1(C-5′),123.1(C-6′),104.5(C-1″),72.0(C-2″),77.1(C-3″),71.4(C-4″),75.7(C-5″),67.4(C-6″),102.3(C-1′″),72.2(C-2′″),72.1(C-3′″),73.9(C-4′″),69.7(C-5′″),17.9(C-6′″)。以上数据与文献[21]对照基本一致,故鉴定化合物17为quercetin-3-O-(6″-O-α-L-rhamnopyranosyl)-β-D-glucoside。
化合物1~17的结构见图1。
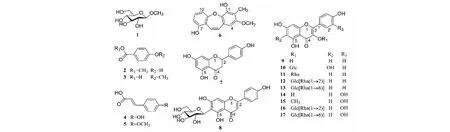
图1 化合物1-17的结构Fig.1 Structures of compounds 1-17
2.2 胰脂肪酶抑制活性筛选结果
按“1.2.2”项方法平行测定三次取平均值,结果显示阳性药奥利司他的IC50=0.021 mmol/L,对从白花洋紫荆花中分离得到的5个化合物的猪胰脂肪酶抑制活性进行了筛选,结果未显示较强的抑制活性,其中化合物13的IC50为0.96 mmol/L,其他化合物的IC50值均大于1.89 mmol/L与阳性药相差100倍以上,结果如表1所示。

表1 不同化合物抑制胰脂肪酶活性的Table 1 IC50 values of different compounds inhibiting
3 结论
从白花洋紫荆花分离得到的17个化合物主成分为黄酮类成分,且多数被报道具有一定的生物活性,主要集中在抗氧化,抗炎,保护心血管和调节血糖等,如葡萄糖苷类化合物β-D-甲基葡萄糖苷(1)对戊巴比妥钠诱发的实验性心衰猫具有加强心肌收缩力,改善心肌顺应性和左室舒缩功能,增加心排血量,升高动脉血压的作用[22]。对香豆酸(4)具有抗氧化,抗炎,免疫调节,抗肿瘤,抗血小板聚集,保护心血管,预防和改善糖尿病及神经保护作用[23]。黄酮类化合物柚皮素(7)、山柰酚(9)、槲皮素(14)、3-O-甲基槲皮素(15)、quercetin-3-O-α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranoside(16)具有广泛的药理活性,如抗氧化,抗炎,抗肿瘤,抗感染、心血管保护和血糖调节等药理活性[24-27]。山柰酚-3-O-鼠李糖苷(11)具有较好的抗幽门螺杆菌活性,并能降低氨苄西林对幽门螺杆菌的MIC[28],为民间用白花洋紫荆花入药提供了理论依据。胰脂肪酶主要是参与脂质的分解代谢,促进甘油三酯、胆固醇、磷脂等在十二指肠中消化,使得膳食脂肪被充分地消化和吸收,从而治疗肥胖等代谢性疾病[29],对分离得到量较多的化合物10、12、13、14、17的猪胰脂肪酶抑制活性进行了筛选,结果显示具有一定抑制活性,但与阳性药奥利司他比较抑制活性较弱,但白花洋紫荆花中含有较多的黄酮类成分,在作为抗氧化、预防衰老等保健品开发方面具有较大的潜在价值。

